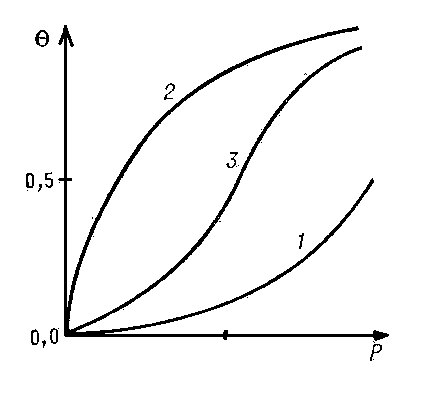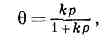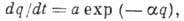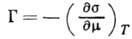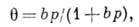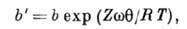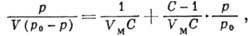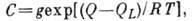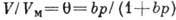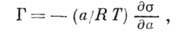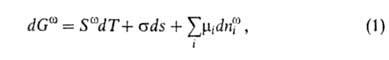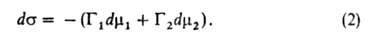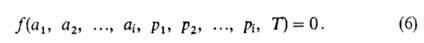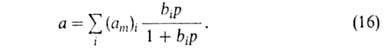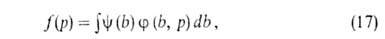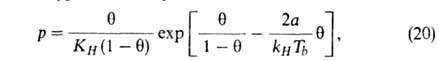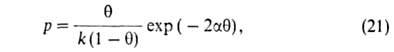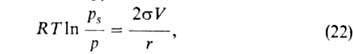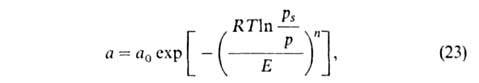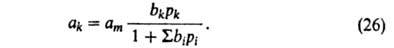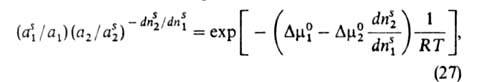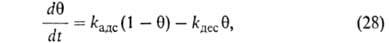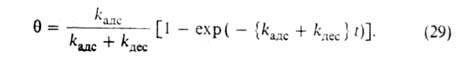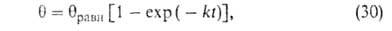Что такое адсорбция
Что такое адсорбция
Адсорбция
Литература : Cерпионова E. H., Промышленная адсорбция газов и паров, M., 1969; Глембоцкий B. A., Физико-химия флотационных процессов, M., 1972; Kельцев H. B., Oсновы адсорбционной техники, M., 1976.
И. T. Балыбердина.
Полезное
Смотреть что такое «Адсорбция» в других словарях:
АДСОРБЦИЯ — (от лат. ad на, при и sorbeo поглощаю), процесс, приводящий к аномально высокой концентрации в ва (а д с о р б а т а) из газообразной или жидкой среды на поверхности её раздела с жидкостью или тв. телом (а д с о р б е н т о м). Частный случай… … Физическая энциклопедия
АДСОРБЦИЯ — (от лат. ad на при и sorbeo поглощаю), поглощение газов, паров или жидкостей поверхностным слоем твердого тела (адсорбента) или жидкости. Адсорбенты обычно имеют большую удельную поверхность до нескольких сотен м²/г. Физическая адсорбция… … Большой Энциклопедический словарь
адсорбция — Самопроизвольное изменение концентрации раствора или газовой смеси вблизи поверхности раздела фаз. Примечание Адсорбирующее твердое тело называется адсорбентом, адсорбируемое вещество адсорбатом. [ГОСТ 17567 81] адсорбция Удерживание физическими… … Справочник технического переводчика
Адсорбция — – поглощение газов, паров или жидкостей поверхностным слоем твердого тела (адсорбента) или жидкости. [Терминологический словарь по бетону и железобетону. ФГУП «НИЦ «Строительство» НИИЖБ и м. А. А. Гвоздева, Москва, 2007 г. 110 стр.]… … Энциклопедия терминов, определений и пояснений строительных материалов
АДСОРБЦИЯ — (от лат. ad на и sorbeo поглощаю) поглощение различных веществ из растворов или воздушной среды поверхностями твердых тел. Может быть физической или химической (с образованием химических соединений), чаще всего сопровождается выделением тепла.… … Экологический словарь
адсорбция — поглощение вещества из раствора или газа поверхностным слоем жидкости или твердого тела (адсорбентом); играет важную роль в биол. системах, широко применяется в биохимии для разделения и очистки веществ. (Источник: «Микробиология: словарь… … Словарь микробиологии
адсорбция — и, ж. adsorption f. <лат. ad при + sorbere поглощать, всасывать. спец. Поглощение, всасывание вещества из раствора или газа поверхностью твердого тела или поверхностным слоем жидкости. Явления адсорбции. Адсорбция газов. Работы по изучению… … Исторический словарь галлицизмов русского языка
адсорбция — – самопроизвольное изменение концентрации растворенного вещества на границе раздела фаз. Общая химия : учебник / А. В. Жолнин [1] Адсорбция – поглощение вещества поверхностью твердого или жидкого сорбента. Словарь по аналитической химии [3] … Химические термины
АДСОРБЦИЯ — (от латинского ad на, при и sorbeo поглощаю), поглощение газов, паров или жидкостей поверхностным слоем твердого тела (адсорбента) или жидкости. В промышленности адсорбцию осуществляют в аппаратах адсорберах. На адсорбции основаны осушка газов,… … Современная энциклопедия
АДСОРБЦИЯ — АДСОРБЦИЯ, притяжение газа или жидкости к поверхности твердого тела или жидкости, в отличие от абсорбции, при которой подразумевается проникновение одного вещества в другое (как, например, губка пропитывается водой). Количество адсорбируемого… … Научно-технический энциклопедический словарь
Адсорбция
Полезное
Смотреть что такое «Адсорбция» в других словарях:
АДСОРБЦИЯ — (от лат. ad на, при и sorbeo поглощаю), процесс, приводящий к аномально высокой концентрации в ва (а д с о р б а т а) из газообразной или жидкой среды на поверхности её раздела с жидкостью или тв. телом (а д с о р б е н т о м). Частный случай… … Физическая энциклопедия
Адсорбция — [adsorptio всасывание, поглощение] поглощение поверхностью фазово инородного тела (адсорбента) каких либо веществ (адсорбатов) из смежной газовой или жидкой среды, протекающее на границе раздела фаз. А. из газовой фазы или из растворов нашла… … Геологическая энциклопедия
АДСОРБЦИЯ — (от лат. ad на при и sorbeo поглощаю), поглощение газов, паров или жидкостей поверхностным слоем твердого тела (адсорбента) или жидкости. Адсорбенты обычно имеют большую удельную поверхность до нескольких сотен м²/г. Физическая адсорбция… … Большой Энциклопедический словарь
адсорбция — Самопроизвольное изменение концентрации раствора или газовой смеси вблизи поверхности раздела фаз. Примечание Адсорбирующее твердое тело называется адсорбентом, адсорбируемое вещество адсорбатом. [ГОСТ 17567 81] адсорбция Удерживание физическими… … Справочник технического переводчика
Адсорбция — – поглощение газов, паров или жидкостей поверхностным слоем твердого тела (адсорбента) или жидкости. [Терминологический словарь по бетону и железобетону. ФГУП «НИЦ «Строительство» НИИЖБ и м. А. А. Гвоздева, Москва, 2007 г. 110 стр.]… … Энциклопедия терминов, определений и пояснений строительных материалов
АДСОРБЦИЯ — (от лат. ad на и sorbeo поглощаю) поглощение различных веществ из растворов или воздушной среды поверхностями твердых тел. Может быть физической или химической (с образованием химических соединений), чаще всего сопровождается выделением тепла.… … Экологический словарь
адсорбция — поглощение вещества из раствора или газа поверхностным слоем жидкости или твердого тела (адсорбентом); играет важную роль в биол. системах, широко применяется в биохимии для разделения и очистки веществ. (Источник: «Микробиология: словарь… … Словарь микробиологии
адсорбция — и, ж. adsorption f. <лат. ad при + sorbere поглощать, всасывать. спец. Поглощение, всасывание вещества из раствора или газа поверхностью твердого тела или поверхностным слоем жидкости. Явления адсорбции. Адсорбция газов. Работы по изучению… … Исторический словарь галлицизмов русского языка
адсорбция — – самопроизвольное изменение концентрации растворенного вещества на границе раздела фаз. Общая химия : учебник / А. В. Жолнин [1] Адсорбция – поглощение вещества поверхностью твердого или жидкого сорбента. Словарь по аналитической химии [3] … Химические термины
АДСОРБЦИЯ — (от латинского ad на, при и sorbeo поглощаю), поглощение газов, паров или жидкостей поверхностным слоем твердого тела (адсорбента) или жидкости. В промышленности адсорбцию осуществляют в аппаратах адсорберах. На адсорбции основаны осушка газов,… … Современная энциклопедия
АДСОРБЦИЯ — АДСОРБЦИЯ, притяжение газа или жидкости к поверхности твердого тела или жидкости, в отличие от абсорбции, при которой подразумевается проникновение одного вещества в другое (как, например, губка пропитывается водой). Количество адсорбируемого… … Научно-технический энциклопедический словарь
адсорбция
Полезное
Смотреть что такое «адсорбция» в других словарях:
АДСОРБЦИЯ — (от лат. ad на, при и sorbeo поглощаю), процесс, приводящий к аномально высокой концентрации в ва (а д с о р б а т а) из газообразной или жидкой среды на поверхности её раздела с жидкостью или тв. телом (а д с о р б е н т о м). Частный случай… … Физическая энциклопедия
Адсорбция — [adsorptio всасывание, поглощение] поглощение поверхностью фазово инородного тела (адсорбента) каких либо веществ (адсорбатов) из смежной газовой или жидкой среды, протекающее на границе раздела фаз. А. из газовой фазы или из растворов нашла… … Геологическая энциклопедия
АДСОРБЦИЯ — (от лат. ad на при и sorbeo поглощаю), поглощение газов, паров или жидкостей поверхностным слоем твердого тела (адсорбента) или жидкости. Адсорбенты обычно имеют большую удельную поверхность до нескольких сотен м²/г. Физическая адсорбция… … Большой Энциклопедический словарь
адсорбция — Самопроизвольное изменение концентрации раствора или газовой смеси вблизи поверхности раздела фаз. Примечание Адсорбирующее твердое тело называется адсорбентом, адсорбируемое вещество адсорбатом. [ГОСТ 17567 81] адсорбция Удерживание физическими… … Справочник технического переводчика
Адсорбция — – поглощение газов, паров или жидкостей поверхностным слоем твердого тела (адсорбента) или жидкости. [Терминологический словарь по бетону и железобетону. ФГУП «НИЦ «Строительство» НИИЖБ и м. А. А. Гвоздева, Москва, 2007 г. 110 стр.]… … Энциклопедия терминов, определений и пояснений строительных материалов
АДСОРБЦИЯ — (от лат. ad на и sorbeo поглощаю) поглощение различных веществ из растворов или воздушной среды поверхностями твердых тел. Может быть физической или химической (с образованием химических соединений), чаще всего сопровождается выделением тепла.… … Экологический словарь
адсорбция — поглощение вещества из раствора или газа поверхностным слоем жидкости или твердого тела (адсорбентом); играет важную роль в биол. системах, широко применяется в биохимии для разделения и очистки веществ. (Источник: «Микробиология: словарь… … Словарь микробиологии
адсорбция — и, ж. adsorption f. <лат. ad при + sorbere поглощать, всасывать. спец. Поглощение, всасывание вещества из раствора или газа поверхностью твердого тела или поверхностным слоем жидкости. Явления адсорбции. Адсорбция газов. Работы по изучению… … Исторический словарь галлицизмов русского языка
адсорбция — – самопроизвольное изменение концентрации растворенного вещества на границе раздела фаз. Общая химия : учебник / А. В. Жолнин [1] Адсорбция – поглощение вещества поверхностью твердого или жидкого сорбента. Словарь по аналитической химии [3] … Химические термины
АДСОРБЦИЯ — (от латинского ad на, при и sorbeo поглощаю), поглощение газов, паров или жидкостей поверхностным слоем твердого тела (адсорбента) или жидкости. В промышленности адсорбцию осуществляют в аппаратах адсорберах. На адсорбции основаны осушка газов,… … Современная энциклопедия
АДСОРБЦИЯ — АДСОРБЦИЯ, притяжение газа или жидкости к поверхности твердого тела или жидкости, в отличие от абсорбции, при которой подразумевается проникновение одного вещества в другое (как, например, губка пропитывается водой). Количество адсорбируемого… … Научно-технический энциклопедический словарь
Адсорбция
Адсорбция (лат. ad — на, при; sorbeo — поглощаю) — это, в широком смысле, процесс изменения концентрации у поверхности раздела двух фаз, а в более узком и употребительном — это повышение концентрации одного вещества (газ, жидкость) у поверхности другого вещества (жидкость, твердое тело).
Содержание
Основные понятия
Адсорбция и хемосорбция
На поверхности раздела двух фаз помимо адсорбции, обусловленной в основном физическими взаимодействиями (главным образом это Ван-дер-Ваальсовы силы), может идти химическая реакция. Этот процесс называется хемосорбцией. Чёткое разделение на адсорбцию и хемосорбцию не всегда возможно. Одним из основных параметров по которым различаются эти явления является тепловой эффект: так, тепловой эффект физической адсорбции обычно близок к теплоте сжижения адсорбата, тепловой эффект хемосорбции значительно выше. Кроме того в отличие от адсорбции хемосорбция обычно является необратимой и локализованной. Примером промежуточных вариантов, сочетающих черты и адсорбции и хемосорбции является взаимодействие кислорода на металлах и водорода на никеле: при низких температурах они адсорбируются по законам физической адсорбции, но при повышении температуры начинает протекать хемосорбция.
Схожие явления
В предыдущем разделе говорилось о случае протекания гетерогенной реакции на поверхности- хемосорбции. Однако бывают случаи гетерогенных реакций по всему объему, а не только на поверхности- это обычная гетерогенная реакция. Поглощение по всему объёму может проходить и под воздействием физических сил- этот случай называется абсорбцией.
| Виды взаимодействий | Взаимодействия только на поверхности | Взаимодействия по всему объёму |
|---|---|---|
| Физические | Адсорбция | Абсорбция |
| Химические | Хемосорбция | Гетерогенная реакция |
Физическая адсорбция
Причиной адсорбции являются неспецифические (то есть не зависящие от природы вещества) Ван-дер-Ваальсовы силы. Адсорбция, осложнённая химическим взаимодействием между адсорбентом и адсорбатом, является особым случаем. Явления такого рода называют хемосорбцией и химической адсорбцией. «Обычную» адсорбцию в случае, когда требуется подчеркнуть природу сил взаимодействия, называют физической адсорбцией.
Физическая адсорбция является обратимым процессом, условие равновесия определяется равными скоростями адсорбции молекул адсорбтива P на вакантных местах поверхности адсорбента S * и десорбции — освобождения адсорбата из связанного состояния S − P:

уравнение равновесияя в таком случае:

где K — константа равновесия, [S − P] и [S * ] — доли поверхности адсорбента, занятые и незанятые адсорбатом, а [P] — концентрация адсорбтива.
Количественно процесс физической мономолекулярной адсорбции в случае, когда межмолекулярным взаимодействием адсорбата можно пренебречь, описывается уравнением Ленгмюра:

где 

Поскольку 

Уравнение Ленгмюра является одной из форм уравнения изотермы адсорбции. Под уравнением изотермы адсорбции (чаще применяют сокращённый термин — изотерма адсорбции) понимают зависимость равновесной величины адсорбции от концентрации адсорбтива a=f(С) при постоянной температуре (T=const). Концентрация адсорбтива для случая адсорбции из жидкости выражается, как правило, в мольных либо массовых долях. Часто, особенно в случае адсорбции из растворов, пользуются относительной величиной: С/Сs, где С — концентрация, Сs — предельная концентрация (концентрация насыщения) адсорбтива при данной температуре. В случае адсорбции из газовой фазы концентрация может быть выражена в единицах абсолютного давления, либо, что особенно типично для адсорбции паров, в относительных единицах: P/Ps, где P — давление пара, Ps — давление насыщенных паров этого вещества. Саму величину адсорбции можно выразить также в единицах концентрации (отношение числа молекул адсорбата к общему числу молекул на границе раздела фаз). Для адсорбции на твёрдых адсорбентах, особенно при рассмотрении практических задач, используют отношение массы или количества поглощённого вещества к массе адсорбента, например мг/г или ммоль/г.
Значение адсорбции
Адсорбция — всеобщее и повсеместное явление, имеющее место всегда и везде, где есть поверхность раздела между фазами. Наибольшее практическое значение имеет адсорбция поверхностно-активных веществ и адсорбция примесей из газа либо жидкости специальными высокоэффективными адсорбентами. В качестве адсорбентов могут выступать разнообразные материалы с высокой удельной поверхностью: пористый углерод (наиболее распространённая форма — активированный уголь), силикагели, цеолиты а также некоторые другие группы природных минералов и синтетических веществ.
Адсорбция (особенно хемосорбция) имеет также важное значение в гетерогенном катализе. Пример адсорбционных установок приведён на странице азотные установки.
Установка для проведения адсорбции называется адсорбером.
АДСОРБЦИЯ
В зависимости от характера взаимодействия молекул адсорбата и адсорбента различают физическую А. и хемосорбцию. Физ. А. обусловлена силами межмолекулярного взаимодействия и не сопровождается существ. изменением электронной структуры молекул адсорбата. Физ. А. может быть как мо-нослойной (с образованием мономолекулярного слоя), так и полимолекулярной (многослойной). При А. электролитов из их растворов обычно возникает двойной электрический слой. Если жидкий адсорбат смачивает пористый адсорбент, то в порах последнего может происходить капиллярная конденсация. При физ. А. адсорбир. молекулы обычно обладают поверхностной подвижностью.
При хемосорбции между атомами (молекулами) адсорбента и адсорбата образуется хим. связь, т. о. хемосорбцию можно рассматривать как хим. реакцию, область протекания к-рой ограничена поверхностным слоем. В нек-рых случаях на одной поверхности могут протекать оба типа А. одновременно. В случае не слишком пористых адсорбентов физ. А. имеет место, как правило, при темп-pax ниже критич. темп-ры конденсации адсорбата, хемосорбция же чаще всего протекает при гораздо более высоких темп-рах. Однако в нек-рых системах физ. А. может протекать при темп-pax, значительно превышающих критич. темп-ру конденсации адсорбата. Как и любые хим. реакции, процессы хемосорбции носят специфичный характер (т. е. адсорбент хемосорбирует не любые молекулы, а лишь те, к-рые вступают в реакцию с атомами поверхности); в нек-рых случаях специфичность может проявляться и при физ. А.
Физ. характеристики А. Количеств. характеристикой А. является величина Г, представляющая собой избыток адсорбата, приходящийся на единицу площади поверхностного слоя, по сравнению с кол-вом адсорбата в единицу объёма фазы адсорбента. Отношение 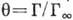
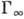
Теория А. Единая теория, к-рая описывала бы любые процессы А., пока не создана; существующие частные теоретич. разработки основываются на разл. моделях. Модель локализованной (или центровой) А. предполагает наличие на поверхности адсорбента т. н. центров А., представляющих собой либо строго определ. участки поверхности, на к-рых образуется сильная адсорбц. связь, либо распределённые по поверхности двумерные ячейки со слабым адсорбц. полем (полем сил межмолекулярного взаимодействия). В последнем случае предполагается наличие плотной упаковки молекул адсорбата на поверхности в пределах рассматриваемой ячейки.
В основе модели двумерной фазы лежит положение о том, что адсорбир. монослой представляет собой неидеальный двумерный газ, однако полимолекулярное покрытие поверхности адсорбента в данной модели не рассматривается. И, наконец, потенциальная модель А. базируется на представлении о потенц. поле поверхности твёрдого тела, в к-ром адсорбир. газ сжат вблизи поверхности и разрежен в наружных слоях. Эти различные в своей основе модели могут приводить к математически идентичным выражениям, хорошо согласующимся с эксперим. данными. Полуэмпирич. теории, основанные
на рассмотренных моделях, не позволяют достаточно строго интерпретировать эксперим. данные, т. к. пока не удаётся учитывать энергетич. неоднородность поверхности, связанную с разл. природой центров А. Осн. термодинамич. ур-нием, описывающим А., является ур-ние Гиббса:
где 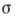
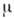
Теория Ленгмюра позволяет вывести ур-ние одной из наиб, простых изотерм А., справедливое при строгой энергетич. однородности поверхности адсорбента, а также при отсутствии на поверхности латерального взаимодействия:
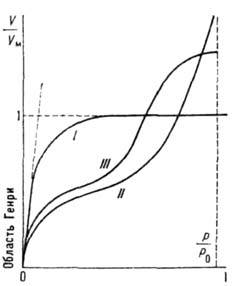
Рис. 1. Наиболее часто встречающиеся изотермы адсорбции.
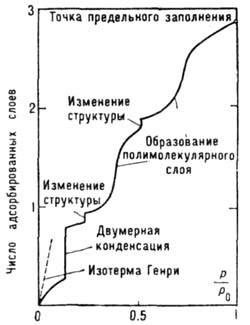
Рис. 2. Обобщённая изотерма адсорбции (изотерма Холси).
На рис. 1 это отражено прямолинейностью нач. участка изотермы, совпадающего с прямой пунктирной линией. Теория Ленгмюра применима к описанию монослойной физ. А. и хемосорбции, но лишь для огранич. числа систем. Узкая область применимости теории Ленгмюра объясняется, по-видимому, энергетич. неоднородностью поверхности, а также латеральным взаимодействием. Последний фактор в наиб. простом приближении можно учесть путём введения в ур-ние Ленгмюра вместо константы b константу
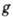
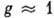
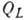
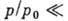
(где 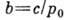
В потенц. теории А. (т. н. теория Поляни) полагается, что А. протекает под действием не зависящего от темп-ры потенциала 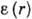
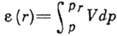
На основании потенц. модели можно для каждой адсорбц. системы построить характеристическую кривую 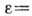
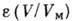
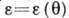
Плавная форма изотерм А., по-видимому, является следствием энергетич. неоднородности поверхности. В то же время адсорбаты и их комплексы с адсорбентами могут претерпевать на поверхности фазовые переходы, проявляющиеся лишь в условиях строгой энергетич. однородности поверхности в форме ступенек и изломов на эксперим. изотермах. Обобщённая (модельная) изотерма Холси (рис. 2) отражает разл.
типы фазовых переходов, соответствующих как субмонослойной области, так и области полимолекулярной А. Возможность всех подобных типов переходов была подтверждена экспериментально.
Все перечисленные модели и теории относятся, в первую очередь, к А. на твёрдых адсорбентах из газовой фазы, однако с небольшими изменениями они пригодны и для описания А. из растворов.
где а— активность растворённого вещества. Соединения, для к-рых 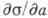
Помимо изотерм А., на практике часто пользуются изостерами А., выражающими зависимость между равновесным давлением и темп-рой А. для определ. кол-ва адсорбир. вещества. При помощи изостер, полученных методом термодесорбции, осуществляют обычно вычисление теплот А., к-рые можно определять также методом калориметрии. Для изучения А. в настоящее время применяется также разнообразный арсенал совр. методов исследования вещества. Для определения кол-ва адсорбир. вещества, числа адсорбц. центров и величины адсорбир. поверхности используют машинные методы анализа эксперим. изотерм, а также гравиметрич. и радиоизотопный методы и высокотемпературную газовую хроматографию.
Поверхность адсорбентов исследуют с помощью методов рентгеновского структурного анализа и электронографии, оже-спектроскопии, мёссбауэровской спектроскопии, рентгеновской и рентгеноэлектронной спектроскопии, масс-спектроскопии, а также электронной микроскопии, мюонного и позитронного методов. Для изучения молекул в адсорбир. состоянии используют флэш-десорбцию (см. Десорбция), все виды оптической и резонансной спектроскопии, дифракцию медленных электронов, магн. методы, методы электронного или ионного проекторов, а также всевозможные электро-хим. методы.
Х и м и я
Коллоидная химия
Адсорбция.
Сорбция
Сорбцией (от латинского sorbeo – поглощаю, втягиваю) называют любой процесс поглощения одного вещества (сорбтива) другим (сорбентом), независимо от механизма поглощения.
В зависимости от механизма сорбции различают адсорбцию, абсорбцию, хемосорбцию и капилярную конденсацию.
Адсорбция это процесс, происходящий на границе раздела фаз. Он затрагиваетолько поверхностные слои, взаимодействующих фаз, и не распространяется на глубинные слои этих фаз.
Адсорбцией называют явление накопления одного вещества на поверхности другого. В общем случае, адсорбцией называют изменение концентрации вещества на границе раздела фаз.
Абсорбция, в отличии от адсорбции, это процесс захватывающий не только поверхность раздела фаз, но распространяющийся на весь объём сорбента.
Примером процесса абсорбции является растворение газов в жидкости.
Хемосорбцией называется поглощение одного вещества другим, сопровождающееся их химическим взаимодействием.
Капиллярная конденсация — сжижение пара в капиллярах, щелях или порах в твердых телах.
Явление конденсации отлично от физической адсорбции.
Таким образом, сорбционные процессы различны по их механизму. Однако, любой сорбционный процесс начинается с адсорбции на границе соприкасающихся фаз, которые могут быть жидкими, газообразными или твёрдыми.
Адсорбция
Напомним, что адсорбцией называют явление накопления одного вещества на поверхности другого. В общем случае, адсорбцией называют изменение концентрации вещества на границе раздела фаз.
Адсорбция происходит на любых межфазовых поверхностях и адсорбироваться могут любые вещества.
Адсорбционное равновесие, т.е. равновесное распределение вещества между пограничным слоем и граничащими фазами является динамическим равновесием и быстро устанавливается.
Адсорбция понижается с понижением температуры.
Поглощаемое вещество, ещё находящееся в объёме фазы, называют адсорбтивом, поглощённое — адсорбатом. Вещество, на поверхности которого происходит адсорбция – адсорбентом.
Адсорбция представляет собой обратимый процесс. Процесс, обратный адсорбции, называется десорбцией.
Удаление адсорбированных веществ с адсорбентов при помощи растворителей называют элюцией.
Различают молекулярную и ионную адсорбцию. Это различение происходит в зависимости от того, что адсорбируется – молекулы или ионы вещества.
Адсорбция на поверхности жидкостей
На поверхности жидкостей могут адсорбироваться частицы веществ, растворённых в жидкостях. Адсорбция сопровождает процесс растворения, влияя на распределение частичек растворённого вещества между поверхностным слоем растворителя и внутренним его объёмом.
В соответствии со вторым началом термодинамики поверхностная энергия жидкостей стремится к минимуму. В чистых растворителях уменьшение этой энергии происходит путём сокращения поверхности.
В растворах поверхностная энергия может понижаться или увеличиваться за счёт изменения концентрации частиц в поверхностном слое жидкости.
Гиббсом было установлено, что распределение растворяемого в жидкости вещества происходит так, чтобы достигалось максимальное уменьшение поверхностного натяжения.
Он же предложил уравнение, определяющее величину адсорбции Г, т.е избытка вещества, накапливающегося в 1 см 2 поверхностного слоя, имеющего толщину примерно в одну молекулу, по сравнению с содержанием этого вещества в таком же объёме внутри жидкости.
Следовательно, адсорбция Г зависит от величины поверхностной активности и концентрации вещества С.
Если при этом поверхностное натяжение уменьшается, то адсорбция Г имеет положительное значение.
Положительная адсорбция. Поверхностно-активные вещества.
Чем сильнее вещество понижает поверхностное натяжение, тем больше оно будет накапливаться в поверхностном слое.
Концентрация растворённого вещества в поверхностном слое станет значительно выше, чем в остальном объёме жидкости. Возникающая разность концентраций неизбежно вызовет диффузию, которая будет направлена из поверхностного слоя внутрь жидкости и явится препятствием для полного перехода всех растворённых частиц в поверхностный слой. Установится подвижное адсорбционное равновесие между растворённым веществом в поверхностном слое и остальном объёме жидкости.
Адсорбцию, сопровождающуюся накоплением вещества в поверхностном слое, называют положительной. Пределом её служит полное насыщение поверхностного слоя адсорбируемым веществом.
Положительно адсорбирующиеся вещества называют также поверхностно-активными веществами (ПАВ). В водных растворах роль ПАВов будут играть вещества с жирной и дифильной природой (жиры, большинство жирных кислот, кетоны, спирты, холестерин и др.).
Отрицательная адсорбция. Поверхностно-инактивные вещества.
Если растворённое вещество увеличивает поверхностное натяжение, то оно будет выталкиваться из поверхностного слоя внутрь адсорбента. Такую адсорбцию называют отрицательной.
Пределом отрицательной адсорбции является полное вытеснение адсорбтива из поверхностного слоя внутрь адсорбента (растворителя).
В результате разности концентраций возникнет диффузия, которая будет направлена в поверхностный слой. Поэтому в поверхностном слое всегда окажется некоторое количество адсорбтива.
Вещества, резко повышающие поверхностное натяжение, почти не содержатся в поверхностном слое разбавленных растворов. Лишь значительное увеличение концентрации подобных растворов приводит к перемещению в поверхностный слой заметных количеств растворённого вещества, что сопровождается увеличением поверхностного натяжения.
Отрицательно адсорбирующиеся вещества называются поверхностно-инактивными.
Адсорбция и поверхносное натяжение биологических жидкостей
Отрицательная и положительная адсорбция различных веществ в крови и протоплазме клеток имеет большое значение для обмена веществ в живых организмах.
Поверхностное натяжение биологических жидкостей значительно ниже, чем воды. Поэтому гидрофобные вещества, например кислоты жирного ряда, стероиды, будут накапливаться у стенок сосудов, клеточных мембран, что облегчает их проникновение сквозь эти мембраны.
Жидкость
Поверхностное натяжение эрг/см 2
Сыворотка крови человека (при 38 С)
Этиловый спирт
Цитоплазма амёб (на границе с маслом)
Для адсорбции из водных растворов большое значение имеет наличие у молекул полярных (гидрофильных) и неполярных (гидрофобных) групп.
Так, в молекуле масляной кислоты имеется полярная группа СООН и гидрофобная углеводородная цепь:
Молекулы обладающие одновременно обеими видами групп, называются дифильными.
У дифильной молекулы с короткой гидрофобной цепью преобладают гидрофильные свойства, поэтому такие молекулы хорошо растворяются в воде, адсорбируясь отрицательно.
С удлинением углеводородной цепи усиливаются гидрофобные свойства молекул и понижается их растворимость в воде.
Следовательно, к поверхностно-активным веществам принадлежат вещества дифильной структуры, имеющие меньшее, чем растворитель, поверхностное натяжение, и растворение которых приводит к положительной адсорбции, вызывая понижение поверхностного натяжения.
Поверхностно-инактивные вещества обладают противоположными свойствами.
Одновременно с увеличением гидрофобных свойств молекул повышается их поверхностная активность. Так удлинение цепи в гомологическом ряду жирных кислот, спиртов, аминов и др. на радикал –СН2– увеличивает их способность к положительной адсорбции в разбавленных растворах в 3,2 раза (правило Траубе-Дюкло).
Поверхностные плёнки
Молекулы веществ с преобладанием гидрофобных свойств (жирные кислоты с большим молекулярным весом и др.) располагаются в основном на поверхности воды, образуя поверхностные плёнки.
При небольшом количестве таких молекул поверхностной плёнки не образуется. Если же молекул много, то они располагаются упорядоченно, одна рядом с другой, причём их гидрофобные части выступают над водной поверхностью, образуя так называемый частокол Лэнгмюра.
Поверхностная плёнка образуется мономолекулярным слоем молекул, каждая из которых занимает на поверхности воды определённую площадь. Толщину слоя и площадь, занимаемую каждой молекулой, можно расчитать.
Жирные кислоты с двумя полярными группами (например, олеиновая кислота) занимает площадь, вдвое большую, а молекулы с тремя полярными группами (например, тристеарин) – втрое большую площадь и т.д.
При избытке вещества с преимущественно гидрофобными свойствами его молекулы располагаются над молекулярной плёнкой.
Образование поверхностных плёнок нередко затрудняет процесс фильтрации.
На границе раздела воздух–вода в пузырьках воздуха, находящихся в растворе, может адсорбироваться поверхностно-активное вещество. Плёнка этого вещества образует как-бы оболочку вокруг пузырька. Такой пузырёк при продавливании через узкие поры в фильтре не способен резко деформироваться и поэтому может закупорить более крупные отверстия в фильтре, чем пузырёк без плёнки.
У водолазов, работающих на больших глубинах, иногда возникает, так называемая, кесонная болезнь. В их скафандры воздух подаётся под давлением и, следовательно, в крови водолазов растворяется повышенное количество газов.
При слишком быстром поднятии на поверхность давление в скафандрах резко понижается, и значительная часть газов крови выделяется в виде пузырьков, на которых образуется поверхностная плёнка из содержащихся в крови поверхностно-активных веществ.
Пузырьки газов закупоривают мелкие сосуды в различных тканях и органах, что приводит к тяжёлому заболеванию или даже гибели человека.
Подобная же паталогия может возникнуть и в результате резкого падения атмосферного давления при разгерметизации скафандров лётчиков и кабин самолётов при высотных полётах.
Для лечения кессонной болезни больного помещают в барокамеру, где создают большое давление. Пузырьки газов вновь растворяются в крови. В течении нескольких суток давление в барокамере медленно снижают. За это время избыточный газ из крови столь же медленно удаляется через лёгкие, не создавая закупорок.
Адсорбция твёрдыми телами
Твёрдыми телами могут адсорбироваться газы и пары, а также молекулы и ионы растворённых веществ.
Природа сил, вызывающих адсорбцию
Адсорбция на твёрдых телах может быть объяснена наличием силовых полей притяжения, возникающих за счёт неуравновешенных связей в кристалической решётке.
На выступающих участках твёрдого адсорбента (на активных центрах) адсорбция идёт особенно сильно. Так выступы на частичке угля в 4,5 раза интенсивнее адсорбируют кислород, чем углубления на его поверхности.
Адсорбционные силы слагаются из валентных сил взаимодействия (химических) и более слабых ван-дер-ваальсовых (физических). Роль тех и других при разных случаях адсорбции различна. Так, в самом начале адсорбции большинства газов, когда их давление мало, наблюдается химическая адсорбция. С увеличением давления она уступает место физической, которая в основном определяет адсорбцию газов.
Адсорбционные силы могут быть достаточно велики. Так, для полного удаления со стекла адсорбированных молекул воды его необходимо сильно нагревать в вакууме.
Адсорбенты, обладающие мощными силовыми полями, оказываются сплошь покрытыми адсорбированными частицами. При незначительных же адсорбционных силах только более активные центры покрываеются адсорбируемыми частицами.
На адсорбцию влияет не только природа адсорбента, но и адсорбтива. Так, на твёрдых адсорбентах сильнее адсорбируются те газы, которые легче сжижаются, т.е. критическая температура которых выше.
Адсорбция представляет собой обратимый процесс. Адсорбированные частицы не остаются не остаются неподвижными. Они удерживаются на адсорбенте всего сотые и тысячные доли секунды и, десорбируясь, замещаются на новые частицы. К тому же они не являются строго фиксированными на адсорбенте, а могут перемещаться по его поверхности. В итоге устанавливается динамическое адсорбционное равновесие между свободными и адсорбированными частицами.
Скорость адсорбции имеет большое значение для практического использования различных адсорбентов.
Например, в противогазе проходящий через коробку воздух должен очень быстро очищаться от примесей отравляющих веществ, что возможно лишь при высоких скоростях адсорбционных процессов.
Необходимо указать, что активированный уголь в противогазе играет роль не только адсорбента ряда отравляющих веществ, но и катализатора реакций разложения некоторых из них.
В частности, активированный уголь катализирует гидролиз фосгена:
Повышение температуры понижает физическую адсорбцию адсорбцию, так как при этом усиливается движение молекул в адсорбционном слое, нарушается ориентация адсорбированных молекул, т.е. увеличивается десорбция.
С другой стороны увеличение температуры увеличивает энергию адсорбированных частиц, что усиливает химическую адсорбцию.
Следовательно, в одних случаях повышение температуры усиливает десорбцию, в других – увеличивает адсорбцию.
Так, для большинства газов повышение температуры уменьшает адсорбцию. В то же время увеличение температуры от –185 до +20°С в 10 раз увеличивает адсорбцию кислорода платиной, так как при этом возрастает химическая адсорбция.
Повышение давления газов и паров увеличивает адсорбцию.
При адсорбции паров наблюдают так называемую капилярную конденсацию, протекающую на угле и других пористых адсорбентах.
Сконденсировавшаяся в капилярах жидкость образует вогнутый мениск, над которым пар оказывается насыщенным при более низком давлении, чем над плоской поверхностью. Это повышает конденсацию паров в капилярах адсорбента.
Капилярная конденсация особенно выражена у легко сжижаемых газов.
Хемосорбция
При хемосорбции вещество вступает с адсорбентом в химическую реакцию, например:
Если вновь образующиеся при хемосорбции молекулы диффундируют в глубь вещества адсорбента, то достижение сорбционного равновесия наступает медленнее, так как оно зависит от скорости диффузии.
Если же при хемосорбции на поверхности сорбента возникают недиффундирующие молекулы, т.е. образуется плёнка, то она тормозит и со временем останавливает процесс хемосорбции.
Так, пластинка алюминия, сорбируя кислород, покрывается плёнкой из оксида оалюминия, что быстро прекращает процесс хемосорбции:
Хемосорбция, как и всякая химическая реакция, может быть экзо- или эндотермической. Следовательно повышение температуры усиливает одни хемосорбционные процессы и ослабляет другие.
Полностью разграничить адсорбцию и хемосорбцию нельзя. Обычно эти два процесса протекают совместно.
АДСОРБЦИЯ
(от лат. ad-на, при и sorbeo-поглощаю), изменение (обычно-повышение) концентрации в-ва вблизи пов-сти раздела фаз («поглощение на пов-сти»). В общем случае причина А.-нескомпенсированность межмол. сил вблизи этой пов-сти, т. е. наличие адсорбц. силового поля. Тело, создающее такое поле, наз. адсорбентом, в-во, молекулы к-рого могут адсорбироваться,-а д с о р б т и в о м, уже адсорбиров. в-во-адсорбатом. Процесс, обратный А., наз. десорбцией.
В теории А. различают статику (система адсорбент-ад-сорбат находится в термодинамич. равновесии) и кинетику (равновесия нет).
Термодинамика. Основы термодинамики А. были созданы Дж. Гиббсом в 70-е гг. 19 в. По Гиббсу, в равновесной двухфазной системе вблизи пов-сти раздела фаз происходит нек-рое изменение локальных значений всех экстенсивных св-в (кроме объема). Однако фазы считаются однородными вплоть до нек-рой геом. пов-сти, разделяющей их. Поэтому значение к.-л. экстенсивного св-ва для системы в целом 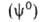
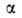
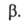
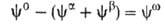
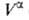
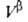
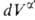
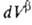
Изложенные представления позволяют привести фундам. термодинамич. ур-ние к виду:
Величина 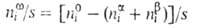
Положение разделяющей пов-сти м. б. выбрано произвольно. В частности, выбор этого положения может удовлетворять условию Г 1 = 0. Такая пов-сть наз. эквимолекулярной. Для нее вводится обозначение Г 2 = Г 2 (1) Отсюда следует осн. адсорбц. ур-ние Гиббса:
Если адсорбтив совершенно не раств. в одной из двух фаз, 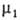
Изотерма адсорбции. В равновесной адсорбц. системе параметры, определяющие равновесие,-это р (или с i) и т-ра Т. Они связаны т. наз. термич. ур-нием:
При А. индивидуального адсорбтива (i=1) это ур-ние принимает вид:
Три частных случая термич. ур-ния (когда Т, р или a-константы) играют особую роль в теории А.:
Конкретный вид ф-ций 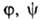
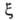
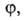
В теории А. обычно решается вопрос о виде ф-ции а= 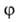
Т. к. система равновесна, то хим. потенциалы адсорбата и адсорбтива одинаковы; энтропия адсорбата вследствие уменьшения подвижности молекул при А. меньше энтропии адсорбтива. Поэтому при инертном адсорбенте энтальпия всегда отрицательна, т. е. А. экзотермична. Учет изменения энтропии адсорбента может изменить этот вывод. Напр., при сорбции полимерами в-в, в к-рых полимер набухает, энтропия последнего (из-за увеличения подвижности макромолекул) может столь сильно возрасти, что А. становится эндотермической. В дальнейшем в статье рассматривается только экзотермич. А.
Модель Ленгмюра требует, чтобы дифференц. теплота и энтропия А. не зависели от степени заполнения пов-сти.
Ур-ние (14)-строгое выражение, соответствующее модели Ленгмюра, однако оно редко оправдывается на опыте, поскольку сама модель идеализирована. Учение об А. с 20-х гг. 20 в. в значит. степени строилось на основе ослабления или исключения того или иного допущения Ленгмюра.
Уже Ленгмюр предложил способ описания А. на неоднородной пов-сти (т. е. при допущении, что не все центры оди наковы). Объединяя одинаковые центры в группы и полагая, что к каждой группе применимо ур-ние (14), можно считать, что А. на всей пов-сти выражается суммой членов ур-ния (14):
Полагая, что число адсорбц. центров м. б. описано непрерывной ф-цией распределения по значениям своб. энергии, Я. Б. Зельдович получил из ф-лы (16) для экспоненциальной ф-ции ур-ние типа (13).
А. на неоднородных пов-стях-большая глава теории А. Ее осн. задача-решение интегрального ур-ния:
где f(р)- т. наз. эмпирич. изотерма А., 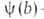
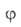
Много попыток сделано в направлении отказа от второго допущения Ленгмюра. На этом пути особое значение приобрела теория полимолекулярной А., предложенная С. Брунауэром, П. Эмметом и Э. Теллером (теория БЭТ). Теория постулирует, что при т-ре ниже критической каждая молекула, адсорбированная в первом слое (теплота адсорбции и с. Широкое распространение теории БЭТ связано с тем, что ее авторы, фактически считая А. нелокализованной, отождествляют константу а т не с числом дискретных адсорбц. центров, а с числом молекул адсорба-та в первом слое при плотнейшей упаковке (при р=
Поэтому, вводя представление о площади 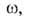
В теорию полимолекулярной А. большой вклад внес Я. де Бур, экспериментально показавший, что зависимость среднего числа слоев (свыше первого) на всех пов-стях, близких по хим. природе, от
Предпринимались попытки учесть в модели Ленгмюра также взаимод. между адсорбиров. молекулами. Так, Т. Хилл и Я. де Бур, считая, что ур-ние состояния адсорбц. слоя есть двухмерный аналог ур-ния Ван-дер-Ваальса, получили след. ур-ние изотермы А.:
где 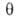
где 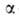
Существует еще один механизм, приводящий к дополнит. А. адсорбтивов ниже их критич. т-ры на пористых адсорбентах при сравнительно высоких значениях
Согласно ур-нию Кельвина:
где 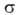
Капиллярную конденсацию используют для определения размеров пор адсорбента. По ур-нию (22) для каждого значения
Объем таких пор определяют по приросту А. в этой точке изотермы. Используя полученные данные, строят кривую распределения объема пор по их радиусам. Метод применим при ref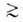
Потенциальная теория адсорбции и теория объемного заполнения микропор. Модель А., принципиально отличную от ленгмюровской, предложил в 1914 М. Поляки. Согласно этой модели, вблизи пов-сти адсорбента существует потенциальное адсорбц. силовое поле, убывающее с расстоянием от пов-сти. Вследствие этого давление адсорбтива, равное вдали от пов-сти р, вблизи нее возрастает и на нек-ром расстоянии достигает значения ps, при к-ром адсорбтив конденсируется. Объем слоя между пов-стыо раздела и геом. местом точек, где р =ps, заполнен жидкостью, к-рой приписываются нормальные значения физ. св-в объемной жидкости. Обратимая изотермич. работа е адсорбц. сил, определяемая по ур-нию 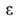
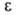
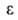
Введя представление о ф-ции распределения объемов пор по значениям хим. потенциала адсорбата в них, М. М. Дубинин и Л. В. Радушкевич получили ур-ние изотермы адсорбции ТОЗМ, к-рое обычно записывают в след. форме:
где 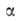
Каждый микропористый адсорбент характеризуется по ТОЗМ двумя параметрами: W- объемом микропор ( константа, связанная с E в ур-нии (23), а у=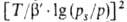
Адсорбция газовых и жидких смесей. Па практике всегда имеют дело не с индивидуальным адсорбтивом, а со смесью газов или с жидкими р-рами. Поэтому требуется обобщение теории А. на случай многокомпонентного адсорбтива. В принципе можно исходить из любой модели А. и распространить ее на этот случай. При А. газовой смеси это достигается не только большим усложнением ур-ний, но и введением в них дополнит. эмпирич. параметров, связанных или с взаимод. разнородных молекул или, в более общем виде, с влиянием одних в-в на коэф. активности других. Только модель Ленгмюра позволяет получить ур-ние изотермы А. смеси без параметров, не входящих в ур-ния для А. индивидуальных в-в. Для этого достаточно учесть, что при адсорбции k-того компонента из смеси iкомпонентов часть адсорбц. центров м. б. занята др. молекулами. Поэтому:
В случае А. жидких р-ров независимо от их концентрации вся пов-сть адсорбента заполнена. Вследствие этого А. молекулы k-того компонента сопровождается вытеснением не-к-рого числа молекул остальных компонентов, т. е. А. носит конкурентный характер.
Различают молекулярную и ионную А. р-ров. Первая происходит при А. р-ров неэлектролитов, вторая-р-ров электролитов. Молекулярная А., как правило, выражается избыточными величинами. Конкурентный характер А. обусловливает то, что величина ам. б. как положительной, так и отрицательной. Выражая А. i-того компонента как ф-цию его мольной доли в р-ре х i-, имеем, что Г i = О при х i = 0 и х i = 1 (возможным изменением объема в-ва в адсорбц. слое пренебрегают). Поэтому изотерма А. имеет один или неск. экстремумов.
Ур-ние изотермы А. бинарных р-ров неэлектролитов, надежно обоснованное термодинамически, имеет вид:
где индекс s указывает на адсорбц. фазу, Ч ( s 2/dn s 1 )показывает, сколько молей второго компонента вытесняется одним молем первого, 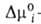
Осн. проблема использования этого и ряда др. уравнений изотермы А.-выяснение зависимости коэф. активности компонентов в адсорбц. слое от его состава. Важнейший вопрос при применении А. для разделения или очистки в-в-подбор селективного адсорбента по отношению к данному компоненту р-ра.
Ионная А., как правило, не носит эквивалентного характера. На пов-сти из р-ра электролита адсорбируются преим. катионы или анионы. Благодаря электрич. (кулонов-ским) силам на пов-сти образуется двойной электрический слой.
Если в состав адсорбента входят ионы или поверхностные функц. группы, способные в данном р-рителе к ионизации, то между адсорбентом и р-ром электролита происходит ионный обмен. Адсорбент в этом случае наз. ионитом.
А., как и любой реальный процесс, происходит во времени. Поэтому полная теория А. должна содержать раздел о кинетике А. Элементарный акт А. осуществляется практически мгновенно (исключение-хемосорбция). Поэтому временные зависимости А. определяются в осн. механизмом диффузии, т. е. подвода адсорбтива к месту А. Если А. на открытой пов-сти не мгновенна, такой процесс происходит во внешнедиффузионной области; при этом законы диффузии не специфичны для А. В случае же пористых адсорбентов, кроме внеш. диффузии, важную роль начинает играть внутр. диффузия, т. е. перенос адсорбтива в порах адсорбента при наличии в них градиента концентрации. Механизм такого переноса может зависеть от концентрации адсорбтива и размеров пор.
Различают молекулярную, кнудсеновскую и поверхностную (фольмеровскую) диффузию. Молекулярная диффузия осуществляется, если длина своб. пробега молекул в порах меньше размера пор, кнудсеновская-если эта длина превышает размер пор. При поверхностной диффузии молекулы перемещаются по пов-сти адсорбента без перехода в объемную фазу. Однако значения коэф. диффузии не одинаковы для разных механизмов диффузии. Во мн. случаях экспериментально не удается установить, как именно происходит диффузия, и поэтому вводят т. наз. эффективный коэф. диффузии, описывающий процесс в целом.
В случае открытой пов-сти, принимая модель Ленгмюра, легко получить кинетич. ур-ние А. Скорость приближения к равновесию 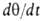
где k адс и k дес— константы скорости соотв. А. и десорбции. Давление в газовой фазе считается постоянным. При интегрировании этого ур-ния от t= 0 до любого значения tполучим:
Отсюда при f 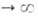
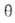
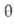
Влияние т-ры на скорость А. выражается ур-нием, аналогичным ур-нию Аррениуса. С увеличением т-ры k адс экспоненциально возрастает. Т. к. диффузия в порах адсорбента связана с преодолением активац. барьеров, температурные зависимости k адс и k дес не одинаковы.
Знание скоростей диффузии важно не только для теории А., но и для расчета пром. адсорбц. процессов. При этом обычно имеют дело не с отдельными зернами адсорбента, а с их слоями. Кинетика процесса в слое выражается очень сложными зависимостями. В каждой точке слоя в данный момент времени величина А. определяется не только видом ур-ния изотермы А. и закономерностями кинетики процесса, но также аэро- или гидродинамич. условиями обтекания зерен газовым или жидкостным потоком. Кинетика процесса в слое адсорбента в отличие от кинетики в отдельном зерне наз. динамикой А., общая схема решения задач к-рой такова: составляется система дифференц. ур-ний в частных производных, учитывающая характеристики слоя, изотерму А., диффузионные характеристики (коэф. диффузии, виды переноса массы по слою и внутри зерен), аэро- и гидродинамич. особенности потока. Задаются начальные и краевые условия. Решение этой системы ур-ний в принципе приводит к значениям величин А. в данный момент времени в данной точке слоя. Как правило, аналитич. решение удается получить только для простейших случаев, поэтому такая задача решается численно с помощью ЭВМ.
При опытном изучении динамики А. через слой адсорбента пропускают газовый или жидкостный поток с заданными характеристиками и исследуют состав выходящего потока как ф-цию времени. Появление поглощаемого в-ва за слоем наз. проскоком, а время до проскока Ч временем защитного действия. Зависимость концентрации данного компонента за слоем от времени наз. выходной кривой. Эти кривые служат осн. эксперим. материалом, позволяющим судить о закономерностях динамики А.
Аппаратурное оформление адсорбционных процессов
По техн. и экономич. соображениям регенерацию не доводят до конца. Поэтому рабочая емкость адсорбента равна разности между максимально достигаемой в данных условиях А. и кол-вом адсорбата, остающегося в адсорбенте после регенерации. Вследствие этого изотермы А., соответствующие процессу в адсорбере, не должны быть слишком крутыми.
В описанной схеме возможны два варианта: 1) целевой продукт адсорбируется из газового потока практически полностью, и тогда он содержится в десорбате, откуда его извлекают тем или иным способом; 2) целевой продукт адсорбируется хуже, чем др. компоненты газовой смеси, и тогда он содержится в выходящем газовом потоке. По первому варианту работают, напр., рекуперационные установки на вискозных произ-вах, улавливающие из отходящих газов и возвращающие в цикл CS2. Производительность таких установок достигает сотен тысяч м 3 очищаемого газа в час; адсорбент-активный уголь с не слишком тонкими микропорами, т. е. уголь, в к-ром константа E по ТОЗМ (см. выше) равна 20-25 кДж/моль. Это значение E0 соответствует не слишком крутой изотерме, что обеспечивает хорошие условия регенерации. Такие угли наз. рекуперационными. Десорбцию осуществляют острым водяным паром. Для экономии энергии холодные и газовые горячие потоки пропускают через теплообменники.
Очень важна осушка газов и жидкостей, напр. нефтяных газов перед их переработкой или прир. газов перед транспортировкой; адсорбенты-силикагель или цеолиты. Десорбцию осуществляют нагреванием. Т. к. десорбция цеолита связана с большими энергозатратами, применяют комбинированный адсорбент: осн. массу влаги поглощают легко регенерируемым силикагелем, а глубокую доосушку-цеолитом.
При тепловой регенерации полный цикл включает А., нагрев адсорбента, его десорбцию и охлаждение. Большое число стадий обусловливает низкую интенсивность и высокую энергоемкость процесса. Поэтому широкое распространение получили т. наз. короткоцикловые установки, весь цикл в к-рых занимает неск. минут. В них газ подается в адсорбер под значит. давлением, к-рое затем сбрасывается, и происходит десорбция. Весь процесс идет почти изотермически (отклонение от изотермичности вызывается только выделением теплоты А. и поглощением теплоты при десорбции). Стадии цикла: А., сброс давления, десорбция, подъем давления. Пример-установки с цеолитом для получения воздуха, обогащенного кислородом.
В установках с псевдоожиженным («кипящим») слоем адсорбента газовый поток, поступающий в адсорбер снизу, приводит адсорбент во взвешенное состояние. При этом резко увеличивается эффективность массообмена между адсорбентом и газом и сокращается длительность А. и десорбции. Такие установки имеют высокую производительность. Их широкому распространению препятствуют высокие требования, предъявляемые к мех. прочности зерен адсорбента (недостаточная прочность обусловливает значит. потери адсорбента вследствие его истирания и уноса из аппарата).
Осн. требования к адсорбентам: большая адсорбц. емкость, т. е. они должны представлять собой дисперсные тела с большой уд. пов-стью или с большим объемом пор; хим. природа пов-сти должна обеспечивать эффективную А. данных в-в в данных условиях; хим. и термич. стойкость, регенерируемость, доступность. наиб. распространение получили активные угли, ксерогели нек-рых оксидов (силика-гели, алюмогели и др.), цеолиты; из непористых адсорбентов-техн. углерод (сажа) и высокодисперсный SiO2 (аэросил, «белая сажа»).
Области применения адсорбционной техники
На явлении А. основаны мн. способы очистки воздуха от вредных примесей (см. Газов очистка), воды (см. Водоподготовка), а также сахарных сиропов при сахароварении, фруктовых соков и др. жидкостей в пищ. пром-сти, отработанных смазочных масел. Удаление влаги как вредной примеси из газов и жидкостей с помощью твердых адсорбентов-одна из важных отраслей адсорбц. техники (см. также Газов осушка).
На адсорбц. процессах основано тонкое разделение смесей в-в и выделение из сложных смесей определенных компонентов. Примеры-разделение изомеров алканов с целью получения нормальных углеводородов для произ-ва ПАВ, разделение нефтей при произ-ве моторных топлив. Для газовых смесей адсорбц. методы разделения используют при получении воздуха, обогащенного кислородом (вплоть до почти чистого О 2); во мн. случаях эти методы успешно конкурируют с ректификационным (см. Воздуха разделение).
Быстро развивающаяся область применения адсорбц. техники-медицина, где она служит для извлечения вредных в-в из крови (метод гемосорбции) и др. физиол. жидкостей. Высокие требования к стерильности ставят очень трудную задачу подбора подходящих адсорбентов. К ним относятся специально приготовленные активные угли.
Лит.: Брунауэр С., Адсорбция газов и паров, пер. с англ., т. 1, М., 1948; де Бур Я, Динамический характер адсорбции, пер. с англ., М., 1962; Адсорбция и пористость, под ред. М. М. Дубинина [и др.], М., 1976; Кельиев Н. В., Основы адсорбционной техники, 2 изд., М., 1984; Young D.M., Crowell A.D., Physical adsorption of gases, L., 1962. М. М. Дубинин, В. В. Серпинский.
АДСОРБЦИЯ
АДСОРБЦИЯ (adsorptio; латинский ad — на, при и sorbeo — поглощаю) — поглощение газов, паров или растворенных веществ поверхностью твердого тела или жидкости.Тело, на поверхности которого происходит адсорбция, называют адсорбентом, адсорбируемое вещество — адсорбтивом или адсорбатом. Адсорбция газов твердыми телами (древесным углем) была открыта шведским химиком Шееле (С. W. Scheelе) в 1773 году и независимо от него итальянцем Фонтаной (F. Foiitana) в 1777 году; адсорбция веществ из растворов древесным углем — русским химиком академиком Т. Е. Ловицем в 1785 году. Возможность адсорбции на поверхности жидкости и связь этого явления с поверхностным натяжением впервые теоретически были доказаны американским математиком и физиком Гиббсом (J. W. Gibbs) в 1876 году Впоследствии было показано, что адсорбция относится к чрезвычайно распространенным явлениям и обнаруживается почти всюду, где газы, пары и растворенные вещества находятся в контакте с поверхностью жидкости или твердого тела.
Различают физическую и химическую адсорбцию. В первом случае адсорбированные молекулы сохраняют свою индивидуальность; при химической адсорбции, называемой также хемосорбцией, молекула адсорбируемого вещества вступает в химическую связь с поверхностью адсорбента. Физическая адсорбция, которую обычно называют просто адсорбция, представляет собой обратимый процесс, заканчивающийся установлением адсорбционного равновесия, при котором скорость адсорбции равна скорости обратного процесса — десорбции. Хемосорбция, как правило, необратима.
Адсорбция часто сопровождается абсорбцией (см.), хемосорбцией и конденсацией паров адсорбтива в порах адсорбента. Во всех этих случаях сложный процесс поглощения называют сорбцией (см.).
Величину адсорбции на поверхности жидкости, граничащей с газом или с другой жидкостью, непосредственно не измеряют, а вычисляют с помощью уравнения Гиббса:
где Г — количество адсорбированного вещества в молях на 1 см 2 поверхности жидкости, С — молярная концентрация адсорбтива в жидкости, R — газовая постоянная из уравнения Клапейрона—Менделеева, Т — абсолютная температура, Δσ — изменение поверхностного натяжения, соответствующее изменению концентрации адсорбтива на ΔС.
Величину адсорбции газа или растворенного вещества на твердом адсорбенте измеряют непосредственно и выражают в молях адсорбированного вещества на 1 г адсорбента. Количество адсорбированного газа обычно определяют по привесу адсорбента, поглотившего газ; величину адсорбции растворенного вещества — по уменьшению его концентрации в растворе.
Зависимость величины адсорбции при постоянной температуре от равновесной концентрации адсорбтива, выраженную графически или в виде уравнения, называют изотермой адсорбции. На рис. представлена типичная экспериментальная изотерма адсорбции. При очень малых концентрациях величина адсорбции пропорциональна концентрации, что находит свое выражение в прямолинейном ходе изотермы адсорбции в области малых концентраций. С дальнейшим ростом концентрации рост величины адсорбции замедляется. При очень больших концентрациях величина адсорбции достигает предельного значения, что объясняется насыщением поверхности адсорбента молекулами адсорбтива, образующими мономолекулярный адсорбционный слой. В тех случаях, когда адсорбционный слой полимолекулярен или адсорбция осложнена капиллярной конденсацией (см. Сорбция), изотерма поглощения имеет более сложный вид.
На практике для аналитического выражения изотермы адсорбция при средних значениях концентраций обычно пользуются уравнением Фрейндлиха:
где а — величина адсорбции в молях на 1 г адсорбента, с — концентрация в молях на 1 л, k и n — константы. Константа k численно равна величине адсорбции при концентрации, равной 1; величина ее определяет высоту кривой над осью абсцисс и меняется в широких пределах в зависимости от природы адсорбента и адсорбтива. Константа п определяет кривизну изотермы; ее численная величина мало изменяется с природой адсорбента и адсорбтива и колеблется в пределах от 0,1 до 0,6. Уравнение Фрейндлиха графически представляет собой параболическую кривую (рис.).
Для более широкой области концентраций чаще применяют уравнение Лангмюра:
где а и с имеют те же значения, что и в уравнении Фрейндлиха, а∞ и α — константы, численные значения которых зависят от природы адсорбента и адсорбтива. Константа их равна предельной величине адсорбции, соответствующей полному насыщению поверхности поглотителя молекулами адсорбтива. Константа α равна отношению константы скорости десорбции к константе скорости адсорбции.
Помимо концентрации адсорбтива, величина адсорбции зависит от природы адсорбента и адсорбтива; Адсорбция возрастает с увеличением удельной поверхности поглотителя. Для органических веществ одного и того же гомологического ряда величина адсорбции возрастает приблизительно в 3 раза с увеличением углеводородной цепи на одну группу CH2 (правило Дюкло—Траубе). Величина адсорбции, как правило, уменьшается с повышением температуры. Величина адсорбции из растворов зависит от природы растворителя: чем лучше вещество растворяется в данном растворителе, тем хуже оно из него адсорбируется.
Адсорбция из растворов сильных электролитов подразделяют на следующие виды: эквивалентная адсорбция, при которой катионы и анионы электролита адсорбируются в эквивалентных количествах; избирательная адсорбция — в этом случае избирательно адсорбируются или катионы, или анионы электролита; поверхность адсорбента при этом приобретает соответственно положительный или отрицательный электрический заряд. Ионообменная адсорбция представляет собой обмен катионов или анионов между адсорбентом и раствором (см. Иониты).
В насыщенном адсорбционном слое молекулы адсорбтива ориентированы, например, на поверхности водных растворов полярные группы адсорбированных молекул погружены в раствор. Представление об ориентации молекул в насыщенном адсорбционном слое сыграло большую роль при изучении структуры биологических мембран.
Практическое значение адсорбционных явлений очень велико. Адсорбция лежит в основе крашения тканей, дубления кож и так далее. Адсорбция является начальной стадией процесса поглощения любых веществ клетками и тканями. С адсорбцией тесно связаны также процессы взаимодействия ферментов с субстратами, антител с антигенами, поляризации и деполяризации биологических мембран.
Адсорбция играет основную роль при протекании многих каталитических реакций (см. Катализ) и в химии коллоидных растворов.
Ряд адсорбентов (уголь, каолин, гидроокись железа, ионообменные смолы и другие) применяют как противоядия (см.) для связывания ядов и токсинов, попавших в желудочно-кишечный тракт, а также для адсорбции кишечных газов при метеоризме (см.). Активированный древесный уголь используют как адсорбент в военных и промышленных противогазах. В технике адсорбции применяют для очистки веществ, в том числе и лекарственных, регенерации ценных летучих растворителей, для разделения и анализа сложных смесей (см. Хроматография).
адсорбция
повышение концентрации компонента в поверхностном слое вещества (на границе раздела фаз) по сравнению с ее значением в каждой объемной фазе
Следует отличать а д сорбцию от а б сорбции, при которой вещество диффундирует в объем жидкости или твердого тела и образует раствор или гель. Термин сорбция объединяет оба понятия. Вещество, на поверхности которого происходит адсорбция, называется адсорбентом, а поглощаемое — адсорбатом. В зависимости от характера взаимодействия между молекулой адсорбата и адсорбентом адсорбцию принято подразделять на физическую адсорбцию (слабые взаимодействие) и хемосорбцию (сильные взаимодействия). Чёткой границы между физической адсорбцией и хемосорбцией не существует; в качестве граничного значения принята энергия связи между адсорбатом и адсорбентом, равная 0,5 эВ на атом или молекулу.
Процесс, обратный адсорбции, называется десорбцией. Если скорости адсорбции и десорбции равны, то говорят об установлении адсорбционного равновесия. В состоянии равновесия количество адсорбированных молекул остаётся постоянным сколь угодно долго, если неизменны внешние условия (давление, температура и состав системы).
На практике адсорбция широко используется для концентрирования веществ, очистки газов и жикостей от примесей. Адсорбционные методы анализа применяются для определения удельной поверхности твердых веществ, оценки размера нанесенных частиц (в том числе наноразмерных) на поверхности носителя и т.п.
Полезное
Смотреть что такое «адсорбция» в других словарях:
АДСОРБЦИЯ — (от лат. ad на, при и sorbeo поглощаю), процесс, приводящий к аномально высокой концентрации в ва (а д с о р б а т а) из газообразной или жидкой среды на поверхности её раздела с жидкостью или тв. телом (а д с о р б е н т о м). Частный случай… … Физическая энциклопедия
Адсорбция — [adsorptio всасывание, поглощение] поглощение поверхностью фазово инородного тела (адсорбента) каких либо веществ (адсорбатов) из смежной газовой или жидкой среды, протекающее на границе раздела фаз. А. из газовой фазы или из растворов нашла… … Геологическая энциклопедия
АДСОРБЦИЯ — (от лат. ad на при и sorbeo поглощаю), поглощение газов, паров или жидкостей поверхностным слоем твердого тела (адсорбента) или жидкости. Адсорбенты обычно имеют большую удельную поверхность до нескольких сотен м²/г. Физическая адсорбция… … Большой Энциклопедический словарь
адсорбция — Самопроизвольное изменение концентрации раствора или газовой смеси вблизи поверхности раздела фаз. Примечание Адсорбирующее твердое тело называется адсорбентом, адсорбируемое вещество адсорбатом. [ГОСТ 17567 81] адсорбция Удерживание физическими… … Справочник технического переводчика
Адсорбция — – поглощение газов, паров или жидкостей поверхностным слоем твердого тела (адсорбента) или жидкости. [Терминологический словарь по бетону и железобетону. ФГУП «НИЦ «Строительство» НИИЖБ и м. А. А. Гвоздева, Москва, 2007 г. 110 стр.]… … Энциклопедия терминов, определений и пояснений строительных материалов
АДСОРБЦИЯ — (от лат. ad на и sorbeo поглощаю) поглощение различных веществ из растворов или воздушной среды поверхностями твердых тел. Может быть физической или химической (с образованием химических соединений), чаще всего сопровождается выделением тепла.… … Экологический словарь
адсорбция — поглощение вещества из раствора или газа поверхностным слоем жидкости или твердого тела (адсорбентом); играет важную роль в биол. системах, широко применяется в биохимии для разделения и очистки веществ. (Источник: «Микробиология: словарь… … Словарь микробиологии
адсорбция — и, ж. adsorption f. <лат. ad при + sorbere поглощать, всасывать. спец. Поглощение, всасывание вещества из раствора или газа поверхностью твердого тела или поверхностным слоем жидкости. Явления адсорбции. Адсорбция газов. Работы по изучению… … Исторический словарь галлицизмов русского языка
адсорбция — – самопроизвольное изменение концентрации растворенного вещества на границе раздела фаз. Общая химия : учебник / А. В. Жолнин [1] Адсорбция – поглощение вещества поверхностью твердого или жидкого сорбента. Словарь по аналитической химии [3] … Химические термины
АДСОРБЦИЯ — (от латинского ad на, при и sorbeo поглощаю), поглощение газов, паров или жидкостей поверхностным слоем твердого тела (адсорбента) или жидкости. В промышленности адсорбцию осуществляют в аппаратах адсорберах. На адсорбции основаны осушка газов,… … Современная энциклопедия
АДСОРБЦИЯ — АДСОРБЦИЯ, притяжение газа или жидкости к поверхности твердого тела или жидкости, в отличие от абсорбции, при которой подразумевается проникновение одного вещества в другое (как, например, губка пропитывается водой). Количество адсорбируемого… … Научно-технический энциклопедический словарь
АДСОРБЦИЯ
— поглощение вещества из газа или раствора поверхностью раздела между ними (или поверхностью твердого тела). Иными словами, А. есть поглощение адсорбата из объема фаз на поверхности адсорбента. А. является частным случаем сорбции.
Молекулы адсорбата, попадая на поверхность адсорбента, удерживаются силовым полем поверхности в течение нек-рого времени, зависящего от природы адсорбата и адсорбента, от температуры Ти давления р, а затем покидают поверхность (десорбируются). В состоянии термодинамического и молекулярного равновесия скорости А. и десорбции равны. Зависимость между относительным давлением 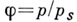
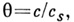
Уравнение Ленгмюра мономолекулярной А. имеет вид
Для однородной поверхности адсорбента при полимолекулярной А. обычно используется уравнение Брунауера [1].
Для капиллярных тел широкое распространение получила эмпирическая формула Поснова [2]
Лит.:[1] Брунауер С., Адсорбция газов и паров, пер. с англ., т. 1, М., 1948; [2] Поснов В. А., «Ж. техн. физики», 1953, № 23, с. 865; [3] Ильин Б. В., Природа адсорбционных сил, М.- Л., 1952; [4] де Бур Я. X., Динамический характер адсорбции, пер. с англ., М., 1962.
Полезное
Смотреть что такое «АДСОРБЦИЯ» в других словарях:
АДСОРБЦИЯ — (от лат. ad на, при и sorbeo поглощаю), процесс, приводящий к аномально высокой концентрации в ва (а д с о р б а т а) из газообразной или жидкой среды на поверхности её раздела с жидкостью или тв. телом (а д с о р б е н т о м). Частный случай… … Физическая энциклопедия
Адсорбция — [adsorptio всасывание, поглощение] поглощение поверхностью фазово инородного тела (адсорбента) каких либо веществ (адсорбатов) из смежной газовой или жидкой среды, протекающее на границе раздела фаз. А. из газовой фазы или из растворов нашла… … Геологическая энциклопедия
АДСОРБЦИЯ — (от лат. ad на при и sorbeo поглощаю), поглощение газов, паров или жидкостей поверхностным слоем твердого тела (адсорбента) или жидкости. Адсорбенты обычно имеют большую удельную поверхность до нескольких сотен м²/г. Физическая адсорбция… … Большой Энциклопедический словарь
адсорбция — Самопроизвольное изменение концентрации раствора или газовой смеси вблизи поверхности раздела фаз. Примечание Адсорбирующее твердое тело называется адсорбентом, адсорбируемое вещество адсорбатом. [ГОСТ 17567 81] адсорбция Удерживание физическими… … Справочник технического переводчика
Адсорбция — – поглощение газов, паров или жидкостей поверхностным слоем твердого тела (адсорбента) или жидкости. [Терминологический словарь по бетону и железобетону. ФГУП «НИЦ «Строительство» НИИЖБ и м. А. А. Гвоздева, Москва, 2007 г. 110 стр.]… … Энциклопедия терминов, определений и пояснений строительных материалов
АДСОРБЦИЯ — (от лат. ad на и sorbeo поглощаю) поглощение различных веществ из растворов или воздушной среды поверхностями твердых тел. Может быть физической или химической (с образованием химических соединений), чаще всего сопровождается выделением тепла.… … Экологический словарь
адсорбция — поглощение вещества из раствора или газа поверхностным слоем жидкости или твердого тела (адсорбентом); играет важную роль в биол. системах, широко применяется в биохимии для разделения и очистки веществ. (Источник: «Микробиология: словарь… … Словарь микробиологии
адсорбция — и, ж. adsorption f. <лат. ad при + sorbere поглощать, всасывать. спец. Поглощение, всасывание вещества из раствора или газа поверхностью твердого тела или поверхностным слоем жидкости. Явления адсорбции. Адсорбция газов. Работы по изучению… … Исторический словарь галлицизмов русского языка
адсорбция — – самопроизвольное изменение концентрации растворенного вещества на границе раздела фаз. Общая химия : учебник / А. В. Жолнин [1] Адсорбция – поглощение вещества поверхностью твердого или жидкого сорбента. Словарь по аналитической химии [3] … Химические термины
АДСОРБЦИЯ — (от латинского ad на, при и sorbeo поглощаю), поглощение газов, паров или жидкостей поверхностным слоем твердого тела (адсорбента) или жидкости. В промышленности адсорбцию осуществляют в аппаратах адсорберах. На адсорбции основаны осушка газов,… … Современная энциклопедия
АДСОРБЦИЯ — АДСОРБЦИЯ, притяжение газа или жидкости к поверхности твердого тела или жидкости, в отличие от абсорбции, при которой подразумевается проникновение одного вещества в другое (как, например, губка пропитывается водой). Количество адсорбируемого… … Научно-технический энциклопедический словарь
Значение слова адсорбция
Начала Современного Естествознания. Тезаурус
(от лат. ad — на, при и sorbeo — поглощаю) — изменение, обычно повышение, концентрации вещества вблизи поверхности раздела фаз («поглощение на поверхности»). Процесс обратный адсорбции — десорбция.
Криминалистическая энциклопедия
поглощение газов, паров и жидкостей поверхностным слоем твердого тела (адсорбента) или жидкости. Используется для забора запаховых следов с места происшествия; лежит в основе многих методов хроматографии.
Стоматологический словарь
Энциклопедический словарь
Словарь Ефремовой
ж.
Поглощение, всасывание вещества из раствора или газа поверхностью твердого тела
или поверхностным слоем жидкости.
Словарь медицинских терминов
поглощение (концентрирование) газов или растворенных веществ на поверхности твердого тела или жидкости.
Большая Советская Энциклопедия
Вещество, на поверхности которого происходит А., называется адсорбентом, а поглощаемое из объёмной фазы ≈ адсорбатом. В зависимости от характера взаимодействия между молекулой адсорбата и адсорбентом А. принято подразделять на физическую А. и хемосорбцию. Менее прочная физическая А. не сопровождается существенными изменениями молекул адсорбата. Она обусловлена силами межмолекулярного взаимодействия, которые связывают молекулы в жидкостях и некоторых кристаллах и проявляются в поведении сильно сжатых газов. При хемосорбции молекулы адсорбата и адсорбента образуют химические соединения. Часто А. обусловлена и физическими и химическими силами, поэтому не существует чёткой границы между физикой А. и хемосорбцией.
Физически адсорбированные молекулы более или менее свободно перемещаются по поверхности, при этом их свойства часто аналогичны свойствам очень тонкого слоя газа, т. н. двухмерного газа. Они могут собираться группами, образуя слой двухмерной жидкости или двухмерного твёрдого тела. Адсорбированные молекулы рано или поздно покидают поверхность ≈ десорбируются. Время, в течение которого молекула находится на поверхности, называется временем А. Времена А. могут колебаться в очень широких пределах. Скоростью А. (соответственно скоростью десорбции) называется количество молекул, адсорбирующихся (или десорбирующихся) за единицу времени, оба значения величин относят к единице поверхности или массы адсорбента. Скорость хемосорбции, как и скорость любого химического процесса, чаще всего увеличивается с повышением температуры (т. н. активированная А., см. Хемосорбция ). Если скорости А. и десорбции равны друг другу, то говорят, что установилось адсорбционное равновесие. В состоянии равновесия количество адсорбированных молекул остаётся постоянным сколь угодно долго, если неизменны внешние условия (давление, температура и др.).
Адсорбированные молекулы не только совершают движение вдоль поверхности адсорбента, но и колеблются, то приближаясь к поверхности, то удаляясь от неё. Чем выше температура, тем интенсивнее колебательное движение, а стало быть, больше вероятность того, что в процессе таких колебаний связь молекулы с поверхностью будет разорвана и молекула десорбируется. Благодаря этому с ростом температуры уменьшается время А. и равновесное количество адсорбированных молекул.
С ростом концентрации или давления адсорбата в объёме увеличивается частота попаданий молекул адсорбата на поверхность адсорбента; пропорционально ей возрастает скорость А. и увеличивается равновесное количество адсорбированных молекул. Кривые зависимости равновесной А. от концентрации или давления адсорбата при постоянной температуре называются изотермами А.
Если адсорбат покрывает поверхность слоем толщиной в одну молекулу, А. называется мономолекулярной. Простейшая изотерма мономолекулярной А. представляет собой прямую линию, выходящую из начала координат, где на оси абсцисс отложено давление адсорбата Р, а на оси ординат степень заполнения поверхности Q, т. е. доля поверхности, покрытая адсорбированными молекулами. Это ≈ т. н. изотерма Генри:
Коэффициент пропорциональности k зависит главным образом от температуры и характера взаимодействия адсорбент ≈ адсорбат.
Уравнение Генри справедливо при очень низких степенях заполнения для однородной поверхности. По мере увеличения степени заполнения всё большую роль начинает играть взаимодействие между адсорбированными молекулами и интенсивность их поверхностной подвижности. Если молекулы адсорбата притягиваются друг к другу, то каждая вновь адсорбирующаяся молекула будет испытывать притяжение и адсорбата и молекул, адсорбированных ранее. Поэтому, по мере заполнения поверхности, силы, удерживающие адсорбированную молекулу, будут увеличиваться и условия для А. будут всё более и более благоприятными. В этом случае с ростом давления изотерма всё круче и круче идёт вверх (см. кривую 1). Однако по мере заполнения поверхности вновь адсорбирующимися молекулами становится всё труднее найти свободное (не занятое др. молекулами адсорбата) место на поверхности. Поэтому с увеличением давления рост А. замедляется и степень покрытия стремится к постоянному значению, равному единице (см. кривую 2, которая характерна при отсутствии взаимного притяжения молекул адсорбата). Если действуют оба эти фактора, то получаются вогнуто-выпуклые изотермы (см. кривую 3).
Выпуклые изотермы (см. кривую 2) часто описывают уравнением Ленгмюра
Здесь а ≈ адсорбционный коэффициент, аналогичный по физическому смыслу константе Генри k. Уравнение Ленгмюра справедливо для мономолекулярной А. на однородной поверхности, если можно пренебречь притяжением молекул адсорбата между собой и их подвижностью вдоль поверхности.
Почти всегда процесс А. сопровождается выделением тепла, называемой теплотой А. Хотя теплота А. не является единственным фактором, характеризующим прочность А., однако чаще всего чем прочнее А., тем больше её теплота. Теплота хемосорбции обычно составляет несколько десятков ккал/моль, теплота физической А. редко превосходит 10 ккал/моль (40 кдж/моль). По мере заполнения неоднородной поверхности теплота А. обычно уменьшается. При переходе в область полимолекулярной А. теплота А. понижается до величины, близкой к теплоте конденсации адсорбата.
А. играет важную роль при теплообмене между газообразными, жидкими и твёрдыми телами. например, молекулы газа, адсорбируясь на горячей поверхности, приобретают энергию, соответствующую температуре поверхности, и после десорбции сообщают эту энергию другим молекулам газа, нагревая его. Это не единственный, но важный механизм теплообмена.
При крашении тканей, в полиграфической промышленности имеют дело с А. молекул красителей. При производстве полимеров наполнителями служат адсорбенты. В вакуумной технике А. на стенках откачиваемой аппаратуры замедляет скорость откачки и ухудшает вакуум, однако, с другой стороны, действие различных сорбционных насосов основано на явлении А. В радиоэлектронной промышленности А. используется для стабилизации электрических свойств полупроводниковых приборов. Вообще во всех явлениях и процессах, где существенны поверхностные свойства, А. играет важную роль.
Лит.: Курс физической химии, т. 1, М., 1964; Бур Я.Х., Динамический характер адсорбции, пер. с англ., М., 1962; Трепнел Б., Хемосорбция, пер. с англ., М., 1958; Бладергрен В., Физ. химия в медицине и биологии, пер. с нем., М., 1951.