Диастолическая дисфункция левого желудочка 1 типа что это такое
Диастолическая дисфункция левого желудочка 1 типа что это такое
Новые возможности медикаментозного лечения диастолической формы хронической сердечной недостаточности
Опубликовано:
Российский кардиологический журнал № 4 (84) / 2010
Адамчик А.С., Крючкова И.В., Рубан Г.М., Благодырева Ю.А.
Кубанский государственный медицинский университет, Краснодар
Проблеме хронической сердечной недостаточности (ХСН) в последние годы уделяется большое внимание, что связано с неуклонным ростом заболеваемости и высоким уровнем смертности населения [1]. В настоящее время наиболее значимыми факторами риска этой патологии считаются артериальная гипертензия (АГ), дислипидемия, ожирение и сахарный диабет, которые, к тому же, имеют тенденцию к сочетанию [2,3]. B 1988 г. американский ученый G. Reaven выдвинул теорию, сформировавшуюся в понятие метаболического синдрома (МС), в основе которой лежит тесная патогенетическая взаимосвязь этих факторов [4,5]. Инсулинорезистентность (ИР) выступает в качестве основного связывающего звена цепи метаболических нарушений и является самостоятельным фактором риска сердечно-сосудистых заболеваний [6]. Риск развития осложнений кардиоваскулярных заболеваний у пациентов с МС возрастает в 3-4 раза [7]. Разработка концепции МС позволила оценить важную роль гиперинсулинемии (ГИ) и ИР в становлении АГ и хронической сердечной недостаточности (ХСН) [8]. На сегодняшний день именно АГ считается наиболее частой причиной развития нарушения диастолической функции левого желудочка (ЛЖ), которая, в свою очередь, приводит к возникновению признаков ХСН при отсутствии снижения сократительной способности миокарда ЛЖ, т. е. развитию диастолической формы ХСН. Вопрос ранней и эффективной терапии данной формы ХСН остается на настоящий момент нерешенным. Различные исследования в этой области дают положительные результаты [9,10,11], однако общепризнанных схем коррекции диастолической дисфункции ЛЖ не разработано. Современные представления o значительной распространенности диастолической дисфункции миокарда ЛЖ и её роли в возникновении сердечной недостаточности диктуют необходимость ранней диагностики этого явления и его своевременной коррекции [12].
Одним из перспективных препаратов в лечении диастолической ХСН является таурин, биологические свойства которого представляют интерес для практической медицины [13]. Таурин является природным кальциевым антагонистом, мембраностабилизатором, антиоксидантом, осморегулятором, а также обладает свойствами нейромодулятора и блокатора симпато-адреналовой системы и ренин-ангиотензин-альдостероновой системы [14, 15, 16, 17, 18, 19]. В клинике дибикор применяется в комплексной терапии сахарного диабета 1 и 2 типов, а также при ХСН [20].
Цель исследования – оценка состояния диастолической функции ЛЖ у пациентов с клиническими проявлениями ХСН и ФВ ЛЖ >50% и возможности медикаментозного воздействия на диастолическую дисфункцию ЛЖ.
Материал и методы
В исследование на условиях добровольного информированного согласия были включены 78 человек с диастолической формой ХСН и метаболическим синдромом, госпитализированных в стационар или обратившихся на кафедру. Выделенная группа пациентов представлена 19 мужчинами и 59 женщинами в возрасте от 31 до 66 лет (средний возраст – 48,5 лет). Критерии включения: ХСН I-III ФК и I-IIА стадии, артериальная гипертензия II стадии 1-3 степеней, ожирение, дислипидемия и нарушение углеводного обмена. Критерии исключения из исследования: ишемическая болезнь сердца, острое нарушение мозгового кровообращения, острый и перенесенный инфаркт миокарда, симптоматические артериальные гипертензии, сахарный диабет 1 и 2 типов.
Наличие МС определяли на основании классификации Adult Treatment Panel III (АТР III), 2001г. [21,22] и International Diabetes Federation (IDF), 2005г. Диагностика нарушений углеводного обмена проводилась согласно классификации ВОЗ 1999г. ХСН выявляли согласно “Российским национальным рекомендациям ВНОК и ОССН”,2007г. и классификацией, предложенной ОССН и утвержденной Российским Съездом кардиологов в 2003 г. [23,24]. Степень ожирения определялась по индексу массы тела (ИМТ) по ВОЗ (1997): нормальная масса – 18 – 24,9 кг/м², избыточная масса – 25 – 29,9 кг/м², ожирение I степени – 30 – 34,9 кг/м², II степени – 35 – 39,9 кг/м², III степени – 40 кг/м² и выше. Для диагностики ФК ХСН использовался тест 6-минутной ходьбы.
Все включенные в исследование пациенты были рандомизированы методом последовательных номеров на 2 сопоставимые по возрасту и полу группы по 39 человек. Пациенты контрольной группы получали эналаприл в дозе 10-20 мг/сут и индапамид 2,5 мг/сут, основной группе был добавлен таурин в дозе 1000 мг/сут. Лечение проводилось в течение 12 месяцев, на протяжении которых все участники исследования соблюдали диету и выполняли дозированную физическую нагрузку. Всем больным проводилось антропометрическое обследование, офисное измерение АД, определение липидного и углеводного статуса и ИР исходно и после лечения. Диастолическая функция ЛЖ (ДФЛЖ) оценивалась в импульсном режиме допплер – ЭхоКГ. Определялись и анализировались следующие параметры трансмитрального кровотока: пиковая скорость раннeго диастолического наполнения ЛЖ (пик Е), пиковая скорoсть предсердного диастолического наполнения (пик А), коэффициент E/А и время замедления кровотока раннего диастолического наполнения (DT). Активная релаксация ЛЖ оценивалась по продолжительности фазы изоволюметрического расслабления, то есть измерялось время изоволюметрического расслабления (ВИР) В соответствии с Российскими национальными рекомендациями ВНОК и ОССН по диагностике и лечению ХСН второго пересмотра (2007), диагностировали три типа нарушения ДФЛЖ: замедленная релаксация (ригидный тип). рестриктивный тип, псевдонормальный тип.
Статистическая обработка результатов проводилась с использованием непараметрических критериев Манна-Уитни и Т-критерия Уилкоксона.
Результаты
Показатели, характеризующие клиническое состояние пациентов и тяжесть ХСН, представлены в табл.1. Как видно из таблицы, положительная динамика критериев оценки клинического состояния пациентов и тяжести ХСН наблюдалась в обеих группах. Однако следует отметить, что количественные параметры изменений отличались на фоне различных схем терапии. По всем параметрам различия между группами через 12 месяцев от начала терапии достигли достоверности. Так, в основной группе на фоне приема дибикора через 12 месяцев терапии произошло достоверное уменьшение ФК ХСН (р
Диастолическая дисфункция левого желудочка
Под диастолической дисфункцией подразумевают патологию, которая сопровождается нарушением кровообращения во время расслабления сердца. Подобная проблема диагностируется преимущественно среди женщин престарелого возраста. И чаще встречается именно диастолическая дисфункция левого желудочка.
Что это такое?

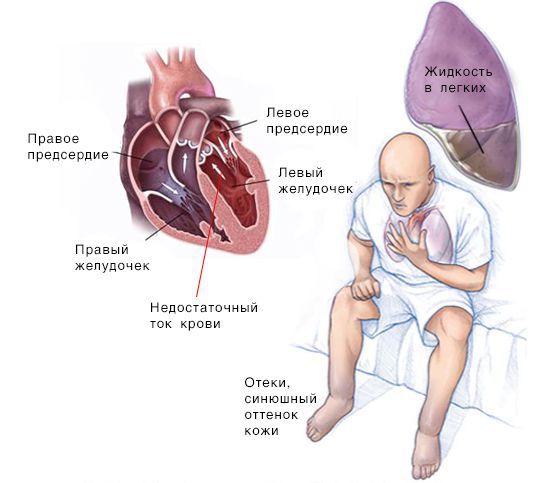
Когда нарушена диастолическая функция левого желудочка, мышечные ткани миокарда утрачивают способность расслабляться в момент диастолы. В результате этого желудочек не получает необходимое количество крови. Чтобы компенсировать ее недостаток, левое предсердие вынуждено усиливать свою работу, пытаясь вобрать в себя больше крови.
Все это негативно сказывается на состоянии предсердия, постепенно приводит к перегрузке, его увеличению в размерах. На фоне систолической дисфункции может произойти застой в венозной системе и легких, что влечет за собой сбои кровоснабжения всех органов человеческого организма. Переход данного патологического состояния в более тяжелую форму способен привести к возникновению сердечной недостаточности хронического характера.
Диастола имеет важное значение, потому что благодаря ей сердечная мышца получает необходимый кислород, который разносится по кровеносной системе через коронарные артерии.
Если она не способна в полной мере выполнять свои задачи, левый желудочек страдает от дефицита кислорода. Это ведет к нарушению обмена в тканях миокарда и ишемии.
Затяжная ишемия губительна по отношению к клеткам, вместо которых образуется соединительная ткань. Такой процесс называют склерозом или фиброзом. Измененная структура тканей становится причиной затрудненного сокращения левого желудочка. В конечном итоге происходит и сбой систолы.
Классификация
Первый вид заболевания – самый распространенный. Он таит в себе серьезную опасность, поскольку на начальной стадии развития протекает практически без каких-либо симптомов. Для него характерно снижение способности перегонять кровь в желудочек из парного кровеносного сосуда легочного ствола. Причиной тому становится недостаточная эластичность стенок миокарда.
Второй вид недуга проявляется на фоне увеличения давления со стороны левого предсердия, что ведет к нарушению функции диастолы. Также его называют псевдонормальным.
Самым тяжелым считается рестриктивный вид патологии, когда существует угроза жизни человека, в связи с серьезными нарушениями в сердце. В подобных ситуациях обычно проводится трансплантация сердца.
Если у человека имеется диастолическая дисфункция левого желудочка по 1 типу, об этом могут свидетельствовать отеки, которые наблюдаются преимущественно вечером. Подобное состояние обусловлено застоем жидкости в организме. Отечность обычно отмечается на нижних конечностях.
При этом пациент может жаловаться на боли в сердце, вызванные ишемией миокарда. Нередко после физической активности появляется одышка. Диастолическая дисфункция левого желудочка 1 типа не должна оставаться без внимания, она требует медикаментозной коррекции.
На начальном этапе развития болезнь может даже не проявляться. При отсутствии должного лечения она будет прогрессировать, в результате чего могут появиться следующие признаки диастолической дисфункции левого желудочка:
Крайне редко у пациентов может отмечаться кашель, который возникает вечером. Его появление указывает на наличие застойных явлений в легких.
Кровоток в сердце проходит 3 этапа:
Речь идет о диастолической дисфункции, когда происходит какой-либо сбой в такой отлаженной системе. Патология данного типа может возникать по причине наличия следующих факторов:
Отклонения в работе сердца провоцируют пагубные привычки в виде курения и употребления алкоголя. Не лучшим образом на состоянии сердечной мышцы сказывается любовь к кофеиносодержащим напиткам.
Как утверждают специалисты в области медицины, основным провоцирующим фактором данного заболевания является ухудшение сокращающей и расслабляющей способности миокарда. Это обычно обусловлено плохой эластичностью его мышечных тканей. Подобное состояние может привести к возникновению ряда болезней, включая инфаркт, гипертрофию миокарда и артериальную гипертонию.
Диастолическая дисфункция также может поражать новорожденных детей. Если у ребенка отмечается усиленное кровоснабжение легких, это может стать причиной того, что:
Такое состояние не считается патологическим, поэтому не требует особого лечения, если возникает у детей сразу после появления на свет. Но если ребенок перенес гипоксию, либо был рожден раньше положенного срока, такая проблема может сохраняться в течение двух недель.
Лечение
Поставить диагноз «диастолическая дисфункция левого желудочка» по 1 типу, 2 или 3, можно только после прохождения пациентом ряда обследований. Для этого необходимо будет сдать общий анализ мочи, биохимию крови. Также может потребоваться проверка работы щитовидной железы, почек, печени.
Самый информативный способ исследования при наличии аномалии сердца – это ЭКГ.
Продолжительность процедуры составляет всего 10 минут. Во время ее проведения на область грудной клетки больного крепятся электроды, которые считывают необходимую информацию. При этом важно, чтобы тело было расслабленным, а дыхание – спокойным. Исследование рекомендуется проводить по прошествии 2-3 часов после еды.

Только после получения результатов комплексного обследования доктор ставит диагноз и определяет дальнейшую тактику лечения. Основные задачи терапии заключаются в следующем:
Для нормализации сердечного ритма используются бета-блокаторы, представленные такими препаратами, как «Конкор» и «Атенололл». Ишемия сердца лечится нитратами. Артериальное давление позволяют привести в норму диуретики типа «Гипотиазида» или «Спиронолактона».
При диастолической дисфункции также показан прием ингибиторов АПФ. Их действие направлено на нормализацию давления. Они обычно назначаются гипертоникам. Ингибиторы, помимо снижения давления, защищают сердце и способствуют расслаблению стенок миокарда. К препаратам этой группы относятся «Каптоприл» и «Фозиноприл».
В профилактических целях врачом может быть рекомендован прием «Аспирина Кардио». С его помощью разжижается кровь, благодаря чему сводятся к минимуму риски закупорки сосудов.
Прогноз
Диастолическая дисфункция левого желудочка по 1 типу, в подавляющем большинстве случаев, имеет благоприятный прогноз, чего нельзя сказать о переходе болезни в рестриктивную форму. Она сопровождается высоким давлением в предсердии и осложняется сопутствующей сердечной недостаточностью. Прогноз в этом случае не всегда утешителен. Чтобы справиться с патологией, может потребоваться трансплантация сердца.
Случаи повторной госпитализации пациентов с диагнозом диастолическая дисфункция составляют 50%. Смертность при такой патологии – 3-7% в год.
Чтобы не допустить развития необратимых процессов, следует повышенное внимание уделять профилактическим мероприятиям. Очень важно правильно питаться, ограничить потребление соли, контролировать прием воды. В рационе должны преобладать свежие овощи, мясо нежирных сортов, крупы и кисломолочные продукты. Блюда будут полезнее, если их готовить на пару или запекать в духовке. Также необходимо полностью отказаться от жареной и острой пищи, алкоголя, курения.
Для подготовки материала использовались следующие источники информации.
Ишемия миокарда и нарушение диастолической функции левого желудочка
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Кафедра кардиологии РМАПО, Москва
В последние годы внимание многих исследователей привлекает возможность изучения функции миокарда в фазу диастолы, т.е. диастолической функции миокарда левого желудочка.
Интерес к данной проблеме основан на том, что в целом ряде исследований продемонстрирована ведущая роль нарушения диастолической функции левого желудочка в развитии сердечной недостаточности при многих заболеваниях. Известно также, что некоторые нарушения ритма сопровождаются явлениями диастолической дисфункции. Все вышесказанное делает проблему изучения процесса расслабления левого желудочка весьма актуальной.
Накопленные на сегодня данные свидетельствуют о том, что диастолическое наполнение левого желудочка определяется многими факторами, среди которых наибольшее значение придают активному расслаблению миокарда левого желудочка в раннюю фазу диастолы, эластическим свойствам самого миокарда, в частности, степени его ригидности, давлению, которое создается в левом предсердии в момент его систолы, состоянию митрального клапана и связанных с ним подклапанных структур [1—4]. При различных заболеваниях сердца патологические изменения самого миокарда левого желудочка могут привести к нарушению диастолической функции левого желудочка.
Принято выделять следующие периоды диастолы: период раннего диастолического наполнения левого желудочка, который состоит из фазы быстрого и медленного наполнения, и период позднего диастолического наполнения левого желудочка, совпадающий с систолой левого предсердия [8,13]. Объем кровотока через митральный клапан и его скорость во время раннего диастолического наполнения определяется активным энергозависимым расслаблением миокарда левого желудочка, жесткостью камеры [2,3] и уровнем давления в левом предсердии в начале диастолы левого желудочка [4,5]. Рядом исследований показано, что расслабление левого желудочка в раннюю диастолу представляет собой активный энергозависимый процесс, управляемый такими основными механизмами, как нагрузка сокращения, расслабления, неоднородность распределения нагрузки [2]. На период раннего диастолического наполнения левого желудочка влияют диастолическая деформация полости желудочка, а также внутрижелудочковое давление в момент открытия митрального клапана [1,2]. Совокупность действия перечисленных факторов создает так называемую присасывающую функцию левого желудочка, которая и определяет перемещение части объема крови из полости левого предсердия в полость левого желудочка. По окончании быстрого наполнения разница в давлении между левыми камерами снижается, наступает фаза медленного наполнения, во время которой градиент между предсердием и желудочком невелик, и кровоток из предсердия в желудочек небольшой. К моменту наступления систолы левого предсердия этот градиент начинает вновь возрастать, что проявляется в повторном ускорении кровотока через митральный клапан [5].
Во время систолы предсердия объем трансмитрального кровотока, поступающий в полость левого желудочка, зависит от давления в левом предсердии во время систолы, от ригидности стенок левого желудочка, конечного диастолического давления в полости желудочка. Дополнительным фактором, влияющим на процесс наполнения, следует считать также вязкость крови [1,2]. В норме объем и скорость кровотока через митральный клапан в период ранней диастолы значительно превышают эти показатели в период систолы предсердий.
Методические вопросы определения диастолической функции
В последние годы с внедрением в широкую практику допплер-кардиографии появилась возможность измерения скоростей трансмитрального кровотока в различные периоды диастолы неинвазивным путем. Следует заметить, что допплерографическое исследование трансмитрального кровотока позволяет надежно верифицировать только фазу раннего быстрого диастолического наполнения и фазу систолы предсердия, поскольку волна L, отражающая медленное диастолическое наполнение, может быть выявлена на допплерограмме только в 25% случаев и к тому же очень вариабельна по величине и продолжительности [1].
При отсутствии нарушений диастолической функции левого желудочка у здоровых лиц молодого и среднего возраста пиковая скорость Е (Еmax) и площадь под кривой Е (интеграл скорости Е, обозначаемый Еi) превышают величину пиковой и интегральной скоростей А (соответственно Аmax и Аi) [1,6—8]. По данным разных авторов, соотношение скоростей периодов раннего и позднего диастолического наполнения левого желудочка колеблется от 1,0 до 2,2 для интегралов скоростей и от 0,9 до 1,7 для пиковых скоростей. Измеряемое при одновременной записи митрального и аортального потоков время изометрического расслабления миокарда левого желудочка также в значительной мере зависит от возраста, наиболее часто оно составляет 74±26 мс [1,2].
В ряде работ показана также взаимосвязь между возрастанием вклада предсердной составляющей диастолического наполнения левого желудочка и возрастом обследуемых, что выражается уменьшением соотношений скоростей периодов раннего и позднего диастолического наполнения за счет возрастания скоростей периода предсердной систолы и уменьшения скоростей периода раннего диастолического наполнения. Следует также отметить, что данные по фазовому анализу диастолы в литературе неполны и неоднородны в терминологическом определении, что требует дальнейшего исследования этого вопроса.
На основании вышеизложенного можно сделать вывод, что в норме диастолическая функция левого желудочка определяется следующими наиболее существенными моментами: диастолической деформацией левого желудочка, давлением в его полости к моменту открытия митрального клапана, ригидностью стенок левого желудочка, сохранностью структур митрального комплекса и реологическими свойствами самой крови.
Нарушение диастолической функции при ишемии миокарда
При наличии хронической ишемии миокарда возрастает жесткость или ригидность его стенок [4,6,9]. В частности, ряд исследователей убедительно показали наличие тесной корреляции между диастолическими свойствами сердца и максимальным потреблением кислорода миокардом в покое и при нагрузке.
На современном уровне разработки этого вопроса патогенетический механизм нарушения диастолического расслабления левого желудочка выглядит следующим образом: недостаточное обеспечение миокарда кислородом приводит к возникновению дефицита макроэргических соединений, что в свою очередь приводит к замедлению процесса раннего диастолического расслабления левого желудочка.
Указанные изменения сказываются на процессе наполнения камеры желудочка в раннюю диастолу: вследствие более медленного, чем обычно, снижения давления в камере левого желудочка, момент, когда уровни давления между желудочком и предсердием сравниваются, достигается позже. Это приводит к увеличению продолжительности периода изометрического расслабления миокарда левого желудочка. После открытия митрального клапана градиент давления между желудочком и предсердием оказывается меньшим, чем в норме, и, следовательно, поток раннего диастолического наполнения уменьшается. Своеобразная компенсация обеспечивается в период систолы предсердия, когда объем крови, необходимый для адекватного наполнения левого желудочка, поступает во время активного сокращения камеры предсердия. Таким образом, предсердный вклад в формирование ударного объема камеры возрастает [1—4, 6, 8, 10]. Вышеуказанные гемодинамические изменения относят к раннему типу нарушения диастолы желудочка, при котором не происходит существенного повышения давления в камере левого предсердия, и, соответственно, изменений гемодинамики малого круга кровообращения и признаков застойной сердечной недостаточности при этом не наблюдается [2,11].
Значительно сложнее выглядит объяснение патогенетических моментов влияния ишемии у больных с нарушением диастолической функции по рестриктивному типу. Для формирования данного вида нарушения диастолы необходимы следующие основные моменты: высокое конечно-диастолическое давление в полости левого желудочка, формируемое значительной жесткостью его миокарда [2,11,12], высокое давление в полости левого предсердия [4,11,13], обеспечивающее адекватное наполнение желудочка в раннюю диастолу, снижение систолической функции левого предсердия. Большинство авторов в этой связи указывают на достаточно редкую встречаемость рестриктивного типа нарушения диастолы у больных ИБС [4 6], поскольку высокая жесткость миокарда чаще связана с его органическим поражением, например, при рестриктивной кардиомиопатии, инфильтративных кардиопатиях [7,8]. Для больных коронарной болезнью сердца характерно наличие очаговой патологии миокарда и формирование высокой его жесткости в связи с длительной, хронической его ишемией и развитием фиброза.
Таким образом, на сегодняшний день достаточно очевидным является факт отрицательного влияния ишемии миокарда на процесс диастолического наполнения левого желудочка. Поэтому целесообразно коснуться также и вопросов диагностики нарушения диастолической функции у рассматриваемой категории больных.
Наряду с инвазивными методами исследования (вентрикулография) и радионуклидными методами (радионуклидная вентрикулография) все большее значение приобретает в последние годы допплер-кардиография [8,11,12]. Общепринятым на сегодня является выделение 2 типов нарушения диастолической функции левого желудочка по данным допплер-кардиографии [8].
1-й тип, при котором в результате нарушения ранней фазы диастолы желудочка уменьшаются скорость и объем кровотока через митральное отверстие в раннюю фазу диастолы (Епик) и увеличиваются объем и скорость кровотока в период предсердной систолы (Апик), при этом отмечается увеличение времени изометрического расслабления миокарда левого желудочка (ВИРМ) и удлинение времени замедления (ВЗ) потока Е.
2-й тип, обозначаемый как псевдонормальный, или рестриктивный, который предполагает наличие значительной ригидности миокарда желудочка, что приводит к повышению диастолического давления в камере желудочка, а затем и в предсердии, причем давление в камере предсердия может значительно превышать давление в полости желудочка к моменту начала диастолы последнего, что обеспечивает наличие значительного градиента давления между камерами в начале диастолы; при этом меняется характер трансмитрального кровотока: увеличивается Епик и уменьшается Апик, укорачиваются и ранее указанные временные интервалы (ВИРМ и ВЗ).
Ряд авторов предлагают разделять нарушения диастолической функции левого желудочка на 3 типа: ранний, псевдонормальный и рестриктивный. Так, Е.Braunwald [2] предлагает дифференцировать псевдонормальный тип нарушения от нормы и рестриктивного типа на основании продолжительности времени замедления пика Е раннего наполнения, который, как известно, укорачивается при псевдонормальном и рестриктивном типах нарушения диастолы. Правомерность такого подхода вызывает сомнения в свете наличия в литературе данных о существенном влиянии на продолжительность временных интервалов диастолы частоты сердечных сокращений в момент исследования.
Другие авторы указывают на возможность дифференциации между псевдонормальным типом нарушения и нормой с помощью оценки потоков в легочных венах. При псевдонормальном типе имеется повышение давления в левом предсердии, что сказывается на характере наполнения левого предсердия [11].
Роль и место цветной допплеровской М-модальной ЭхоКГ в дифференциальной диагностике между вышеуказанными типами наполнения левого желудочка на сегодняшний день не вполне ясны. Ряд авторов считает, что указанная методика помогает отличить псевдонормальный тип наполнения от рестриктивного и нормы [1,2], в то же время остается открытым вопрос о степени и характере влияния на точность измерений в этом режиме таких факторов, как частота сердечных сокращений, вязкость крови, состояние миокарда левого предсердия и др. Думается, что цветное допплеровское картирование в этой ситуации не имеет принципиальных преимуществ перед обычной допплерограммой, потому что при М-модальной развертке цветного допплеровского изображения также проводится измерение временных интервалов, описанных выше, а значит, сохраняется и влияние всех ранее указанных ограничивающих факторов.
Важной представляется возможность изучения сегментарной диастолической функции при помощи метода допплеровской визуализации тканей с М-модальной разверткой [8,11]. Применение этого метода дает возможность оценить не только общее состояние диастолической функции, но и характер расслабления отдельных сегментов, что особенно важно при оценке влияния ишемии миокарда на эти параметры в покое и при проведении нагрузочных проб.
Клиническое значение диастолической дисфункции левого желудочка и возможности медикаментозного воздействия
ИБС является одной из самых частых причин возникновения диастолической дисфункции левого желудочка [1,4,6] вследствие нарушения раннего диастолического расслабления на фоне острой или хронической ишемии, повышения жесткости миокарда в месте постинфарктного рубца и формирования соединительной ткани на фоне хронической ишемии. Кроме того, повышение жесткости гипертрофированного интактного миокарда у больных ИБС может быть связано с ишемией на фоне коронарной недостаточности вследствие стеноза артерии, кровоснабжающей этот участок миокарда, и в результате относительной коронарной недостаточности, которая часто имеет место при гипертрофии. Известно также, что диастолическая дисфункция может возникать и без нарушения систолической функции левого желудочка [2,14]. Но нарушение диастолической функции даже в изолированном виде приводит к существенному ухудшению центральной гемодинамики и может способствовать возникновению или прогрессированию существовавшей ранее систолической сердечной недостаточности [11,14].
Прогноз у больных ишемической болезнью сердца, у которых имеется диастолическая дисфункция, более неблагоприятный [1,2,14], что делает актуальной проблему ее медикаментозной коррекции.
Вопросам медикаментозной терапии нарушения диастолической функции у больных ИБС посвящено мало работ. Кроме того, на сегодняшний день нет ни одного крупного исследования по этому вопросу. В научной литературе за последние годы опубликованы в основном экспериментальные работы на животных, посвященные изучению влияния антиангинальных препаратов различных групп, а также ингибиторов АПФ (эналаприл – SOLVD – investigators) на процесс диастолического расслабления миокарда [15,16,17,18]. По результатам этих исследований наибольшая эффективность отмечена при применении антагонистов кальция, b-адреноблокаторов, ингибиторов АПФ. Так, например, E.Omerovic и соавт. (1999) продемонстрировали положительный эффект селективного b1-блокатора метопролола на состояние систолической и диастолической функции левого желудочка при инфаркте миокарда.
Существуют и отдельные клинические работы, посвященные этому вопросу. A.Tsoukas и соавт. (1999), изучая влияние комбинированной терапии диуретиками и ингибиторами АПФ на состояние центральной гемодинамики у больных с рестриктивным типом трансмитрального кровотока и сниженной фракцией выброса левого желудочка (
Литература
1. Барац С.С., Закроева А.Г. Диастолическая дисфункция сердца по показателям трансмитрального кровотока и потока в легочных венах: дискуссионные вопросы патогенеза, терминологии и классификации. Кардиология 1998; 5: 69—76.
2. E. Braunwald ed., Heart disease, 5th Ed., W.B. Saunders company 1997.
3. Caash W.H., Apstein C-S., Levine H.J. et al. Diastolic properties of the left ventricle. In.- The LV-basic and clinical aspects. Ed. H.J.Levine. Boston. 1985; 143.
4. Choong C.Y. Left ventricle: diastolic function — its principles and evaluation.-Principles and practice of echocardiography. Ed. A.Weiman. Philadelphia. Lea and Febiger. 1994; 1721—9.
5. Bonow P.O., Frederick 1.М., Bacliarach S.J. et al. Atrial systole and left ventricular filling in Hypertrophic cardiomyopathy: effect of verapamil. Amer J Cardiology 1983; 51: 1386.
6. Бащинский С.Е., Осипов М.А. Диагностическая ценность изучения диастолической функции левого желудочка при проведении стресс-допплер-эхокардиографии у больных ишемической болезнью сердца. Кардиология 1991; 9: 28—31.
7. Bessen M., Gardin J-N. Evaluation of left ventricular diastolic function. Cardiol.Clinics 1990; 18: 315—32.
8. Feigenbaum H. Echocardiography.- 5th Edition.- Lea & Ebiger.-Philadelphia. 1994; 166—72,189—91.
9. Желнов В.В., Павлова И.Ф., Симонов В.И., Батищев А.А. Диастолическая функция левого желудочка у больных ишемической болезнью сердца. Кардиология 1993; 5: 12—4.
10. Добротворская Т.Е., Супрун Е.К., Шуков А.А. Влияние эналаприла на систолическую и диастолическую функцию левого желудочка при застойной сердечной недостаточности. Кардиология 1994; 12: 106—12.
11. Christopher P., Appleton M.D. Doppler assesement of left venricular diastolic function: the refinements continue. JACC 1993; 21(7): 1697—700.
12. Cecconi M.,Manfrin M., Zanoli R. et al. Doppler echocardiographic evaluation of left ventricular end-diastolic pressure in patients with coronary artery disease. J Am Soc Echocardiol 1996; 110: 241—50.
13. Castello D., Vaughn M., Dressler F.A. et al. Relation between pulmonary venous flow and pulmonary weige pressure: influence of cardiac output. Amer Heart J 1995; 130: P.127—31.
14. Vasan R.S., Benjamin E.J., Levy D. Congestive heart failure with normal left ventricular systolic function. Arch Intern Med. 1996: 156: 146—57.
15. Barbier Р., Tamborini G., Alioto G., Pepi M. Acute filling pattern changes of the failing left ventricle after captopril as related to ventricular structure. Cardiology 1996; 87: 153—60.
16. Goldstein S. Beta-blockers: insights into the mechanism of action in patients with left ventricular dysfunction. J Heart Failure. 1996: 13: 115.
17. Poultur H., Rousseau M.F., van Eyll C., et. al. Effects with long-term enalapril therapy on left ventricular diastolic properties in patients with depressed ejection fraction. SOLVD Investigators. Circulation 1993 Aug 88: 2 481-91
18. Sasaki M.,Oki T., Inchi A., Tabata T., et. al. Relationship between the angiotensin converting enzyme gene polymorphism and the effects of enalapril on left ventricular hypertrophy and impaired diastolic filling in essential hypertension: M-mode and pulsed Doppler echocardiographic studies. J Hypertens 1996 Dec 14: 12 1403-8
Диастолическая дисфункция левого желудочка
Врач ультразвуковой диагностики
Палий К.А.
Под диастолической дисфункцией понимают неспособность левого желудочка наполняться и поддерживать ударный объём без компенсаторного увеличения предсердного давления наполнения.
В значительной степени она определяется способностью миокарда к расслаблению и податливостью (жесткостью) стенки. Нарушение диастолической функции левого желудочка может наблюдаться как в комбинации со снижением систолической функции левого желудочка, так и изолированно (например, при заболеваниях, сопровождающихся гипертрофией левого желудочка). Усиленный фиброз миокарда, развивающийся при старении, также может причиной значительной диастолической дисфункцией.
Для понимания подходов к оценке диастолического наполнения левого желудочка требуется знание четырех фаз диастолы.
Вышеописанные фазы диастолы могут быть легко прослежены с помощью импульсно – волновой допплерографии, визуализирующей изменения скорости трансмитрального потока крови.
Типичная кривая скорости трансмитрального потока имеет два пика: первый из них (пик Е) соответствует фазе быстрого раннего наполнения желудочков, тогда как второй относительно низкоскоростной пик (А) имеет более низкую амплитуду и совпадает по времени с сокращением предсердия. Для оценки диастолической функции левого желудочка предложено использовать большое число характеристик пиков Е и А, однако на практике рутинно используются лишь некоторые из них: максимальная скорость пика Е, максимальная скорость пика А, соотношение максимальных скоростей Е/А и время замедления пика Е.
По мере нарушения диастолической функции левого желудочка конечное диастолическое давление в его полости начинает расти, что, в свою очередь, вызывает рост давления в левом предсердии. В результате характер потока крови между левым предсердием и левым желудочком изменяется, что может быть зафиксировано с помощью импульсно –волновой допплерографии входящего трансмитрального потока.
Известно 4 основных типа диастолического наполнения левого желудочка:
Факторы, влияющие на изменение трансмитрального кровотока, можно разделить на физиологические и патологические. В свою очередь патологические подразделяются на внесердечные и сердечные.
Среди физиологических причин выделяются такие как возраст, частота сердечных сокращений, положение пациента, дыхание, преднагрузка (например, изменение профиля трансмитрального кровотока при нагрузочных пробах).
Внесердечные факторы, влияющие на трансмитральный кровоток: ожирение, диабет, почечная недостаточность, синдром ночного апноэ.
Сердечные причины: артериальная гипертензия (АГ), ишемическая болезнь сердца (ИБС), кардиомиопатии, хроническая сердечная недостаточность (ХСН), пороки сердца, миокардиты, заболевания перикарда и др.
Таким образом, эхокардиография является единственным доступным неинвазивным методом оценки диастолической функции левого желудочка, которая имеет важное клиническое значение.
Диастолическая дисфункция рассматривается как дебют в нарушении функции желудочков при различных заболеваниях сердца.
Степень диастолической дисфункции может указывать на тяжесть заболевания у больных с одинаковой степенью систолической дисфункции.
Выраженность диастолической дисфункции может выступать в качестве объективного маркера эффективности проводимого лечения или течения заболевания.
Райдинг Э. Эхокардиография. Практическое руководство/ Элисдэйр Райдинг; пер. с англ. – 4 –е изд. – М.: МЕДпресс-информ, 2016. – 280с.
Рыбакова М. К. Практическое руководство по ультразвуковой диагностике. Эхокардиография / М. К. Рыбакова и др. – М.: Издательский дом Видар-М. 2008. – 512 с.
Диастолическая сердечная недостаточность и жесткость сосудов
Профессор Драпкина О.М.: – Спасибо большое. Уважаемые коллеги, я сегодня говорила о фиброзе миокарда, и, в принципе, говоря о фиброзе миокарда, так или иначе касаешься диастолической сердечной недостаточности. Мы в клинике и на кафедре занимаемся этой проблемой, соответственно, сейчас тоже есть определенные возможности поделиться тем опытом, который мы накопили.
Мы говорим о диастолической сердечной недостаточности, мы говорим об артериальной гипертензии и говорим, что все-таки нарушенная диастола – это участь пациентов с высоким риском артериальной гипертензии. Но когда высок риск артериальной гипертензии по SCORE, мы знаем, что это и выраженное поражение органов-мишеней и более трех факторов риска или, например, метаболический синдром, когда есть другие факторы риска (сегодня Сергей Руджерович рассказывал, и мы вместе вспоминали исследование «Юпитер», где в качестве маркера у здоровых людей было повышение высокочувствительного C-реактивного белка).
Таким образом, возникает вопрос. Мы все время говорим: «Пациенты к нам приходят с инфарктом миокарда, потому что мы неправильно лечили артериальную гипертензию». А если мы правильно лечили артериальную гипертензию? Тогда получится гипертрофия миокарда и, соответственно, повышение жесткости. Так что же получается, что хроническая сердечная недостаточность с сохраненной фракцией выброса – это правильное лечение артериальной гипертензии и что другого пути нет?
Конечно, это не так. Но тем не менее этим слайдом мне бы хотелось привлечь внимание к такому постулату: отсрочить инфаркт миокарда у пациента с артериальной гипертензией – это не единственная наша задача. Спектр наших задач гораздо больше, в том числе предотвратить вот эту ступень, когда пациент перешагивает от просто гипертоника к гипертонику с хронической сердечной недостаточностью, как правило с сохраненной фракцией выброса.
Поэтому еще раз несколько слов о терминологии. Речь пойдет о сердечной недостаточности с сохраненной фракцией выброса. В принципе, это и есть правильный термин, но мы, медицинское сообщество, разрешаем друг другу называть эту сердечную недостаточность диастолической сердечной недостаточностью – наверное, просто для сокращения.
Эпидемиология известна. Есть немного разные данные – европейские и наши. По данным исследования ЭПОХА, более 70 % пациентов с сердечной недостаточностью имеют сохраненную фракцию выброса. Конечно, это удел пожилых, поскольку мы все боремся за то, что население у нас становится старше, мы все боремся за продолжительность жизни. Это приведет к тому, что пациентов с диастолической сердечной недостаточностью тоже будет больше, и нам их надо будет долгие годы каким-то образом вести.
Вот, на мой взгляд, интересные данные. Ежегодная смертность пациентов с диастолической сердечной недостаточностью, она действительно несколько ниже. Но когда посмотрели на смертность через три года, то она практически выравнивается. Но, самое главное, статистика говорит, что среди больных с хронической сердечной недостаточностью с фракцией выброса более 50 % за три года в живых остается менее 60 %, значит 40 % – погибает.
Но вот, я бы сказала, шокирующие меня данные. Если прогноз на фоне лечения при сердечной недостаточности с сохраненной фракцией выброса улучшается (и мы здесь видим диапазон с 1987 года, когда мы в основном говорили о кардиоренальной теории хронической сердечной недостаточности), то, обратите внимание, уважаемые коллеги, ничего не происходит с улучшением прогноза пациентов с сохраненной фракцией выброса – как 60 % их умирало через три года, собственно говоря, после постановки диагноза, так все и остается. Это поднимает вопрос о том, что мы, наверное, пока не знаем точно, как лечить эту форму хронической сердечной недостаточности.
Ну, и очень коротко я хотела бы напомнить те основные знания, которые мы получаем из курса физиологии на третьем курсе, так называемом экваторе (студенты говорят «экватор»; третий курс прошел – значит прошел половину обучения в институте). Вот эта кривая «давление-объем в левом желудочке», и как раз изменение этой кривой характеризует основные изменения, которые возникают у пациентов с жестким миокардом и сначала с диастолической дисфункцией, а затем – с диастолической сердечной недостаточностью.
Итак, окончание диастолы как бы знаменует фазу изоволюмического сокращения. Мы видим, что здесь давление в левом желудочке стремительно нарастает без изменения его объема. Открывается аортальный клапан и происходит та самая систола, или фаза изгнания. Как раз в тени этой систолы всегда была диастола, поскольку мы оценивали работу сердца именно по тому, как оно сокращается, по сократительной функции.
Затем период систолы закрывается, закрывается, естественно, аортальный клапан, и происходит как раз та самая интересная на сегодняшний момент, на момент сегодняшнего моего повествования, стадия – это диастола. Первый период, он как раз характеризуется стадией изоволюмического расслабления (мы видим, что она очень похожа на стадию изоволюмического сокращения), то есть резкое снижение давления в левом желудочке, открывается митральный клапан, и наконец происходит стадия наполнения. Надо понимать, что эта стадия – это достаточно энергоемкий процесс, поэтому для того, чтобы диастола была совершенной, нужно достаточное количество макроэргов.
Ну, и закрывается митральный клапан, и мы видим (там, где точка, которая показывает закрытие митрального клапана), что окончание диастолы происходит на таком положительном конечном диастолическом давлении. Так вот, если левый желудочек жесткий, то этот небольшой подъем будет более крутым, и давление, которое будет в левом желудочке, оно будет выше.
График двумерный, поэтому здесь невозможно – я во всяком случае не смогла – показать время, так называемое «тау», изоволюмического расслабления. Это очень важный показатель, и мы к нему вернемся чуть ниже.
Таким образом, мы можем суммировать те факторы, которые влияют на диастолу. Суммировать мы их можем, разбив на две, на мой взгляд, абсолютно неравнозначные, но достаточно важные группы. Первая – это, конечно, работа желудочка, это раннее диастолическое наполнение желудочка. И как раз такие факторы, как: эластический возврат крови в левый желудочек, сократительная функция левого желудочка, жесткость левого желудочка в диастолу, свойства легочных вен, площадь отверстия митрального клапана, – и дают 80-типроцентный вклад в полноценную диастолу.
Но есть еще маленький вклад, и тем не менее о нем тоже не стоит забывать, особенно, когда к нам приходит, например, пациент с нарушениями ритма, и хроническая сердечная недостаточность переходит к черте декомпенсированной. Это вклад предсердия. И здесь очень важны: интервал PQ, сократительная функция самого предсердия (сейчас есть методы, которые оценивают эту сократительную функцию, они не инвазивные – эхокардиографические), частота сердечных сокращений (понятно, чем реже сердце бьется, тем лучше диастола) и активность симпатической нервной системы.
Таким образом, портрет типичного пациента с артериальной гипертензией и с диастолической сердечной недостаточностью – это пожилая женщина (чаще это женщина, хотя, конечно, это может быть и мужчина) с длительным анамнезом артериальной гипертензии, все-таки плохо леченой; с букетом другой патологии, который тоже вносит вклад в возможные процессы фиброзов в сердце таких пациентов: это сахарный диабет, это ишемическая болезнь сердца, это суправентрикулярное нарушение ритма, дисфункция почек, которую мы как раз определяем по скорости клубочковой фильтрации, и с фиброзом сосудов.
Ключевые различия есть, и мы их можем обнаружить уже на этапе знакомства с пациентом и на этапе его обследования. Глухие тоны сердца характерны для систолической сердечной недостаточности со сниженной фракцией выброса. При сохраненной фракции выброса тоны могут быть вполне приличные, и даже первый тон может быть сохранен.
Чаще всего мы слышим и в том и в другом случае ритм галопа, и как раз если мы говорим о систолической сердечной недостаточности, то она себя проявляет появлением протодиастолического ритма галопа – за счет S3, дополнительного тона, третьего тона. А, наконец, диастолическая сердечная недостаточность, где больший вклад предсердий, измученных высоким конечным диастолическим давлением в левом желудочке, – это S4.
Диастолическая сердечная недостаточность иногда быстро прогрессирует до оттека легких. И вот тоже удивительные данные. Дмитрий Александрович, я хочу с вами их обсудить. Оказывается (попалась мне такая статья), когда… Пациенты с отеком легких, совершенно клинически оправданный отек легких, поступают в отделение интенсивной терапии, и им всем измерили фракцию выброса левого желудочка. Потом купировали отек легких и опять измерили фракцию выброса левого желудочка. Так вот, никакой закономерности не было. Казалось бы, купировали отек легких – фракция выброса должна повыситься, или поступили с отеком легких – фракция выброса должна быть низкой. Были пациент с высокой фракцией выброса во время кульминации отека легких, и наоборот.
Как вы думаете, как нам, клиницистам, это оценивать, ведь мы так часто уповаем на этот параметр – фракцию выброса?
Профессор Затейщиков Д.А.: – Ну, как говорится, тем хуже для фракции выброса. На самом деле, уже давно многие говорят, что фракция выброса – это, так скажем, не очень хороший параметр. И, очевидно, с появлением новых неинвазивных методик – томографии, магнитно-резонансной томографии – мы получим в руки более точный способ оценки. И, возможно, то, что мы сегодня принимаем за эту самую диастолическую дисфункцию, частично перейдет все-таки в другой разряд, в разряд систолической. Трудно сказать.
Но в любом случае, на мой взгляд, это еще раз показывает, что это не единственный параметр: систола – не только систола, но и что-то еще.
Профессор Драпкина О.М.: – И все-таки клиника, клиническая картина – это то, что должно определять в основном наше отношение к этому больному и к его прогнозу.
Вернемся к слайдам. Таким образом, споры есть, они не закончены. Один это синдром, в котором спровоцированная диастола является как бы предтечей сниженной фракции выброса, или это два синдрома? Есть и сторонники, есть и противники различных теорий. Честно говоря, я стою на позиции того, что это все-таки два разных синдрома. Потому что даже портрет этих сердец, который мы видим при патологоанатомическом вскрытии, он настолько разный, что возникает сразу вопрос, как можно такие разные сердца лечить одинаковыми подходами? Ну, это вопрос, наверное, пока вечный, ответа на него нет.
Тем не менее мы таких пациентов должны лечить, мы должны диагностировать сердечную недостаточность с сохраненной фракцией выброса. На помощь, как всегда, приходят алгоритмы.
Алгоритм Европейского общества кардиологов тоже во главу угла ставит клиническую картину хронической сердечной недостаточности. Но переведя на рельсы нашей ежедневной практики, это тучная пациентка, которая пришла с одышкой. Затем нормальная или лишь незначительно сниженная систолическая функция. Опять переводим на наши реалии, это женщина, пришедшая с одышкой, нами прослушанная, осмотренная, мы видим, что она тучная, мы видим, что есть мелкопузырчатые хрипы в легких.
Мы ее отправляем для уточнения диагноза на эхокардиографическое исследование и с удивлением видим, что фракция выброса нормальная. Это не повод отправлять эту пациентку к пульмонологу, это повод сделать такой пациентке как минимум тест шестиминутной ходьбы. И мы увидим, что она может пройти не те 450 метров, которые не относят ее к пациентке с сердечной недостаточностью.
Затем, действительно, большое внимание уделяется биомаркерам хронической сердечной недостаточности, в частности натрийуретическому пептиду и его концевому фрагменту. Если он больше 220 и у нас имеются доплеровские признаки, то есть мы делаем обычное доплеровское исследование и видим при оценке потоков, что отношение E к A меньше 0,5, или всего лишь левое предсердие большое, или у пациента есть фибрилляция предсердий, – то мы можем сказать, что перед нами пациент с диастолической сердечной недостаточностью.
Но, на самом деле, трудностей больше, чем каких-то обоснованных фактов, поскольку ни один из эхо-кардиографических критериев не обладает сегодня достаточной точностью. Мы говорим, что тканевой доплер – очень хорош, и вот это отношение E/E ’ – наиболее хорошо, но тоже не идеально характеризует диастолу. Малодоступно провести (как раз то, о чем мы сейчас говорили) МРТ и различные инвазивные исследования гемодинамики. Ну и, на мой взгляд, не определены точные пороговые значения различных биологических маркеров сердечной недостаточности.
Отсюда возникает вопрос: может быть, нам стоит поискать возможные механизмы развития диастолы на периферии? Почему? Во-первых, при диастолической сердечной недостаточности возникают и определенные моменты жесткости аорты, а ведь аорта – это второе сердце, если она эластична. Если происходит повышение жесткости вообще сосудов, то вот эти отраженные волны (мы чуть ниже сейчас о них скажем), которые собираются на периферии, идут к центру, к сердцу. Идут они, получается, как раз в момент систолы, приходят чуть позже, чем должны были прийти, и сталкиваются с вновь формирующейся пульсовой волной.
Опять вопрос: на периферии ли начинается диастолическая сердечная недостаточность? Мы знаем, что сосуды при артериальной гипертензии – и виновники, и жертва. Потому что само высокое давление действует на сосуды, и в то же время жесткость сосудов, по другим причинам спазм может привести к высокому артериальному давлению.
Если говорить об основных механизмах, то, наверное, основным механизмом, который виновен в развитии диастолической сердечной недостаточности, служит как раз повышение преднагрузки ввиду жесткости периферических сосудов. Увеличивается, как я уже сказала, скорость распространение пульсовых волн, повышается преднагрузка на левый желудочек и повышается центральное пульсовое давление. Вот сейчас центральному пульсовому давлению, или давлению в аорте, и вариабельности давления как раз отдают наибольшее значение в прогнозе гипертоников.
Как это происходит? Представим наши сосуды. В принципе, это трубки. Они эластичные. И если они эластичные, как показано на первом рисунке, на выброс потока крови – большого потока крови, поскольку кровь распространяется с высокой скоростью… Эластичный сосуд как бы демпфирует эту волну, то есть он немножко расширяется, а потом приходит в норму, и мы видим такую схематичную пульсовую волну, которая показана под эластичной аортальной капиллярной трубкой.
Если сосуд жесткий, то он не может демпфировать волну, он не может немножко расслабиться и затем снова сократиться. И это приводит к так называемому феномену аугментации пульсовых волн.
Вот, уважаемые коллеги, мы можем на этой схеме рассмотреть этот феномен. Серой линией показана пульсовая волна, которая отражает выброс крови из левого желудочка в аорту. Пунктирной линией, которая смещена чуть вправо, изображена отраженная волна, которая идет уже от периферии, от наших сосудов, которые обладают демпфирующими способностями, к центру. И когда наслаиваются эти две волны друг на друга, происходит наличие волны типа «С», или пульсовая волна типа «С», которой характеризуются все здоровые люди.
Сейчас стрелками будет показано то, что происходит у гипертоников, что происходит при жесткой аорте. Итак, этот график смещается влево, этот график смещается вверх, и происходит формирование так называемой волны типа «А» или «В», которая характеризует увеличение преднагрузки на миокард левого желудочка, и снижение диастолического артериального давления.
Таким образом, анализ этой проблематики, на мой взгляд, дает возможность дать схему в помощь практикующему врачу. Повышение жесткости сосудов приводит к повышению центрального систолического давления в аорте и снижению диастолического, отсюда пульсовое давление – увеличивается. Повышенное систолическое давление в аорте приводит к повышению преднагрузки на левый желудочек. Гипертрофия и сама преднагрузка на левый желудочек и нарушение релаксации приводят к субэндокардиальной ишемии. Низкое диастолическое давление в аорте приводит к снижению коронарной перфузии, поскольку коронарная артерия наполняется именно во время диастолы. Вот это диастолическое давление не очень низкое тоже важно. Исследование аорты подтвердило, что снижать диастолическое давление ниже 70 для сердечнососудистых катастроф плохо. Присоединяющийся миокардиальный фиброз приводит к диастолической дисфункции.
Мы решили провести пилотное исследование, для того чтобы: оценить степень повреждения эндотелия и сосудов разного калибра у пациентов с диастолической сердечной недостаточностью; сравнить различные методы оценки эндотелиальной функции – фотоплетизмографический и с помощью АнгиоСкана; и посмотреть, что же происходит на фоне терапии, основанной на разных классах препаратов – ингибиторов АПФ и блокаторов кальциевых каналов.
Не забыли мы обратить внимание и на биологические маркеры. Наряду с хорошо известным N-концевым прогормоном мозгового натрийуретического пептида мы посмотрели у пациентов с диастолической сердечной недостаточностью и уровень галектина-3. Это маркер, или такой биологический субстрат, который в большей степени отвечает за фиброз – всего: печени, сосудов, сердца и так далее.
Представлен дизайн исследования. Пациенты – высокого риска с сохраненной фракцией выброса. Всеми возможными методами мы анализируем эндотелиальную функцию, рандомизируем пациентов на группу лечения на основе блокаторов кальциевых каналов и на основе ингибиторов АПФ (в качестве ингибитора был выбран амприлан). Наблюдаем пациентов в течение 3-5 недель в стационаре и затем повторяем те же самые исследования.
Уважаемые коллеги, я не буду останавливаться на общих характеристиках групп пациентов, лишь скажу, что они были сопоставимые по возрасту, по индексу массы тела, по различным клиническим характеристикам.
Первый день исследования, или старт исследования, был для нас крайне важен, поскольку мы определяли все те показатели, которые можно посмотреть при контурном анализе пульсовой волны: и продолжительность систолы, и возраст сосудистой стенки, и индекс аугментации, индекс жесткости. Кроме того, в этот же день мы делали окклюзионную пробу, как бы подтверждали друг другом – и фотоплетизмографическим методом и по данным УЗИ.
Конечно, выполнение вот этого показало нам, что с помощью УЗИ смотреть эндотелиальную функцию и окклюзионную пробу крайне сложно: пять минут сидеть в определенном положении, на пять минут пережать артерию, 300 мм ртутного столба накачать… Поэтому, конечно, фотоплетизмографический метод, он нас покорил именно простотой.
Вот так приблизительно выглядела волна типа «С» при нормальных сосудах.
Результаты. Первый вывод, который мы сделали: у всех пациентов с диастолической сердечной недостаточностью есть изменения пульсовой волны. Регистрируются волны типа «В» и «А», которые характеризуются как раз высокой амплитудой и большим размахом между систолой и диастолой.
Результаты контурного анализа пульсовой волны до начала терапии. Мы видим, что они не различаются, наши пациенты, ни по индексу жесткости, ни по индексу отражения, ни по давлению в центральном сосуде.
Что оказалось на фоне терапии? Хорошо и то и другое. То есть чем ниже мы снижаем давление, тем лучше для сосуда нашего гипертоника. Но тем не менее на индекс жесткости чуть большее значение оказывал амприлан. И на давление в аорте тоже чуть большее значение оказывал амприлан.
Результаты пробы с реактивной гиперемией, это окклюзионная проба. Тоже мы видим, что и та и другая группа продемонстрировали хорошие результаты. Тем не менее несколько большее влияние ингибиторов АПФ на сосудистую стенку тоже было доказано в данном исследовании.
Средний уровень гормонов NT-proBNP составил 153, средний уровень галектина-3 – 0.98.
Оценка функции сосудов эндотелия происходила вот таким образом. Мы видим, что после окклюзионной пробы, которая длилась пять минут… нам бы хотелось увидеть прирост диаметра в плечевой артерии, а внизу как раз показано то, что происходит с пульсовыми волнами.
Мы нашли, что есть связь между уровнем NT-proBNP и очень многими параметрами, как то: тестом 6-тиминутной ходьбы, оценкой пациента по Шкале оценки клинического состояния, которую мы используем у пациентов с сердечной недостаточностью.
Не было выявлено корреляции между уровнем NT-proBNP и фракцией выброса левого желудочка и параметрами диастолической дисфункции.
Что касается галектина-3, то оказалось, что, один раз повысившись, галектин-3 уже не менялся. Что, в общем-то, согласуется с данными литературы. И поэтому мы предлагаем именно совместное применение галектина-3 и натрийуретического пептида, это в большей степени может быть оценено нами как прогноз течения заболевания.
Вот это комбинированное применение. В первой графе – значение, во второй графе – интерпретация. И риск неблагоприятного исхода, мы видим, наиболее высокий, когда есть высокий уровень галектина-3 и натрийуретических пептидов.
Ну и наконец, клинический пример. Пожилая пациентка, ей больше 60 лет. Мы видим, что ее сосуды жесткие. И индекс жесткости, и индекс реактивности, и индекс аугментации высоки. На фоне применения амприлана мы видим изменение пульсовой волны, это видно, так сказать, визуально. Кроме того, это, конечно, видно и по тем расчетным индексам, которые есть. Обратите внимание, индекс реактивности снизился с 24 практически до 8.9, и насколько снизилось центральное давление!
Это, естественно, нашло свое отражение в улучшении эндотелиальной функции. То есть прирост… верхняя картинка по сравнению с нижней картинкой… мы видим увеличение амплитуды пульсовых волн в 1.3 раза.
Таким образом, уважаемые коллеги, анализ данной проблемы дает возможность сделать пока такие предварительные выводы. Наверное, правомочно высказывание о том, что диастолическая сердечная недостаточность начинается с периферии, во всяком случае жесткость сосудов определенный вклад в изменение диастолы вносит.
Второй вывод: биологические маркеры хронической сердечной недостаточности опять достойны дальнейшего изучения, и новый маркер галектин-3 для прогноза пациентов с диастолической сердечной недостаточностью, наверное, будет очень многообещающим.
Ну и наконец, наше исследование продемонстрировало то, что снизьте давление чем-нибудь, снизьте до нормальных значений, до тех значений, которые нам дают рекомендации. Но все же применение ингибиторов АПФ, и в частности амприлана, в нашем исследовании позволяло говорить о лучшем влиянии на функцию эндотелия и о лучшем влиянии на функцию резистентности сосудов у пациентов с артериальной гипертензией и диастолической сердечной недостаточностью. Спасибо за внимание.
Что такое сердечная недостаточность? Причины возникновения, диагностику и методы лечения разберем в статье доктора Гринберг Марины Витальевны, кардиолога со стажем в 33 года.
Определение болезни. Причины заболевания
Сердечная недостаточность — синдром, при котором нарушена способность сердца перекачивать кровь. Заболевание проявляется одышкой, повышенной утомляемостю, хрипами в лёгких, отёками голеней и стоп.
Выделяют острую и хроническую формы:
Распространённость
В России хроническая сердечная недостаточность чаще регистрируется у женщин. Возможно, это связано с более пристальным их вниманием к своему здоровью.
Причины хронической сердечной недостаточности
Сердечная недостаточность не является самостоятельным заболеванием, это результат развития многих сердечно-сосудистых болезней. Она возникает в основном из-за атеросклероза, ишемической болезни сердца и гипертонии.
Другие факторы риска:
Причины острой сердечной недостаточности
Острая сердечная недостаточность может возникнуть как обострение хронической формы заболевания, а также на фоне инфаркта миокарда, разрыва хорд митрального клапана и других тяжёлых состояний.
Симптомы сердечной недостаточности
В начале заболевания симптомы сердечной недостаточности отмечаются исключительно при физических нагрузках.
Реакция со стороны сердца. Из-за нарушения кровообращения появляется одышка — частое и глубокое дыхание, не соответствующее уровню нагрузки. При повышении давления в лёгочных сосудах возникает кашель, иногда с кровью. При физической активности и употреблении большого количества пищи может усилиться сердцебиение. Пациент жалуется на чрезмерную утомляемость и слабость. С течением времени симптомы нарастают и теперь беспокоят не только при физической активности, но и в состоянии покоя.
Реакции со стороны печени. Сердечную недостаточность сопровождает застой крови в сосудах печени, из-за чего возникает чувство тяжести и боли под правым ребром.
Патогенез сердечной недостаточности
Сердце, подобно насосу, нагнетает кровь в сосуды и перекачивает её из одной части тела в другую:
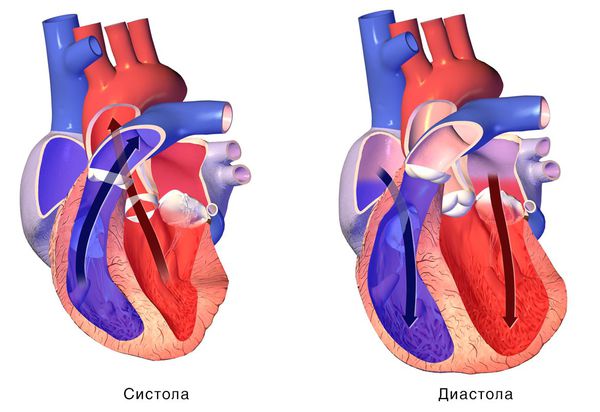
При сокращении сердечной мышцы, называемой систолой, кровь выталкивается из сердца. При расслаблении сердечной мышцы, или диастоле, она возвращается в сердце.
Если расслабляющая или сократительная способность сердца уменьшается, то развивается сердечная недостаточность. Это происходит, как правило, из-за слабости сердечной мышцы и/или потери её эластичности. В результате сердце качает недостаточно крови. Она может также накапливаться в тканях и вызывать застой.
Скопление крови, поступающей в левую часть сердца, приводит к застою в лёгких и затруднению дыхания. Скопление крови, приходящей в правую половину сердца, вызывает застой жидкости в других частях тела, например в печени и ногах.
При сердечной недостаточности, как правило, поражены обе половины сердца. Но одна из них может страдать от заболевания сильнее, чем другая. В таких случаях выделяют правостороннюю и левостороннюю сердечную недостаточность.
Классификация и стадии развития сердечной недостаточности
Выделяют следующие формы сердечной недостаточности:
Недостаточность левого желудочка сердца
Левосторонняя сердечная недостаточность бывает левожелудочковой и левопредсердной. Для неё свойственно снижение выброса левого желудочка и/или застой крови на пути к левым отделам сердца, то есть в венах малого круга кровообращения.
Симптомы при левосторонней сердечной недостаточности (СН): слабость, головокружения, бледность кожи, одышка и быстрая утомляемость.
Недостаточность правого желудочка сердца
Симптомы при правосторонней СН: периферические отёки, цианоз и скопление жидкости в брюшной полости.
Изолированная сердечная недостаточность встречается редко и кратковременно. В последующем нарушение затрагивает все камеры сердца и развиваются типичные симптомы болезни.
Систолическая и дистолическая сердечная недостаточность
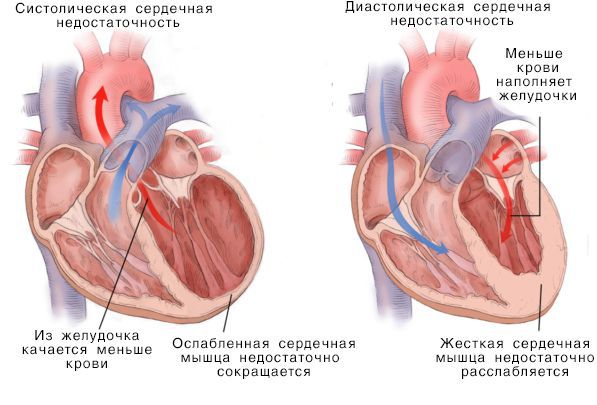
Нарушение насосной функции левого желудочка может быть вызвано систолической и диастолической дисфункцией. Систолическая дисфункция более распространена и связана со снижением сократимости миокарда — мышечной ткани сердца. В большинстве случаев причиной систолической хронической сердечной недостаточности становится ИБС, сочетаясь с артериальной гипертензией и сахарным диабетом.
Помимо привычных терминов “диастолическая сердечная недостаточность” и «систолическая сердечная недостаточность», используются названия “сердечная недостаточность с сохраненной фракцией выброса ЛЖ (СНСФВ)” и «сердечная недостаточность со сниженной фракцией выброса (СН СФВ)».
Острая и хроническая сердечная недостаточность
Симптомы при хронической и острой СН различаются лишь интенсивностью и сроками развития.
Стадии развития сердечной недостаточности
Современная классификация хронической сердечной недостаточности объединяет модифицированную классификацию Российской кардиологический школы по стадиям, которые могут только ухудшаться (В. Х. Василенко, М. Д. Стражеско, 1935 г.), и международную классификацию по функциональным классам, которые определяются способностью больного переносить физическую нагрузку (тест с 6-ти минутной ходьбой) и могут ухудшаться или улучшаться (Нью-Йоркская классификация кардиологов). [2]
Классификация ХСН Российского общества специалистов по сердечной недостаточности
| ФК | ФК ХСН (могут изменяться на фоне лечения) | НК | Стадии ХСН (не меняются на фоне лечения) |
|---|---|---|---|
| 1ФК | Ограничений физической активности нет; повышенная нагрузка сопровождается одышкой и/или медленным восстановлением | 1 ст | Скрытая сердечная недостаточность |
| 11ФК | Незначительное ограничение физической активности: утомляемость, одышка, сердцебиение | 11а ст | Умеренно выраженные нарушения гемодинамики в одном из кругов кровообращения |
| 111ФК | Заметное ограничение физической активности: по сравнению с привычными нагрузками сопровождается симптомами | 11б ст | Выраженные нарушения гемодинамики в обоих кругах кровообращения |
| 1У ФК | Симптомы СН присутствуют в покое и усиливаются при минимальной физической активности | 111 ст | Выраженные нарушения гемодинамики и необратимые структурные изменения в органах-мишенях. Финальная стадия поражения сердца и других органов |
Классификация сердечной недостаточности Нью-Йоркской кардиологической ассоциации
Класс I. Заболевание сердца не ограничивает физическую активность. Обычная нагрузка не вызывает усталость, сердцебиение и одышку.
Класс II. Болезнь незначительно ограничивает физическую активность. В покое симптомов нет. Обычная физическая нагрузка вызывает усталость, сердцебиение или одышку.
Класс III. Физическая активность значительно ограничена. В покое симптомов нет. Небольшая физическая активность вызывает усталость, сердцебиение или одышку.
Осложнения сердечной недостаточности
Осложнения хронической сердечной недостаточности:
Диагностика сердечной недостаточности
Лечение сердечной недостаточности
Этапы оказания помощи пациенту с острой сердечной недостаточностью
При сердечной недостаточности не стоит заниматься самолечением. Своевременное обращение к врачу поможет избежать негативных последствий.
Цели терапии
Правильно подобранная медикаментозная терапия способна улучшить качество жизни и значительно продлить её продолжительность у больных даже с тяжелыми формами хронической сердечной недостаточности (по данным литературы — до 10 лет). [4]
Стандарты диагностики и лечения сердечной недостаточности, которые утверждены Минздравом, предписывают определенные исследования и манипуляции для пациентов, обратившихся с симптомами, напоминающими сердечную недостаточность; там же есть список лекарственных средств, но без указания, кто и как должен это лечить. Терапевты в поликлиниках не имеют соответствующей подготовки и не могут грамотно оказывать помощь этим больным.
Нужна ли госпитализация при сердечной недостаточности
Причиной госпитализации является декомпенсация — выраженное нарастание отёков и одышки, тахикардия и нарушение сердечного ритма.
В России сегодня почти нет специализированных отделений, где принимали бы больных с этим заболеванием, проводили бы дифференциальную диагностику и подбирали лечение (в Западной Европе введена врачебная специальность «специалист по сердечной недостаточности»). Кто реально занимается индивидуальным подбором лекарственных препаратов для больного? Терапевт, который назначает преимущественно фуросемид (мочегонный препарат), выводящий калий, снижающий давление и ускоряющий наступление летального исхода?
Кардиологические отделения районных больниц, куда с огромным трудом можно госпитализировать тяжелого больного на очень короткий срок, где опять же назначат фуросемид и лишь выведут избыточно накопленную жидкость, а через 1-2 месяца опять наступит ухудшение (правило 4-х госпитализаций: время между каждой последующей госпитализацией сокращается, состояние ухудшается, после 4-й госпитализации больных не остается!) В то время как современные препараты в постепенно повышающихся дозах могут обеспечить гемодинамическую разгрузку сердца, улучшить состояние пациента, уменьшить потребность в госпитализациях, продлить жизнь больного.
При хронической сердечной недостаточности показано сохранять режим питания и нагрузок и непрерывно принимать лекарственные препараты. Одно-двухдневный пропуск может ухудшить состояние, симптомы могут вернуться, и станет неизбежной госпитализация. Хроническая сердечная недостаточность часто встречается у людей пожилого возраста и сочетается с энцефалопатией, и помощь близких может значительно повысить их приверженность к лечению. Нужно обучение правильному питанию, режиму дня, контролю за задержкой жидкости (за рубежом эти функции выполняет специально обученная медсестра, которая осуществляет патронаж больного).
Острая или тяжелая форма хронической сердечной недостаточности подразумевает постельный режим, полный психический и физический покой. В остальных случаях показаны умеренные нагрузки, которые не сказываются на самочувствии. Следует потреблять не более 500-600 мл жидкости в сутки, соли – 1-2 г. Назначается витаминизированное, легкоусвояемое диетическое питание, олигомерные питательные смеси.
Медикаментозное лечение
Если развивается приступ острой сердечной недостаточности левого желудочка (отёк легких), больной подлежит госпитализации, где ему оказывают неотложную помощь. Лечение заключается в введении диуретиков, нитроглицерина, препаратов, которые повышают сердечный выброс (добутамин, дофамин), проводятся ингаляции O2.
Если развивается асцит, показано проведение пункционного удаления жидкости из брюшной полости, при возникновении гидроторакса — плевральная пункция.
Поскольку сердечная недостаточность сопровождается выраженной гипоксией тканей, пациентам показана кислородная терапия. [10]
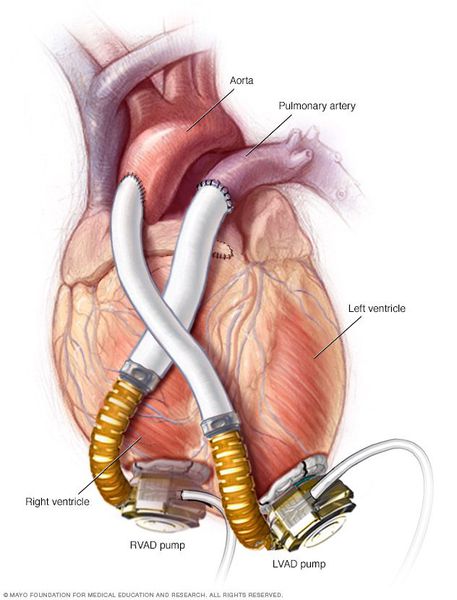
Хирургические и механические методы лечения
Питание и режим дня при сердечной недостаточности
Пациенту с сердечной недостаточностью следует уменьшить употребление жидкости до одного литра в сутки. Также следует исключить солёности, пряности и копчёности.
При заболевании нужно больше двигаться и выполнять посильные нагрузки: чаще ходить пешком и заниматься лёгкой гимнастикой.
Прогноз. Профилактика
До 1990-х годов 60 − 70 % пациентов с хронической сердечной недостаточностью умирали в течение пяти лет. Современная терапия позволила уменьшить смертность: сейчас в России при этой болезни она составляет 6 % в год, а среди пациентов с клинически выраженными формами — 12 % [16]
Отдалённый прогноз зависит от степени тяжести заболевания, образа жизни, эффективности подобранного лечения и приверженности ему, сопутствующих заболеваний и т. д.
Успешное лечение на ранних стадиях может полностью компенсировать состояние пациентов; при третьей стадии сердечной недостаточности прогноз самый печальный.
Чтобы сердечная недостаточность не прогрессировала, нужно соблюдать рекомендованный режим физической активности, регулярно и без пропусков принимать назначенные лекарства и регулярно наблюдаться у кардиолога.
Диастолическая функция сердца при дисплазии соединительной ткани

В статье приведен анализ литературных данных по вопросам диагностики состояния диастолической функции у лиц молодого возраста с признаками дисплазии соединительной ткани. Обсуждается проблема диагностики доклинической диастолической дисфункции левого желу
The article analyzes literature data on the diagnostics of diastolic function condition in young patients with signs of connective tissue dysplasia. The problem of diagnostics of pre-clinical left-ventricular diastolic dysfunction was discussed, as well as possible influence of peculiarities of connective-tissue cardiac frame in patients with connective tissue dysplasia on functional condition of auricles and left-ventricular diastolic function.
Состояние диастолической функции сердца является значимым предиктором кардиоваскулярных событий и сердечной недостаточности [1–4]. Несмотря на то, что в последнее время был сделан большой шаг вперед в эхокардиографической оценке диастолической функции левого желудочка [5], разграничение нормальной и нарушенной диастолической функции остается сложной задачей [6].
Изменения диастолической функции сердца появляются рано. Доклиническая диастолическая дисфункция (pre-clinical diastolic dysfunction) левого желудочка (ЛЖ) в широком смысле проявляется признаками нарушения диастолической функции в отсутствие проявлений застойной сердечной недостаточности и с нормальной систолической функцией. Эта стадия нарушения диастолической функции ЛЖ не до конца понятна, но, несомненно, имеет определенное клиническое значение. В нескольких оригинальных исследованиях было показано, что доклиническая диастолическая дисфункция ЛЖ является распространенным явлением и с течением времени прогрессирует до симптомной сердечной недостаточности. Показано, что пациенты с ишемической болезнью сердца, артериальной гипертензией или сахарным диабетом имеют значительно более высокий риск прогрессирования доклинической диастолической дисфункции ЛЖ до сердечной недостаточности и смерти. С учетом этих результатов и высокой распространенности сердечной недостаточности понимание доклинической диастолической дисфункции необходимо для снижения заболеваемости и смертности от сердечной недостаточности [7].
Есть мнение, что парадигма, в которой диастолическая дисфункция ЛЖ проходит в своем развитии стадии от нарушения релаксации до повышенной жесткости желудочков, не подходит для применения у детей, и с этим мнением нельзя не согласиться относительно лиц молодого возраста [8].
Выявление ранних признаков нарушения диастолической функции, безусловно, должно основываться на комплексной оценке большого количества эхокардиографических параметров: размера и объемов левого предсердия (ЛП), допплеровских показателей трансмитрального потока и потока легочных вен, данных тканевой допплерографии и двумерного отслеживания пятен серой шкалы (speckle tracking imaging или 2D-strain) [5, 9]. Улучшить оценку диастолы может ее рассмотрение в единстве с систолической функцией [8]. Однако у каждого из многочисленных параметров эхокардиографической оценки диастолической функции ЛЖ имеются ограничения использования, а методика оценки требует дальнейшего развития перед тем, как быть использованной в ежедневной практике у детей и лиц молодого возраста.
Размеры тела в значительной степени определяют размеры ЛП. Для оценки этого влияния размер ЛП должен быть индексирован к размерам тела: для этой цели используют площадь поверхности тела [16, 17]. Но интерпретация полученных изменений нормированного объема ЛП может быть затруднена конституциональными особенностями телосложения, что справедливо не только для лиц с ожирением, но и с недостаточной массой тела, что наблюдается при дисплазии соединительной ткани (ДСТ).
Гендерные различия в размере ЛП почти полностью обусловлены различиями в размере тела. У лиц без сердечно-сосудистых заболеваний индекс объема ЛП не зависит от возраста [16, 18].
Принципиальная роль левого предсердия — регуляция наполнения ЛЖ и эффективности работы сердечно-сосудистой системы за счет функционирования ЛП в качестве резервуара для крови, поступающей из легочных вен во время систолы желудочков, проводника, или шунта, крови (в том числе напрямую из легочных вен в ЛЖ) во время ранней диастолы и помпы в позднюю диастолу [19].
Состояние резервуарной функции ЛП зависит от его способности к растяжению, что связано как с упругими свойствами миокарда предсердий, так и с состоянием соединительнотканного каркаса сердца. У лиц с ДСТ соединительнотканный каркас сердца более растяжим из-за структурно-функциональных особенностей соединительной ткани. В результате генетических мутаций, приводящих к ДСТ, цепи коллагена и эластина формируются неправильно и образованные ими структуры не выдерживают должных механических нагрузок. Также резервуарная функция левого предсердия зависит от величины смещения основания сердца к верхушке во время систолы желудочков и конечно-систолического объема ЛЖ, то есть сократительной функции ЛЖ [20, 21]. В результате этого движения основания сердца резко снижается давление в ЛП и возникает «присасывающий» эффект для потока легочных вен.
Функция ЛП как проводника крови в ЛЖ в фазу ранней диастолы зависит не только от растяжения ЛП, но и от растяжения и расслабления ЛЖ.
Эффективность сократительной функции левого предсердия определяется величиной и продолжительностью сокращения ЛП и зависит от величины венозного возврата (преднагрузка), конечно-диастолического давления в ЛЖ (постнагрузки) и его систолического резерва [21].
У здоровых лиц есть определенное соотношение этих фракций кровотока — 40%, 35% и 25% для фракции резервуара, шунта и помпы соответственно [19]. При изменении условий наполнения ЛЖ происходит коррекция этой пропорции для поддержания ударного объема ЛЖ [18]. В частности, при замедлении расслабления желудочков уменьшается вклад фракции пассивного опорожнения ЛП из-за снижения градиента давления между ЛП и ЛЖ в раннюю диастолу, но компенсаторно увеличивается его резервуарная и контрактильная фракции. Увеличение фракции пассивного опорожнения ЛП, когда ЛП в основном работает в качестве кондуита крови в ЛЖ, наблюдается при прогрессировании диастолической дисфункции до псевдонормального и рестриктивного паттернов. При этом резервуарная и контрактильная функции ЛП значительно нарушены.
В ряде работ, посвященных изучению диастолической функции на фоне ДСТ, выявлено уменьшение соотношения Е/А трансмитрального кровотока, увеличение времени замедления кровотока в раннюю диастолу (DT) и времени изоволюмического расслабления ЛЖ (IVRT) [22–26], что связывалось с недостатком макроэргов, принимающих непосредственное участие в процессе расслабления ЛЖ. Изменения диастолической функции ЛЖ на ранних стадиях сердечно-сосудистых заболеваний традиционно связывают также с замедлением расслабления ЛЖ, тем более что именно этот показатель способен относительно быстро меняться с течением времени, а упругие свойства соединительнотканного каркаса сердца считаются константой. При ДСТ характеристики соединительной ткани и связанной с ее свойствами способности растягиваться и обеспечивать, в частности, резервуарную функцию ЛП, значительно отличаются от таковой у лиц без ДСТ, что может быть связано как с чрезмерной деградацией коллагена соединительной ткани, так и с синтезом неполноценных волокон коллагена, не способных выполнять в полной мере свои физиологические функции.
Единичные работы были посвящены структурной неполноценности и снижению регенеративной способности соединительной ткани у лиц с ДСТ при присоединении кардиологической патологии, в частности инфаркта миокарда. При этом наличие ДСТ влияет на характер течения, частоту и тяжесть осложнений при инфаркте миокарда. Есть данные о более частом развитии дезадаптивного варианта постинфарктного ремоделирования сердца на фоне ДСТ, характеризующегося преобладанием процессов дилатации полости ЛЖ со снижением его сократительной способности над процессами гипертрофии миокарда, а также большей частотой развития суправентрикулярных и желудочковых нарушений ритма [27, 28]. Также есть данные о наличии грубых нарушений диастолической функции ЛЖ после перенесенного инфаркта миокарда, более выраженных на фоне ДСТ, что объяснялось наследственными особенностями организации соединительнотканного каркаса сердца в формировании патофизиологических механизмов адаптации при постинфарктном кардиосклерозе [29], то есть изменениями процессов репаративного фиброза и качеством образующейся рубцовой ткани. Детальный анализ биохимических маркеров постинфарктного репаративного фиброза показал, что при развитии острой сердечной недостаточности усилен обмен коллагена, увеличено содержание сульфатированных гликозаминогликанов при активации матриксной металлопротеиназы-2 и тканевого ингибитора матриксных металлопротеиназ-1. При нарушении ритма отмечено усиление обмена коллагена, протеогликанов и снижение содержания фибронектина на фоне повышенного уровня тканевого ингибитора матриксных металлопротеиназ-1. При аневризме сердца ускорена деградация коллагена на фоне низкого содержания сульфатированных гликозаминогликанов, матриксной металлопротеиназы-9, но высокого содержания тканевого ингибитора матриксных металлопротеиназ-1 [30].
При изучении вопросов регуляции процессов ремоделирования соединительной ткани выявлено наличие изменения процессов аутоиммунитета к коллагенам разных типов и цитокинового профиля у пациентов с пролапсом митрального клапана [31], анализ экспрессии молекул адгезии у молодых пациентов с ДСТ позволяет не только установить нарушения в клеточной регуляции соединительнотканного гомеостаза, но и определить особенности дисбаланса адгезивных молекул в зависимости от характера диспластического фенотипа [32].
Таким образом, лица с ДСТ, по всей видимости, имеют более высокий риск развития сердечной недостаточности, особенно при присоединении сердечно-сосудистых заболеваний, хотя имеют минимальные структурные изменения (изменения геометрии ЛЖ, особенности структуры и функции клапанного аппарата сердца, малые аномалии развития) без признаков сердечной недостаточности, что требует пристального внимания и дальнейших исследований. С учетом влияния состояния диастолической функции ЛЖ на прогноз и частого вовлечения сердечно-сосудистой системы у лиц с ДСТ необходимо мониторировать состояние диастолической функции ЛЖ, особенно при присоединении кардиологической патологии, ожидая ее ухудшение. Эхокардиография может предоставить ценные сведения для понимания происходящих в сердце процессов, однако возможности подходов к лечению выявленных функциональных и структурных изменений до сих пор весьма ограничены [33]. Изучение метаболизма компонентов внеклеточного матрикса миокарда и диастолической функции сердца необходимо для поиска мишеней фармакологического воздействия и разработки своевременной стратегии лечения.
Литература
ФГБОУ ВО ОмГМУ Минздрава России, Омск
Диастолическая функция сердца при дисплазии соединительной ткани/ Ю. В. Терещенко, Г. И. Нечаева, В. В. Потапов, М. И. Шупина, Е. Н. Логинова, Е. В. Надей, Т. П. Кабаненко
Для цитирования: Лечащий врач № 7/2019; Номера страниц в выпуске: 46-48
Теги: сердце, структурные изменения, функциональные изменения, миокард
Проблемы диастолической дисфункции левого желудочка: определение, патофизиология, диагностика
ГОУ ВПО Первый Московский государственный университет им. И.М. Сеченова Минздравсоцразвития РФ, 119992 Москва, ул. Трубецкая, 8, стр. 2
Благодаря успехам в диагностике, диастолическая дисфункция левого желудочка, ассоциируемая с неблагоприятным прогнозом, часто диагностируется в популяции людей старше 45 лет. В литературе развернута широкая дискуссия по основным теориям определения, физиологии, патофизиологии, диагностики данного состояния. Наиболее значимые концепции приведены в настоящем обзоре.
Нарушение диастолической функции левого желудочка (ЛЖ) привлекает все большее внимание клиницистов как один из ключевых механизмов развития сердечно-сосудистой патологии. Диастолическая дисфункция (ДД) ЛЖ, как правило, является неотъемлемым спутником таких заболеваний, как ишемическая болезнь сердца (ИБС), сердечная недостаточность (СН) [1—3] (рис. 1).
Рисунок 1. Место диастолической дисфункции ЛЖ в континууме прогрессирования ишемической болезни сердца.
Материалы рисунка L J.Shaw и соавт. [4] модифицированы.
Проявления ДД неспецифичны, зачастую бессимптомны. Так, благодаря эпидемиологическим исследованиям стало известно, что у лиц старше 45 лет ДД ЛЖ определяется в 25—30% случаев [3—5]. Многие врачи до сих пор считают, что данная бессимптомная патология является возрастной нормой и не придают ей значения. Однако умеренная и выраженная ДД ЛЖ имеет независимое прогностичес-кое неблагоприятное значение; ее сохранение после терапевтических вмешательств также указывает на худший прогноз [6].
Проблемы патологии диастолы связаны с трудностью методологии диагностики: определения, понимания физиологии, патофизиологии [3, 7, 8]. В обзоре рассматривается ряд концепций, связанных с диастологией, широко обсуждаемых в настоящее время.
Физиология и патофизиология диастолы
Физиология диастолы. Диастола охватывает при традиционном понимании изоволюмическое расслабление и фазы наполнения сердечного цикла (3-я или 4-я фаза в зависимости от концепции авторов), имеет активные и пассивные компоненты [9, 10]. Диастолическая функция является способностью, позволяющей желудочку наполняться при низком предсердном давлении [11].
Диастолическое расслабление ЛЖ, как правило, характеризуют по показателям инвазивной катетеризации, так как это наиболее точный количественный метод [12]. Однако данная инвазивная диагностика имеет общеизвестные значимые ограничения при использовании в повседневной клинической практике.
Исследование выполняется с помощью тройного сенсорного микроманометрового катетера, введенного в полость ЛЖ. С его помощью определяют и записывают параметры: 1) в левом предсердии (ЛП); 2) в базальной части ЛЖ; 3) в апикальной части ЛЖ. Используется общепринятая методология J.L. Weiss и соавт. [13]. Катетерное исследование ЛЖ является «золотым стандартом» в диагностике диастолы. График отношения давление—объем (dP/dV) в настоящее время все чаще определяется одновременным измерением давления с помощью микроманометра и объема с использованием эхокардиографии (ЭхоКГ) [14—17], а не только контрастной вентрикулографии, как ранее.
Инвазивными показателями диастолической функции ЛЖ, которые чаще используются, являются следующие:
1) конечное диастолическое давление (КДД) ЛЖ [18, 19] (исследователи используют минимальное диастолическое давление ЛЖ или среднее диастолическое давление ЛЖ, или соотношение давления и времени (dp/dt);
2) время постоянного расслабления,τ[16, 17];
3) константа жесткости ЛЖ (в) и функциональная камерная жесткость ЛЖ (b) (рис. 2).
Рисунок 2. График отношения давление/объем (dP/dV).
Характеризует общие пассивные механические свойства камеры левого желудочка (ЛЖ). По характеру наклона кривой линии судят о жесткости желудочка. Податливость или эластичность ЛЖ обратно пропорциональна жесткости. Выделяют две величины βи b, которые наиболее значимы в определении жесткости ЛЖ. Константа жесткости ЛЖ, Р (линия 1), оценивается по наклону уравнения линейной регрессии, связанного с координатами конечнодиастолического давления и объема для каждого состояния гемодинамики. Функциональная камерная жесткость ЛЖ, β(линия 2), для каждого отдельного гемодинамического состояния является линией наклона графика dP/dV от минимального диастолического давления до конечно-диастолического давления [11, 13, 14, 27, 28]. Имеется множество нелинейных уравнений, используемых для представления графика отношения dP/dV, но нет единственного принятого уравнения [22, 29]. Материалы рисунка M.S. Maurer и соавт. [5] модифицированы.
Время постоянного расслабления определяется по участку изоволюмического состояния ЛЖ — графика измерения внутрижелудочкового давления ЛЖ [9, 10, 17, 21, 22].
Пассивные механические свойства камер (пассивный компонент диастолы) определяются как степень миоклеточной гипертрофии (масса миокарда), свойства цитоскелетного (степень фиброза) [5] и внеклеточного матрикса (инфильтрация различными патологическими веществами) [12], геометрии камер сердца (ремоделирование), состояние перикарда. Вклад каждого по отдельности фактора в общие пассивные механические свойства камеры сердца трудно оценить количественно. Интегральный показатель определяется по графику отношения давление—объем (конечное диастолическое давление [КДД]), объем — отношение [КДД ОО] или графику давление— объем [dP/dV]) (см. рис. 2) [3, 5, 24—26].
Публикации в СМИ
Недостаточность сердечная хроническая диастолическая
Диастолическая сердечная недостаточность — нарушение расслабления и наполнения левого желудочка, обусловленное его гипертрофией, фиброзом или инфильтрацией и приводящее к увеличению в нём конечного диастолического давления и проявлениям сердечной недостаточности.
Статистические данные. Диастолическая сердечная недостаточность составляет 20–30% от всех случаев сердечной недостаточности. Она может сочетаться с систолической сердечной недостаточностью.
Этиология • ИБС (с ИМ или без него) • Гипертрофическая кардиомиопатия • Амилоидоз сердца • Артериальная гипертензия • Клапанные пороки сердца • СД • Констриктивный перикардит.
Патогенез. В результате снижения податливости и нарушения наполнения левого желудочка в нём повышается конечное диастолическое давление, что приводит к снижению сердечного выброса. Происходит увеличение давления в левом предсердии, малом круге кровообращения. В последующем может возникать правожелудочковая сердечная недостаточность.
Клинические проявления и диагностика. Обязательными признаками диастолической сердечной недостаточности считают следующие.
• Признаки хронической сердечной недостаточности — симптомы увеличения давления в левом предсердии: одышку при физической нагрузке, ортопноэ, ритм галопа, хрипы в лёгких, отёк лёгких.
• Признаки нормальной или слегка сниженной сократительной функции левого желудочка — определяют по данным ЭхоКГ •• Фракция выброса не менее 45% •• Индекс внутреннего конечного диастолического размера левого желудочка менее 3,2 см/м2 поверхности тела •• Индекс конечного диастолического объёма левого желудочка менее 102 мл/м2 поверхности тела.
• Признаки патологического наполнения и расслабления левого желудочка, ненормального диастолического растяжения левого желудочка — определяют по данным ЭхоКГ (иногда катетеризации полостей сердца) •• Время изоволюмического расслабления левого желудочка более 92 мс (для возраста менее 30 лет), более 100 мс (для возраста 30–50 лет), более 105 мс (для возраста старше 50 лет) •• Отношение амплитуды пика Е к амплитуде пика А менее 1 (для возраста менее 50 лет), менее 0,5 (для возраста более 50 лет) •• Конечное диастолическое давление левого желудочка более 16 мм рт.ст. или среднее давление заклинивания лёгочных капилляров более 12 мм рт.ст. (по данным катетеризации полостей сердца).
Лечение
• Проводят немедикаментозные мероприятия, аналогичные таковым при хронической систолической сердечной недостаточности, включающие ограничение потребления поваренной соли, жидкости, оптимизацию физической активности.
• Из ЛС используют следующие группы •• -Адреноблокаторы — снижают ЧСС и удлиняют диастолу •• Блокаторы медленных кальциевых каналов (верапамил, дилтиазем) оказывают действие, подобное действию -адреноблокаторов •• Нитраты применяют при наличии ИБС, но использовать их необходимо осторожно из-за возможного избыточного уменьшения преднагрузки, что может вызывать артериальную гипотензию •• Диуретики необходимо применять осторожно из-за избыточного уменьшения преднагрузки и уменьшения сердечного выброса •• Ингибиторы АПФ уменьшают гипертрофию левого желудочка и улучшают расслабление левого желудочка •• Сердечные гликозиды при диастолической сердечной недостаточности противопоказаны, поскольку они могут способствовать дальнейшему ухудшению диастолического расслабления левого желудочка. Положительные инотропные средства (в т.ч. сердечные гликозиды) назначают только при сопутствующей систолической сердечной недостаточности.
Прогноз. Смертность от диастолической сердечной недостаточности составляет 8% в год.
МКБ-10 • I50 Сердечная недостаточность
Код вставки на сайт
Недостаточность сердечная хроническая диастолическая
Диастолическая сердечная недостаточность — нарушение расслабления и наполнения левого желудочка, обусловленное его гипертрофией, фиброзом или инфильтрацией и приводящее к увеличению в нём конечного диастолического давления и проявлениям сердечной недостаточности.
Статистические данные. Диастолическая сердечная недостаточность составляет 20–30% от всех случаев сердечной недостаточности. Она может сочетаться с систолической сердечной недостаточностью.
Этиология • ИБС (с ИМ или без него) • Гипертрофическая кардиомиопатия • Амилоидоз сердца • Артериальная гипертензия • Клапанные пороки сердца • СД • Констриктивный перикардит.
Патогенез. В результате снижения податливости и нарушения наполнения левого желудочка в нём повышается конечное диастолическое давление, что приводит к снижению сердечного выброса. Происходит увеличение давления в левом предсердии, малом круге кровообращения. В последующем может возникать правожелудочковая сердечная недостаточность.
Клинические проявления и диагностика. Обязательными признаками диастолической сердечной недостаточности считают следующие.
• Признаки хронической сердечной недостаточности — симптомы увеличения давления в левом предсердии: одышку при физической нагрузке, ортопноэ, ритм галопа, хрипы в лёгких, отёк лёгких.
• Признаки нормальной или слегка сниженной сократительной функции левого желудочка — определяют по данным ЭхоКГ •• Фракция выброса не менее 45% •• Индекс внутреннего конечного диастолического размера левого желудочка менее 3,2 см/м2 поверхности тела •• Индекс конечного диастолического объёма левого желудочка менее 102 мл/м2 поверхности тела.
• Признаки патологического наполнения и расслабления левого желудочка, ненормального диастолического растяжения левого желудочка — определяют по данным ЭхоКГ (иногда катетеризации полостей сердца) •• Время изоволюмического расслабления левого желудочка более 92 мс (для возраста менее 30 лет), более 100 мс (для возраста 30–50 лет), более 105 мс (для возраста старше 50 лет) •• Отношение амплитуды пика Е к амплитуде пика А менее 1 (для возраста менее 50 лет), менее 0,5 (для возраста более 50 лет) •• Конечное диастолическое давление левого желудочка более 16 мм рт.ст. или среднее давление заклинивания лёгочных капилляров более 12 мм рт.ст. (по данным катетеризации полостей сердца).
Лечение
• Проводят немедикаментозные мероприятия, аналогичные таковым при хронической систолической сердечной недостаточности, включающие ограничение потребления поваренной соли, жидкости, оптимизацию физической активности.
• Из ЛС используют следующие группы •• -Адреноблокаторы — снижают ЧСС и удлиняют диастолу •• Блокаторы медленных кальциевых каналов (верапамил, дилтиазем) оказывают действие, подобное действию -адреноблокаторов •• Нитраты применяют при наличии ИБС, но использовать их необходимо осторожно из-за возможного избыточного уменьшения преднагрузки, что может вызывать артериальную гипотензию •• Диуретики необходимо применять осторожно из-за избыточного уменьшения преднагрузки и уменьшения сердечного выброса •• Ингибиторы АПФ уменьшают гипертрофию левого желудочка и улучшают расслабление левого желудочка •• Сердечные гликозиды при диастолической сердечной недостаточности противопоказаны, поскольку они могут способствовать дальнейшему ухудшению диастолического расслабления левого желудочка. Положительные инотропные средства (в т.ч. сердечные гликозиды) назначают только при сопутствующей систолической сердечной недостаточности.
Прогноз. Смертность от диастолической сердечной недостаточности составляет 8% в год.
МКБ-10 • I50 Сердечная недостаточность
Современные подходы к лечению больных гипертрофической кардиомиопатией
Полувековая история изучения проблемы гипертрофической кардиомиопатии (ГКМП) отражает значительную эволюцию знаний в области этиологии, патогенеза, диагностики, клинического течения, прогноза и вариантов лечения этого заболевания. За указанный период тол
Полувековая история изучения проблемы гипертрофической кардиомиопатии (ГКМП) отражает значительную эволюцию знаний в области этиологии, патогенеза, диагностики, клинического течения, прогноза и вариантов лечения этого заболевания. За указанный период только в англоязычных изданиях опубликованы более 1000 крупных научных работ. ГКМП — одна из основных и, вероятно, наиболее распространенных форм кардиомиопатий, заболеваний миокарда, сопровождающихся его дисфункцией (Report of the 1995 WHO/ISFC Task Force on the Definition and Classification of Cardiomyopathy) [1].
В 2003 г. создан Международный комитет (ACC/ESC), объединивший американских и европейских экспертов по ГКМП, и опубликовано сообщение, суммировавшее основные положения, включая стратегию лечебных мероприятий [2].
Определение заболевания носит описательный характер. Так, по современным представлениям, ГКМП является преимущественно генетически обусловленным заболеванием мышцы сердца, характеризующимся комплексом специфических морфофункциональных изменений и неуклонно прогрессирующим течением с высокой угрозой развития тяжелых, жизнеугрожающих аритмий и внезапной смерти (ВС). ГКМП характеризуется массивной гипертрофией миокарда левого и/или реже правого желудочка, чаще асимметричного характера за счет утолщения межжелудочковой перегородки (МЖП), нередко с развитием обструкции (систолического градиента давления) выходного тракта ЛЖ при отсутствии видимых причин (артериальная гипертония, пороки и специфические заболевания сердца). Основным методом диагностики остается эхокардиографическое исследование. В зависимости от наличия или отсутствия градиента систолического давления в полости ЛЖ, ГКМП разделяют на обструктивную и необструктивную, что имеет важное практическое значение при выборе тактики лечения. При этом различают 3 гемодинамических варианта обструктивной ГКМП: с субаортальной обструкцией в покое (так называемой базальной обструкцией); с лабильной обструкцией, характеризующейся значительными спонтанными колебаниями внутрижелудочкового градиента давления без видимой причины; с латентной обструкцией, которая вызывается только при нагрузке и провокационных фармакологических пробах (в частности, вдыханием амилнитрита, при приеме нитратов или внутривенном введении изопротеренола).
Типичными являются морфологические изменения: аномалия архитектоники сократительных элементов миокарда (гипертрофия и дезориентация мышечных волокон), развитие фибротических изменений мышцы сердца, патология мелких интрамиокардиальных сосудов [3, 4].
В настоящее время наблюдается повсеместный рост числа зарегистрированных случаев этой патологии как за счет внедрения в практику современных методов диагностики, так и, вероятно, в связи с истинным увеличением числа больных ГКМП [8, 9]. Согласно данным последних исследований, распространенность заболевания в общей популяции является более высокой, чем считалось ранее, и составляет 0,2% [10, 11]. ГКМП может диагностироваться в любом возрасте, от первых дней до последней декады жизни, однако преимущественно заболевание выявляется у лиц молодого трудоспособного возраста [12, 13]. Ежегодная смертность больных ГКМП колеблется в пределах от 1 до 6%: у взрослых больных составляет 1–3% [14, 15], а в детском и подростковом возрасте у лиц с высоким риском ВС — 4–6% [16, 17].
Общепризнанна концепция о преимущественно наследственной природе ГКМП [18, 19]. В литературе широкое распространение получил термин «семейная гипертрофическая кардиомиопатия». К настоящему времени установлено, что более половины всех случаев заболевания являются наследуемыми [20, 21], при этом основной тип наследования — аутосомно-доминантный. Оставшиеся приходятся на так называемую спорадическую форму; в этом случае у пациента нет родственников, болеющих ГКМП или имеющих гипертрофию миокарда. Считается, что большинство, если не все случаи спорадической ГКМП, также имеют генетическую причину, т. е. вызваны случайными мутациями.
ГКМП — это генетически гетерогенное заболевание, причиной которого являются более 200 описанных мутаций нескольких генов, кодирующих белки миофибриллярного аппарата [2, 22]. К настоящему времени известны 10 белковых компонентов сердечного саркомера, выполняющих контрактильную, структурную или регуляторную функции, дефекты которых наблюдаются при ГКМП. Причем в каждом гене множество мутаций могут становиться причиной заболевания (полигенное мультиаллельное заболевание).
Наличие той или иной ассоциированной с ГКМП мутации признается «золотым» стандартом диагностики заболевания. При этом описанные генетические дефекты характеризуются разной степенью пенетрантности, выраженностью морфологических и клинических проявлений. Тяжесть клинической картины зависит от присутствия и степени гипертрофии. Мутации, которые ассоциируются с высокой пенетрантностью и плохим прогнозом, выражаются большей гипертрофией левого желудочка и толщиной МЖП, чем те, которые характеризуются низкой пенетрантностью и имеют хороший прогноз. Так, было показано, что лишь отдельные мутации ассоциированы с плохим прогнозом и высокой частотой ВС. К ним относятся замены Arg 403 Gln, Arg 453 Cys, Arg 719 Trp, Arg 719 Gln, Arg 249 Gln в гене тяжелой цепи β-миозина, InsG 791 в гене миозин-связывающего белка С и Asp 175 Asn в гене α-тропомиозина [23, 24, 25, 26]. Для мутаций в гене тропонина Т характерна умеренная гипертрофия миокарда, однако прогноз достаточно неблагоприятен, а вероятность внезапной остановки сердца высока [27]. Другие генетические аномалии, как правило, сопровождаются доброкачественным течением и благоприятным прогнозом или занимают промежуточное положение по тяжести вызываемых ими проявлений.
Таким образом, ГКМП характеризуется крайней гетерогенностью вызывающих ее причин, морфологических, гемодинамических и клинических проявлений, разнообразием вариантов течения и прогноза, что существенно затрудняет выбор адекватных и наиболее эффективных лечебных подходов по контролю и коррекции имеющихся нарушений. При этом отчетливо выделяются 5 основных вариантов течения заболевания и исходов:
Вариабельность прогноза определяет необходимость детальной стратификации риска фатальных осложнений заболевания, поиск доступных прогностических предикторов и критериев оценки проводимого лечения.
По современным представлениям, лечебная стратегия определяется в процессе разделения больных на категории в зависимости от описанных выше вариантов течения и прогноза (рис.).
Все лица с ГКМП, включая носителей патологических мутаций без фенотипических проявлений болезни и пациентов с бессимптомным течением заболевания, нуждаются в динамическом наблюдении, в ходе которого оцениваются характер и выраженность морфологических и гемодинамических нарушений. Особое значение имеет выявление факторов, определяющих неблагоприятный прогноз и повышенный риск ВС (в частности, скрытых прогностически значимых аритмий).
К общим мероприятиям относятся ограничение значительных физических нагрузок и запрещение занятий спортом, способных вызывать усугубление гипертрофии миокарда, повышение внутрижелудочкового градиента давления и риска ВС. Для предупреждения инфекционного эндокардита в ситуациях, связанных с развитием бактериемии, при обструктивных формах ГКМП рекомендуется антибиотикопрофилактика, аналогичная таковой у больных с пороками сердца.
До настоящего времени окончательно не решен вопрос о необходимости проведения активной медикаментозной терапии у наиболее многочисленной группы больных с бессимптомной или малосимптомной формами ГКМП и низкой вероятностью ВС. Противники активной тактики обращают внимание на то, что при благоприятном течении заболевания продолжительность жизни и показатели смертности не отличаются от таковых в общей популяции [28, 29]. Некоторые же авторы указывают на то, что использование в этой группе пациентов β-адреноблокаторов и антагонистов кальция (верапамил) может приводить к сдерживанию гемодинамических нарушений и клинической симптоматики [30, 31]. При этом никто не оспаривает тот факт, что выжидательная тактика в случаях бессимптомного или малосимптомного течения ГКМП возможна лишь при отсутствии признаков внутрижелудочковой обструкции, обмороков и серьезных нарушений сердечного ритма, отягощенной наследственности и случаев ВС у близких родственников.
Следует признать, что лечение ГКМП, генетически обусловленного заболевания, обычно распознаваемого на поздней стадии, пока может быть в большей степени симптоматическим и паллиативным. Тем не менее к основным задачам лечебных мероприятий относятся не только профилактика и коррекция основных клинических проявлений заболевания с улучшением качества жизни пациентов, но и положительное влияние на прогноз, предупреждение случаев ВС и прогрессирования заболевания.
Основу медикаментозной терапии ГКМП составляют препараты с отрицательным инотропным действием: β-адреноблокаторы и блокаторы кальциевых каналов (верапамил). Для лечения весьма распространенных при этом заболевании нарушений сердечного ритма используются также дизопирамид и амиодарон.
β-адреноблокаторы стали первой и остаются и по сей день наиболее эффективной группой лекарственных средств, применяемых в лечении ГКМП. Они оказывают хороший симптоматический эффект в отношении основных клинических проявлений: одышки и сердцебиения, болевого синдрома, включая стенокардию, не менее чем у половины больных ГКМП [32, 33, 34], что обусловлено, в основном, способностью этих препаратов уменьшать потребность миокарда в кислороде. Благодаря отрицательному инотропному действию и уменьшению активации симпатоадреналовой системы при физическом и эмоциональном напряжении, β-блокаторы предотвращают возникновение или повышение субаортального градиента давления у больных с латентной и лабильной обструкцией, существенно не влияя на величину этого градиента в покое. Убедительно показана способность β-блокаторов улучшать функциональный статус пациентов в условиях курсового и длительного применения [35]. Хотя препараты не оказывают прямого влияния на диастолическое расслабление миокарда, они могут улучшать наполнение ЛЖ косвенно — за счет уменьшения частоты сердечных сокращений и предупреждения ишемии сердечной мышцы [36]. В литературе имеются данные, подтверждающие способность β-блокаторов сдерживать и даже приводить к обратному развитию гипертрофии миокарда [37, 38]. Однако другие авторы подчеркивают, что вызываемое β-блокаторами симптоматическое улучшение не сопровождается регрессией гипертрофии ЛЖ и улучшением выживаемости больных [39]. Хотя эффект этих препаратов в отношении купирования и предупреждения желудочковых и суправентрикулярных аритмий и внезапной смерти не доказан, ряд специалистов все же считают целесообразным их профилактическое назначение больным ГКМП высокого риска, включая пациентов молодого возраста с отягощенным случаями внезапной смерти семейным анамнезом [40].
Предпочтение отдается β-блокаторам без внутренней симпатомиметической активности. Наибольший опыт накоплен по применению пропранолола (обзидан, анаприлин). Его назначают начиная с 20 мг 3-4 раза в день, с постепенным увеличением дозы под контролем пульса и артериального давления (АД) до максимально переносимой в большинстве случаев 120–240 мг/сут. Следует стремиться к применению возможно более высоких доз препарата, так как отсутствие эффекта терапии β-блокаторами, вероятно, связано с недостаточной дозировкой. При этом нельзя забывать о том, что повышение дозировок существенно увеличивает риск известных побочных эффектов.
В настоящее время широко изучается возможность эффективного применения нового поколения кардиоселективных β-блокаторов пролонгированного действия, в частности атенолола, конкора и др. При этом существует мнение о том, что кардиоселективные β-блокаторы у больных ГКМП не имеют преимуществ перед неселективными, так как в больших дозах, к достижению которых следует стремиться, селективность практически утрачивается. Следует отметить, что рекомендуемый к применению у больных ГКМП с тяжелыми суправентрикулярными и желудочковыми аритмиями соталол сочетает в себе свойства неселективных β-блокаторов и антиаритмических средств III класса (кордароноподобный эффект).
Применение блокаторов медленных кальциевых каналов при ГКМП основано на снижении уровня свободного кальция в кардиомиоцитах и нивелировании асинхронии их сокращения, улучшении расслабления миокарда и снижении его сократимости, подавлении процессов гипертрофии миокарда. Среди блокаторов кальциевых каналов препаратом выбора, благодаря наибольшей выраженности отрицательного инотропного действия и наиболее оптимальному профилю фармакологических свойств, является верапамил (изоптин, финоптин). Он обеспечивает симптоматический эффект у 65–80% больных, включая случаи рефрактерности к лечению β-блокаторами, что обусловлено способностью препарата уменьшать ишемию миокарда, в том числе безболевую, и улучшать его диастолическое расслабление и податливость ЛЖ [41, 42, 43]. Это свойство верапамила обеспечивает повышение толерантности больных к физической нагрузке и снижение субаортального градиента давления в покое при меньшей по сравнению с β-блокаторами способности к уменьшению внутрижелудочковой обструкции в случаях физического и эмоционального напряжения и провокации изопротеренолом. Одновременно верапамил снижает периферическое сосудистое сопротивление вследствие вазодилататорного действия [44]. И хотя этот эффект чаще всего нивелируется непосредственным положительным влиянием на диастолическую функцию ЛЖ, у отдельных больных с базальной внутрижелудочковой обструкцией в сочетании с повышенным конечно-диастолическим давлением ЛЖ и склонностью к системной артериальной гипотензии при уменьшении постнагрузки внутрижелудочковый градиент давления может резко возрастать. Это способно приводить к развитию отека легких, кардиогенного шока и даже внезапной смерти [45]. Подобные грозные осложнения фармакотерапии верапамилом описаны также у больных необструктивной ГКМП с высоким давлением в левом предсердии, у которых они обусловлены отрицательным инотропным действием препарата. Очевидно, как важно соблюдать осторожность при начале лечения верапамилом этой категории больных. Прием препарата следует начинать в условиях стационара с малых доз — 20–40 мг 3 раза в день с постепенным их повышением при хорошей переносимости до снижения частоты сердечных сокращений в покое до 50–60 уд/мин. Клинический эффект наступает обычно при приеме не менее 160–240 мг препарата в сутки; более удобны в условиях длительного применения пролонгированные формы (изоптин-ретард, верогалид-ретард). С учетом благоприятного влияния верапамила на диастолическую функцию и величину субаортального градиента давления в ЛЖ, а также доказанной способности увеличивать выживаемость больных ГКМП по сравнению с плацебо [46], целесообразно его профилактическое назначение у асимптоматичных больных ГКМП высокого риска.
Место дилтиазема в лечении ГКМП окончательно не определено. Имеются данные, что в средней дозе 180 мг/сут за 3 приема он оказывает столь же выраженное, как 240 мг верапамила, благотворное влияние на диастолическое наполнение ЛЖ и одинаковый симптоматический эффект, однако в меньшей степени улучшает физическую работоспособность больных [47].
В нашей клинике продолжается проспективное наблюдение (от 1 до 5 лет) более 100 больных ГКМП. Больные были рандомизированы на 3 сопоставимые по количеству, полу, возрасту и тяжести клинических проявлений группы. Пациентам произвольно назначались атенолол или изоптин-ретард; в третьей группе преобладали лица с тяжелыми желудочковыми нарушениями ритма, и им был рекомендован прием соталола. Оценка эффективности различных вариантов медикаментозного лечения проводилась в условиях длительного (не менее 1 года) применения препаратов. Суточные дозы при двухкратном режиме приема титровались индивидуально и составили в среднем 85, 187, 273 мг для атенолола, изоптина и соталола соответственно. Длительная терапия привела к улучшению клинического состояния соответственно у 77, 72 и 83% пациентов каждой группы, что выражалось в достоверном уменьшении основных симптомов, проявлений сердечной недостаточности (СН), увеличении мощности и времени выполненной нагрузки и улучшении показателей качества жизни (на 25, 32 и 34% соответственно). При этом выявлены достоверное (p
С. А. Габрусенко, кандидат медицинских наук
Ю. В. Сафрыгина
В. Г. Наумов, доктор медицинских наук, профессор
Ю. Н. Беленков, доктор медицинских наук, профессор
НИИ кардиологии им. А. Л. Мясникова РК НПК МЗ РФ, Москва