Эрадикационная терапия что это такое
Эрадикационная терапия что это такое
Современные схемы эрадикационной терапии инфекции Helicobacter pylori
Современные схемы эрадикационной терапии инфекции Helicobacter pylori
Для проведения эрадикационной терапии инфекции Helicobacter pylori врач должен выбрать схему лечения оптимальную для конкретного больного. Часто это оказывается не таким простым, так как важным бывает учитывать целый ряд факторов: необходимо остановиться на каком-то определенном режиме терапии, подобрать конкретные компоненты этой схемы, установить продолжительность лечения, проанализировать клиническую ситуацию, разумно оценить стоимость лекарств, входящих в схему.
Основные принципы эрадикационной терапии инфекции H.pylori известны. Процитируем их по тексту «Рекомендаций по диагностике и лечению инфекции Helicobacter pylori у взрослых при язвенной болезни желудка и двенадцатиперстной кишки» Российской Гастроэнтерологической Ассоциации и Российской группы по изучению H.pylori [1]: Основой лечения является использование комбинированной (трехкомпонентной) терапии:
Второе Маастрихтское соглашение устанавливает на первое место среди показаний к антигеликобактерной терапии язвенную болезнь желудка и язвенную болезнь двенадцатиперстной кишки, не зависимо от фазы заболевания (обострение или ремиссия), включая их осложненные формы. Эрадикационная терапия при язвенной болезни является необходимым лечебным мероприятием, и обоснованность ее использования при этом заболевании базируется на очевидных научных фактах. Второе Маастрихтское соглашение подчеркивает, что при неосложненной язвенной болезни двенадцатиперстной кишки нет необходимости продолжать антисекреторную терапию после проведения курса эрадикационной терапии. Ряд клинических исследований показал, что после удачного эрадикационного курса заживление язвы, действительно, не требует дальнейшего назначения медикаментов. Рекомендуется также проводить диагностику инфекции H.pylori у больных язвенной болезнью, получающих поддерживающую или курсовую терапию антисекреторными средствами, с назначением антибактериального лечения. Проведение эрадикации у этих больных дает существенный экономический эффект, что связано с прекращением длительного приема антисекреторных препаратов.
В качестве показаний для эрадикационной терапии названы также MALT-лимфома, атрофический гастрит, состояние после резекции желудка по поводу рака. Кроме того, антигеликобактерная терапия может быть показана лицам, являющимся ближайшими родственниками больных раком желудка, и проведена по желанию пациента (после подробной консультации с врачом).
Важно отметить, что число возможных схем антигеликобактерной терапии сокращено. Для тройной терапии предлагается всего две пары антибиотиков. Для квадротерапии в качестве антибактериальных агентов предусмотрены только тетрациклин и метронидазол.
Терапия первой линии: Ингибитор протонной помпы (или ранитидин висмут цитрат) в стандартной дозе 2 раза в день + кларитромицин 500 мг 2 раза в день + амоксициллин 1000 мг 2 раза в день или метронидазол 500 мг 2 раза в день.
Тройная терапия назначается как минимум на 7 дней.
В случае отсутствия успеха лечения назначается терапия второй линии: Ингибитор протонной помпы в стандартной дозе 2 раза в день + Висмута субсалицилат/субцитрат 120 мг 4 раза в день + метронидазол 500 мг 3 раза в день + тетрациклин 500 мг 4 раза в день. Квадротерапия назначается как минимум на 7 дней.
Если препараты висмута не могут быть использованы, в качестве второго лечебного курса предлагаются тройные схемы лечения на основе ингибиторов протонной помпы. В случае отсутствия успеха второго курса лечения дальнейшая тактика определяется в каждом конкретном случае.
Последним тезисом Согласительного доклада является следующий: антибиотики, специфически направленные против H.pylori, пробиотики и вакцины могут войти в арсенал антигеликобактерной терапии в будущем, но в настоящее время эти препараты и лечебные подходы находятся в стадии разработки, и практических рекомендаций не существует.
Из рекомендаций Второго Маастрихтского соглашения исключена схема лечения блокатор протонного насоса + амоксициллин + производное нитроимидазола (метронидазол). Эта комбинация является привычной для России, где метронидазол в силу своей низкой стоимости и «традиционного» использования в качестве «репаранта» при язвенной болезни является практически неизменным антигеликобактерным агентом. К сожалению, при наличии штамма H.pylori, резистентного к производным нитроимидазола, эффективность данной схемы лечения значительно снижается, что доказано не только в европейских иссследованиях, но и в России. По результатам рандомизированного контролируемого мультицентрового исследования эрадикация инфекции в группе, получавшей метронидазол 1000 мг, амоксициллин 2000 мг и омепразол 40 мг в сутки на протяжении 7 дней была достигнута в 30% случаев (доверительный интервал для вероятности 95% составил 17%-43%) (В.Т. Ивашкин, П.Я. Григорьев, Ю.В. Васильев и соавт., 2001). Таким образом, можно только присоединиться к мнению европейских коллег, которые исключили эту схему из рекомендаций.
К сожалению, эрадикационная терапия инфекции H.pylori не обладает стопроцентной эффективностью. Не со всеми положениями Второго Маастрихтского соглашения можно однозначно согласиться, и без вдумчивого анализа перенести их в нашу страну.
Так российские врачи часто используют схемы тройной терапии на основе препарата висмута в качестве лечения первой линии. Мультицентровое исследование Российской группы по изучению H.pylori (2000 г.) показало доступность и эффективность такого подхода в нашей стране, в том числе на примере схемы субцитрат коллоидного висмута + амоксициллин + фуразолидон.
Антигеликобактерная терапия должна совершенствоваться, и Второе Маастрихтское соглашение имеет существенное значение для ее оптимизации.
Таблица 1. СХЕМЫ ЭРАДИКАЦИОННОЙ ТЕРАПИИ ИНФЕКЦИИ Helicobacter pylori
по Маастрихтскому соглашению (2000)
| Терапия первой линии Тройная терапия Омепразол 20 мг 2 раза в день или | Лансопразол 30 мг 2 раза в день или Пантопразол 40 мг 2 раза в день + кларитромицин 500 мг 2 раза в день + амоксициллин 1000 мг 2 раза в день или + кларитромицин 500 мг 2 раза в день + метронидазол 500 мг 2 раза в день Ранитидин висмут цитрат 400 мг 2 раза в день | + кларитромицин 500 мг 2 раза в день + амоксициллин 1000 мг 2 раза в день или + кларитромицин 500 мг 2 раза в день + метронидазол 500 мг 2 раза в день Терапия второй линии | Квадротерапия Омепразол 20 мг 2 раза в день или | Лансопразол 30 мг 2 раза в день или Пантопразол 40 мг 2 раза в день + Висмута субсалицилат/субцитрат 120 мг 4 раза в день + метронидазол 500 мг 3 раза в день + тетрациклин 500 мг 4 раза в день
| |||
Литература
Современные аспекты эрадикации Helicobacter pylori
Helicobacter pylori — одна из самых распространенных инфекций в мире. Эти бактерии играют ключевую роль в развитии гастрита, язвенной болезни, В-клеточной лимфомы и рака желудка. Эрадикационная терапия считается успешной, если обеспечивает частоту излечения более 80%.
Резистентность к антибиотикам
Резистентность к антибиотикам — ведущий фактор неудачной терапии первой и второй линии. Резистентность варьирует в разных странах, есть также региональные различия (табл.). Это объясняет, почему невозможно предложить стандартизированную терапию, которая могла бы быть применена во всем мире. Кроме того, устойчивость непрерывно изменяется вследствие злоупотребления антибиотиками для лечения других заболеваний и вследствие миграции населения. Ряд авторов считают, что периодически должны проводиться исследования чувствительности к антибиотикам, чтобы использовать в лечении антибиотики с более низкой резистентностью. Консенсус Маастрихт III (2005) также подчеркивает роль устойчивости к антибиотикам при выборе терапии не только первой, но и второй линии [15]. Фактически тройная терапия, которая включает кларитромицин, должна назначаться только в тех регионах, где резистентность к этому антибиотику не превышает 15–20%. Широкое использование кларитромицина для лечения инфекций дыхательных путей, особенно у детей, и метронидазола в гинекологии и при паразитарных инвазиях в развивающихся странах увеличило первичную устойчивость H. pylori к этим двум антибиотикам. Резистентность к метронидазолу в некоторых регионах достигает 100%. В развитых странах, после проведенных исследований, в качестве замены кларитромицина и метронидазола предложены фторхинолоны, к которым H. pylori все еще имеет низкую резистентность. Однако H. pylori может легко развить устойчивость к фторхинолонам, так что они могут быть полезны только в ближайшее время.
Терапия первой линии
Следует подчеркнуть, что в связи с ростом лекарственной резистентности H. pylori к антибиотикам для эрадикации целесообразно применять оригинальные ингибиторы протонной помпы (эзомепразол) и оригинальный кларитромицин (Клацид).
Ингибиторы протонной помпы (ИПП) в основе тройной схемы были терапией первой линии в течение более десяти лет. Согласно Маастрихт III [15] традиционное лечение первой линии — ИПП (два раза в день), амоксициллин (1 г два раза в день) и кларитромицин (500 мг два раза в день) назначают в течение 10 дней. Современный метаанализ [4] продемонстрировал, что 10-дневная и 14-дневная тройная терапия давали большую частоту эрадикации, чем 7-дневный курс лечения. XXII ежегодная конференция европейской группы по изучению Helicobacter (EHSG), прошедшая в сентябре 2009 г. в г. Порту (Португалия), подтвердила лидирующие позиции тройной терапии для эрадикации H. pylori [18].
Маастрихт III (2005) рекомендовал четырехкомпонентную схему в качестве альтернативной терапии первой линии [15]. Для лечения по этой схеме используются следующие препараты: ИПП в стандартной дозе 2 раза в день + Де-нол (висмута трикалия дицитрат) 120 мг 4 раза в день + амоксициллин 1000 мг 2 раза в день + кларитромицин 500 мг 2 раза в день в течение 10 дней. С учетом роста резистентности к кларитромицину четырехкомпонентная терапия в настоящее время занимает лидирующие позиции.
В 2008 г. Европейской группой по изучению H. pylori последовательная терапия была рекомендована в качестве терапии первой линии: 5 дней — ИПП + амоксициллин 1000 мг 2 раза в день; затем 5 дней — ИПП + кларитромицин 500 мг 2 раза в день + тинидазол 500 мг 2 раза в день [20]. Исследования показывают, что последовательная терапия ведет к эрадикации в 90%, то есть превосходит эффективность стандартной тройной терапии. Частота побочных эффектов и отсутствие комплаенса при этом такие же, как при тройной терапии.
В метаанализе 10 клинических исследований 2747 пациентов [12] последовательная терапия оказалась эффективнее стандартной тройной терапии для эрадикации инфекции H. pylori у пациентов, впервые проходящих лечение. Частота эрадикации H. pylori была 93,4% (91,3–95,5%) при последовательной терапии (n = 1363) и 76,9% (71,0–82,8%) при стандартной тройной терапии (n = 1384). Большинство пациентов, включенных в эти исследования, были итальянцами, поэтому необходимо дальнейшее международное исследование. Частота эрадикации у кларитромицин-резистентных пациентов при последовательной терапии составила 83,3%, тройной терапии — 25,9% (отношение шансов (ОШ) 10,21; достоверный интервал (ДИ) 3,01–34,58; р
В. В. Цуканов*,
О. С. Амельчугова*,
П. Л. Щербаков**, доктор медицинских наук, профессор
*НИИ медицинских проблем Севера Сибирского отделения РАМН, Красноярск
**ЦНИИ гастроэнтерологии, Москва
Антигеликобактерная эрадикационная терапия – выход из тупика или движение вглубь лабиринта?
К настоящему времени установлено, что эрадикация Helicobacter pylori может ускорить сроки рубцевания язвы, улучшить качество жизни пациента и уменьшить частоту рецидивов, но не позволяет ликвидировать заболевание. Это связано с тем, что Helicobacter pylori является не облигатно-патогенным, а условно-патогенным микробом. Соответствен но, стратегия эрадикационной терапии при заболеваниях, ассоциированных с условно-патогенной микрофлорой, в том числе с Helicobacter pylori, как минимум является ошибочной.
Уровень развития современной медицины, как и любого другого направления в науке, зависит от объема знаний и навыков, накопленных многими десятками предшествующих поколений. В то же время следует признать, что мы, как и современники Гиппократа, двигаемся вперед путем совершения проб и ошибок. Можно согласиться с тем, что число этих ошибок уменьшилось, но в целом оно еще очень велико. Достаточно упомянуть тот факт, что в нас тоящее время в каждом разделе медицины с периодичностью 3-5 лет происходит пересмотр рекомендаций по вопросам диагностики и лечения различных заболеваний. Ранее же ревизия сложившихся представлений занимала столетия и даже тысячелетия.
Открытие антибиотиков без преувеличения является одним из величайших достижений медицины, поскольку их использование позволило радикально сократить смертность от инфекционных заболеваний во всем мире. В конце ХХ века на слизистой оболочке желудка и двенадцатиперстной кишки пациентов с язвенной болезнью были выявлены грамотрицательные, неспорообразующие бак терии – Helicobacter pylori. Включение в программу лечения гастродуоденальных язв антибиотиков, обладающих антигеликобактерной активностью, в комбинации с блокаторами протонной помпы, позволило добиться максимального сокращения сроков рубцевания язвы, которое почти в 100% случаев сопровождалось эрадикацией бактерии. Данный факт послужил основанием для вывода о том, что H. pylori в сочетании с гиперхлоргидрией являются главными причинами язвенной болезни. Таким образом, о язвенной болезни стали говорить как об инфекционном заболевании. Однако лечением таких пациентов по-прежнему за ни маются не инфекционисты, а гастроэнтерологи. Поскольку выздоровлению пациентов инфекционных отделений всегда предшествует эрадикация инфекционного агента – виновника заболевания, данный подход был распространен и на пациентов с язвенной болезнью.
Длительное время существовало стойкое убеждение, что с эрадикацией H. pylori будет ликвидирована и язвенная болезнь. Прошло более 30 лет с момента открытия микроорганизма, в связи с чем появилась возможность подвести определенные итоги. Воздержимся пока от собственных оценок и обратимся к высказыванию И.В. Маева – одного из ревностных приверженцев версии о главной роли H. pylori в патогенезе язвенной болезни. «Несмотря на уже многолетнюю активную борьбу … с H. pylori-инфекцией, распространенность язвенной болезни как в нашей стране, так и в большинстве стран мира не снижается. Стабильно высокой (на уровне 10%) остается и частота ее грозных осложнений (перфорации, пенетрации, кровотечения и др.)» [1].
Приведенная фраза фактически является авторитетным признанием того, что утверждение о ведущей роли H. pylori в патогенезе язвенной болезни является ошибочным. Действи тельно, в значительной части случаев язвенная болезнь развивается без всякого участия H. pylori (H. pylori-негативные формы болезни). В США частота язвенной болезни, не ассоциированной с H. pylori, варьируется от 39 до 52%, а в Австралии достигает 45% [2,3]. Представленные данные наглядно демонстрируют, что роль H. pylori без достаточных оснований чрезмерно демонизирована.
Поскольку принципы лечения гастродуоденальных язв тесно увязаны с представлением о роли H. pylori, возникает вопрос, отразилось ли это на алгоритме антибактериальной терапии больных? На данный вопрос в целом можно ответить утвердительно. Корректировка схем лечения действительно осуществляется каждые несколько лет. Последние рекомендации сформулированы в Маастрихт-V-Флорентийском консенсусе [4]. Значительная часть всех пяти вариантов Мааст рихт ского консенсуса посвящена рассмотрению вопроса: что делать, если неэффективна та или иная схема терапии? Соответственно, в последнем варианте, как и в четырех предыдущих изданиях, преимущественно обсуждается тактика преодоления резистентности H. pylori к используемым антибиотикам. При этом стратегический вопрос о целесообразности обязательного достижения эрадикации H. pylori даже не возникает, он автоматически, в течение более 30 лет, переносится из одних рекомендаций в другие, хотя, как уже отмечалось, заболеваемость язвенной болезнью на планете за данный период не снижается. Более того, в новых рекомендациях без достаточных оснований расширяется круг заболеваний и синдромов, при которых рекомендуется проводить эрадикационную терапию.
Недавно, на страницах данного журнала Я.С. Цим мерман опубликовал дискуссионную статью, в которой привел целый ряд фактов, заставляющих усомниться в гипертрофированной роли H. pylori и в адекватности стратегии консервативной терапии гастродуоденальных язв. С учетом собственного опыта мы целиком разделяем точку зрения Я.С. Циммермана о том, что авторысоставители «Маастрихтских консенсусов» по существу монополизировали право определять показания к эрадикации H. pylori и методику проведения эрадикационной терапии, провозгласив стратегию на тотальную ликвидацию H. pylori (test and treat strategy: выявлять и уничтожать!), что научно бездоказательно и практически неосуществимо [5]. Твердо убеждены, что подобный подход является однобоким, ошибочным и требует учета альтернативных фактов. С учетом изложенного в предлагаемой статье мы постараемся более подробно остановиться на дискуссионных моментах, касающихся вопросов стратегии антигеликобактерной эрадикационной терапии.
В противовес утверждению о главной роли H. pylori в патогенезе гастродуоденальных язв считаем необходимым напомнить хорошо известный факт, установленный еще В.Х. Василенко (1970 г.) – «Язвы заживают при лечении, без лечения и вопреки лечению» [6]. С учетом того, что у значительной части больных возникновение заболевания возможно и при отсутствии H. py lori, данное наблюдение убедительно свидетельствует о существовании причин, которые играют более важную роль в патогенезе гастродуоденальных язв, чем наличие микроба. Считаем, что в патогенезе гастродуоденальных язв среди многочисленных факторов риска ведущими являются «немодифицируемые»: наследственность, пол и возраст человека. Непосредственная же реализация их роли осуществляется за счет имеющейся врожденной или приобретенной локальной гипоплазии сосудов в двенадцатиперстной кишке или желудке, которая также относится к категории немодифицируемых факторов [7]. Помимо немодифицируемых, в патогенезе гастродуоденальных язв важную вспомогательную роль играет огромное количество факторов, которые считаются «модифицируемыми»; к их числу относится и H. pylori. С учетом выраженного положительного ответа на антигеликобактерную терапию есть основание сделать вывод, что среди модифицируемых факторов H. pylori играет одну из главных ролей.
Опыт последних тридцати с лишним лет показал, что эрадикация геликобактера, сокращая сроки рубцевания язв, одновременно ведет к снижению соотношения гастродуоденальных язв, ассоциированных и не ассоциированных с H. pylori, но при этом, вопреки ожиданиям, не ведет к ликвидации язвенной болезни [8]. Большой интерес представляют наблюдения хирургов, установивших, что частота рецидивов после успешно выполненных органосберегающих операций (стволовой ваготомии с экономной резекцией язвы) составляет 0% в течение более 25 лет после вмешательства. При этом положительный H. pylori-статус у оперированных больных выявляют с той же частотой, что и в популяции [9,10]. Важно отметить рост смертности от осложнений длительно не рубцующихся гастродуоденальных язв, что дает повод провести переоценку показаний к проведению планового оперативного лечения при указанных состояниях. Приведенные примеры наглядно демонстрируют, что в значительном числе случаев успешное хирургическое устранение части стенки желудка или двенадцатиперстной кишки, включающей участок локальной гипоплазии сосудов, является гораздо более эффективной мерой, чем эрадикация H. pylori.
Негативный парадокс обсуждаемой проблемы заключается в том, что к настоящему времени данный микроб без достаточных оснований рассматривается в качестве главной причины возникновения уже целого ряда других заболеваний. Показания к их эрадикационной терапии были сформулированы еще консенсусом «Маастрихт II». В последующих согласительных документах дополнительно указывался ряд новых патологических состояний, при которых также рекомендовалось проведение эрадикационной терапии. К настоящему времени показаниями к диагностике и лечению H. pylori служат следующие [4,11]:
При этом игнорируется тот факт, что данный подход находится в противоречии с представлениями о патогенезе, особенностях течения, лечения и исходов классических облигатно- и условно-патогенных инфекций [12]. Известно, что биомасса микробов, заселяющих желудочно-кишечный тракт взрослого человека, составляет 2,5–3 кг и более и включает в себя до 450–500 видов. Около 90% данного микробиоценоза представлено облигатной (обязательной) нормальной микрофлорой, выполняющей множество жизненно важных функций [13]. Без преувеличения, значение данной микрофлоры сопоставимо с ролью такого важного органа, как печень. Остальная часть микробиоценоза представлена факультативной (возможной, необязательной) микрофлорой, часто встречающейся у здоровых людей и являющейся условно-патогенной [14]. Условно-патогенными считают микроорганизмы, представляющие собой большую группу грибов, бактерий, простейших и вирусов. Они являются нормальными обитателями кожи и слизистых оболочек, мирно сосуществующими с организмом человека, что свидетельствует о том, что иммунная система хозяина не воспринимает их как угрозу и ведет себя нейтрально. При этом они способны долгое время существовать в окружающей среде.
H. pylori относится к категории условно-патогенных инфекций. Особенностью микроорганизмов данного типа является то, что они многие годы и даже всю жизнь могут находиться в организме человека, не проявляя признаков какой-либо агрессии. Агрессивные свойства данные инфекционные агенты проявляют лишь в условиях пассивного проникновения во внутреннюю среду в больших количествах и (или) резкого снижения общего и местного иммунитета человека (нарушение целостности покровов, бактерицидной активности секретов, подавление фагоцитарной реакции, снижение числа микробов-антагонистов и др.). Это связано с тем, что условно-патогенные микробы, в отличие от облигатно-патогенных, не обладают факторами активного проникновения во внутреннюю среду, подавления защитных сил организма, не выделяют экзотоксины. Патогенное влияние на организм они оказывают с помощью эндотоксина и ферментов-токсинов [12].
Данные больные являются заразными, поэтому они нуждаются в изоляции от окружающих и соблюдении требований противоэпидемического режима и должны получать лечение в специализированных инфекционных отделениях. В подобных случаях убедительным и вполне обоснованным выглядит требование добиваться, в обязательном порядке, эрадикации инфекционных агентов, вызвавших данное заболевание.
Таким образом, в возникновении перечисленных патологических состояний H. pylori играет роль важного модифицируемого, но не главного фактора риска. В этой связи, утверждение, что при всех перечисленных состояниях антигеликобактерная терапия должна быть эрадикационной, вызывает большие сомнения. Накоп ленный мировой опыт допускает эмпирическое использование антибактериальных препаратов сразу после установления диагноза при заболеваниях, ассоциированных с условно-патогенной флорой (пневмонии, инфекции желчевыводящих, мочевыводящих путей и др.). При этом учитываются результаты предшествующих эпидемиологических исследований по региону, лечение пациентов данной категории осуществляется вне инфекционного стационара – в общетерапевтических, хирургических и других отделениях. Часто в результате лечения удается достичь и эрадикации агента, причастного к возникновению пневмонии или другого подобного заболевания, однако задача обязательного достижения подобной цели не стоит. Более того, прием антибиотиков прекращается задолго до того, как ликвидированы пневмоническая инфильтрация и основные лабораторные и клинические прояв ления. Таким образом, главной целью лечения заболеваний, ассоциированных с условно-патогенной флорой, является не эрадикация условно-патогенных бактерий, а достижение клинического выздоровления при острой болезни или ремиссии хронического заболевания. Принципиальным является тот факт, что после выздоровления не ставится задача контроля степени эрадикации возбудителя заболевания, более того, после успешного завершения лечения возбудитель часто так и остается неизвестным [17].
Отсутствие убедительных доказательств целесообразности эрадикации H. pylori при гастродуоденальных язвах делает еще менее обоснованным утверждение о необходимости добиваться той же цели при прочих перечисленных выше заболеваниях. Обсуждения заслуживают, прежде всего, хронический гастрит и функциональная диспепсия, ассоциированные с H. pylori, и рак желудка. Считается, что при естественном течении H. pylori-ассоциированнного хронического гастрита у 1-2% больных нарушается стройная система клеточного обновления слизистой оболочки желудка. Это ведет к атрофии и прогрессированию морфологических изменений в слизистой оболочке, что способствует формированию рака желудка («каскад Correa») [18].
Заболеваемость раком желудка характеризуется примерно 10-кратными географическими колебаниями, что может свидетельствовать о более важной роли этнической и наследственной предрасположенности. Рак желудка очень часто встречается в странах Восточной Азии (Японии и Корее), Южной Америке и Восточной Европе и значительно реже в Южной Азии, Северной Америке, Северной и Восточной Африке, Австралии, Новой Зеландии [19,20]. Особый интерес представляет тот факт, что в африканской популяции, где отмечается максимальная распространенность H. pylori (до 97%), рак желудка распространен в минимальной степени, а в Японии, где распространенность H. pylori составляет около 43%, заболеваемость раком этой локализации высокая. С учетом изложенного, трудно согласиться с утверждением, что инфекция H. pylori является канцерогеном 1 группы для человека [21]. Сомнение в обоснованности данного утверждения усиливается еще более, если обратиться к статистике распространенности рака желудка в России за период 2005-2015 гг. (рис. 1) [22].
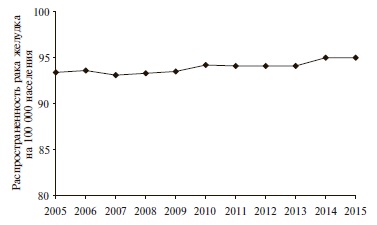
Приведенные данные наглядно свидетельствуют о том, что внедрение в практику эрадикационной стратегии не способствует снижению распространенности рака желудка в России. Более того, отмечается его статистически недостоверный, но неуклонный рост за период 2005-2010 гг., что делает сомнительным утверждение о целесообразности проведения эрадикационной терапии с целью профилактики возникновения данного вида онкопатологии.
Большой интерес представляет исследование, которое в течение около 7,5 лет проводилось в китайской провинции, где отмечается высокая заболеваемость раком желудка. Пациенты с сопоставимым риском возникновения рака желудка были распределены на две группы и получали плацебо (n=813) или эрадикационную терапию (n=817). В первые 5 лет кумулятивная заболеваемость раком желудка была выше в группе плацебо, однако к концу исследования частота его в сравниваемых группах достоверно не различалась [23]. Приведенные данные наглядно свидетельствуют о том, что эрадикационная терапия может на несколько лет замедлить скорость прогрессирования рака желудка, но не способна его предотвратить. В литературе приводятся данные о том, что эрадикационная терапия является эффективным элементом профилактики рака лишь в тех случаях, когда ее назначают до развития преднеопластических состояний. Установлено, что III и IV стадии атрофического гастрита по системе OLGA ассоциируются с повышенным риском развития рака желудка [24]. Эрадикационная терапия у пациентов с кишечной метаплазией не приводит к обратному развитию последней, она может лишь замедлить прогрессирование метаплазии до неоплазии.
Все схемы эрадикационной терапии, сформулированные в пяти Маастрихтских рекомендациях, предлагаются не в качестве рекомендаций, возможных к использованию, а вменяются в виде обязательств, непременных к исполнению. В этой связи представляет интерес наблюдение о распространенности язвенной болезни у лиц, занятых в производстве антибиотиков. При этом установлено, что средний возраст больных с дуоденальными язвами (39,8 лет), занятых в производстве антибиотиков, соответствовал таковому больных с язвами двенадцатиперстной кишки контрольной группы, работа которых не была связана с данным производством. В то же время, средний возраст пациентов с язвами желудка в основной группе (38,7 лет) был ниже возраста, характерного для лиц с язвами данной локализации (40-50 лет) в контроле. Это дает основание говорить о том, что продолжительный контакт человека с антибиотиком ведет к росту резистентности условнопатогенной флоры, что, в конечном счете, способствует более раннему возникновению язвы желудка у лиц, работа которых связана с производством антибиотиков [25].
Суммарная распространенность хронического гаст рита и функциональной диспепсии сопоставима с распространенностью H. pylori в популяции (не менееполовины населения). Известно, что при естественном течении хронического гастрита 1-2 из 100 человек могут умереть от рака желудка. При III и IV стадии атрофического гастрита эрадикационная терапия бесполезна. Требование о необходимости проведения эрадикации на более ранних стадиях означает, что в программу лечения следует включать не менее 50% населения планеты. В то же время, ранее приведенные примеры свидетельствуют о том, что, во-первых, эрадикационная терапия не остановит прогрессирования ни хронического гастрита, ни функциональной диспепсии. Во-вторых, у 1-2 из 100 человек с хроническим гастритом опухоль может развиться на несколько лет позже, чем при естественном течении заболевания, но умрут они, в любом случае, от рака желудка. Что касается остальных 98-99 пациентов, то они, фактически, превращаются в «живой термостат-инкубатор» для выращивания огромного количества новых штаммов бактерий, резистентных к новым антибиотикам.
Завершая обсуждение роли H. pylori в патогенезе и лечении H. pylori-ассоциированных заболеваний, можно сделать ряд выводов, которые дают основание усом ниться в достаточной обоснованности и целесообразности стратегии эрадикационной терапии при отмеченных заболеваниях. Если ориентироваться на распространенность H. pylori и ассоциированных с ним заболеваний, ситуацию в целом можно рассматривать как грозную пандемию, охватившую территорию всей планеты. Однако при более близком рассмотрении становится ясно, что сравнение с пандемией носит исключительно формальный характер. Как известно, классическим примером пандемии является «черная смерть», или эпидемия чумы, которая наблюдалась в Европе в XIV веке. Она почти одновременно буйствовала на территории Африки и Евразии. Последствия инфекции были ужасны: Европа опустела, потеряв по некоторым подсчетам до 40% населения, на территории Китая и Индии вымерли несколько сотен городов и деревень, количество мертвых в Африке и вовсе не подлежит подсчету. Таким образом, одной из главных особенностей пандемии является не только высокая распространенность инфекции в популяции, но и исключительно высокий риск смерти при заражении. При этом абсолютное большинство лиц с H. pylo riассоциированными заболеваниями представлено пациентами с хроническим гастритом, которые даже не знают о существовании у них ни гастрита, ни H. pylori. Сам же гастрит представляет угрозу для жизни лишь у 1-2 из 100 человек. С учетом представленных фактов термин пандемия для данной ситуации не подходит.
Следующая особенность состоит в том, что возбудители пандемических заболеваний все без исключения относятся к категории облигатно-патогенных, в то время как H. pylori является условно-патогенным. Важно подчеркнуть, что у выздоровевших после заразных болезней людей иммунная система вырабатывает барьер от определенного возбудителя: стойкий, нестойкий или пожизненный. При этом далеко не у всех переболевших классическим инфекционным заболеванием, вызванным облигатно-патогенным возбудителем, вырабатывается пожизненный иммунитет. Например, к числу болезней, после которых образуется стойкий иммунитет на всю жизнь, относят краснуху, эпидемический паротит, гепатит А, дифтерию, корь, полиомиелит, ветряную оспу. Нестойкий или кратковременный иммунитет формируется после таких заболеваний, как коклюш, гепатит В, грипп, туберкулез, брюшной тиф, дизентерия. К условно-патогенным возбудителям иммунная система относится нейтрально, поэтому нет оснований отрицать, что H. pylori после эрадикации может неоднократно возвращаться к одному и тому же человеку.
Эрадикация облигатно-патогенного возбудителя тож дественна полному выздоровлению инфекционного больного, эрадикация же H. pylori, как показало время, ведет лишь к сокращению сроков рубцевания язвы и к более продолжительной ремиссии, но не к ликвидации самого заболевания. Распространенность рака желудка, как отмечено ранее, не только не снижается, но продолжает расти. С учетом изложенного при остром возникновении или рецидиве гастродуоденальных язв проведение антигеликобактерной терапии следует признать целесообразным. При этом главным критерием эффективности лечения следует считать достижение ремиссии заболевания (купирование клинических проявлений, рубцевание язвы). Однако, поскольку эрадикация не является гарантией предотвращения рецидива заражения H. pylori и не сопровождается ликвидацией «H. рylori-ассоциированных заболеваний», лечебную стратегию, предписывающую обязательно добиваться эрадикации геликобактера, следует считать ошибочной.
Лапина Т.Л. Эрадикационная терапия инфекции Helicobacter pylori.
Эрадикационная терапия инфекции Helicobacter pylori
В качестве показаний для обязательного проведения лечения, направленного на уничтожение H. pylori, выступают:
• Состояние после резекции желудка по поводу рака;
• Близкое родство с лицами, страдающими раком желудка (то есть, эрадикация H. pylori показана лицам, являющимся ближайшими родственниками больных раком желудка).
• Желание пациента (после полной консультации врача).
Приведенный выше перечень показаний был предложен участниками Маастрихтской конференции еще в 2000 году. За прошедшие 5 лет удалось накопить достаточно новых фактов, которые подтверждают правильность выбора этих состояний для обязательной противогеликобактерной терапии. Объективно показано, что именно уничтожение H. pylori при язвенной болезни приводит не только к успешному заживлению язвы, но к существенному снижению частоты рецидивов заболевания, а также к предотвращению осложнений заболевания. Эрадикационная терапия H. pylori при атрофическом гастрите, у родственников больных раком желудка, а также после резекции желудка по поводу рака расценивается как профилактическое мероприятие по предотвращению предраковых изменений слизистой оболочки желудка и собственно рака.
Благодаря высокой частоте актуальными проблемами современной гастроэнтерологии можно назвать гастроэзофагеальную рефлюксную болезнь и гастропатию, индуцированную нестероидными противовоспалительными средствами. Значение H. pylori в патогенезе этих заболеваний спорно, и проведение антигеликобактерной терапии должно быть подчинено ряду положений.
Взаимоотношения гастропатии, индуцированной нестероидными противовоспалительными средствами (НПВС), и H. pylori авторы международных рекомендаций также суммировали в нескольких положениях.
• Эрадикация H. pylori показана лицам, которые вынуждены длительно принимать НПВС, но этого курса недостаточно для предотвращения возникновения язв.
• Перед началом курса НПВС следует провести антигеликобактерную терапию для профилактики язвообразоваиия и кровотечения.
• При необходимости длительного приема аспирина и при наличии кровотечения в анамнезе следует проводить тест для определения инфекции H. pylori и при положительном результате назначать антигеликобактерное лечение.
• При необходимости длительного приема НПВС и наличии язвенной болезни и/или кровотечения поддерживающая терапия ингибиторами протонной помпы более эффективна, чем эрадикация инфекции H. pylori (для предотвращения язвообразоваиия и кровотечения).
Схемы для успешной эрадикационной терапии H. pylori разработаны эмпирически, как по их компонентам, так и по дозам лекарственных средств, так и по продолжительности лечения. Они отвечают определенным требованиям по эффективности (воспроизводимый в различных популяциях стабильно высокий процент уничтожения микроорганизма) и безопасности.
Таблица 1. Схемы эрадикационной терапии инфекции H. pylori (1-й линии)
| 1-й компонент схемы | 2-й компонент схемы | 3-й компонент схемы |
| ингибитор протонной помпы: лансопразол 30 мг 2 р\сут или омепразол 20 мг 2 р\сут или пантопразол 40 мг 2 р\сут или рабепразол 20 мг р\сут или эзомепразол 10 мг 2 р\сут | кларитромицин 500 мг 2 р\сут | амоксициллин 1000 мг 2 р\сут |
| или ранитидин висмут цитрат 400 мг 2 р\сут | или метронидазол 500 мг 2 р\сут |
Таблица 2. Схемы четырехкомпонентной эрадикационной терапии инфекции H. pylori (2-й линии)
| 1-й компонент схемы | 2-й компонент схемы | 3-й компонент схемы | 4-й компонент схемы |
| ингибитор протонной помпы: лансопразол 30 мг 2 р\сут или омепразол 20 мг 2 р\сут или пантопразол 40 мг 2 р\сут или рабепразол 20 мг р\сут или эзомепразол 10 мг 2 р\сут | висмута субсалици- лат\субцитрат 120 мг 4 р\сут | метронидазол 500 мг 3 р\сут | тетрациклин 500 мг 4 р\сут |
Таким образом, следует сделать заключение о том, что круг показаний для проведения эрадикационной терапии H. pylori расширяется. Стандартизованная тройная терапия остается надежным инструментом в лечении заболеваний, ассоциированных с H. pylori.
Эрадикационная терапия инфекции Helicobacter pylori.
Клиника пропедевтики внутренних болезней, гастроэнтерологии и гепатологии им. В.Х. Василенко ММА им. И.М. Сеченова.
Выбор схемы эрадикационной терапии при helicobacter pylori в случае необходимости повторного лечения
Опубликовано в журнале:
«Врач», 2008, №4, с. 64-67
Т. Лапина, кандидат медицинских наук,
ММА им. И. М. Сеченова
Лечение при инфекции Helicobacter pylori (Hp) можно считать детально разработанным: по комбинации лекарственных средств, их дозам и продолжительности курса оно стандартизировано. В России эта терапия утверждена в соответствующих стандартах медицинской помощи и Формулярной системе. Национальные рекомендации многих европейских стран и отечественные стандарты по диагностике и лечению при Нр основаны на алгоритмах, разработанных под эгидой Европейской группы по изучению этой инфекции. Поскольку первые конференции по выработке данного консенсуса прошли в Маастрихте, рекомендации носят название Маастрихтских (конференции проходили в 1996, 2000 и 2005 гг.).
Схемы эрадикационной терапии строго регламентированы, кажется, что такое лечение не должно вызывать вопросов. Однако выполнение любого стандарта на практике не всегда сопровождается стопроцентной эффективностью. Большинство наиболее острых вопросов касаются выбора схемы лечения после неудачи первой (а иногда второй и третьей) попытки.
Почему же при Нр иногда требуется проведение повторного курса эрадикационной терапии (в англоязычной литературе для его обозначения используют термин «терапия второй, третьей линии»)? В качестве показателя, свидетельствующего об оптимальности схемы лечения, все Маастрихтские рекомендации [9, 16, 17] называют 80% эрадикацию Нр. Это означает, что процент эрадикации микроорганизма по критерию intention-to-treat должен быть равен или превышать 80%. Этот «целевой» процент успешной эрадикации предложен на основании анализа данных множества клинических исследований различных схем лечения, их доступности и переносимости; он учитывает и характеристики Нр (чувствительность микроорганизма к лекарственным средствам, особенности среды обитания). Стабильно высокий процент уничтожения микроорганизма должен быть легко воспроизводим при лечении в разных популяциях и разных регионах и странах.
Решающее значение имеет, безусловно, терапия первой линии, которая должна быть нацелена на достижение эрадикации Hр у максимального числа больных. В качестве терапии первой линии Маастрихтские рекомендации III предлагают следующие трехкомпонентные схемы лечения (табл. 1): ингибитор протонной помпы в стандартной дозировке 2 раза в день+кларитромицин – 500 мг 2 раза в день+амоксициллин – 1000 мг 2 раза в день или метронидазол – 400 или 500 мг 2 раза в день. Минимальная продолжительность тройной терапии – 7 дней, однако оказалось, что для данной схемы более эффективен 14-дневный курс лечения (на 12%; 95% доверительный интервал – ДИ: 7–17%) [12]. Тем не менее 7-дневная тройная терапия может быть признана приемлемой, если местные исследования показывают, что она высокоэффективна. Рекомендуется одинаковая терапия первой линии для всех стран, хотя в разных странах могут быть одобрены разные дозы лекарственных средств [17].
Таблица 1. Схемы стандартной тройной терапии при Нр
| 1-й компонент | 2-й компонент | 3-й компонент |
| Ингибитор протонной помпы: лансопразол – 30 мг 2 раза в день или омепразол – 20 мг 2 раза в день или пантопразол – 40 мг 2 раза в день или рабепразол – 20 мг 2 раза в день или эзомепразол – 20 мг 2 раза в день | Кларитромицин – 500 мг 2 раза в день | Амоксициллин – 1000 мг 2 раза в день или Метронидазол – 400 или 500 мг 2 раза в день |
Четырехкомпонентная схема лечения включает в себя ингибитор протонной помпы в стандартной дозе 2 раза в день+висмута субсалицилат/трикалия дицитрат – 120 мг 4 раза в день+метронидазол – 500 мг 3 раза в день+тетрациклин – 500 мг 4 раза в день (табл. 2). В Маастрихтских рекомендациях II за четырехкомпонентной схемой была закреплена позиция терапии второй линии [16]. Одно из новых положений Маастрихтских рекомендаций III – возможность применения такой схемы в определенных клинических ситуациях, как терапии первой линии (альтернативная терапия первой линии) [17].
Таблица 2. Схемы четырехкомпонентной эрадикационной терапии при Нр
| 1-й компонент | 2-й компонент | 3-й компонент | 4-й компонент |
| Ингибитор протонной помпы: лансопразол – 30 мг 2 раза в день или омепразол – 20 мг 2 раза в день или пантопразол – 40 мг 2 раза в день или рабепразол – 20 мг 2 раза в день или эзомепразол – 20 мг 2 раза в день | Висмута субсалицилат/ субцитрат – 120 мг 4 раза в день | Метронидазол – 500 мг 3 раза в день | Тетрациклин – 500 мг 4 раза в день |
Почему претерпели изменения представления об оптимальной терапии первой линии в Маастрихтских рекомендациях? Почему поиск лучших режимов лечения не прекращается? Появились результаты клинических исследований стандартной тройной терапии (ингибитор протонной помпы +амоксициллин+кларитромицин) в разных странах, согласно которым «целевая» эрадикация не достигается, т.е. она ниже 80% [14]. Наиболее значимая причина снижения эффективности стандартной эрадикационной терапии – резистентность микроорганизма к антимикробным агентам. В Маастрихтских рекомендациях III большое внимание уделено вопросам планирования лечения в зависимости от чувствительности Hp к антибактериальным средствам. Так, комбинация «ингибитор протонной помпы+кларитромицин+амоксициллин или метронидазол» остается рекомендуемой терапией первой линии для популяций с частотой резистентных штаммов к кларитромицину менее 15–20%. В популяциях с частотой резистентности к метронидазолу менее 40% предпочтительнее схема «ингибитор протонной помпы+кларитроми-цин+метронидазол» [17].
Остановимся подробнее на проблеме резистентности Hp к антибиотикам. Согласно международным данным, резистентность Нр к амоксициллину либо равна 0, либо она менее 1%. Имеются крайне редкие сообщения о формировании резистентности из-за мутации pbp-1A-гена. Таким образом, резистентность к амоксициллину – крайне редкое явление, не имеющее клинического значения. Такую же редкость представляет собой резистентность к тетрациклину, которая во многих странах вообще не описана. Она обусловлена мутацией 3 смежных нуклеотидов в гене 16S rRNA (AGA 926–928→TTC). По экспериментальным данным, если мутация возникает лишь в 1 или 2 из этих нуклеотидов, резистентность клинически незначима; лишь тройственная мутация приводит к стабильной резистентности, которая способна оказать влияние на исходы лечения [18].
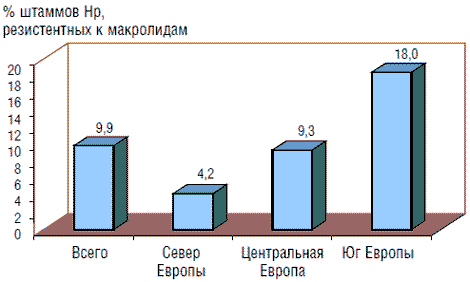
Принципиальное значение имеет чувствительность Hp к кларитромицину и метронидазолу. Количество резистентных штаммов Hp к кларитромицину, по данным мультицентрового европейского исследования, в среднем составляет 9,9% (95% ДИ: 8,3–11,7). Выявлены существенные различия этого показателя: в странах Северной Европы частота резистентности к кларитромицину низкая (4,2%; 95% ДИ: 0–10,8%); в Центральной и Восточной Европе она выше (9,3%; 95% ДИ: 0–22%) и самая высокая – на юге Европы (18%; 95% ДИ: 2,1–34,8%) (рис. 1) [13]. Риск возникновения резистентности к кларитромицину связан с частотой назначения макролидов в данной группе населения. В связи с тем что в ряде европейских стран в педиатрической практике широко назначали макролиды по поводу, например, респираторных заболеваний, частота резистентности штаммов Hp к кларитромицину у детей весьма высока, что делает проблемой выбор тактики эрадикационной терапии.
Рис. 1. Распространенность штаммов Hp, резистентных к макролидам, в европейских странах (по Glupczynski Y. и соавт., 2000)
Ответственна за резистентность к кларитромицину мутация гена 23S rDNA, которая ведет к нарушению пространственной конфигурации рибосомы. Признано, что она способствует развитию перекрестной резистентности к макролидным антибиотикам; вместе с тем не ясно, все ли макролиды, разными путями проникающие в слизистую оболочку желудка, могут приводить к селекции резистентных штаммов in vivo.
Различны и данные о влиянии резистентности к кларитромицину на исходы эрадикационной терапии. Максимальный из описанных эффектов следующий: 87,8% эрадикации Hp при наличии чувствительных штаммов, 18,3% – при наличии резистентных штаммов [18].
Количество штаммов Hp, резистентных к метронидазолу, в Европе и США колеблется от 20 до 40%. Известно, что в развивающихся странах число метронидазолрезистентных штаммов выше. Наибольшее значение для селекции резистентных штаммов имеет применение метронидазола в популяции. Механизм формирования резистентности к метронидазолу до конца не ясен: подозревают изменения гена rdxA, но точные мутации не известны [18].
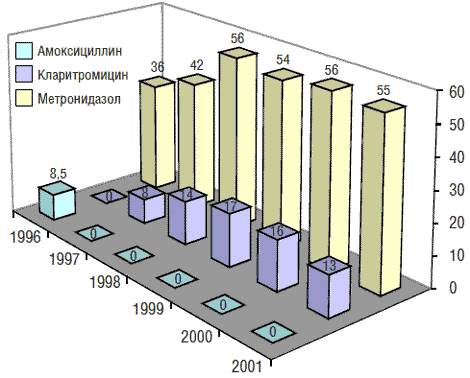
Наблюдение (1996–2001) за динамикой резистентности к производным нитроимидазола (метронидазол), макролидам (кларитромицин) и β-лактамам (амоксициллин) у штаммов Hp, выделенных в Москве, показало, что она отличается от таковой в Европе (рис. 2). Так, во взрослой популяции уровень первичной резистентности Hp к метронидазолу уже в 1996 г. превысил среднеевропейский показатель (25,5%) и составил 36,1%. На протяжении 1996–1999 гг. отмечалось увеличение числа первично резистентных штаммов Hp к метронидазолу, а затем оно не выявлялось [2].
Рис. 2. Динамика резистентности (в %) к метронидазолу, кларитромицину и амоксициллину у штаммов Hp, выделенных от взрослых в Москве в 1996–2001 гг. (Кудрявцева Л., 2004)
В отличие от данных, полученных в Европе в 1996 г., где во взрослой популяции уровень первичной резистентности Hp к макролидам (кларитромицин) составлял 7,6%, в Москве в то время штаммов Hp, резистентных к этому антибиотику, выявлено не было. Относительный прирост количества штаммов Hp, первично резистентных к кларитромицину, среди взрослой популяции за 1-й год наблюдения составил 8%, за 2-й – 6,4%, за 3-й – 2,7%. В 2000 г. уровень резистентности Hp к кларитромицину несколько снизился: если в 1999 г. он составлял 17,1%, то в 2000 г. – 16,6%. В 2001 г. наметилась явная тенденция к снижению этого показателя (13,8%).
В 1996 г. в Москве было выделено 3 штамма Hp, резистентных к амоксициллину; в дальнейшем такие находки не повторялись, и эти данные можно считать единственными в РФ и уникальными [2].
Последние доступные данные о чувствительности Hp к антибиотикам в Москве относятся к 2005 г. : у взрослых количество резистентных к метронидазолу штаммов составило 54,8%, к кларитромицину – 19,3%; у детей – соответственно 23,8 и 28,5% (Кудрявцева Л., 2006: персональное сообщение).
Таким образом, исходя из последних данных, в России сложились неблагоприятные условия для проведения стандартной тройной терапии вследствие высоких показателей резистентности Нр и к кларитромицину, и к метронидазолу. Тем не менее результаты отечественных клинических исследований свидетельствуют о большем значении для исходов терапии в нашей стране резистентности к метронидазолу, чем к кларитромицину. Чрезвычайное распространение штаммов, резистентных к метронидазолу, значительно ограничивает использование этого антибактериального агента. Так, по данным В. Ивашкина и соавт., в контролируемом исследовании схема «ингибитор протонной помпы+амоксициллин+метронидазол» (одобренная Маастрихтскими рекомендациями I и исключенная их вторым пересмотром) была успешной лишь в 30% случаев [1]. Что же касается резистентности к макролидам, то следует помнить, что контингент больных, из биопсийного материала которых были выделены штаммы для определения резистентности, был особый, в частности среди них было много стационарных пациентов. Кроме того, при анализе штаммов, полученных от лиц, проживающих в разных городах РФ, были выявлены существенные различия. Так, штаммов Hp, резистентных к кларитромицину, в Абакане зарегистрировано не было (табл. 3) [2]. Это заставляет предположить, что их распространенность за пределами Москвы и Санкт-Петербурга ниже среднеевропейского уровня.
Таблица 3. Частота антибиотикорезистентности Hp в разных городах России в 2001 г. (Кудрявцева Л. и соавт., 2004)
| Резистентность штаммов Hp | Города | ||
| Москва | Санкт-Петербург | Абакан | |
| К метронидазолу | 55,5 | 40 | 79,4 |
| К кларитромицину | 13,8 | 13,3 | 0 |
| К амоксициллину | 0 | 0 | 0 |
Не следует забывать, что обеспечивают высокий процент уничтожения Нр не только антибактериальные компоненты схемы лечения, но и ингибиторы протонной помпы. Было убедительно доказано, что без ингибитора протонной помпы при применении только 2 тех же антибиотиков в тех же дозировках эрадикация Нр снижается на 20–50%. Именно ингибиторы протонной помпы служат базисными препаратами схемы, обеспечивая путем мощного подавления желудочной секреции благоприятные условия для реализации действия антибиотиков. Если качество ингибитора протонной помпы низкое и он мало влияет на интрагастральный рН, то и процент эрадикации микроорганизма не будет достигать «целевого» рубежа. С другой стороны, высокий антихеликобактерный эффект свидетельствует об успешном контроле желудочной секреции ингибитором протонной помпы и о качестве этого лекарственного средства.
В большом числе отечественных клинических исследований продемонстрирована успешность стандартной тройной терапии даже при ее 7-дневной продолжительности. Так, в работе В. Пасечникова и соавт. (2004) больные с обострением язвенной болезни двенадцатиперстной кишки (92 человека) получали стандартную тройную терапию в течение 7 дней: Омез® (омепразол, «Д-р Редди`с Лабораторис Лтд.») в дозе 40 мг/сут в сочетании с амоксициллином (2000 мг/сут) и кларитромицином (1000 мг/сут). Затем была проведена рандомизация: пациенты 1-й группы продолжали получать омепразол (40 мг/сут) еще 2 нед; пациенты 2-й группы не получали никакого лечения. Эрадикация Hp была успешной у 82,6% больных (intention-to-treat; per protocol – 91,6%). В 1-й группе она составила 84,2% (intention-to-treat; per protocol – 92,8%), во 2-й – 82,2% (intention-to-treat; per protocol – 90,2%). Принципиальное значение имеет тот факт, что заживление язвы достигнуто у 91,5% больных, получавших монотерапию Омезом® после антихеликобактерного курса, и у 93,3% больных, получавших только недельный курс эрадикации Hp и никакого лечения в дальнейшем [4]. Таким образом, в данном исследовании 7-дневная стандартная тройная терапия способствовала достижению «целевого» процента эрадикации и более того – заживлению язвы даже без продолжения монотерапии омепразолом, что косвенно свидетельствует об эффективности антихеликобактерного курса.
Предпринимаются самые разные попытки повысить эффективность стандартной тройной терапии. Так, имеются данные о том, что сочетание антихеликобактерной схемы с пробиотиком приводит к повышению показателя эрадикации Hp и снижает частоту нежелательных явлений [10, 20]. Недавно в Москве было предпринято исследование с добавлением к стандартной тройной терапии пребиотика лактулозы (Нормазе). Омез® (40 мг/сут) в сочетании с амоксициллином (2000 мг/сут) и кларитромицином (1000 мг/сут) назначали на 12 дней и в одной группе больных сочетали с Нормазе. Эрадикация Hp в этой группе достигнута в 85% случаев, в другой – в 90% случаев (различие недостоверно). Несмотря на то что лактулоза не способствовала увеличению эрадикации Hp (процент все же превзошел «целевой» рубеж), она уменьшила частоту нарушений стула и метеоризм [3].
Терапия первой линии – стандартная тройная – не утратила актуальности для России. От точного соблюдения этого стандарта врачом и пациентом зависит успех эрадикации Нр. Чем выше ее показатель, тем меньше вероятность повторного лечения. Наиболее обоснованным способом повышения эффективности стандартной тройной терапии следует признать увеличение ее продолжительности до 14 дней [7, 11, 12].
Как надо планировать терапию второй линии при неудаче применения первой линии? Следует избегать назначения антибиотиков, которые пациент уже получал. Это – один из основополагающих (но не общепризнанных) постулатов, на которых строится такое планирование [7]. С точки зрения экспертов – авторов Маастрихтских рекомендаций III, наиболее правильным выбором в данной ситуации является квадротерапия с препаратом висмута [17]. К такому же выводу пришли и авторы Американских рекомендаций по диагностике и лечению Hp [7]. При анализе нескольких десятков клинических исследований с применением квадротерапии в качестве терапии второй линии средний показатель эрадикации микроорганизма составил 76% (60–100%) [15]. Данная схема доступна, относительно дешева и эффективна. К ее недостаткам относят большое число таблеток и капсул, которые приходится принимать ежедневно (до 18 штук в сутки), четырехкратный режим дозирования и сравнительно часто развивающиеся нежелательные явления [7].
В некоторых странах препараты висмута недоступны, и в качестве схем второй линии Маастрихтские рекомендации III предлагают варианты тройной терапии: ингибитор протонной помпы и амоксициллин, а в качестве антибактериального агента фигурируют тетрациклин или метронидазол [17]. В России нет систематизированного опыта использования таких схем, хотя имеются данные о весьма низкой эффективности 7-дневной тройной терапии: ингибитор протонной помпы+амоксициллин+метронидазол [1].
Как терапию третьей линии Маастрихтские рекомендации III позиционируют тройную терапию с представителем рифамицинов – рифабутином – и хинолонов – левофлоксацином.
В группе больных с неудавшимся курсом стандартной тройной терапии 12-дневное лечение ингибитором протонной помпы в сочетании с амоксициллином и рифабутином (150 мг) привело к эрадикации Hp в 91% случаев, причем доказанная резистентность к метронидазолу и кларитромицину не сказалась на результате [5]. Привлекательная сторона применения рифабутина – очень малая вероятность формирования резистентности к нему Hp (описана лишь в единичных случаях). Механизм формирования резистентности (перекрестной ко всем рифамицинам) – это точечная мутация rpoB-гена [18]. Маастрихтские рекомендации III настаивают на осторожном назначении этого антибиотика, так как его широкое применение может привести к селекции резистентных штаммов Mycobacteria.
Удобной в применении и достаточно эффективной кажется тройная терапия с левофлоксацином: ингибитор протонной помпы в стандартной дозе дважды в сутки в сочетании с амоксициллином (2000 мг/сут) и левофлоксацином (500 мг/сут). В качестве терапии второй линии после неудачной стандартной тройной терапии эта схема дает высокий результат [8]. Но с применением левофлоксацина связана проблема формирования резистентности к хинолонам вследствие целого ряда мутаций гена gyrA. В недавно опубликованном французском исследовании, в котором изучали большое число штаммов Hp, резистентность выявлена у 17,2% из них [6]. В работе итальянских авторов (с гораздо меньшим числом изученных штаммов) резистентность к левофлоксацину установлена в 30,3% случаев; показатель успешной эрадикации чувствительного к данному антибиотику микроорганизма – 75% против 33,3% при наличии резистентности [19].
В последних рекомендациях экспертов и обзорах по данной проблеме очень пристальное внимание уделяется новой схеме эрадикации Hp – последовательной терапии [7, 10, 11, 14]. Курс последовательной терапии занимает 10 дней: на первые 5 дней назначают ингибитор протонной помпы в стандартной дозе дважды в сутки в сочетании с амоксициллином (2000 мг/сут); затем в течение еще 5 дней – ингибитор протонной помпы в стандартной дозе дважды в сутки в сочетании с кларитромицином (1000 мг/сут) и тинидазолом (1000 мг/сут). В итальянском исследовании [21] при последовательной терапии эрадикация Hp (intention-to-treat) составила 91 против 78% в группе сравнения (10-дневная стандартная тройная терапия). В группе пациентов, инфицированных штаммами, резистентными к кларитромицину, этот показатель достиг 89 против 29%.
Для исключения неудачи в эрадикации Hp стандартную тройную терапию следует назначать в полном объеме по дозам и при возможности – на 14 дней. Выбор схем лечения в случае неудачи терапии первой линии достаточно широк и позволяет учесть индивидуальные особенности пациента.
Эрадикация Нelicobacter pylori – пути достижения эффективности
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Представлены данные о хеликобактериозе, побочных эффектах эрадикационной терапии Нelicobacter (Н.) pylori, адъювантном варианте эрадикации.
Эрадикационная терапия не всегда является успешной, что сопряжено с растущей резистентностью штаммов Н. pylori к антибактериальным препаратам, а также с низкой комплаентностью пациентов, прекращением терапии из-за развития побочных эффектов. Использование пробиотических препаратов, в частности Lactobacillus (L.) reuteri, позволяет улучшить переносимость эрадикационной терапии, а также снизить количество и активность Н. pylori.
Применение штамма L. reuteri, обладающего выраженной антихеликобактерной активностью, в качестве адъюванта антихеликобактерной терапии представляется перспективным.
Н. pylori – неинвазивный микроб, колонизирующий преимущественно поверхностные слои слизистой оболочки (CO) желудка. Представляет собой грамотрицательную спиралевидную бактерию, имеющую на одном своем конце 4–5 жгутиков. Н. pylori сумел адаптироваться к резко кислой среде желудка благодаря небольшому размеру генома и способности к быстрым мутациям в неблагоприятных условиях для его жизнедеятельности. С помощью униполярно расположенных жгутиков Н. pylori перемещается в слое желудочной слизи в поисках оптимальных условий для колонизации CO желудка. При возникновении угрозы для существования спиралевидные формы Н. pylori трансформируются в кокковые, у которых резко снижен обмен веществ и редуцирована репродуктивная способность, но повышена устойчивость к неблагоприятным внешним воздействиям. Это позволяет им выжить при транзите через кишечник и сохраняться во внешней среде (в фекалиях, возможно, в почве и/или воде). Главным источником Н. pylori-инфекции является сам человек, а основным путем инфицирования – фекально-оральный; орально-оральный путь имеет вспомогательное значение [10, 23].
Попадая в желудок, бактерия продуцирует уреазу, которая расщепляет мочевину желудочного содержимого, вследствие чего образуются аммиак и СО2. Аммиак способствует защите микроба от соляной кислоты и вызывает повреждение СО желудка. Выделяя фермент муциназу, Н. pylori разрушает белок муцин, содержащийся в желудочной слизи, в результате чего создаются условия для проникновения бактерии через слой слизи и адгезии ее на эпителий СО желудка [4, 7].
В микробиоме желудка Н. pylori является «хозяином», хотя эффект его доминирования неясен [25]. Существует 196 штаммов Н. pylori [24]. Маркерами вирулентности Н. pylori могут служить такие гены, как cagА (способствующий индукции воспаления и секреции цитотоксичных веществ), vacА (продуцирующий вакуолизирующий цитотоксин), iceА (наиболее токсичен ice А1, способствующий адгезии Н. pylori на эпителиоцитах СО желудка) [5, 10].
Примерно 60% населения земного шара инфицировано H. рylori; распространена инфекция преимущественно в развивающихся странах, а также у пожилых. Длительное время остается асимптомной. Эффективной вакцины для предотвращения инфекции в настоящее время не существует [13, 28].
Н. pylori-инфекция является наиболее частой причиной (60–75%) развития неатрофического антрального гастрита, который постепенно (в течение 15–18 лет) может эволюционировать в антральный атрофический хронический гастрит, распространяться в антрокардиальном направлении, поражая фундальный отдел желудка, а в части случаев вызывать развитие мультифокального атрофического хронического гастрита, появление в СО желудка очагов кишечной метаплазии, эпителиальной дисплазии, неоплазии (предрака). С Н. рylori ассоциированы язвенная болезнь, реже – рак желудка и МАLТ-лимфома желудка [10, 23].
Протеазы, высвобождающиеся полиморфноядерными лейкоцитами в ответ на инфекцию Н. pylori, разрушают эпителий желез СО желудка, что в конце концов ведет к развитию атрофии [6, 15]. Кроме того, инфекция Н. pylori способствует выработке антител, которые перекрестно реагируют с париетальными клетками и могут вызвать их атрофию. В свою очередь, ахлоргидрия способствует размножению бактерий в желудке, трансформирующих нитраты в нитриты и приводящих к образованию N-нитрозосоединений, обладающих канцерогенными свойствами. Под действием Н. pylori изменяется баланс между процессами пролиферации и апоптоза, в результате чего нарушается физиологическая регенерация СО желудка, увеличивается образование свободных радикалов, аммиака, оксида азота, также обладающих канцерогенными свойствами. При длительном существовании инфекции Н. pylori возможны мутации гена р53, обеспечивающего противоопухолевую защиту, в результате чего могут появляться эпителиальные клетки с поврежденной ДНК и прогрессировать явления дисплазии эпителия. Инфекция Н. pylori приводит к снижению содержания аскорбиновой кислоты, β-каротина, α-токоферола, обеспечивающих противоопухолевую защиту [6, 14]. В 1994 г. Международным агентством по изучению рака (IARC) Н. pylori отнесен к канцерогенам 1 класса («определенно доказанным»). Наличие инфекции Н. pylori повышает риск развития рака желудка в 4–20 раз [6, 19].
Известно, что некоторые популяции с высоким уровнем инфицирования Н. pylori (в странах Восточной Азии) имеют высокую заболеваемость раком желудка, тогда как другие высокоинфицированные (в странах Южной и Западной Африки) имеют низкую частоту развития рака. Этот феномен назван «африканской загадкой» и может быть объяснен разностью генотипов Н. pylori, особенно cagА и vacА [25].
Основой лечения заболеваний, ассоциированных с Н. pylori, является эрадикация этой инфекции. Известно, что риск возникновения пептической язвы и рака желудка возрастает с повышением уровня инфицирования Н. pylori, следовательно, подавление Н. pylori-инфекции снижает риск этих заболеваний [20]. Кроме того, эрадикация Н. рylori признана наиболее перспективной стратегией снижения заболеваемости раком желудка [1, 21].
Последнее согласительное совещание «Маастрихт-4» (2010 г.) ограничило число применяемых схем эрадикации инфекции Н. pylori до 5:
– стандартная 3-компонентная терапия (ингибитор протонной помпы (ИПП) в стандартной дозе 2 р./сут + амоксициллин по 1000 мг 2 р./сут + кларитромицин 500 мг 2 р./сут в течение 7–14 дней;
– 4-компонентная терапия с препаратами висмута (ИПП в стандартной дозе 2 р./сут + тетрациклин 500 мг 4 р./сут + метронидазол 500 мг 3 р./сут + висмута трикалия дицитрат 120 мг 4 р./сут) в течение 10–14 дней;
– последовательная терапия (в течение первых 5 дней – ИПП в стандартной дозе 2 р./сут + амоксициллин по 1000 мг 2 р./сут, следующие 5 дней – ИПП в стандартной дозе 2 р./сут + кларитромицин 500 мг 2 р./сут + метронидазол 500 мг 3 р./сут;
– 4-компонентная терапия без препаратов висмута (ИПП в стандартной дозе 2 р./сут + амоксициллин 1000 мг 2 р./сут + кларитромицин 500 мг 2 р./сут + еще один антибактериальный препарат, например метронидазол 500 мг 3 р./сут) в течение 10–14 дней;
– 3-компонентная терапия с левофлоксацином (ИПП в стандартной дозе 2 р./сут + амоксициллин 1000 мг 2 р./сут + левофлоксацин 500 мг 2 р./сут) в течение 10–14 дней.
В зонах с низкой ( Литература
Только для зарегистрированных пользователей
Схема эрадикации H.pylori, одобренная Российской Гастроэнтерологической ассоциацией и Европейской группой по изучению H.pylori
Этиологические факторы развития пептической язвы
Лечение язвенной болезни:
Соблюдения жесткой диеты не требуется
Омепразол + Кларитромицин + Тинидазол
Также Омепразол
ТинидазолИнгибитор синтеза ДНК бактерийБолее быстрое, чем у метронидазола действие на ДНК Нр, более высокая активность in vitro, быстрее проникает в бактерии
Эффективность схемы эрадикации, доказанная по всему миру
(данные мета-анализа) 8Количество исследований Всего пациентов Эффективность эрадикации 53 3057 89-91%
Данные метанализа (Arkham et al, 1996) показали, что эффективность эрадикации не зависит от дозы кларитромицина 7
Эрадикация H. рylori: современный взгляд на старую проблему
*Пятилетний импакт фактор РИНЦ за 2020 г.

Читайте в новом номере
Распространенность инфекции Helicobacter pylori (H. pylori) остается на очень высоком уровне во всем мире и в России колеблется от 65 до 86% в зависимости от региона. H. pylori представляет собой этиологический фактор развития таких заболеваний, как гастрит, язвенная болезнь желудка и двенадцатиперстной кишки, MALT-лимфома, является доказанным канцерогеном для рака желудка. Поэтому наиболее эффективной мерой профилактики рака желудка является эрадикационная терапия H. pylori. Согласно Киотскому глобальному консенсусу по Helicobacter pylori-ассоциированному гастриту (сентябрь 2015 г.), всем лицам, инфицированным H. pylori, должна быть предложена эрадикационная терапия, если для этого нет каких-либо препятствий (коморбидность, высокая вероятность реинфекции в популяции). Российские и международные рекомендации говорят о том, что в регионах, где резистентность к кларитромицину не превышает 15–20%, в качестве схемы первой линии лечения должна применяться 14-дневная стандартная тройная терапия. В регионах с высокой резистентностью к кларитромицину может использоваться квадротерапия с препаратом висмута. У пациентов, не ответивших на стандартную тройную терапию, в качестве терапии второй линии может быть рекомендована квадротерапия с висмутом или 14-дневная тройная терапия с левофлоксацином. Мерами, позволяющими повысить эффективность эрадикации, являются назначение удвоенной дозы ИПП, подробное объяснение пациенту режима приема лекарственных препаратов.
Ключевые слова: Helicobacter pylori, эрадикация, язвенная болезнь, рак желудка, ИПП.
Для цитирования: Евсютина Ю.В. Эрадикация H. рylori: современный взгляд на старую проблему // РМЖ. Гастроэнтерология. 2016. № 11. С. 673–677.
Для цитирования: Евсютина Ю.В. Эрадикация H. рylori: современный взгляд на старую проблему. РМЖ. 2016;11:673-677.
Eradication of H. рylori: a modern solution for an old problem
Evsyutina Yu.V.
I.M. Sechenov First Moscow State Medical University, Moscow, Russia
The prevalence of Helicobacter pylori (H. pylori) remains high throughout the world and varies across Russian regions, ranging from to 65% to 86%. H. pylori is the causative agent for a number of conditions, i.e., gastritis, gastric and duodenal ulcer, and MALT lymphoma. This pathogen is also recognized as a carcinogen for gastric cancer. Hence, the most effective preventive measure for gastric cancer is H. pylori eradication. The Kyoto global consensus report on Helicobacter pylori gastritis (September 2015) stated that eradication therapy should be recommended to all patients infected with H. pylori if there are no contraindications (i.e., comorbidities, high reinfection probability in the population, etc.). According to the Russian and international guidelines, in areas with low clarithromycin resistance rate (less than 15-20%), 14-day triple therapy should be prescribed as a first-line treatment. In areas with high clarithromycin resistance rate, bismuth-containing quadruple therapy should be used. In non-responders to the triple therapy, bismuth-containing quadruple therapy or 14-day levofloxacin-containing triple therapy should be considered. A double dose of proton pump inhibitor and a detailed explanation of drug regimen may increase the efficacy of eradication treatment.
Key words: Helicobacter pylori, eradication, peptic ulcer, gastric cancer, proton pump inhibitor.
For citation: Evsyutina Yu.V. Eradication of H. рylori: a modern solution for an old problem // RMJ. Gastroenterology. 2016. № 11. P. 673–677.
В статье приведен современный взгляд проблему эрадикации H. рylori
Последовательная терапия эрадикации инфекции Helicobacter pylori
Результаты систематического обзора и мета-анализа
Инфекция H. pylori является причиной развития язв желудка и 12-ти перстной кишки, MALT-лимфом желудка и рака желудка. В настоящее время предложено большое количество схем эрадикационной терапии: стандартная тройная терапия с применением амоксициллина, кларитромицина и ингибитора протонной помпы (ИПП); квадротерапия на основе препаратов висмута, последовательная и сопутствующая терапии. Одной из глобальных проблем на настоящий момент является растущая резистентность к кларитромицину и метронидазолу. Чтобы преодолеть эту проблему, в клинической практике все чаще стала применяться последовательная терапия, включающая назначение на первые пять дней ИПП и амоксициллина в дозе 1 г 2 раза в день и на последующие пять дней – ИПП, кларитромицин 500 мг 2 раза в день и препарата из группы нитромидазолов в дозе 500 мг 2 раза в день. Недавние исследования, сравнивающие эту схему терапии с тройной терапией, дают обнадеживающие результаты и позволяют говорить об эффективности новой эрадикационной схеме.
Цель
Сравнить последовательную эрадикационную терапию с другими схемами эрадикации инфекции H. pylori.
Материалы и методы
В исследование были включены рандомизированные контролируемые исследования (РКИ), найденные по данным поиска в таких базах данных как Medline (c 1950 по май 2013), Embase (c 1980 по мая 2013) и Cochrane Central Register of Controlled Trials (по май 2013), в которых проводилось сравнение последовательной терапии с другими эрадикационными схемами у пациентов старше 18 лет.
Результаты
Последовательная терапия против 7-дневной тройной терапии.
По результатам 22 РКИ эффективнее оказалась последовательная терапия (RR=1,21, 95% CI: 1,17-1,25). Всего проводилось сравнение 2449 пациентов, у которых применялась последовательная терапия с 2566, у которых проводилась 7-ми дневная тройная терапия, эффективность эрадикации составила 86,5% (95% CI: 82,9-89,7%) и 71,5 (95% CI: 68,4-74,5%) соответственно.
В одном из исследований сравнивалась эффективность последовательной терапии с тройной терапией с применением ИПП, амоксициллина и метронидазола и ИПП, амоксициллина и кларитромицина, последовательная терапия оказалась эффективнее первой на 15,9% и второй на 24,0%.
Последовательная терапия против 10-дневной тройной терапии.
По результатам 14 РКИ была показано лишь небольшое отличие в эффективности последовательной схемы эрадикации (RR=1,11, 95% CI: 1,04-1,19).
Всего в исследования было включено 1368 пациента, у которых проводилось лечение компонентами последовательной схемы и 1376 больных, у которых эрадикация осуществлялась с использованием 10-ти дневной тройной терапии, эффективность составила 84,3% и 75,3% соответственно.
Последовательная терапия против 14-дневной тройной терапии.
Результаты 7 исследований позволяют говорить об отсутствии различий в эффективности при сравнении двух вышеперечисленных схем (RR=1,00, 95% CI: 0,94-1,06).
Последовательная терапия против квадротерапии на основе препаратов висмута.
Анализ результатов 3 РКИ не показал преимуществ одной эрадикационной схемы перед другой (RR=1,01, 95% CI: 0,95-1,06).
Эффективность эрадикации у 546 пациентов, у которых применялась последовательная терапия составила 86,2%, а у 545 пациентов, у которых проводилась эрадикация препаратами, входящими в состав квадротерапии – 84,9%.
Результаты исследований, не вошедших в мета-анализ
Последовательная терапия против последовательной терапии с применением левофлоксацина. В трех исследованиях сравнивалась эффективность последовательной терапии с применением кларитромицина и последовательной терапии, в которой вместо кларитромицина применялся левофлоксацин в дозе от 500 до 1000 мг в сутки.
Среди 240 пациентов, у которых применялась схема с использованием 1000 мг левофлоксацина в сутки процент эрадикации составил 90,0%, а среди 240 пациентов у которых проводилась классическая последовательная терапия с применением кларитромицина, эффективность была 78,7%. Частота побочных эффектов была примерно одинаковой (24,3% и 24,4% соответственно).
При сравнении терапии с использованием 500 мг в день левофлоксацина (n=241) и классической последовательной схемы эрадикации (n=240) эффективность в первом случае составляла 89,8%, а во втором – 79,5%. Частота развития побочных эффектов составляла 13,8% и 14,3% соответственно. Анализ результатов позволил сделать вывод о том, что последовательная схема эрадикации с применением левофлоксацина эффективнее, чем последовательная схема с применением кларитромицина.
Сравнение 10-дневной и 14-дневной последовательных схем эрадикации.
В двух РКИ сравнивалась длительность последовательной терапии: у 340 пациентов проводилась 10-ти дневная последовательная терапия и у 340 – 14-ти дневная. Эффективность проводимой терапии составила 87,6% и 89,7% соответственно, что не доказало, что увеличение длительности терапии повышает ее эффективность.
Заключение
Результаты мета-анализа показывают, что последовательная схема эрадикации инфекции Helicobacter pylori эффективнее, чем 7-ми дневная стандартная тройная терапия и показывает похожую эффективность при сравнении со схемами эрадикации, назначаемыми более чем на 10 дней и включающими более 2-х антимикробных препаратов.
Эрадикация хеликобактер пилори: какой препарат выбрать?

Ещё полвека назад существовало несколько теорий, предлагающих свой вариант причин появления язвенной болезни желудка и кишечника. Переломным моментом стал 1979 год, когда в результате научного исследования было доказано, что первоисточник этой проблемы – бактерия хеликобактер пилори (Helicobacter pylori), в норме благополучно существующая в ЖКТ более половины всех представителей человечества. Любое снижение иммунной защиты – благополучный повод для размножения колоний хеликобактер пилори. Для лечения хелиобактериоза созданы схемы эрадикции патогенной бактерии из организма человека.
Схема эрадикционной терапии хеликобактер пилори

При выборе врачом схемы эрадикционной терапии в каждом конкретном случае приходится учитывать следующие факторы:
Прогнозируемая длительность лечения;
Клиническая картина данного случая хелиобактериоза;
Стоимость препаратов, входящих в схему лечения.
Российская Гастроэнтерологическая ассоциация и Российская группа по изучению Helicobacter pylori рекомендует принять за основу комбинированную трёхкомпонентную схему терапии, удовлетворяющую следующим принципам:
Способность провести эрадикцию бактерии не менее чем в 80% случаев;
Отсутствие побочных эффектов, вынуждающих лечащего врача отменить схему лечения, или провоцирующих больного на прекращение приёма препаратов (допускается до 5% таких случаев);
эффективность даже при коротком курсе не дольше 1-2 недель.
В основе методики назначения эрадикционной терапии лежат рекомендации, выработанные мировым сообществом гастроэнтерологов в Маастрихте в 1996 г., и обновленные в 2000 г.
Рекомендации Второго Маастрихтского соглашения по проведению антихеликобактерной терапии:
При неосложнённых случаях язвенной болезни после курса эрадикционной терапии не требуется использование антисекреторных препаратов.
Показания для эрадикционной терапии кроме язвенной болезни: MALT-лимфома, атрофический гастрит, близкие родственные связи с больным раком желудка, состояние после резекции по поводу рака желудка, желание пациента.
Лечение инфекции Helicobacter pylori должно предусматривать возможность неудачи первой линии эрадикционной терапии и необходимость использования второй линии в случае сохранения бактерии в организме. В схему первой линии эрадикции (тройную терапию) предлагается включить 2 антибиотика: Кларитромицин + Амоксициллин (или Метронидазол) и ингибитор протонной помпы (или Ранитидин). Она длится не более 7 дней. При неудаче рекомендуется применять схему второй линии (квадротерапию), включающую в себя 2 антибиотика: Тетрациклин + Метронидазол, препараты висмута и ингибитор протонной помпы. Длительность использования квадротерапии – 7 дней.
В настоящее время в практике не применяются специфические антибактериальные препараты, пробиотики и вакцины, направленные исключительно против Helicobacter pylori, они пока находятся в стадии разработки.
Разработчики Маастрихтских рекомендаций исключили из схемы лечения привычную для России комбинацию: Амоксициллин + Метронидазол + блокатор протонной помпы из-за повышения резистентности Helicobacter pylori к производным нитроимидазолов. Исследования российских учёных подтвердили низкую эффективность этой комбинации (всего 30%). Российские гастроэнтерологи в эрадикционной терапии первой линии часто используют доступную и эффективную тройную терапию, включающую в себя препараты висмута + Амоксициллин + Фуразолидон. Совершенствование антихеликобактерной терапии продолжается, В 2005 году в Нидерландах были разработаны современные схемы эрадикционной терапии первой, второй, третьей линии.
Первая линия эрадикции хеликобактер пилори

трёхкомпонентная схема первой линии получила своё название за то, что она состоит из трёх препаратов:
ингибитор протонной помпы на основе Омепразола, регулирующий активность кислой среды желудочного сока.
Ингибиторы протонной помпы позволяют избавиться от множества негативных проявлений язвы и гастрита, вызванных повышенной кислотностью среды желудка, а так же избежать чрезмерно строгих ограничений, вносимых в рацион питания больного язвенной болезнью. Тем не менее, ограничения всё-таки сохраняются, хотя и не такие строгие.
Допускается замена Амоксициллина на антибиотик Нифурател или на Метронидазол. По показаниям гастроэнтеролог может назначить в схему 4 препарат, имеющий в основе производные висмута. В норме такие лекарства включают в эрадикционную схему второй линии, но их свойства положительно влияют на течение процесса купирования воспалительного процесса. На поверхности желудка образуется защитное покрытие, снимающее симптомы воспаления и боль.
Облегченная схема для больных пожилого возраста:
Ингибитор протонной помпы;
Для увеличения эффективности стандартной терапии первой линии предлагается удвоить срок её применения – с 7 до 14 дней. Ожидаемая эффективность – до 95%. При неэффективности лечения врач рекомендует перейти на вторую линию эрадикционной терапии.
Вторая линия эрадикции хеликобактер пилори

Четыре компонента эрадикционной схемы второй линии:
2 антибиотика: Тетрациклин + Метронидазол, или Амоксициллин + препарат из группы нитрофуранов;
Ингибитор протонной помпы;
Препараты на основе висмута – отличные цитопротекторы, восстанавливающие структуру клеток слизистой желудка и кишечника и их устойчивость к агрессивному воздействию кислоты и продуктов жизнедеятельности Helicobacter pylori. Кроме того, они обладают бактерицидным действием, до минимума снижают риск рецидивов хелиобактериоза. При планировании схемы эрадикции второй линии не рекомендуется использовать уже применяемые ранее антибиотики. Эффективная, доступная и дешевая схема квадротерапия с висмутом тоже не лишена недостатков:
Большое количество принимаемых таблеток (18 штук в сутки);
Частые побочные эффекты;
4-х кратный режим дозирования.
Для усиления эффективности терапии препаратами висмута на время лечения из рациона исключают фрукты, соки, молоко. Длительность терапии второй линии – 10-14 дней.
Третья линия эрадикции хеликобактер пилори

Исключительно редко приходится переходить на третью линию эрадикционной терапии, но такая возможность всё-таки существует. Перед началом реализации третьей схемы пациента тестируют на чувствительность штамма Helicobacter pylori к антибиотикам.
Препараты 3 линии:
Два антибиотика, не использовавшихся ранее и показавших при лабораторной диагностике наивысшую степень эффективности;
Ингибиторы протонной помпы.
Лекарственные средства на основе висмута (трикалий дицитрат висмута) обладают комплексным действием:
Снимают проявления диспепсии (вздутие живота, изжогу, гастралгию);действуют в отношении Helicobacter pylori, как эффективное бактерицидное средство;
Стимулируют регенерацию повреждений более глубоких слоёв стенок желудка.
Терапия третьей линии по Маастрихтским рекомендациям третьего созыва включает препараты из группы рифамицинов (Рифабутин) и хинолонов (Левофлоксацин). Такое сочетание стало эффективным в 91% случаев. Резистентность Helicobacter pylori к Рифабутину очень мала, поэтому его включение в протокол лечения совместно и Амоксициллином и ингибитором протонной помпы позволяет повысить эффективность терапии и даже игнорировать резистентность бактерии к Метронидазолу и Кларитромицину.
Выбор препаратов при необходимости проведения повторного курса эрадикционной терапии

И первая, и вторая, и даже третья схема терапии Helicobacter pylori может быть неэффективной, когда процент эрадикции составляет 80% или менее случаев целевого достижения цели лечения. Эффективность лечения снижается по причине резистентности бактерии к антибиотикам, поэтому исследователи проблемы не прекращают поиск лучших схем.
Не вызывает опасения резистентность Helicobacter pylori к Амоксициллину (менее 1%), к Тетрациклину (близка к 0).
Количество резистентных штаммов бактерии к другим антибактериальным препаратам:
Это объясняется частым назначением антибиотиков из группы макролидов в педиатрической и терапевтической практике. Немаловажное значение в успешности эрадикционной терапии имеют ингибиторы протонной помпы, создающие в ЖКТ благоприятную среду для применения антибиотиков. При низком качестве препаратов этой группы эффективность антибактериальных средств тоже снижается.
Проводятся исследования о добавлении к стандартной терапии пробиотика, позволяющего уменьшить частоту стула и проявления метеоризма.
Появилась новая схема эрадикции бактерии – последовательная терапия, занимающая 10 дней. Её используют при неудаче использования схемы первой линии.
В первые 5 дней принимают:
Ингибитор протонной помпы – 2 раза в сутки;
Амоксициллин – 2000 мг/сутки.
В следующие 5 дней:
Ингибитор протонной помпы – 2 раза в сутки;
Кларитромицин – 1000 мг/сутки;
Тинидазол – 1000 мг/сутки.
По данным исследования, даже у пациентов, заражённых Helicobacter pylori с высокой резистентностью к Кларитромицину, эрадикция повысилась с 29% до 89%. У остальных больных с неудачной эрадикцией первой линии показатель повысился с 78% до 91%.
Протокол лечения хеликобактер пилори у взрослых
Основные протоколы эрадикции Helicobacter pylori у взрослых, рекомендованные Торонтским и Маастрихтским консенсусом 2016 года:
Эрадикационная терапия H.pylori как основа профилактики рака желудка
Владимир Трофимович Ивашкин, академик РАМН, доктор медицинских наук:
– Сейчас у нас состоится симпозиум Российской гастроэнтерологической ассоциации. И в рамках этого симпозиума пройдет международный совет экспертов, и он будет посвящен обсуждению вопроса канцеропревенции, то есть первичной преимущественно, желательно, конечно, первичной профилактике рака органов пищеварительной системы. Удалось ли что-нибудь сделать Российской гастроэнтерологической ассоциации, которая уделяет очень много времени и усилий по, во-первых, образованию врачей, в первую очередь, и, во-вторых, по продвижению современных методов профилактики онкологических заболеваний в области органов пищеварения? И я должен ответить на этот вопрос в определенной степени утвердительно, положительно. Наиболее часто встречающиеся заболевания органов пищеварительной системы – это рак желудка и колоректальный рак. Раки других органов, пищевода, поджелудочной железы, печени и так далее, конечно, всех нас тревожат, и они все, безусловно, нас заставляют искать возможности их профилактики. Но все-таки наиболее распространенные формы злокачественных заболеваний в области гастроэнтерологии – это рак желудка и колоректальный рак, рак толстой кишки. И я должен сказать, что все-таки Россия в числе других экономически развитых стран, то есть экономически развитые европейские страны и североамериканские страны, сейчас вошла в тренд снижения заболеваемости раком желудка. Так, Татьяна Львовна?
Татьяна Львовна Лапина, доцент, кандидат медицинских наук:
– Да, абсолютно верно, я эту статистику, с вашего разрешения, покажу.
Ивашкин В.Т.:
– И вот Татьяна Львовна эту статистику… Разные могут быть причины, вернее, даже разные есть причины. В том числе, улучшение качества питания населения, улучшение гигиены питания, все более и более широкое внедрение в нашу практику холодильников, рефрижераторов, которые позволяют продукты… более разнообразное питание, большее содержание витаминов в рационе, большее содержание в рационе антиоксидантов. Это на таком, популяционном уровне. Это, безусловно, нельзя отрицать. Это социальный вклад в эту проблему. Но мы, безусловно, должны отметить заслугу гастроэнтерологов, которые сумели убедить врачебное сообщество в том, что очень важным кофактором развития рака желудка является инфекция Helicobacter pylori. И все более и более расширяющееся понимание этого фактора привело к двум, по крайней мере, очень значимым следствиям. Первое следствие – общее снижение заболеваемости раком желудка в российской популяции, постепенное, тренд. И второе – гораздо меньшая частота хирургических вмешательств у пациентов с неосложненными язвами двенадцатиперстной, главным образом, кишки и желудка, антрального отдела желудка. Это два очень важных фактора. И, таким образом, в декабре проводился экспертный совет на Каширском шоссе в онкологическом центре российском по канцеропревенции. Так что не все безнадежно, наоборот, при значительных усилиях, наших с вами, в том числе, усилиях, есть перспектива постепенного снижения заболеваемости раком желудка и других форм рака. Сейчас Татьяна Львовна, я думаю, подтвердит нам, что наши усилия заслуживают одобрения и продолжения.
Лапина Т.Л.:
– Да, Владимир Трофимович. Я действительно должна сказать, что в России на протяжении конца прошлого и начала нынешнего века наблюдается тенденция к снижению заболеваемости раком желудка. Но, тем не менее, актуальность профилактики рака желудка не должна ни у кого вызывать сомнения. Действительно, рак желудка по данным нашей статистики занимает твердое четвертое место по заболеваемости. И показатель заболеваемости, соответственно, в 2011 году составил 26,8 на 100 тысяч населения. В чем проблема? Проблема в том, что, к сожалению, показатель смертности рака желудка составляет 23,23 на 100 тысяч населения. И по смертности рак желудка занимает второе место и у мужчин, и у женщин. И это говорит о том, что вероятно мы недостаточно активно внедряем меры раннего выявления опухоли, потому что чем позже поставлен диагноз, тем, естественно, хуже прогноз. Высчитано, что кумулятивный риск умереть от злокачественного новообразования желудка у мужчин в России составляет 2,6%, у женщин – 1%. Итак, о чем мы должны говорить? Мы, конечно, должны говорить о том, что вообще является современно парадигмой, общепринятой в мире и, в том числе, в европейских странах о том, что инфекция пилорического хеликобактера – наиболее доказанный фактор риска рака желудка. И, соответственно, стратегия профилактики рака желудка должна подразумевать элиминацию этой инфекции. Я цитирую положение четвертого Маастрихтского консенсуса, который очень деликатно рекомендует стратегию screen-and-treat по отношению к инфекции пилорического хеликобактера в популяции, где рак желудка составляет проблему здравоохранения.
Я думаю, что наша статистика показывает, что рак желудка и есть проблема здравоохранения в нашей стране. Итак, screen-and-treat. Соответственно, нужно наладить скрининг инфекции пилорического хеликобактера и проводить лечение инфекции пилорического хеликобактера не просто у пациента с дуоденальной язвой, а у пациента, по сути дела, без каких-либо имеющихся жалоб. Посильна ли нам сейчас эта задача, для нашей огромной страны с высокой частотой инфекции пилорического хеликобактера в популяции, которая в некоторых регионах превышает показатели 90%? Конечно, это очень и очень сложный вопрос. Вот эти вопросы профилактики рака желудка заложены в рекомендациях Российской гастроэнтерологической ассоциации по диагностике и лечению инфекции пилорического хеликобактера у взрослых, потому что Российская гастроэнтерологическая ассоциация называет желательным проведение эрадикационной терапии у лиц, имеющих инфекцию пилорического хеликобактера и у лиц, имеющих хронических гастрит.
То есть по рекомендации Российской гастроэнтерологической ассоциации врач должен задуматься о проведении эрадикации у любого Helicobacter pylori-позитивного пациента. И мне действительно очень приятно сказать, Владимир Трофимович, что, наверное, из таких умозрительных представлений о том, что заниматься профилактикой новообразований хорошо, Российская гастроэнтерологическая ассоциация действительно идет очень быстро к внедрению чисто практических, ясных для врача общей практики мероприятий, направленных на профилактику рака желудка. И создание таких рекомендаций и публикация их в авторитетном «Российском журнале гастроэнтерологии, гепатологии и колопроктологии» – это заметный шаг к реальной профилактике рака желудка. Мы совершенно четко даем инструмент для проведения эрадикационной терапии. Мы называем в качестве терапии первой линии стандартную тройную терапию: ингибитор протонной помпы, кларитромицин, амоксициллин. И благодаря тому, что в России имеет место широкое признание значения солей висмута, в том числе, и висмута трикалия дицитрата и в гастроэнтерологии, и в эрадикационной терапии в качестве такого компонента, который может быть использован в квадротерапии, мы рекомендуем висмут трикалия дицитрат. Это квадротерапия как альтернативная первая линия лечения или вторая линия лечения при неудаче стандартной тройной терапии.
Речь идет о схеме: ингибитор протонной помпы, тетрациклин, метронидазол, висмут трикалия дицитрат. Мы можем усилить стандартную тройную терапию путем очень простых и понятных для любого практикующего врача мер. Мы можем, во-первых, назначать более длительные схемы лечения, и сейчас, в общем, ни для кого не является неожиданным, что врач назначает эрадикационную терапию на 10-14 дней, а не на 7 дней, как, скажем, было более принято лет десять назад. Мы можем увеличить дозу ингибитора протонной помпы, мы можем добавить Saccharomyces boulardii, но, в том числе, не является, опять же, неожиданным для практикующего врача то, что добавление к стандартной терапии препарата висмута также может добавить к проценту эрадикации инфекции пилорического хеликобактера. Четвертый Маастрихтский консенсус рекомендует нам совершенно определенные показания с точки зрения профилактики рака желудка для проведения эрадикационной терапии. Это ближайшие родственники больных раком желудка, это, скажем так, вариант третичной профилактики рака желудка у пациентов после эндоскопической резекции или субтотальной резекции желудка по поводу рака, это больные с гастритом, называется выраженный пангастрит, гастрит с преимущественным поражением тела желудка, наличие выраженной атрофии. Это больные, которым проводится лечение с подавлением желудочной кислотности продолжительностью более одного года, больным со значимыми внешними факторами риска рака желудка: курение, профессиональные вредности. И, наконец, просто желание пациента, его страх заболеть раком желудка.
Соответственно, Российская гастроэнтерологическая ассоциация в ряде регионов приветствует региональные программы по организованному скринингу рака желудка, которые основаны на выделении популяции риска среди лиц старше 45 лет по уровню сывороточного пепсиногена. И, конечно, мы делаем очень большую работу для того, чтобы каждый практический врач на своем рабочем месте понимал, что его задача – проведение оппортунистического скрининга инфекции пилорического хеликобактера. Итак, задача организованного скрининга – выявить больных гастритом. Тех самых больных гастритом, которые проименованы в четвертом Маастрихтском консенсусе: выраженный пангастрит, гастрит с преимущественным поражением тела желудка, выраженная атрофия. Для этого существуют простые инструменты. В первую очередь, это изучение сывороточных маркеров атрофии различных отделов желудка и очень простой сывороточный маркер пепсиноген 1. Снижение пепсиногена 1 достоверно, и это доказано работами и под руководством Владимира Трофимовича Ивашкина, и в разных регионах России, коррелирует со степенью атрофии тела желудка.
Немножко сложнее вопросы диагностики инфекции пилорического хеликобактера, потому что мы должны, с одной стороны, говорить о серологических методах выявления инфекции для проведения скрининговых манипуляций. И мы должны, конечно, хорошо понимать, что для диагностики лечения, излечения пациента от инфекции пилорического хеликобактера самое важное место занимает дыхательный тест с мочевиной, меченной углеродом С13. И это имеет принципиально большое значение, именно в этих двух направлениях, мне думается, надо развивать диагностику инфекции пилорического хеликобактера с точки зрения практического здравоохранения. Проблемы, которые стоят перед врачом общей практики, перед участковым терапевтом, который понимает, что такое проведение оппортунистического скрининга, действительно очень велики. В первую очередь, врач, к которому приходит пациент по любому показанию, должен задуматься о наличии у пациента инфекции пилорического хеликобактера и понять, когда он обязательно должен этого пациента направить на определение антител к инфекции пилорического хеликобактера и назначить ему такое лечение. Он должен проводить другие меры профилактики рака желудка.
Например, объяснить вред курения, добиться прекращения курения у пациента, добиться нормализации веса, знать профессиональные вредности, которые приводят к раку желудка. И, конечно, работать с изменением рациона питания, что тоже, в общем, достаточно сложно, и здесь нужно четко представлять, что необходимо изменить рацион питания на более здоровое с увеличением дозы свежих фруктов и овощей, молочных продуктов, цельнозерновых продуктов. При этом снизить содержание соли, маринада, алкоголя. Мне бы хотелось акцентировать внимание практикующих врачей на двух очень четких аспектах, которые в любом случае заставляют подумать о необходимости диагностики и лечения инфекции пилорического хеликобактера с точки зрения профилактики рака желудка. Это наличие ближайших родственников, больных раком желудка. Мы знаем, что семейный анамнез – фактор риска рака желудка, и мне бы хотелось остановиться на одном из последних исследований случай-контроль, это американская популяция. В качестве контролей были изучены 147 больных раком пищевода, 182 пациента аденокарциномы кардии и 285 пациентов дистальной аденокарциномы.
Это исследование, в том числе, достаточно интересно тем, что выявляет разные факторы риска для разных опухолей желудочно-кишечного тракта. И очень важно, что еще раз было доказано, что с высокой статистической показательностью семейный анамнез рака желудка связан с дистальной аденокарциномой, отношение шансов больше 2. И при раннем начале заболевания, диагноз установлен до 50 лет, отношение шансов, по сути дела, составляет 3. И еще один момент, на который любой практический врач, мне кажется, должен обратить внимание и подумать о проведении профилактической эрадикационной терапии. Это больные, которым проводится лечение с подавлением желудочной кислотности продолжительностью более 1 года. И таких пациентов достаточно много, потому что это пациенты с гастроэзофагеальной рефлюксной болезнью, которые очень часто встречаются в российской популяции, и пациенты, которые принимают ингибиторы протонной помпы для профилактики НПВС-гастропатии.
Здесь, наверное, нечего добавить к очередному положению четвертого Маастрихтского консенсуса, длительное лечение ингибитором протонной помпы Helicobacter pylori-позитивных лиц, ассоциировано с перемещением популяции, в основном, в тело желудка с развитием там активного гастрита и ускорением процесса потери специализированных желез, то есть к ускорению формирования атрофического гастрита тела желудка. И, безусловно, сейчас, конечно, нет четких данных о том, что лечение инфекции пилорического хеликобактера у таких пациентов снижает частоту рака желудка, но я думаю, что на практическом уровне мы очень хорошо понимаем, что так оно и должно быть. Вот, собственно, мне кажется, основное, что мы должны пропагандировать среди практикующих врачей, в первую очередь, среди врачей общей практики и участковых терапевтов с точки зрения повседневной работы по профилактике рака желудка. Спасибо.
Более быстрое, чем у метронидазола действие на ДНК Нр, более высокая активность in vitro, быстрее проникает в бактерии
Эффективность схемы эрадикации, доказанная по всему миру
(данные мета-анализа) 8| Количество исследований | Всего пациентов | Эффективность эрадикации | 53 | 3057 | 89-91% |
| ||
Данные метанализа (Arkham et al, 1996) показали, что эффективность эрадикации не зависит от дозы кларитромицина 7
Эрадикация H. рylori: современный взгляд на старую проблему
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Распространенность инфекции Helicobacter pylori (H. pylori) остается на очень высоком уровне во всем мире и в России колеблется от 65 до 86% в зависимости от региона. H. pylori представляет собой этиологический фактор развития таких заболеваний, как гастрит, язвенная болезнь желудка и двенадцатиперстной кишки, MALT-лимфома, является доказанным канцерогеном для рака желудка. Поэтому наиболее эффективной мерой профилактики рака желудка является эрадикационная терапия H. pylori. Согласно Киотскому глобальному консенсусу по Helicobacter pylori-ассоциированному гастриту (сентябрь 2015 г.), всем лицам, инфицированным H. pylori, должна быть предложена эрадикационная терапия, если для этого нет каких-либо препятствий (коморбидность, высокая вероятность реинфекции в популяции). Российские и международные рекомендации говорят о том, что в регионах, где резистентность к кларитромицину не превышает 15–20%, в качестве схемы первой линии лечения должна применяться 14-дневная стандартная тройная терапия. В регионах с высокой резистентностью к кларитромицину может использоваться квадротерапия с препаратом висмута. У пациентов, не ответивших на стандартную тройную терапию, в качестве терапии второй линии может быть рекомендована квадротерапия с висмутом или 14-дневная тройная терапия с левофлоксацином. Мерами, позволяющими повысить эффективность эрадикации, являются назначение удвоенной дозы ИПП, подробное объяснение пациенту режима приема лекарственных препаратов.
Ключевые слова: Helicobacter pylori, эрадикация, язвенная болезнь, рак желудка, ИПП.
Для цитирования: Евсютина Ю.В. Эрадикация H. рylori: современный взгляд на старую проблему // РМЖ. Гастроэнтерология. 2016. № 11. С. 673–677.
Для цитирования: Евсютина Ю.В. Эрадикация H. рylori: современный взгляд на старую проблему. РМЖ. 2016;11:673-677.
Eradication of H. рylori: a modern solution for an old problem
Evsyutina Yu.V.
I.M. Sechenov First Moscow State Medical University, Moscow, Russia
The prevalence of Helicobacter pylori (H. pylori) remains high throughout the world and varies across Russian regions, ranging from to 65% to 86%. H. pylori is the causative agent for a number of conditions, i.e., gastritis, gastric and duodenal ulcer, and MALT lymphoma. This pathogen is also recognized as a carcinogen for gastric cancer. Hence, the most effective preventive measure for gastric cancer is H. pylori eradication. The Kyoto global consensus report on Helicobacter pylori gastritis (September 2015) stated that eradication therapy should be recommended to all patients infected with H. pylori if there are no contraindications (i.e., comorbidities, high reinfection probability in the population, etc.). According to the Russian and international guidelines, in areas with low clarithromycin resistance rate (less than 15-20%), 14-day triple therapy should be prescribed as a first-line treatment. In areas with high clarithromycin resistance rate, bismuth-containing quadruple therapy should be used. In non-responders to the triple therapy, bismuth-containing quadruple therapy or 14-day levofloxacin-containing triple therapy should be considered. A double dose of proton pump inhibitor and a detailed explanation of drug regimen may increase the efficacy of eradication treatment.
Key words: Helicobacter pylori, eradication, peptic ulcer, gastric cancer, proton pump inhibitor.
For citation: Evsyutina Yu.V. Eradication of H. рylori: a modern solution for an old problem // RMJ. Gastroenterology. 2016. № 11. P. 673–677.
В статье приведен современный взгляд проблему эрадикации H. рylori
Последовательная терапия эрадикации инфекции Helicobacter pylori
Результаты систематического обзора и мета-анализа
Инфекция H. pylori является причиной развития язв желудка и 12-ти перстной кишки, MALT-лимфом желудка и рака желудка. В настоящее время предложено большое количество схем эрадикационной терапии: стандартная тройная терапия с применением амоксициллина, кларитромицина и ингибитора протонной помпы (ИПП); квадротерапия на основе препаратов висмута, последовательная и сопутствующая терапии. Одной из глобальных проблем на настоящий момент является растущая резистентность к кларитромицину и метронидазолу. Чтобы преодолеть эту проблему, в клинической практике все чаще стала применяться последовательная терапия, включающая назначение на первые пять дней ИПП и амоксициллина в дозе 1 г 2 раза в день и на последующие пять дней – ИПП, кларитромицин 500 мг 2 раза в день и препарата из группы нитромидазолов в дозе 500 мг 2 раза в день. Недавние исследования, сравнивающие эту схему терапии с тройной терапией, дают обнадеживающие результаты и позволяют говорить об эффективности новой эрадикационной схеме.
Цель
Сравнить последовательную эрадикационную терапию с другими схемами эрадикации инфекции H. pylori.
Материалы и методы
В исследование были включены рандомизированные контролируемые исследования (РКИ), найденные по данным поиска в таких базах данных как Medline (c 1950 по май 2013), Embase (c 1980 по мая 2013) и Cochrane Central Register of Controlled Trials (по май 2013), в которых проводилось сравнение последовательной терапии с другими эрадикационными схемами у пациентов старше 18 лет.
Результаты
Последовательная терапия против 7-дневной тройной терапии.
По результатам 22 РКИ эффективнее оказалась последовательная терапия (RR=1,21, 95% CI: 1,17-1,25). Всего проводилось сравнение 2449 пациентов, у которых применялась последовательная терапия с 2566, у которых проводилась 7-ми дневная тройная терапия, эффективность эрадикации составила 86,5% (95% CI: 82,9-89,7%) и 71,5 (95% CI: 68,4-74,5%) соответственно.
В одном из исследований сравнивалась эффективность последовательной терапии с тройной терапией с применением ИПП, амоксициллина и метронидазола и ИПП, амоксициллина и кларитромицина, последовательная терапия оказалась эффективнее первой на 15,9% и второй на 24,0%.
Последовательная терапия против 10-дневной тройной терапии.
По результатам 14 РКИ была показано лишь небольшое отличие в эффективности последовательной схемы эрадикации (RR=1,11, 95% CI: 1,04-1,19).
Всего в исследования было включено 1368 пациента, у которых проводилось лечение компонентами последовательной схемы и 1376 больных, у которых эрадикация осуществлялась с использованием 10-ти дневной тройной терапии, эффективность составила 84,3% и 75,3% соответственно.
Последовательная терапия против 14-дневной тройной терапии.
Результаты 7 исследований позволяют говорить об отсутствии различий в эффективности при сравнении двух вышеперечисленных схем (RR=1,00, 95% CI: 0,94-1,06).
Последовательная терапия против квадротерапии на основе препаратов висмута.
Анализ результатов 3 РКИ не показал преимуществ одной эрадикационной схемы перед другой (RR=1,01, 95% CI: 0,95-1,06).
Эффективность эрадикации у 546 пациентов, у которых применялась последовательная терапия составила 86,2%, а у 545 пациентов, у которых проводилась эрадикация препаратами, входящими в состав квадротерапии – 84,9%.
Результаты исследований, не вошедших в мета-анализ
Последовательная терапия против последовательной терапии с применением левофлоксацина. В трех исследованиях сравнивалась эффективность последовательной терапии с применением кларитромицина и последовательной терапии, в которой вместо кларитромицина применялся левофлоксацин в дозе от 500 до 1000 мг в сутки.
Среди 240 пациентов, у которых применялась схема с использованием 1000 мг левофлоксацина в сутки процент эрадикации составил 90,0%, а среди 240 пациентов у которых проводилась классическая последовательная терапия с применением кларитромицина, эффективность была 78,7%. Частота побочных эффектов была примерно одинаковой (24,3% и 24,4% соответственно).
При сравнении терапии с использованием 500 мг в день левофлоксацина (n=241) и классической последовательной схемы эрадикации (n=240) эффективность в первом случае составляла 89,8%, а во втором – 79,5%. Частота развития побочных эффектов составляла 13,8% и 14,3% соответственно. Анализ результатов позволил сделать вывод о том, что последовательная схема эрадикации с применением левофлоксацина эффективнее, чем последовательная схема с применением кларитромицина.
Сравнение 10-дневной и 14-дневной последовательных схем эрадикации.
В двух РКИ сравнивалась длительность последовательной терапии: у 340 пациентов проводилась 10-ти дневная последовательная терапия и у 340 – 14-ти дневная. Эффективность проводимой терапии составила 87,6% и 89,7% соответственно, что не доказало, что увеличение длительности терапии повышает ее эффективность.
Заключение
Результаты мета-анализа показывают, что последовательная схема эрадикации инфекции Helicobacter pylori эффективнее, чем 7-ми дневная стандартная тройная терапия и показывает похожую эффективность при сравнении со схемами эрадикации, назначаемыми более чем на 10 дней и включающими более 2-х антимикробных препаратов.
Эрадикация хеликобактер пилори: какой препарат выбрать?
Ещё полвека назад существовало несколько теорий, предлагающих свой вариант причин появления язвенной болезни желудка и кишечника. Переломным моментом стал 1979 год, когда в результате научного исследования было доказано, что первоисточник этой проблемы – бактерия хеликобактер пилори (Helicobacter pylori), в норме благополучно существующая в ЖКТ более половины всех представителей человечества. Любое снижение иммунной защиты – благополучный повод для размножения колоний хеликобактер пилори. Для лечения хелиобактериоза созданы схемы эрадикции патогенной бактерии из организма человека.
Схема эрадикционной терапии хеликобактер пилори
При выборе врачом схемы эрадикционной терапии в каждом конкретном случае приходится учитывать следующие факторы:
Прогнозируемая длительность лечения;
Клиническая картина данного случая хелиобактериоза;
Стоимость препаратов, входящих в схему лечения.
Российская Гастроэнтерологическая ассоциация и Российская группа по изучению Helicobacter pylori рекомендует принять за основу комбинированную трёхкомпонентную схему терапии, удовлетворяющую следующим принципам:
Способность провести эрадикцию бактерии не менее чем в 80% случаев;
Отсутствие побочных эффектов, вынуждающих лечащего врача отменить схему лечения, или провоцирующих больного на прекращение приёма препаратов (допускается до 5% таких случаев);
эффективность даже при коротком курсе не дольше 1-2 недель.
В основе методики назначения эрадикционной терапии лежат рекомендации, выработанные мировым сообществом гастроэнтерологов в Маастрихте в 1996 г., и обновленные в 2000 г.
Рекомендации Второго Маастрихтского соглашения по проведению антихеликобактерной терапии:
При неосложнённых случаях язвенной болезни после курса эрадикционной терапии не требуется использование антисекреторных препаратов.
Показания для эрадикционной терапии кроме язвенной болезни: MALT-лимфома, атрофический гастрит, близкие родственные связи с больным раком желудка, состояние после резекции по поводу рака желудка, желание пациента.
Лечение инфекции Helicobacter pylori должно предусматривать возможность неудачи первой линии эрадикционной терапии и необходимость использования второй линии в случае сохранения бактерии в организме. В схему первой линии эрадикции (тройную терапию) предлагается включить 2 антибиотика: Кларитромицин + Амоксициллин (или Метронидазол) и ингибитор протонной помпы (или Ранитидин). Она длится не более 7 дней. При неудаче рекомендуется применять схему второй линии (квадротерапию), включающую в себя 2 антибиотика: Тетрациклин + Метронидазол, препараты висмута и ингибитор протонной помпы. Длительность использования квадротерапии – 7 дней.
В настоящее время в практике не применяются специфические антибактериальные препараты, пробиотики и вакцины, направленные исключительно против Helicobacter pylori, они пока находятся в стадии разработки.
Разработчики Маастрихтских рекомендаций исключили из схемы лечения привычную для России комбинацию: Амоксициллин + Метронидазол + блокатор протонной помпы из-за повышения резистентности Helicobacter pylori к производным нитроимидазолов. Исследования российских учёных подтвердили низкую эффективность этой комбинации (всего 30%). Российские гастроэнтерологи в эрадикционной терапии первой линии часто используют доступную и эффективную тройную терапию, включающую в себя препараты висмута + Амоксициллин + Фуразолидон. Совершенствование антихеликобактерной терапии продолжается, В 2005 году в Нидерландах были разработаны современные схемы эрадикционной терапии первой, второй, третьей линии.
Первая линия эрадикции хеликобактер пилори
трёхкомпонентная схема первой линии получила своё название за то, что она состоит из трёх препаратов:
ингибитор протонной помпы на основе Омепразола, регулирующий активность кислой среды желудочного сока.
Ингибиторы протонной помпы позволяют избавиться от множества негативных проявлений язвы и гастрита, вызванных повышенной кислотностью среды желудка, а так же избежать чрезмерно строгих ограничений, вносимых в рацион питания больного язвенной болезнью. Тем не менее, ограничения всё-таки сохраняются, хотя и не такие строгие.
Допускается замена Амоксициллина на антибиотик Нифурател или на Метронидазол. По показаниям гастроэнтеролог может назначить в схему 4 препарат, имеющий в основе производные висмута. В норме такие лекарства включают в эрадикционную схему второй линии, но их свойства положительно влияют на течение процесса купирования воспалительного процесса. На поверхности желудка образуется защитное покрытие, снимающее симптомы воспаления и боль.
Облегченная схема для больных пожилого возраста:
Ингибитор протонной помпы;
Для увеличения эффективности стандартной терапии первой линии предлагается удвоить срок её применения – с 7 до 14 дней. Ожидаемая эффективность – до 95%. При неэффективности лечения врач рекомендует перейти на вторую линию эрадикционной терапии.
Вторая линия эрадикции хеликобактер пилори
Четыре компонента эрадикционной схемы второй линии:
2 антибиотика: Тетрациклин + Метронидазол, или Амоксициллин + препарат из группы нитрофуранов;
Ингибитор протонной помпы;
Препараты на основе висмута – отличные цитопротекторы, восстанавливающие структуру клеток слизистой желудка и кишечника и их устойчивость к агрессивному воздействию кислоты и продуктов жизнедеятельности Helicobacter pylori. Кроме того, они обладают бактерицидным действием, до минимума снижают риск рецидивов хелиобактериоза. При планировании схемы эрадикции второй линии не рекомендуется использовать уже применяемые ранее антибиотики. Эффективная, доступная и дешевая схема квадротерапия с висмутом тоже не лишена недостатков:
Большое количество принимаемых таблеток (18 штук в сутки);
Частые побочные эффекты;
4-х кратный режим дозирования.
Для усиления эффективности терапии препаратами висмута на время лечения из рациона исключают фрукты, соки, молоко. Длительность терапии второй линии – 10-14 дней.
Третья линия эрадикции хеликобактер пилори
Исключительно редко приходится переходить на третью линию эрадикционной терапии, но такая возможность всё-таки существует. Перед началом реализации третьей схемы пациента тестируют на чувствительность штамма Helicobacter pylori к антибиотикам.
Препараты 3 линии:
Два антибиотика, не использовавшихся ранее и показавших при лабораторной диагностике наивысшую степень эффективности;
Ингибиторы протонной помпы.
Лекарственные средства на основе висмута (трикалий дицитрат висмута) обладают комплексным действием:
Снимают проявления диспепсии (вздутие живота, изжогу, гастралгию);действуют в отношении Helicobacter pylori, как эффективное бактерицидное средство;
Стимулируют регенерацию повреждений более глубоких слоёв стенок желудка.
Терапия третьей линии по Маастрихтским рекомендациям третьего созыва включает препараты из группы рифамицинов (Рифабутин) и хинолонов (Левофлоксацин). Такое сочетание стало эффективным в 91% случаев. Резистентность Helicobacter pylori к Рифабутину очень мала, поэтому его включение в протокол лечения совместно и Амоксициллином и ингибитором протонной помпы позволяет повысить эффективность терапии и даже игнорировать резистентность бактерии к Метронидазолу и Кларитромицину.
Выбор препаратов при необходимости проведения повторного курса эрадикционной терапии
И первая, и вторая, и даже третья схема терапии Helicobacter pylori может быть неэффективной, когда процент эрадикции составляет 80% или менее случаев целевого достижения цели лечения. Эффективность лечения снижается по причине резистентности бактерии к антибиотикам, поэтому исследователи проблемы не прекращают поиск лучших схем.
Не вызывает опасения резистентность Helicobacter pylori к Амоксициллину (менее 1%), к Тетрациклину (близка к 0).
Количество резистентных штаммов бактерии к другим антибактериальным препаратам:
Это объясняется частым назначением антибиотиков из группы макролидов в педиатрической и терапевтической практике. Немаловажное значение в успешности эрадикционной терапии имеют ингибиторы протонной помпы, создающие в ЖКТ благоприятную среду для применения антибиотиков. При низком качестве препаратов этой группы эффективность антибактериальных средств тоже снижается.
Проводятся исследования о добавлении к стандартной терапии пробиотика, позволяющего уменьшить частоту стула и проявления метеоризма.
Появилась новая схема эрадикции бактерии – последовательная терапия, занимающая 10 дней. Её используют при неудаче использования схемы первой линии.
В первые 5 дней принимают:
Ингибитор протонной помпы – 2 раза в сутки;
Амоксициллин – 2000 мг/сутки.
В следующие 5 дней:
Ингибитор протонной помпы – 2 раза в сутки;
Кларитромицин – 1000 мг/сутки;
Тинидазол – 1000 мг/сутки.
По данным исследования, даже у пациентов, заражённых Helicobacter pylori с высокой резистентностью к Кларитромицину, эрадикция повысилась с 29% до 89%. У остальных больных с неудачной эрадикцией первой линии показатель повысился с 78% до 91%.
Протокол лечения хеликобактер пилори у взрослых
Основные протоколы эрадикции Helicobacter pylori у взрослых, рекомендованные Торонтским и Маастрихтским консенсусом 2016 года:
Эрадикационная терапия H.pylori как основа профилактики рака желудка
Владимир Трофимович Ивашкин, академик РАМН, доктор медицинских наук:
– Сейчас у нас состоится симпозиум Российской гастроэнтерологической ассоциации. И в рамках этого симпозиума пройдет международный совет экспертов, и он будет посвящен обсуждению вопроса канцеропревенции, то есть первичной преимущественно, желательно, конечно, первичной профилактике рака органов пищеварительной системы. Удалось ли что-нибудь сделать Российской гастроэнтерологической ассоциации, которая уделяет очень много времени и усилий по, во-первых, образованию врачей, в первую очередь, и, во-вторых, по продвижению современных методов профилактики онкологических заболеваний в области органов пищеварения? И я должен ответить на этот вопрос в определенной степени утвердительно, положительно. Наиболее часто встречающиеся заболевания органов пищеварительной системы – это рак желудка и колоректальный рак. Раки других органов, пищевода, поджелудочной железы, печени и так далее, конечно, всех нас тревожат, и они все, безусловно, нас заставляют искать возможности их профилактики. Но все-таки наиболее распространенные формы злокачественных заболеваний в области гастроэнтерологии – это рак желудка и колоректальный рак, рак толстой кишки. И я должен сказать, что все-таки Россия в числе других экономически развитых стран, то есть экономически развитые европейские страны и североамериканские страны, сейчас вошла в тренд снижения заболеваемости раком желудка. Так, Татьяна Львовна?
Татьяна Львовна Лапина, доцент, кандидат медицинских наук:
– Да, абсолютно верно, я эту статистику, с вашего разрешения, покажу.
Ивашкин В.Т.:
– И вот Татьяна Львовна эту статистику… Разные могут быть причины, вернее, даже разные есть причины. В том числе, улучшение качества питания населения, улучшение гигиены питания, все более и более широкое внедрение в нашу практику холодильников, рефрижераторов, которые позволяют продукты… более разнообразное питание, большее содержание витаминов в рационе, большее содержание в рационе антиоксидантов. Это на таком, популяционном уровне. Это, безусловно, нельзя отрицать. Это социальный вклад в эту проблему. Но мы, безусловно, должны отметить заслугу гастроэнтерологов, которые сумели убедить врачебное сообщество в том, что очень важным кофактором развития рака желудка является инфекция Helicobacter pylori. И все более и более расширяющееся понимание этого фактора привело к двум, по крайней мере, очень значимым следствиям. Первое следствие – общее снижение заболеваемости раком желудка в российской популяции, постепенное, тренд. И второе – гораздо меньшая частота хирургических вмешательств у пациентов с неосложненными язвами двенадцатиперстной, главным образом, кишки и желудка, антрального отдела желудка. Это два очень важных фактора. И, таким образом, в декабре проводился экспертный совет на Каширском шоссе в онкологическом центре российском по канцеропревенции. Так что не все безнадежно, наоборот, при значительных усилиях, наших с вами, в том числе, усилиях, есть перспектива постепенного снижения заболеваемости раком желудка и других форм рака. Сейчас Татьяна Львовна, я думаю, подтвердит нам, что наши усилия заслуживают одобрения и продолжения.
Лапина Т.Л.:
– Да, Владимир Трофимович. Я действительно должна сказать, что в России на протяжении конца прошлого и начала нынешнего века наблюдается тенденция к снижению заболеваемости раком желудка. Но, тем не менее, актуальность профилактики рака желудка не должна ни у кого вызывать сомнения. Действительно, рак желудка по данным нашей статистики занимает твердое четвертое место по заболеваемости. И показатель заболеваемости, соответственно, в 2011 году составил 26,8 на 100 тысяч населения. В чем проблема? Проблема в том, что, к сожалению, показатель смертности рака желудка составляет 23,23 на 100 тысяч населения. И по смертности рак желудка занимает второе место и у мужчин, и у женщин. И это говорит о том, что вероятно мы недостаточно активно внедряем меры раннего выявления опухоли, потому что чем позже поставлен диагноз, тем, естественно, хуже прогноз. Высчитано, что кумулятивный риск умереть от злокачественного новообразования желудка у мужчин в России составляет 2,6%, у женщин – 1%. Итак, о чем мы должны говорить? Мы, конечно, должны говорить о том, что вообще является современно парадигмой, общепринятой в мире и, в том числе, в европейских странах о том, что инфекция пилорического хеликобактера – наиболее доказанный фактор риска рака желудка. И, соответственно, стратегия профилактики рака желудка должна подразумевать элиминацию этой инфекции. Я цитирую положение четвертого Маастрихтского консенсуса, который очень деликатно рекомендует стратегию screen-and-treat по отношению к инфекции пилорического хеликобактера в популяции, где рак желудка составляет проблему здравоохранения.
Я думаю, что наша статистика показывает, что рак желудка и есть проблема здравоохранения в нашей стране. Итак, screen-and-treat. Соответственно, нужно наладить скрининг инфекции пилорического хеликобактера и проводить лечение инфекции пилорического хеликобактера не просто у пациента с дуоденальной язвой, а у пациента, по сути дела, без каких-либо имеющихся жалоб. Посильна ли нам сейчас эта задача, для нашей огромной страны с высокой частотой инфекции пилорического хеликобактера в популяции, которая в некоторых регионах превышает показатели 90%? Конечно, это очень и очень сложный вопрос. Вот эти вопросы профилактики рака желудка заложены в рекомендациях Российской гастроэнтерологической ассоциации по диагностике и лечению инфекции пилорического хеликобактера у взрослых, потому что Российская гастроэнтерологическая ассоциация называет желательным проведение эрадикационной терапии у лиц, имеющих инфекцию пилорического хеликобактера и у лиц, имеющих хронических гастрит.
То есть по рекомендации Российской гастроэнтерологической ассоциации врач должен задуматься о проведении эрадикации у любого Helicobacter pylori-позитивного пациента. И мне действительно очень приятно сказать, Владимир Трофимович, что, наверное, из таких умозрительных представлений о том, что заниматься профилактикой новообразований хорошо, Российская гастроэнтерологическая ассоциация действительно идет очень быстро к внедрению чисто практических, ясных для врача общей практики мероприятий, направленных на профилактику рака желудка. И создание таких рекомендаций и публикация их в авторитетном «Российском журнале гастроэнтерологии, гепатологии и колопроктологии» – это заметный шаг к реальной профилактике рака желудка. Мы совершенно четко даем инструмент для проведения эрадикационной терапии. Мы называем в качестве терапии первой линии стандартную тройную терапию: ингибитор протонной помпы, кларитромицин, амоксициллин. И благодаря тому, что в России имеет место широкое признание значения солей висмута, в том числе, и висмута трикалия дицитрата и в гастроэнтерологии, и в эрадикационной терапии в качестве такого компонента, который может быть использован в квадротерапии, мы рекомендуем висмут трикалия дицитрат. Это квадротерапия как альтернативная первая линия лечения или вторая линия лечения при неудаче стандартной тройной терапии.
Речь идет о схеме: ингибитор протонной помпы, тетрациклин, метронидазол, висмут трикалия дицитрат. Мы можем усилить стандартную тройную терапию путем очень простых и понятных для любого практикующего врача мер. Мы можем, во-первых, назначать более длительные схемы лечения, и сейчас, в общем, ни для кого не является неожиданным, что врач назначает эрадикационную терапию на 10-14 дней, а не на 7 дней, как, скажем, было более принято лет десять назад. Мы можем увеличить дозу ингибитора протонной помпы, мы можем добавить Saccharomyces boulardii, но, в том числе, не является, опять же, неожиданным для практикующего врача то, что добавление к стандартной терапии препарата висмута также может добавить к проценту эрадикации инфекции пилорического хеликобактера. Четвертый Маастрихтский консенсус рекомендует нам совершенно определенные показания с точки зрения профилактики рака желудка для проведения эрадикационной терапии. Это ближайшие родственники больных раком желудка, это, скажем так, вариант третичной профилактики рака желудка у пациентов после эндоскопической резекции или субтотальной резекции желудка по поводу рака, это больные с гастритом, называется выраженный пангастрит, гастрит с преимущественным поражением тела желудка, наличие выраженной атрофии. Это больные, которым проводится лечение с подавлением желудочной кислотности продолжительностью более одного года, больным со значимыми внешними факторами риска рака желудка: курение, профессиональные вредности. И, наконец, просто желание пациента, его страх заболеть раком желудка.
Соответственно, Российская гастроэнтерологическая ассоциация в ряде регионов приветствует региональные программы по организованному скринингу рака желудка, которые основаны на выделении популяции риска среди лиц старше 45 лет по уровню сывороточного пепсиногена. И, конечно, мы делаем очень большую работу для того, чтобы каждый практический врач на своем рабочем месте понимал, что его задача – проведение оппортунистического скрининга инфекции пилорического хеликобактера. Итак, задача организованного скрининга – выявить больных гастритом. Тех самых больных гастритом, которые проименованы в четвертом Маастрихтском консенсусе: выраженный пангастрит, гастрит с преимущественным поражением тела желудка, выраженная атрофия. Для этого существуют простые инструменты. В первую очередь, это изучение сывороточных маркеров атрофии различных отделов желудка и очень простой сывороточный маркер пепсиноген 1. Снижение пепсиногена 1 достоверно, и это доказано работами и под руководством Владимира Трофимовича Ивашкина, и в разных регионах России, коррелирует со степенью атрофии тела желудка.
Немножко сложнее вопросы диагностики инфекции пилорического хеликобактера, потому что мы должны, с одной стороны, говорить о серологических методах выявления инфекции для проведения скрининговых манипуляций. И мы должны, конечно, хорошо понимать, что для диагностики лечения, излечения пациента от инфекции пилорического хеликобактера самое важное место занимает дыхательный тест с мочевиной, меченной углеродом С13. И это имеет принципиально большое значение, именно в этих двух направлениях, мне думается, надо развивать диагностику инфекции пилорического хеликобактера с точки зрения практического здравоохранения. Проблемы, которые стоят перед врачом общей практики, перед участковым терапевтом, который понимает, что такое проведение оппортунистического скрининга, действительно очень велики. В первую очередь, врач, к которому приходит пациент по любому показанию, должен задуматься о наличии у пациента инфекции пилорического хеликобактера и понять, когда он обязательно должен этого пациента направить на определение антител к инфекции пилорического хеликобактера и назначить ему такое лечение. Он должен проводить другие меры профилактики рака желудка.
Например, объяснить вред курения, добиться прекращения курения у пациента, добиться нормализации веса, знать профессиональные вредности, которые приводят к раку желудка. И, конечно, работать с изменением рациона питания, что тоже, в общем, достаточно сложно, и здесь нужно четко представлять, что необходимо изменить рацион питания на более здоровое с увеличением дозы свежих фруктов и овощей, молочных продуктов, цельнозерновых продуктов. При этом снизить содержание соли, маринада, алкоголя. Мне бы хотелось акцентировать внимание практикующих врачей на двух очень четких аспектах, которые в любом случае заставляют подумать о необходимости диагностики и лечения инфекции пилорического хеликобактера с точки зрения профилактики рака желудка. Это наличие ближайших родственников, больных раком желудка. Мы знаем, что семейный анамнез – фактор риска рака желудка, и мне бы хотелось остановиться на одном из последних исследований случай-контроль, это американская популяция. В качестве контролей были изучены 147 больных раком пищевода, 182 пациента аденокарциномы кардии и 285 пациентов дистальной аденокарциномы.
Это исследование, в том числе, достаточно интересно тем, что выявляет разные факторы риска для разных опухолей желудочно-кишечного тракта. И очень важно, что еще раз было доказано, что с высокой статистической показательностью семейный анамнез рака желудка связан с дистальной аденокарциномой, отношение шансов больше 2. И при раннем начале заболевания, диагноз установлен до 50 лет, отношение шансов, по сути дела, составляет 3. И еще один момент, на который любой практический врач, мне кажется, должен обратить внимание и подумать о проведении профилактической эрадикационной терапии. Это больные, которым проводится лечение с подавлением желудочной кислотности продолжительностью более 1 года. И таких пациентов достаточно много, потому что это пациенты с гастроэзофагеальной рефлюксной болезнью, которые очень часто встречаются в российской популяции, и пациенты, которые принимают ингибиторы протонной помпы для профилактики НПВС-гастропатии.
Здесь, наверное, нечего добавить к очередному положению четвертого Маастрихтского консенсуса, длительное лечение ингибитором протонной помпы Helicobacter pylori-позитивных лиц, ассоциировано с перемещением популяции, в основном, в тело желудка с развитием там активного гастрита и ускорением процесса потери специализированных желез, то есть к ускорению формирования атрофического гастрита тела желудка. И, безусловно, сейчас, конечно, нет четких данных о том, что лечение инфекции пилорического хеликобактера у таких пациентов снижает частоту рака желудка, но я думаю, что на практическом уровне мы очень хорошо понимаем, что так оно и должно быть. Вот, собственно, мне кажется, основное, что мы должны пропагандировать среди практикующих врачей, в первую очередь, среди врачей общей практики и участковых терапевтов с точки зрения повседневной работы по профилактике рака желудка. Спасибо.