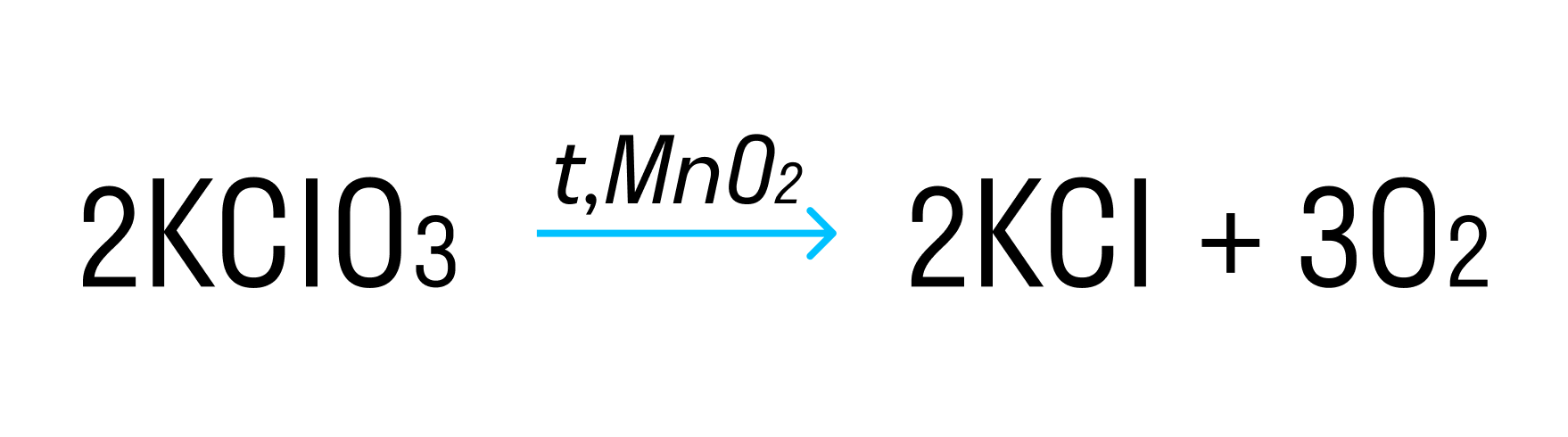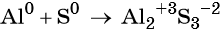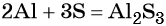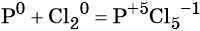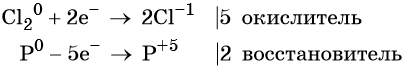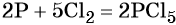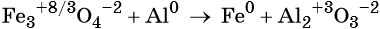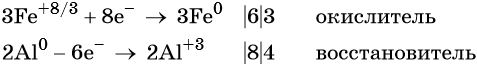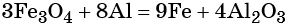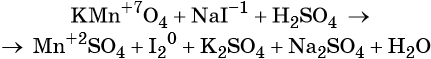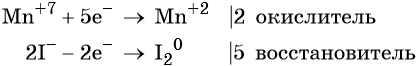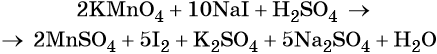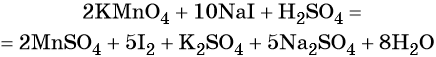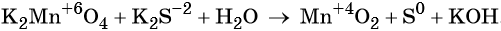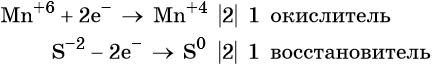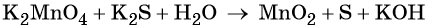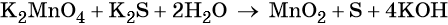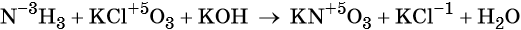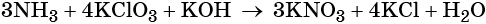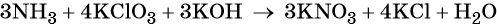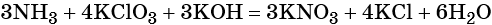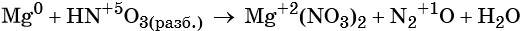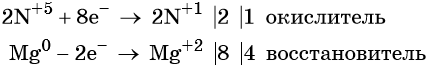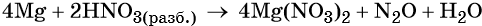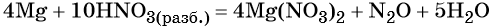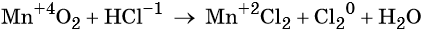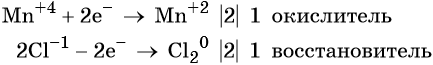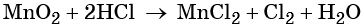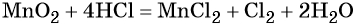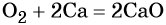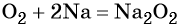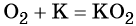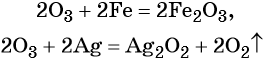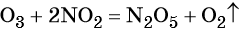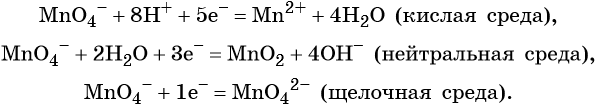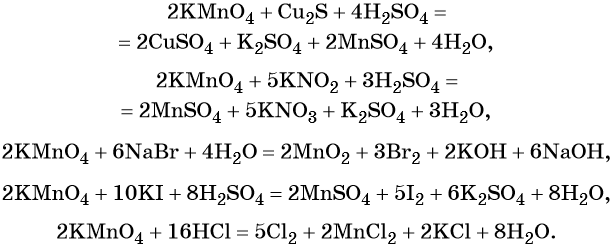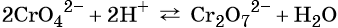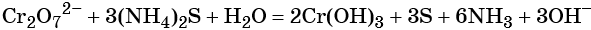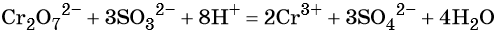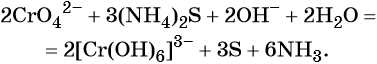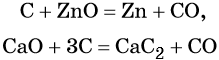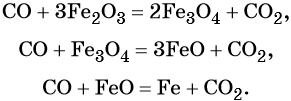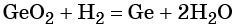Как делать овр
Как делать овр
Окислительно-восстановительные реакции
11 класс, ЕГЭ/ОГЭ
Что такое ОВР
Окислительно-восстановительная реакция (ОВР) — это реакция, которая протекает с изменением степеней окисления.
В такой реакции всегда участвуют вещество-окислитель и вещество-восстановитель. Другие вещества могут выступать в качестве среды, в которой протекает данная реакция.
Конечно, в каждом правиле есть исключения. Например, реакция диспропорционирования галогенов в горячем растворе щелочи выглядит так: Br2 + KOH = KBrO3 + KBr + H2O. Здесь и окислителем, и восстановителем является простое вещество бром (Br2).
Теперь посмотрим внимательнее на вещества — участники окислительно-восстановительных реакций.
Окислитель — вещество, в состав которого входит ион или атом, который в процессе реакции будет принимать электроны, тем самым понижая свою степень окисления.
Восстановитель — вещество, в состав которого входит ион или атом, который в процессе реакции будет отдавать электроны, тем самым повышая свою степень окисления.
Из определений понятно, что реакция включает два противоположных по действиям явления: процесс окисления и процесс восстановления. Процесс восстановления — это процесс принятия электронов, а процесс окисления — процесс отдачи электронов. Оба процесса протекают одновременно: окислитель восстанавливается, а восстановитель окисляется.
Вот мы и узнали общие закономерности протекания окислительно-восстановительных реакций. Теперь давайте разберемся, какие вещества могут быть окислителями, а какие — восстановителями, и может ли одно вещество проявлять те и другие свойства.
Примеры веществ-окислителей
Только окислителями могут быть элементы в высшей своей степени окисления. Например, S +6 в серной кислоте (H2SO4), N +5 в азотной кислоте (HNO3) или солях-нитратах, Cr +6 в хроматах (CrO4 2− ) и дихроматах (Cr2O7 2− ) соответственно, а также Mn +7 (MnO 4− ).
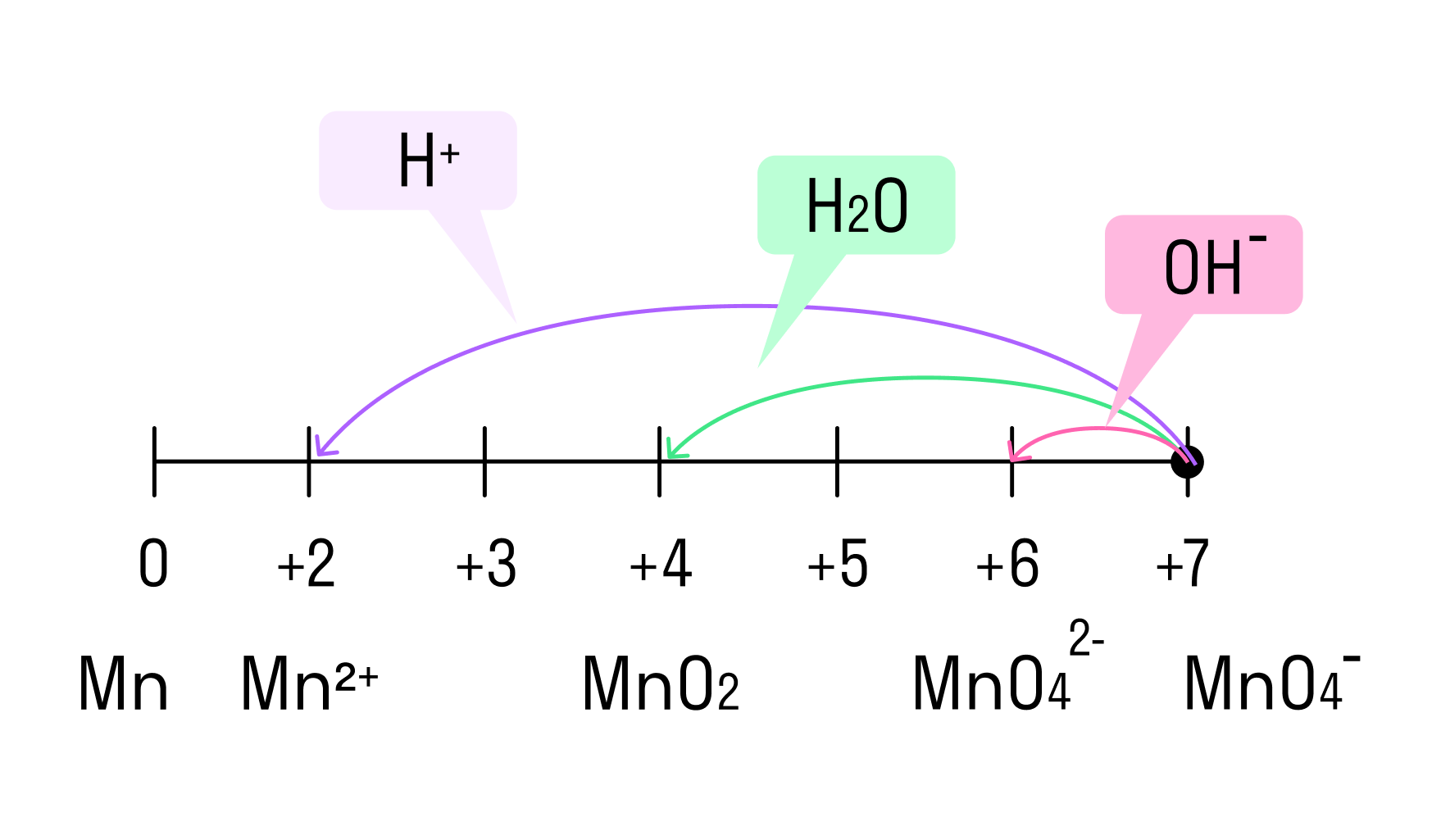
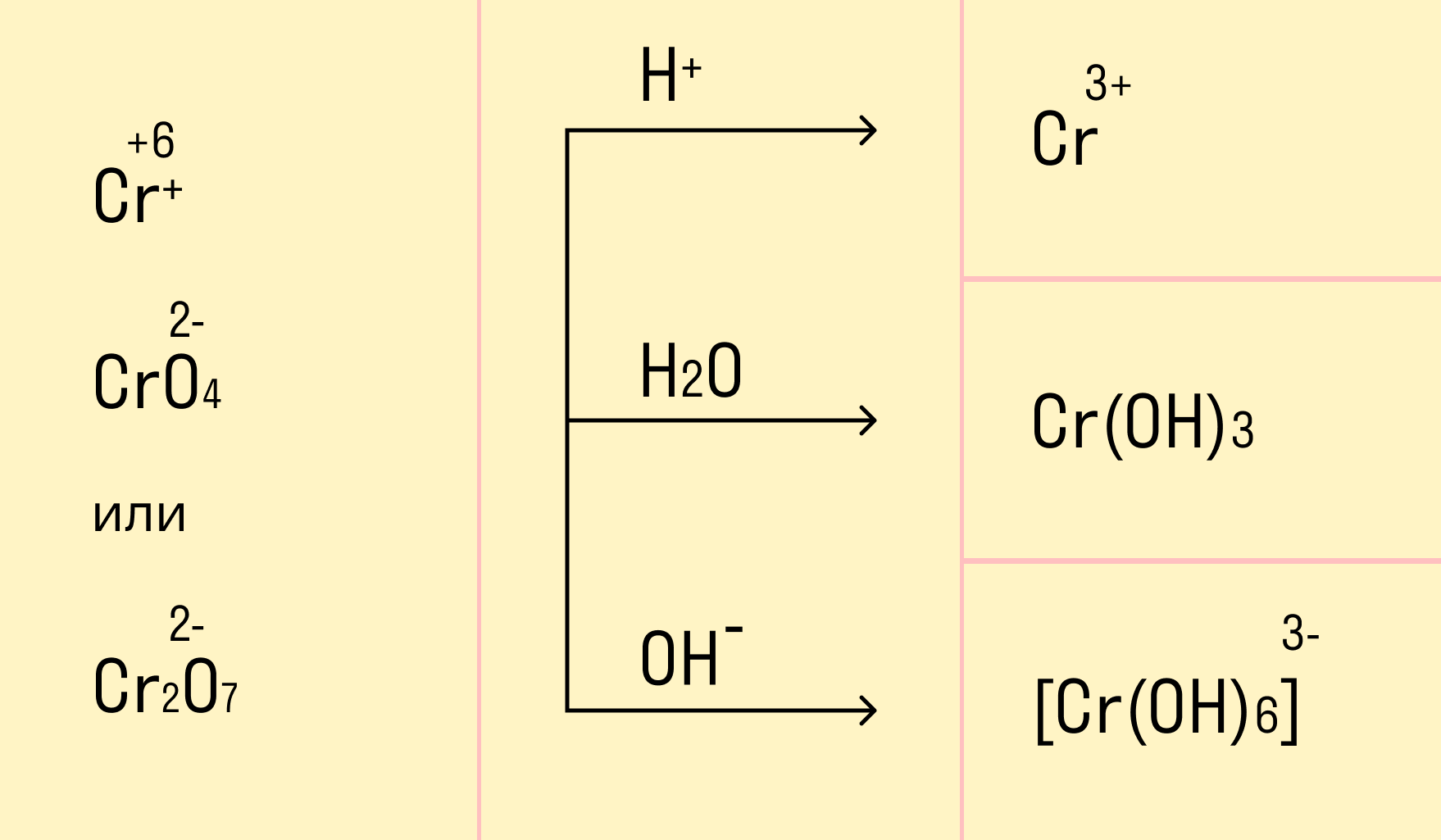
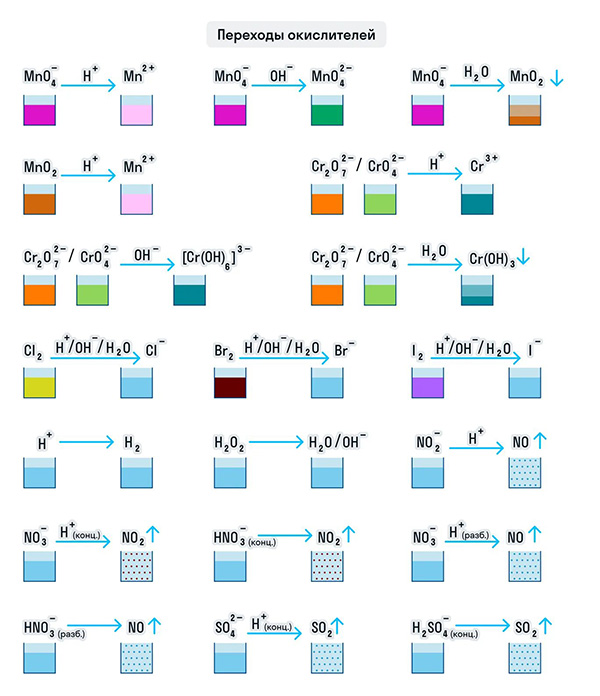
В зависимости от среды проведения реакции Mn +7 и Cr +6 ведут себя по-разному. Рассмотрим на схемах:
И марганец, и хром в кислой среде (H + ) образуют соли той кислоты, которая образовывала среду. В нейтральной среде (H2O) марганец превращается в оксид бурого цвета, а хром — в серо-зеленый нерастворимый в воде гидроксид. В щелочной среде (OH − ) марганец превращается в манганат (MnO4 2− ), а хром — в комплексное соединение светло-зеленого цвета.
Только окислителями могут быть простые вещества-неметаллы. Например, представители VIIA группы — галогены. Проявляя окислительные свойства в кислой среде, галогены восстанавливаются до соответствующих им галогеноводородных кислот: HF, HCl, HBr, HI. В щелочной среде образуются соли галогеноводородных кислот.
Кислород превращается в анион с устойчивой степенью окисления −2. А сера ведет себя как окислитель по отношению к водороду и металлам, образуя при этом сероводород и сульфиды.
Только окислителями могут быть и протон водорода (H + ) и катионы металлов в их высших степенях окисления при нескольких возможных. Ион Н + при взаимодействии с восстановителями переходит в газообразный водород (H2), а катионы металлов — в ионы с более низкой степенью окисления: 2CuCl2 + 2KI = CuCl + 2KCl + I2.
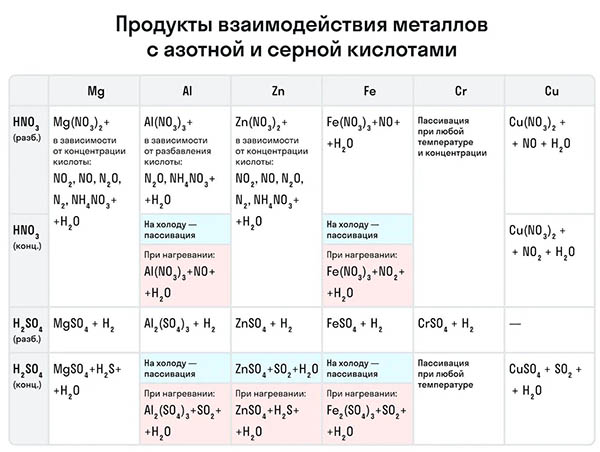
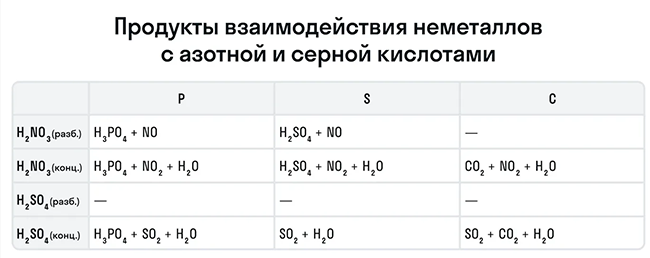
Рассмотрим как ведут себя сильные кислоты-окислители — азотная и серная. В зависимости от их концентрации меняются и продукты реакции.
Эти кислоты проявляют окислительные способности и с некоторыми неметаллами, окисляя их до соответствующих кислот в высшей степени окисления неметалла-восстановителя.
Для удобства мы собрали цвета переходов важнейших веществ-окислителей в одном месте.
Примеры веществ-восстановителей
Типичными восстановителями могут быть щелочные (IA) и щелочноземельные (IIA) металлы, цинк и алюминий, а также катионы металлов в своих низших степенях окисления при нескольких возможных. Например:
Типичными восстановителями также могут быть бескислородные кислоты и их соли. Например, H2S + 4Cl2 + 4H2O = 8HCl + H2SO4.
Гидриды активных металлов (щелочных и щелочноземельных) тоже являются типичными восстановителями. Например, NaH + H2O = NaOH + H2.
Для удобства мы собрали цвета переходов важнейших веществ-восстановителей в одном месте.
Окислительно-восстановительная двойственность
Окислительно-восстановительная двойственность — это способность атома проявлять как свойства окислителя, так и свойства восстановителя в зависимости от условия протекания химической реакции.
Разберем вещества, атомы которых обладают окислительно-восстановительной двойственностью.
По отношению к водороду и металлам сера играет роль окислителя: S + H2 = H2S.
При взаимодействии с сильными окислителями повышает свою степень окисления до +4 или +6: S + KMnO4 = K2SO4 + MnO2.
Кислородсодержащие соединения серы в степени окисления +4
Сера в сульфитах и сернистой кислоте при взаимодействии с сильными окислителями повышает степень окисления до +6: SO2 + 2HNO3 (конц) = H2SO4 + 2NO2.
С восстановителями соединения серы проявляют окислительные свойства, восстанавливаясь до степени окисления 0 или −2: SO2 + C = CO2 + S.
Пероксид водорода
Атом кислорода в пероксиде водорода находится в промежуточной степени окисления –1, и в присутствии восстановителей может понижать степень окисления до –2: 4H2O2 + PbS = PbSO4 + 4H2O.
Атом кислорода в пероксиде водорода находится в промежуточной степени окисления –1, и в присутствии окислителей может повышать степень окисления до 0: 3H2O2 + 2KMnO4 = 3O2 + 2MnO2 + 2KOH + 2H2O.
Простое вещество йод
Окислительная способность проявляется у йода в реакции с такими восстановителями, как сероводород, фосфор и металлы: I2 + H2S = S + 2HI.
Йод при взаимодействии с более сильными окислителями играет роль восстановителя: I2 + 5Cl2 + 6H2O = 2HIO3 + 10HCl.
Азотистая кислота и нитриты
При взаимодействии с более сильными окислителями азот повышает степень окисления до +5 и превращается либо в азотную кислоту из азотистой, либо в нитрат-анион из нитрит-аниона: 5NaNO2 + 2KMnO4 + 3H2SO4 = 5NaNO3 + 2MnSO4 + K2SO4 + 3H2O.
При взаимодействии с сильными восстановителями обычно происходит восстановление до NO (иногда до других соединений азота в более низких степенях окисления): 2HNO2 + 2HI = 2NO + I2 + 2H2O.
Для удобства мы собрали представителей типичных окислителей и восстановителей в одну схему.
Классификация окислительно-восстановительных реакций
Окислительно-восстановительные реакции можно поделить на четыре типа:
Рассмотрим каждую по отдельности.
Межмолекулярная ОВР — это реакция, окислитель и восстановитель которой являются различными веществами.
2KI + Br2 = 2KBr + I2, где Br2 — окислитель, а KI — восстановитель (за счёт I −1 ).
Внутримолекулярная ОВР — это реакция, в которой один атом является окислителем, а другой восстановителем в рамках одного соединения.
Пример такой окислительно-восстановительной реакции:
где Cl +5 — окислитель, а O −2 — восстановитель.
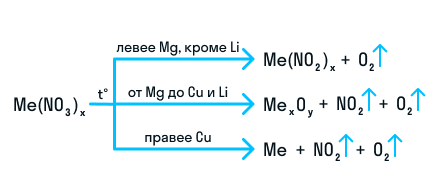
Термическое разложение нитратов — это внутримолекулярная ОВР. Вот схема разложения нитратов в зависимости от металла, входящего в состав соли.
Исключение — разложение нитрата железа (II): 4Fe(NO3)2 = 2Fe2O3 + 8NO2 + O2. Здесь железо окисляется до +3 вопреки правилам. Иначе разлагается при нагревании и нитрат аммония: NH4NO3 = N2O + 2H2O.
Окислительно-восстановительная реакция контрпропорционирования — это реакция, в которой атомы одного и того же химического элемента в разных степенях окисления входят в состав разных веществ, при этом образуя новые молекулы одного и того же продукта.
Основные правила составления ОВР
Подобрать среди исходных веществ окислитель и восстановитель, а также вещество, которое отвечает за среду — при необходимости. Для этого нужно расставить степени окисления элементов и сравнить их окислительно-восстановительные свойства.
Составить уравнение реакции и записать продукты реакции. Следует помнить, что в кислой среде образуются соли одно-, двух- и трехзарядных катионов, а для создания среды чаще всего используют серную кислоту. В кислой среде невозможно образование оснóвных оксидов и гидроксидов, так как они вступят в реакцию с кислотой. В щелочной среде не могут образовываться кислоты и кислотные оксиды, а образуются соли.
Уравнять методом электронного баланса или методом полуреакций.
Составим алгоритм для уравнивания окислительно-восстановительных реакций методом электронного баланса.
Главное условие протекания ОВР — общее число электронов, отданных восстановителем, должно быть равно общему числу электронов, принятых окислителем.
Определите атомы, которые меняют свои степени окисления в ходе реакции.
Выпишите, сколько электронов принял окислитель и отдал восстановитель. Если восстановителей несколько, выписываем все.
Найдите НОК для суммарно отданных/принятых электронов.
Расставьте первые полученные коэффициенты перед окислителем и одним или несколькими восстановителями.
Уравняйте все присутствующие металлы в уравнении реакции.
Уравняйте кислотные остатки.
Уравняйте водород — в обеих частях его должно быть одинаковое количество.
Проверьте себя по кислороду — если все посчитано верно, то он сойдется.
Окислительно-восстановительные реакции для «чайников»
Все химические реакции делятся на два вида:
Второй тип реакций называют окислительно-восстановительными.
Возникает логичный вопрос, а почему, собственно, такие реакции получили название окислительно-восстановительных, а, не, скажем, окислительно-изменительных? И, вообще, что это за «зверь» такой окисление?
Для того, чтобы обстоятельно ответить на эти вопросы, предварительно следует разобрать такие понятия, как «валентность», «электроотрицательность» и «степень окисления».
| Окислительно-восстановительные реакции сопровождаются перемещением электронов от одних атомов (молекул, ионов) к другим |
Изложение дальнейшего материала ведется с учетом того, что читатель знаком с понятиями «атом» и «электрон». Вкратце лишь напомним, что атом элемента состоит из ядра (положительно заряженного) и электронов (отрицательно заряженных), которые вращаются по своим орбиталям вокруг ядра.
Что происходит, когда атом отдает свои электроны? Поскольку электроны являются отрицательно заряженными частицами, то, уменьшение их количества автоматически приводит к увеличению заряда атома.
Атом (молекула, ион), получивший электрон, наоборот, уменьшает свой заряд.
ВНИМАНИЕ! Теперь начнём «путать следы».
В общем, надо признать, что такая терминология не лишена логики, ведь, если переложить язык химии на повседневную жизнь, то:
Продолжаем «путать следы» дальше.
Подводим краткий итог сказанному:
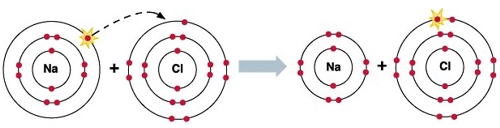
На рисунке выше показано взаимодействие атома натрия с атомом хлора, в ходе которого, натрий отдает один свой электрон атому хлора. В этой реакции натрий является элементом-восстановителем, в ходе реакции он окисляется (степень окисления натрия увеличивается); атом хлора является элементом-окислителем, в ходе реакции он восстанавливается (степень окисления хлора уменьшается).
Следует понимать, что в окислительно-восстановительных реакциях кол-во отдаваемых электронов веществом-восстановителем, обязательно равно кол-ву электронов, принятых веществом-окислителем. Если кредитор дал взаймы 100 долларов, то заемщик получил кредит в 100 долларов.
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе
Окислительно-восстановительные реакции. Окислитель и восстановитель
Окислительно-восстановительными называют реакции, которые сопровождаются изменением степеней окисления химических элементов, входящих в состав реагентов.
Окислением называют процесс отдачи электронов атомом, молекулой или ионом, который сопровождается повышением степени окисления.
Восстановлением называют процесс присоединения электронов атомом, молекулой или ионом, который сопровождается понижением степени окисления.
Окислителем называют реагент, который принимает электроны в ходе окислительно-восстановительной реакции. (Легко запомнить: окислитель — грабитель.)
Восстановителем называют реагент, который отдаёт электроны в ходе окислительно-восстановительной реакции.
Окислительно-восстановительные реакции делят на реакции межмолекулярного окисления-восстановления, реакции внутримолекулярного окисления-восстановления, реакции диспропорционирования и реакции конмутации.
Для составления окислительно-восстановительных реакций используют метод электронного баланса.
Составление уравнения окислительно-восстановительной реакции осуществляют в несколько стадий.
Пример 1. Реакция алюминия с серой. Записываем схему реакции и указываем изменение степеней окисления:
Атом серы присоединяет два электрона, изменяя свою степень окисления от 0 до –2. Он является окислителем. Атом алюминия отдаёт три электрона, изменяя свою степень окисления от 0 до +3. Он является восстановителем.
Составляем уравнение электронного баланса и уравниваем число присоединённых и отданных электронов:
Подставляем найденные коэффициенты в уравнение реакции и окончательно получаем:
Пример 2. Окисление фосфора хлором. Записываем схему реакции и указываем изменение степеней окисления:
Степень окисления хлора изменяется от 0 до –1, при этом молекула хлора присоединяет два электрона. Хлор является окислителем.
Атом фосфора отдаёт пять электронов, изменяя свою степень окисления от 0 до +5. Он является восстановителем.
Составляем уравнение электронного баланса и уравниваем число присоединённых и отданных электронов:
Электронное уравнение для хлора записывают именно так, поскольку окислителем является молекула хлора, состоящая из двух атомов, и каждый из этих атомов изменяет свою степень окисления от 0 до –1. Коэффициент 5 относится к молекуле хлора в левой части уравнения, а количество атомов хлора в правой части уравнения 5 × 2 = 10.
Подставляем найденные коэффициенты в уравнение реакции и окончательно получаем:
Пример 3. Восстановление оксида железа (II, III) алюминием. Записываем схему реакции и указываем изменение степеней окисления:
Степень окисления железа изменяется от +8/3 до 0, при этом три иона железа (поскольку в исходном оксиде их содержится именно три) присоединяют восемь электронов (3 × 8/3 = 8). Железо является окислителем.
Алюминий отдаёт три электрона, изменяя свою степень окисления от 0 до +3. Он является восстановителем.
Составляем уравнение электронного баланса и уравниваем число присоединенных и отданных электронов:
Электронное уравнение для алюминия записывают именно так, поскольку в состав оксида алюминия входят два атома алюминия. Таким образом, в левой части уравнения основной коэффициент перед оксидом железа (II, III) будет равен 3, а перед алюминием 4 × 2 = 8.
Количество атомов железа в правой части уравнения реакции составит 3 × 3 = 9. Количество молекул оксида алюминия будет равно 8/2 = 4. Окончательно получаем:
Проверяем баланс по кислороду. В левой части уравнения 3 × 4 = 12. В правой части уравнения 4 × 3 = 12. Таким образом, число атомов каждого элемента в отдельности в левой и в правой части химического уравнения равны между собой, и реакция уравнена правильно.
Этот пример наглядно показывает, что дробная степень окисления хотя и не имеет физического смысла, но позволяет правильно уравнять окислительно-восстановительную реакцию.
Очень часто окислительно-восстановительные реакции проходят в растворах в нейтральной, кислой или щелочной среде. В этом случае химические элементы, входящие в состав вещества, образующего среду реакции, свою степень окисления не меняют.
Пример 4. Окисление йодида натрия перманганатом калия в среде серной кислоты. Записываем схему реакции, указываем степени окисления элементов, участвующих в процессах окисления и восстановления:
Атом марганца принимает пять электронов, изменяя свою степень окисления от +7 до +2. Перманганат калия является окислителем.
Составляем уравнение электронного баланса и уравниваем число присоединённых и отданных электронов введением множителей:
Найденные коэффициенты подставим в уравнение реакции перед соответствующими формулами веществ в левой и правой частях.
Серная кислота является средой реакции. Ни один из элементов, входящих в состав этого соединения, свою степень окисления не меняет, но сульфат-анион связывает выделяющиеся в результате реакции катионы калия, натрия и марганца. Подсчитаем число сульфат-ионов в правой части. Оно равно 2 + 1 + 5 = 8. Следовательно, перед серной кислотой следует поставить коэффициент 8. Число атомов водорода в левой части уравнения равно 8 × 2 = 16. Отсюда вычисляем коэффициент для воды: 16/2 = 8.
Таким образом, уравнение реакции будет иметь вид:
Правильность баланса проверяем по кислороду. В левой части его 2 × 4 = 8 (перманганат калия); в правой — 8 × 1 = 8 (вода). Следовательно, уравнение составлено правильно.
Пример 5. Окисление сульфида калия манганатом калия в водной среде. Записываем схему реакции, указываем степени окисления элементов, участвующих в процессах окисления и восстановления:
Ион марганца принимает два электрона, изменяя свою степень окисления от +6 до +4. Манганат калия является окислителем.
Составляем уравнение электронного баланса и уравниваем число присоединённых и отданных электронов введением множителей:
Основные коэффициенты в уравнении реакции равны единице:
Вода является средой реакции. Ни один из элементов, входящих в состав этого соединения, свою степень окисления не меняет.
Гидроксид-ионы связывают выделяющиеся в результате реакции катионы калия. Таких катионов четыре (2 × 2), число атомов водорода также 4 (4 × 1), поэтому перед молекулой воды ставим коэффициент два (4/2 = 2):
Пример 6. Окисление аммиака хлоратом калия в щелочной среде. Записываем схему реакции, указываем степени окисления элементов, участвующих в процессах окисления и восстановления:
Хлор принимает шесть электронов, изменяя свою степень окисления от +5 до –1. Хлорат калия является окислителем.
Азот отдаёт восемь электронов, изменяя свою степень окисления от –3 до +5. Аммиак является восстановителем.
Составляем уравнение электронного баланса, уравниваем число присоединённых и отданных электронов введением множителей, сокращаем кратные коэффициенты:
Проставляем найденные основные коэффициенты в уравнение реакции:
Гидроксид калия является средой реакции. Ни один из элементов, входящих в состав этого соединения, свою степень окисления не меняет.
Катионы калия связывают выделяющиеся в результате реакции нитрат-ионы. Таких анионов три. Следовательно, перед гидроксидом калия ставим коэффициент три:
Число атомов водорода в левой части уравнения равно девяти в аммиаке (3 × 3) = 9 и трём в гидроксиде калия (3 × 1), а их общее число 9 + 3 = 12. Следовательно, перед водой ставим коэффициент (12/2) = 6. Окончательно уравнение реакции будет иметь вид:
Убеждаемся ещё раз в правильности расстановки коэффициентов, сравнивая число атомов кислорода в левой и правой его частях. Оно равно 15.
Довольно часто одно и то же вещество одновременно является окислителем и создаёт среду реакции. Такие реакции характерны для концентрированной серной кислоты и азотной кислоты в любой концентрации. Кроме того, в подобные реакции, но в качестве восстановителя, вступают галогенводородные кислоты с сильными окислителями.
Пример 7. Окисление магния разбавленной азотной кислотой. Записываем схему реакции и указываем изменение степеней окисления:
Степень окисления азота изменяется от +5 до +1, при этом два атома азота присоединяют восемь электронов. Азотная кислота является окислителем.
Магний отдаёт два электрона, изменяя свою степень окисления от 0 до +2. Он является восстановителем.
Составляем уравнение электронного баланса и уравниваем число присоединённых и отданных электронов:
Подставляем найденные коэффициенты перед окислителем и восстановителем в левой части уравнения реакции и перед продуктами окисления и восстановления в правой части уравнения реакции:
При этом в правой части уравнения реакции имеется 4 × 2 = 8 нитрат-ионов, не изменивших свою степень окисления. Очевидно, что для этого в правую часть уравнения реакции следует добавить ещё 8 молекул HNO3. Тогда общее количество молекул азотной кислоты в правой части уравнения составит 2 + 8 = 10.
В этих молекулах содержатся 10 × 1 = 10 атомов водорода. Такое же количество атомов водорода должно быть и в правой части уравнения. Следовательно, перед молекулой воды следует подставить коэффициент 10/2 = 5, и уравнение окончательно будет иметь вид:
Окончательно проверяем правильность баланса, подсчитывая число атомов кислорода в левой и правой частях уравнения. В левой части 10 × 3 = 30. В правой части (2 × 3) × 4 = 24 в нитрате магния, 1 в оксиде азота (I) и 5 × 1 = 5 в молекуле воды. Итого 24 + 1 + 5 = 30. Таким образом, реакция полностью уравнена.
Пример 8. Взаимодействие соляной кислоты с оксидом марганца (IV). Записываем схему реакции и указываем изменение степеней окисления:
Степень окисления марганца изменяется от +4 до +2, при этом марганец присоединяет два электрона. Оксид марганца (IV) является окислителем.
Составляем электронное уравнение и уравниваем число присоединённых и отданных электронов, сокращаем кратные коэффициенты:
При этом коэффициент 1 изначально относится к двум хлорид-ионам и к одной молекуле Cl2. Подставляем найденные коэффициенты перед окислителем и восстановителем в левой части уравнения реакции и перед продуктами окисления и восстановления в правой части уравнения реакции:
При этом в правой части уравнения реакции имеется 1 × 2 = 2 хлорид-иона, не изменивших свою степень окисления. Эти хлорид-ионы в окислительно-восстановительной реакции не участвовали. Очевидно, что для этого в правую часть уравнения реакции следует добавить 2 молекулы HCl. Тогда общее количество молекул HCl в правой части уравнения составит 2 + 2 = 4. В этих молекулах будет содержаться 4 × 1 = 4 атома водорода. Такое же количество атомов водорода должно быть и в правой части уравнения. Тогда перед молекулой воды следует подставить коэффициент 4/2 = 2, и уравнение в окончательном виде будет иметь вид:
Проверяем правильность баланса, подсчитывая число атомов кислорода в левой и правой частях уравнения. В левой части оно составляет 1 × 2 = 2 в оксиде марганца (IV), а в правой части 2 × 1 = 2 в молекуле воды. Таким образом, реакция полностью уравнена.
В качестве окислителя могут выступать нейтральные атомы и молекулы, положительно заряженные ионы металлов, сложные ионы и молекулы, содержащие атомы металлов и неметаллов в состоянии положительной степени окисления и др.
Ниже приведены сведения о некоторых наиболее распространенных окислителях, имеющих важное практическое значение.
Кислород. Сильный окислитель, окислительная способность значительно возрастает при нагревании. Кислород взаимодействует непосредственно с большинством простых веществ, кроме галогенов, благородных металлов Ag, Au, Pt и благородных газов, с образованием оксидов:
Взаимодействие натрия с кислородом приводит к пероксиду натрия:
Более активные щелочные металлы (K, Rb, Cs) при взаимодействии с кислородом дают надпероксиды типа ЭО2:
В своих соединениях кислород, как правило, проявляет степень окисления –2. Применяется кислород в химической промышленности, в различных производственных процессах в металлургической промышленности, для получения высоких температур. С участием кислорода идут многочисленные чрезвычайно важные жизненные процессы: дыхание, окисление аминокислот, жиров, углеводов. Только немногие живые организмы, называемые анаэробными, могут обходиться без кислорода.
Реакции, иллюстрирующие окислительные свойства кислорода при его взаимодействии с различными неорганическими веществами, приведены в уроке 14.
Озон. Обладает ещё большей по сравнению с кислородом окислительной способностью. Озон окисляет все металлы, за исключением золота, платины и некоторых других, при этом, как правило, образуются соответствующие высшие оксиды элементов, реже — пероксиды и озониды, например:
Озон окисляет оксиды элементов с промежуточной степенью окисления в высшие оксиды.
Перманганат калия способен окислять сульфиды в сульфаты, нитриты в нитраты, бромиды и йодиды — до брома и йода, соляную кислоту до хлора и т. д.:
Хромат и бихромат калия. Эти соединения широко применяют в качестве окислителей в неорганических и органических синтезах. Взаимные переходы хромат- и бихромат-ионов очень легко протекают в растворах, что можно описать следующим уравнением обратимой реакции:
Соединения хрома (VI) — сильные окислители. В окислительно-восстановительных процессах они переходят в производные Cr (III). В нейтральной среде образуется гидроксид хрома (III), например:
В кислой среде образуются ионы Cr 3+ :
В щелочной — производные анионного комплекса [Cr(OH)6] 3– :
В качестве восстановителя могут выступать нейтральные атомы, отрицательно заряженные ионы неметаллов, положительно заряженные ионы металлов в низшей степени окисления, сложные ионы и молекулы, содержащие атомы в промежуточной степени окисления, электрический ток на катоде и др.
Ниже приведены сведения о некоторых наиболее распространённых восстановителях, имеющих важное практическое значение.
Углерод. Углерод широко применяют в качестве восстановителя в неорганических синтезах. При этом в качестве продуктов окисления может образовываться углекислый газ, или оксид углерода (II). При восстановлении оксидов металлов могут образовываться свободные металлы, реже — карбиды металлов.
Восстановительные свойства углерод проявляет также в реакции получения водяного газа:
Полученную смесь водорода и оксида углерода (II) широко применяют для синтеза органических соединений.
Оксид углерода (II). Широко применяют в металлургии при восстановлении металлов из их оксидов, например:
Водород. Широко применяют в качестве восстановителя в неорганических синтезах (водородотермия) для получения чистого вольфрама, молибдена, галлия, германия и т. д.:
Тренировочные задания
Используя метод электронного баланса, расставьте коэффициенты, определите окислитель и восстановитель в уравнении реакции, схема которой:
1. Al + H2O + KNO3 + KOH → K[Al(OH)4] + NH3↑.
Окислительно-восстановительные реакции
Окислительно-восстановительные реакции — это химические реакции, сопровождающиеся изменением степени окисления у атомов реагирующих веществ. При этом некоторые частицы отдают электроны, а некоторые получают.
Окислители и восстановители
Окислители — это частицы (атомы, молекулы или ионы), которые принимают электроны в ходе химической реакции. При этом степень окисления окислителя понижается. Окислители при этом восстанавливаются.
Восстановители — это частицы (атомы, молекулы или ионы), которые отдают электроны в ходе химической реакции. При этом степень окисления восстановителя повышается. Восстановители при этом окисляются.
Химические вещества можно разделить на типичные окислители, типичные восстановители, и вещества, которые могут проявлять и окислительные, и восстановительные свойства. Некоторые вещества практически не проявляют окислительно-восстановительную активность.
К типичным окислителям относят:
Типичные восстановители – это, как правило:
Большинство остальных веществ может проявлять как окислительные, так и восстановительные свойства.
Типичные окислители и восстановители приведены в таблице.
В лабораторной практике наиболее часто используются следующие окислители :
Классификация окислительно-восстановительных реакций
Окислительно-восстановительные реакции обычно разделяют на четыре типа: межмолекулярные, внутримолекулярные, реакции диспропорционирования (самоокисления-самовосстановления), и реакции контрдиспропорционирования.
C 0 + 4H N +5 O3(конц) = C +4 O2 ↑ + 4 N +4 O2 ↑+ 2H2O.
Внутримолекулярные реакции – это такие реакции, в которых разные элементы из одного реагента переходят в разные продукты, например:
Реакции диспропорционирования (самоокисления-самовосстановления) – это такие реакции, в которых окислитель и восстановитель – один и тот же элемент одного реагента, который при этом переходит в разные продукты:
3Br2 + 6 KOH → 5KBr + KBrO3 + 3 H2O,
Репропорционирование (конпропорционирование, контрдиспропорционирование ) – это реакции, в которых окислитель и восстановитель – это один и тот же элемент, который из разных реагентов переходит в один продукт. Реакция, обратная диспропорционированию.
Основные правила составления окислительно-восстановительных реакций
Окислительно-восстановительные реакции сопровождаются процессами окисления и восстановления:
Окисление — это процесс отдачи электронов восстановителем.
Восстановление — это процесс присоединения электронов окислителем.
В окислительно-восстановительных реакциях соблюдается электронный баланс: количество электронов, которые отдает восстановитель, равно количеству электронов, которые получает окислитель. Если баланс составлен неверно, составить сложные ОВР у вас не получится.
Используется несколько методов составления окислительно-восстановительных реакций (ОВР): метод электронного баланса, метод электронно-ионного баланса (метод полуреакций) и другие.
«Опознать» ОВР довольно легко — достаточно расставить степени окисления во всех соединениях и определить, что атомы меняют степень окисления:
Выписываем отдельно атомы элементов, меняющих степень окисления, в состоянии ДО реакции и ПОСЛЕ реакции.
Степень окисления меняют атомы марганца и серы:
Mn +7 + 1e = Mn +6
Марганец поглощает 1 электрон, сера отдает 2 электрона. При этом необходимо, чтобы соблюдался электронный баланс. Следовательно, необходимо удвоить число атомов марганца, а число атомов серы оставить без изменения. Балансовые коэффициенты указываем и перед реагентами, и перед продуктами!
Схема составления уравнений ОВР методом электронного баланса:
Внимание! В реакции может быть несколько окислителей или восстановителей. Баланс необходимо составить так, чтобы ОБЩЕЕ число отданных и полученных электронов было одинаковым.
Общие закономерности протекания окислительно-восстановительных реакций
Самый очевидный фактор, определяющий — среда раствора реакции — кислая, нейтральная или щелочная. Как правило (но не обязательно), вещество, определяющее среду, указано среди реагентов. Возможны такие варианты:
Среда протекания реакции позволяет определить состав и форму существования остальных продуктов ОВР. Основной принцип — продукты образуются такие, которые не взаимодействуют с реагентами!
Обратите внимание! Е сли среда раствора кислая, то среди продуктов реакции не могут присутствовать основания и основные оксиды, т.к. они взаимодействуют с кислотой. И, наоборот, в щелочной среде исключено образование кислоты и кислотного оксида. Это одна из наиболее частых, и наиболее грубых ошибок.
При увеличении температуры большинство ОВР, как правило, проходят более интенсивно и более глубоко.
Рассмотрим наиболее типичные лабораторные окислители.
Основные схемы окислительно-восстановительных реакций
Схема восстановления перманганатов
В составе перманганатов есть мощный окислитель — марганец в степени окисления +7. Соли марганца +7 окрашивают раствор в фиолетовый цвет.
Перманганаты, в зависимости от среды реакционного раствора, восстанавливаются по-разному.
3 K2S + 2 KMnO4 + 4 H2O = 2 MnO2↓ + 3 S↓ + 8 KOH,
Распространенной ошибкой в этой реакции является указание на взаимодействие серы и щелочи в продуктах реакции. Однако, сера взаимодействует с щелочью в довольно жестких условиях (повышенная температура), что не соответствует условиям этой реакции. При обычных условиях правильно будет указывать именно молекулярную серу и щелочь отдельно, а не продукты их взаимодействия.
При составлении этой реакции также возникают трудности. Дело в том, что в данном случае написание молекулы среды (КОН или другая щелочь) в реагентах не требуется для уравнивания реакции. Щелочь принимает участие в реакции, и определяет продукт восстановления перманганата калия, но реагенты и продукты уравниваются и без ее участия. Этот, казалось бы, парадокс легко разрешим, если вспомнить, что химическая реакция — это всего лишь условная запись, которая не указывает на каждый происходящий процесс, а всего лишь является отображением суммы всех процессов. Как определить это самостоятельно? Если действовать по классической схеме — баланс-балансовые коэффициенты-уравнивание металла, то вы увидите, что металлы уравниваются балансовыми коэффициентами, и наличие щелочи в левой части уравнения реакции будет лишним.
Перманганаты окисляют:
KMnO4 + неМе (низшая с.о.) = неМе 0 + другие продукты
KMnO4 + неМе (промежуточная с.о.) = неМе(высшая с.о.) + др. продукты
KMnO4 + Ме 0 = Ме (стабильная с.о.) + др. продукты
Схема восстановления хроматов/бихроматов
Соединения хрома VI окисляют:
Хромат/бихромат + неМе (отрицательная с.о.) = неМе 0 + другие продукты
Хромат/бихромат + неМе (промежуточная положительная с.о.) = неМе(высшая с.о.) + др. продукты
Хромат/бихромат + Ме 0 = Ме (стабильная с.о.) + др. продукты
Хромат/бихромат + P, As (отрицательная с.о.) = P, As +5 + другие продукты
Разложение нитратов
Например:
Активные металлы в природе встречаются в виде солей (KCl, NaCl).
Металлы средней активности чаще всего в природе встречаются в виде оксидов (Fe2O3, Al2O3 и др.).
Неактивные металлы в природе встречаются в виде простых веществ.
Некоторые исключения!
Разложение нитрата аммония :
При нагревании нитрат аммония разлагается. При температуре до 270 о С образуется оксид азота (I) («веселящий газ») и вода:
Результирующая степень окиcления азота — среднее арифметическое степени окисления атомов азота в исходной молекуле.
При более высокой температуре оксид азота (I) разлагается на простые вещества — азот и кислород :
При разложении нитрита аммония NH4NO2 также происходит контрдиспропорционирование.
Термическое разложение нитрата марганца (II) сопровождается окислением металла:
Нитрат железа (II) при низких температурах разлагается до оксида железа (II), при нагревании железо окисляется до степени окисления +3:
Нитрат никеля (II) разлагается до нитрита при нагревании до 150 о С под вакуумом и до оксида никеля при более высоких температурах (разложения нитрата никеля в ЕГЭ по химии не должно быть, но это не точно)).
Окислительные свойства азотной кислоты
Это связано с тем, что в составе кислоты есть очень сильный окислитель — азот в степени окисления +5. При взаимодействии с восстановителями — металлами образуются различные продукты восстановления азота.
Азотная кислота + металл = соль металла + продукт восстановления азота + H2O
Некоторые закономерности позволят верно определять основной продукт восстановления металлами азотной кислоты в реакции:
пассивация металлов — это перевод поверхности металла в неактивное состояние за счет образования на поверхности металла тонких слоев инертных соединений, в данном случае преимущественно оксидов металлов, которые не реагируют с концентрированной азотной кислотой
Для приближенного определения продуктов восстановления азотной кислоты при взаимодействии с разными металлами я предлагаю воспользоваться принципом маятника. Основные факторы, смещающие положение маятника: концентрация кислоты и активность металла. Для упрощения используем 3 типа концентраций кислоты: концентрированная (больше 30%), разбавленная (30% или меньше), очень разбавленная (меньше 5%). Металлы по активности разделим на активные (до алюминия), средней активности (от алюминия до водорода) и неактивные (после водорода). Продукты восстановления азотной кислоты располагаем в порядке убывания степени окисления:
Чем активнее металл, тем больше мы смещаемся вправо. Чем больше концентрация или меньше степень разбавления кислоты, тем больше мы смещаемся влево.
Взаимодействие металлов с серной кислотой
Например :
Концентрированная серная кислота взаимодействует с металлами, стоящими в ряду напряжений как до, так и после водорода.
H2SO4 (конц) + металл = соль металла + продукт восстановления серы (SO2, S, H2S) + вода
Основные принципы взаимодействия концентрированной серной кислоты с металлами:
1. Концентрированная серная кислота пассивирует алюминий, хром, железо при комнатной температуре, либо на холоду;
2. Концентрированная серная кислота не взаимодействует с золотом, платиной и палладием ;
3. С неактивными металлами концентрированная серная кислота восстанавливается до оксида серы (IV).
Cu 0 + 2H2 S +6 O4(конц) = Cu +2 SO4 + S +4 O2 + 2H2O
4. При взаимодействии с активными металлами и цинком концентрированная серная кислота образует серу S либо сероводород H2S 2- (в зависимости от температуры, степени измельчения и активности металла).
Пероксид водорода
При взаимодействии с окислителями перекись окисляется до молекулярного кислорода (степень окисления 0): O2. Например :
ОВР — Очень Важные Реакции
Так уж исторически сложилось, что одной из самых сложных задач школьной химии всегда являлись окислительно-восстановительные реакции. Электронные конфигурации атомов, комплексные соединения, и даже устройство солей перксеноновой кислоты не вызывают у детей столько оторопи, сколько уравнивание ОВР. Так как часть нашей команды занимается созданием сервисов для школьников, мы захотели помочь решить проблему с поиском окислительно-восстановительных реакций. Разумеется, нам очень не хотелось потворствовать списыванию, поэтому мы постарались сделать наш сервис обучающим, чтобы любому школьнику стало понятно, как же уравниваются те самые ОВР.
В первую очередь для всех имеющихся у нас окислительно-восстановительных реакций мы стали показывать соответствующие полуреакции.
Например, вот так:
Как можно заметить из скриншота, к полуреакциям прилагаются и все коэффициенты, а если навести мышкой на каждый из них, то всплывающая подсказка покажет, что он означает. Но, как я уже упоминал, нашей целью было не столько предоставить школьникам источник для списывания, сколько объяснить им, как происходит процесс уравнивания. Поэтому за заметной кнопкой «Показать, как уравнять эту реакцию» скрывается другая половина нашей фичи. Если первая половина автоматически генерирует полуреакции и их коэффициенты, то вторая пошла ещё дальше — она создаёт для каждой реакции набор слайдов, демонстрирующих, как необходимо действовать школьнику, чтобы уравнять реакцию самостоятельно. Насколько мы можем судить, ни один оффлайновый или онлайновый учебник не предложит настолько полных и подробных примеров.
Посмотрите и вы:
Мы в лице разработчиков химии искренне надеемся, что все, кто до сих пор не мог разобраться, как же уравниваются подобные реакции, теперь сможет сделать это сам без всяких проблем.
Правила составления окислительно-восстановительных реакций
Основные правила составления окислительно-восстановительных реакций
Существует несколько основных правил, которые сильно упрощают составление окислительно-восстановительных реакций. Более подробно эти и другие правила рассматривается на других страницах этого раздела, но для ЕГЭ достаточно знать правила из этого списка.
Реакции простых веществ: металлов и неметаллов с щелочами, кислотами и солями:
1.1) Из металлов только Al, Zn и Be взаимодействуют со щелочами с выделением водорода:
Zn + 2NaOH + 2H2O → Na2[Zn(OH)4] + H2
Be + 2NaOH + 2H2O → Na2[Be(OH)4] + H2
2Al + 2NaOH + 6H2O → 2Na[Al(OH)4] + 3H2
1.2) Из неметаллов только S, P, Si и галогены реагируют с щелочами:
3S + 6NaOH → Na2SO3 + 2Na2S + 3H2O
P4 + 3NaOH + 3H2O → PH3
Si + 2NaOH + H2O → Na2SiO3 + 2H2
Cl2 + 2NaOH → NaCl + NaClO + H2O (аналогично для Br2, I2)
3Cl2 + 6NaOH → 5NaCl + NaClO3 + 3H2O (при нагревании, аналогично для Br2, I2)
2.1) Металлы ( стоящие в ряду активности металлов до H2) реагируют с кислотами-неокислителями с выделением водорода:
2HCl + Fe → FeCl2 + H2
H2SO4(р) + Fe → FeSO4 + H2
2.2) Все металлы, кроме Pt и Au, реагируют с кислотами-окислителями без выделения водорода:
2H2SO4(к) + 2Ag → Ag2SO4 + SO2 
6H2SO4(к) + 2Fe  → Fe2(SO4)3 + 3SO2 
2.3) Более сильные металлы вытесняют более слабые из растворов их солей:
Fe + CuSO4 → FeSO4 + Cu
3) Неметаллы не реагируют с кислотами-неокислителями:
C + HCl → реакция не идет
4) Такие неметаллы, как S, C, P могут реагировать с солями, проявляющими окислительные свойства (KClO3, KNO3 в расплавленном состоянии):
6P + 5KClO3 → 3P2O5 + 5KCl
C + 2KNO3 (расплав) → CO2 
S + 2KNO3 (расплав) → SO2 
5) Важная реакция получения фосфора:
5C + 3SiO2 + Ca3(PO4)2 → 5CO 
6) Из неметаллов только S, C, и P реагируют с кислотами-окислителями (в рамках ЕГЭ), а также I2 с HNO3(к):
C + H2SO4(конц.) → CO2 

S + 2H2SO4(конц.) → 3SO2 
2P + 5H2SO4(конц.) → 2H3PO4 + 5SO2 
C + 4HNO3(конц.) → CO2 + 4NO2 
P + 5HNO3(конц.)  → H3PO4 + 5NO2 
S + 6HNO3(конц.) → H2SO4 + 6NO2 
I2 + 10HNO3(конц.) → 2HIO3 + 10NO2
Фосфор
1) Наиболее устойчивая степень окисления фосфора +5, следовательно, любые другие соединения фосфора окисляются сильными окислителями до этой степени окисления (с образованием P2O5 или фосфат-иона):
PH3 + 8KMnO4 + 11KOH → K3PO4 + 8K2MnO4 + 7H2O
6P + 5KClO3 → 5KCl + 3P2O5
3P2O3 + 4HNO3 + 7H2O → 6H3PO4 + 4NO
Азот
1) Аммиак, как правило, окисляется до азота N2:
8NH3 + 3KBrO4 → 3KBr + 4N2 
2NH3 + 3CuO → 3Cu + N2
Исключением является каталитическое окисление аммиака:
4NH3 + 5O2 → 4NO 
Обычное горение аммиака протекает с образованием N2 (как и горение любых органических азотсодержащих соединений):
4NH3 + 3O2 → 2N2 
2) Нитрит-ионы окисляются до нитрат-ионов:
3KNO2 + K2Cr2O7 + 4H2SO4 → 3KNO3 + Cr2(SO4)3 + K2SO4 + 4H2O
3KNO2 + 2KMnO4 + H2O → 3KNO3 + 2MnO2 
3) Нитрит-ионы восстанавливаются до азота в реакциях с солями аммония:
NaNO2 + NH4Cl → N2
Ca(NO2)2 + (NH4)2SO4 → 2N2
4) Нитрит-ионы восстанавливаются до оксида азота (II) в реакциях с типичными восстановителями: HI, йодидами, солями Fe +2 и др.:
2KNO2 + 2KI + 2H2SO4 → 2NO 
HNO2 + 2HI → 2NO
Следующий тип реакций встречается в вариантах Ю.Н. Медведева.
5) Нитрат-ионы являются сильными окислителями при сплавлении с соединениями Cr, Mn, Fe в щелочной среде и с некоторыми неметаллами (восстанавливаются до нитритов):
3NaNO3 + Cr2O3 + 4KOH → 3NaNO2 + 2K2CrO4 + 2H2O
KNO3 + MnO2 + K2CO3 → KNO2 + K2MnO4 + CO2
2NaNO3 + FeSO4 + 4NaOH → 2NaNO2 + Na2FeO4 + Na2SO4 + 2H2O
2KNO3(расплав) + C → 2KNO2 + CO2
2KNO3(расплав) + S → 2KNO2 + SO2
6) Нитрат-ионы являются сильными окислителями в кислотной среде:
2KNO3 + Cu + 2H2SO4 → CuSO4 + 2NO2 
7) Восстановление нитратов до аммиака в реакциях с такими металлами, как Al, Zn, Mg (встречается очень редко):
3NaNO3 + 8Al + 5NaOH +18H2O → 3NH3 
NaNO3 + 4Zn + 7NaOH + 6H2O → NH3 
KNO3 + 4Mg + 6H2O → NH3 

Кислород
1) Перекись водорода окисляется до кислорода O2 типичными окислителями:
KMnO4, K2Cr2O7, галогены, соли кислородсодержащих кислот хлора (например, KClO3) и некоторыми другими.
5H2O2 + KMnO4 + 3H2SO4 → 2MnSO4 + K2SO4 + 5O2 
3H2O2 + 2KNO3 + H2SO4 → K2SO4 + 2NO 

H2O2 + Na2SO3 → Na2SO4 + H2O
H2O2 + KNO2 → KNO3 + H2O
3H2O2 + 2NaCrO2 + 2NaOH → 2Na2CrO4 + 4H2O
Галогены
1) Галогены диспропорционируют в щелочах:
Cl2 + 2NaOH → NaCl + NaClO + H2O (аналогично для Br2, I2)
3Cl2 + 6NaOH → 5NaCl + NaClO3 + 3H2O (при нагревании, аналогично для Br2, I2)
5HClO3 + 6P + 9H2O → 5HCl + 6H3PO4
KClO3 + 6Fe(OH)2 + 18HCl → 6FeCl3 + KCl + 15H2O
2Cl2 + H3PO2 + 7KOH → K3PO4 + 4KCl + 5H2O
2Br2 + CrCl2 + 8NaOH → Na2CrO4 + 2NaCl + 4NaBr + 4H2O
Исключение: соединения йода в высоких степенях окисления могут восстанавливаться до I2, а не до йодид-иона
KIO3 + 5KI + 3H2SO4 → 3I2 + 3K2SO4 + 3H2O.
3) Галогенид-ионы окисляются, как правило, до простых веществ: Cl2, Br2, I2:
14HCl + K2Cr2O7 → 3Cl2 + 2CrCl3 + 2KCl + 7H2O
16HCl + 2KMnO4  → 5Cl2 + 2MnCl2 + 2KCl + 8H2O
4) Йодид меди восстанавливает серную кислоту до SO2, тогда как йодиды активных металлов до H2S:
2CuI + 4H2SO4(конц.) → I2 + 2SO2 + 2CuSO4 + 4H2O
8KI + 5H2SO4(конц.) → 4I2 + H2S + 4K2SO4 + 4H2O
5) Концентрированной серной кислотой окисляются только бромид- и йодид-ионы. В первом случае образуется SO2, во втором H2S.
2KBr + 2H2SO4(конц.) → Br2 + SO2 + K2SO4 + 2H2O
8KI + 5H2SO4(конц.) → 4I2 + H2S + 4K2SO4 + 4H2O.
6) Более сильные галогены вытесняют менее сильные из галогенидов. В ряду F2, Cl2, Br2, I2 окислительные свойства ослабевают.
Все галогены вытесняют серу из сульфидов:
(NH4)2S + Br2 → S + 2NH4Br.
Сера
1) Сульфид-ионы обычно окисляются до S типичными окислителями: Br2, I2, растворами солей K2Cr2O7, KMnO4 и др.:
3Na2S + K2Cr2O7 + 7H2SO4 → 3S 
5Na2S + 2KMnO4 + 16HCl → 5S 
H2S + Br2 → S 
H2S + H2O2 → S 
2) С H2SO4(к) сероводород и сульфиды реагируют с образованием SO2, аналогично реакции кислоты с серой:
S + H2SO4(конц.) → 3SO2 
H2S + 3H2SO4(конц.) → 4SO2 
3) Окисление H2S и сульфидов до сульфат-ионов протекает в реакциях с такими окислителями, как Cl2 в воде, H2O2, HNO3(конц.) при нагревании:
H2S + 4Cl2 + 4H2O → H2SO4 + 8HCl
H2S + 8HNO3(конц.) → H2SO4 + 8NO2 
PbS + 4H2O2 → PbSO4 + 4H2O (черный сульфид свинца превращается в белый сульфат)
4) Сульфит-ионы любыми окислителями окисляются до сульфат-иона:
3Na2SO3 + 2KMnO4 + H2O → 2MnO2 + 2Na2SO4 + 2KOH
3K2SO3 + 2K2CrO4 + 5H2O → 2Cr(OH)3 + 3K2SO4 + 4KOH.
Медь
1) Соединения Cu +2 окисляют соединения S +4 и I – (восстанавливаясь до Cu +1 ):
2CuCl2 + SO2 + 2H2O → 2CuCl 
2Cu(NO3)2 + 4KI → 2CuI 

В реакции с аммиаком выделяется металлическая медь:
3CuO + 2NH3 → N2 
2) Йодиды меди реагируют с H2SO4(к) с образованием SO2, тогда как йодиды щелочных металлов с образованием H2S:
2CuI + 4H2SO4 → 2CuSO4 + I2 + 2SO2 + 4H2O
8KI + 5H2SO4(конц.) → 4K2SO4 + 4I2 + H2S + 4H2O
3) Медь по-разному реагирует с галогенами:
Cu + Cl2 → CuCl2
Cu + Br2 → CuBr2
2Cu + I2 → 2CuI (соль меди +1)
4) Медь в степени окисления +2 восстанавливается самой медью:
CuO + Cu → Cu2O (t)
CuCl2 + Cu → 2CuCl (t).
Железо
Fe2O3 + 6HI → 2FeI2 + I2 
2FeCl3 + 3Na2S → 2FeS 

2FeCl3 + H2S → 2FeCl2 + S 
2FeCl3 + Na2SO3 +H2O → 2FeCl2 + Na2SO4 + 2HCl
2FeCl3 + Cu → CuCl2 + 2FeCl2 (соль железа +2)
Fe2(SO4)3 + Cu → CuSO4 + 2FeSO4 (соль железа +2)
2Fe(NO3)3 + Fe → 3Fe(NO3)2 (соль железа +2)
2) В кислой среде соединения Fe +2 окисляются такими окислителями, как KMnO4, K2Cr2O7, Na2O2, HNO3, H2SO4(к) и др. до солей Fe +3 :
6FeCl2 + Na2Cr2O7 + 14HCl → 6FeCl3 + 2CrCl3 + 2NaCl + 7H2O
2FeSO4 + Na2O2 + 2H2SO4 → Fe2(SO4)3 + Na2SO4 + 2H2O
3) В щелочной среде образуется гидроксид железа (III):
FeCl2 + KMnO4 + 3KOH → K2MnO4 + Fe(OH)3 + 2KCl
2FeSO4 + 2KMnO4 + 6NaOH → K2MnO4 + 2Fe(OH)3 + Na2MnO4 + 2Na2SO4
4) Железо по-разному реагирует с галогенами:
2Fe + 3F2 → 2FeF3
2Fe + 3Cl2 → 2FeCl3
2Fe + 3Br2 → 2FeBr3
Fe + I2 → FeI2 (соль железа +2)
Марганец
1) В кислой среде образуются соли Mn +2 :
K2MnO4 + 8HBr → MnBr2 + 2Br2 + 2KBr + 4H2O
2KMnO4 + 5SO2 + 2H2O → 2MnSO4 + K2SO4 + 2H2SO4
2) В щелочной среде образуется манганат-ион MnO4 2– (зеленого цвета):
MnSO4 + 2Br2 + 8KOH → K2MnO4 + 4KBr + Na2SO4 + 4H2O
2KMnO4 + 2FeSO4 + 6NaOH → K2MnO4 + 2Fe(OH)3 
3) В нейтральной среде образуется осадок бурого цвета MnO2:
3MnSO4 + 2KMnO4 + 2H2O → 5MnO2 
2KMnO4 + 3K2S + 4H2O → 2MnO2 

K2MnO4 + Na2S + 2H2O → S 

Хром
1) Восстановление дихроматов в кислой среде протекает с образованием солей Cr +3 :
Na2Cr2O7 + 6NaI + 7H2SO4 → Cr2(SO4)3 + 3I2 
K2Cr2O7 + 6FeSO4 + 7H2SO4 → Cr2(SO4)3 + 3Fe2(SO4)3 + K2SO4 + 7H2O
K2Cr2O7 + 3KNO2 + 8HNO3 → 2Cr(NO3)3 + 5KNO3 + 4H2O
2) Окисление соединений Cr +2 в кислой среде протекает с образованием солей Cr +3 :
6CrCl2 + K2Cr2O7 + 14HCl → 8CrCl3 + 2KCl + 7H2O
2CrCl2 + 4H2SO4(конц.) → Cr2(SO4)3 + SO2 + 4HCl + 2H2O
3) Окисление соединений Cr +3 очень сильными окислителями с щелочами или с карбонатами щелочных металлов протекает с образованием хроматов (типичные окислители: KNO3, Cl2, KClO3, H2O2 и др. в щел. среде):
Cr2O3 + 3KNO3 + 2K2CO3 → 2K2CrO4 + 3KNO2 + 2CO2
Cr2(SO4)3 + 3Cl2 + 16KOH → 2K2CrO4 + 6KCl + 3K2SO4 + 8H2O
2Cr(OH)3 + KClO3 + 4NaOH → 2Na2CrO4 + KCl + 5H2O
2Cr(OH)3 + 3H2O2 + 4KOH → 2K2CrO4 + 8H2O
4) Соединения Cr +6 в различных средах:
В щелочной среде устойчивы соли хромовой кислоты (хроматы, желтого цвета), например, Na2CrO4.
В кислой среде устойчивы соли дихромовой кислоты (дихроматы, оранжевого цвета), например, Na2Cr2O7.
CrO3 + 2KOH → K2CrO4 + H2O
2K2CrO4 + H2SO4 → K2Cr2O7 + K2SO4 + H2O (в кислотной среде желтая окраска переходит в оранжевую).
Na2Cr2O7 + 2NaOH → 2Na2CrO4 + H2O (в щелочной среде оранжевая окраска переходит в желтую).
Среда раствора
1) С карбонатами щелочных металлов реакции протекают аналогично щелочной среде реакции:
Cr2O3 + 3KNO3 + 2K2CO3 → 2K2CrO4 + 3KNO2 + 2CO2
MnO2 + KNO3 + K2CO3 → K2MnO4 + KNO2 + CO2
2) Если в реакцию вступает оксид серы (IV) SO2 в нейтральном растворе, то реакция протекает аналогично кислой среде раствора:
2KMnO4 + 5SO2 + 2H2O → 2MnSO4 + K2SO4 + 2H2SO4.
Поэтому очень важно не зубрить окислительно-восстановительные реакции, а знать какие соединения проявляют окислительные, а какие восстановительные свойства, и знать основные правила, приведенные выше.
Окислительно-восстановительные реакции в химии
Содержание:
Окислительно—восстановительные реакции (ОВР) – это реакции, при протекании которых происходит изменение степени окисления химических элементов, входящих в состав реагентов. Степень окисления – условный (формальный) заряд атома в химическом соединении, который находят, считая химические связи в соединении чисто ионными.
На странице -> решение задач по химии собраны решения задач и заданий с решёнными примерами по всем темам химии.
Окислительно-восстановительные реакции
Окислительно-восстановительные реакции — это химические реакции, сопровождающиеся изменением степени окисления у атомов реагирующих веществ. При этом некоторые частицы отдают электроны, а некоторые получают.
Электролиз
Теория окислительно-восстановительных реакций
Все химические реакции можно разделить на два типа. К первому из них относятся реакции, протекающие без изменения степени окисления атомов, входящих в состав реагирующих веществ. Например:
Как видно, степень окисления каждого из атомов до и после реакции осталась без изменения.
Ко второму типу относятся реакции, идущие с изменением степени окисления атомов реагирующих веществ. Например:
Здесь в первой реакции атомы хлора и кислорода, а во второй — атомы брома и хлора изменяют степень окисления.
Реакции, протекающие с изменением степени окисления атомов, входящих в состав реагирующих веществ, называются окислительно-восстановительными.
Изменение степени окисления связано с оттягиванием или перемещением электронов.
Окислительно-восстановительные реакции — самые распространенные и играют большую роль в природе и технике. Они являются основой жизнедеятельности. С ними связаны дыхание и обмен веществ в живых организмах, гниение и брожение, фотосинтез в зеленых частях растений. Их можно наблюдать при сгорании топлива, в процессах коррозии металлов и при электролизе. Они лежат в основе металлургических процессов и круговорота элементов в природе. С их помощью получают аммиак, щелочи, азотную, соляную и серную кислоты и многие другие ценные продукты. Благодаря окислительно-восстановительным реакциям происходит превращение химической энергии в электрическую — в гальванических элементах и аккумуляторах. Они же лежат в основе мероприятий по охране природы. Поэтому эти реакции преобладают и в школьном курсе неорганической химии.
Рассмотрим основные положения теории окислительно-восстановительных реакций.
1. Окислением называется процесс отдачи электронов атомом, молекулой или ионом. Например:
При окислении степень окисления повышается.
2. Восстановлением называется процесс присоединения электронов атомом, молекулой или ионом. Например:
При восстановлении степень окисления понижается.
3. Атомы, молекулы или ионы, отдающие электроны, называются восстановителями. Во время реакции они окисляются. Атомы, молекулы или ионы, присоединяющие электроны, называются окислителями. Во время реакции они восстанавливаются. Так как атомы, молекулы и ионы входят в состав определенных веществ, то и эти вещества соответственно называются восстановителями или окислителями.
4. Окисление всегда сопровождается восстановлением, и наоборот, восстановление всегда связано с окислением, что можно выразить уравнениями:
Поэтому окислительно-восстановительные реакции представляют собой единство двух противоположных процессов — окисления и восстановления.
Число электронов, отдаваемых восстановителем, равно числу электронов, присоединяемых окислителем.
При этом, независимо от того, переходят ли электроны с одного атома на другой полностью или же лишь частично оттягиваются к одному из атомов, условно говорят только об отдаче и присоединении электронов.
Рис. 7.1. Схема гальванического элемента, построенного на основе окислительно-восстановительной реакции
Приведенная на рис. 7.1 схема представляет собой гальванический элемент, построенный на основе окислительно-восстановительной реакции. Он состоит из двух полуэлементов, в первом протекает процесс окисления восстановителя:
а во втором — процесс восстановления окислителя;
Поскольку эти процессы протекают одновременно, то, умножив последнее уравнение на коэффициент 2 (для уравнивания числа отданных и присоединенных электронов) и суммируя почленно приведенные уравнения, получим уравнение реакции:
Всякая окислительно-восстановительная реакция может служить источником электрического тока, если она протекает в гальваническом элементе.
Важнейшие восстановители и окислители
Восстановители и окислители могут быть как простыми веществами, т. е. состоящими из одного элемента, так и сложными.
В соответствии с их местом в периодической системе элементов атомы большинства металлов содержат на внешнем энергетическом уровне 1—2 электрона. Поэтому в химических реакциях они отдают валентные электроны, т. е. окисляются. Металлы обладают восстановительными свойствами.
В периодах с повышением порядкового номера элемента восстановительные свойства простых веществ понижаются, а окислительные возрастают и становятся максимальными у галогенов. Так, например, в III периоде натрий — самый активный в периоде восстановитель, а хлор—самый активный в периоде окислитель.
У элементов главных подгрупп с повышением порядкового номера усиливаются восстановительные свойства и ослабевают окислительные. Лучшие восстановители — щелочные металлы, а наиболее активные из них Fr и Cs. Лучшие окислители — галогены. Элементы главных подгрупп IV—VII групп (неметаллы) могут как отдавать, так и принимать электроны и проявлять восстановительные и окислительные свойства. Исключение составляет фтор. Он проявляет только окислительные свойства, так как обладает наибольшей относительной электроотрицательностью (см. табл. 2.2).
Элементы побочных подгрупп (четных рядов больших периодов) имеют металлический характер, так как на внешнем уровне их атомов содержится 1—2 электрона. Поэтому их простые вещества являются восстановителями. Таким образом, в отличие от простых веществ металлов, выступающих в роли восстановителей, простые вещества — неметаллы проявляют себя и как окислители, и как восстановители.
Окислительные или восстановительные свойства сложных веществ зависят от степени окисления атома данного элемента. Например, 
Важнейшие восстановители и окислители приведены в табл. 7.1.
Таблица 7.1. Важнейшие восстановители и окислители
Составление уравнении окислительно-восстановительных реакции
Применяются два метода составления уравнений окислительно-восстановительных реакций — метод электронного баланса и метод полуреакций.
Метод электронного баланса
В этом методе сравнивают степени окисления атомов в исходных и конечных веществах, руководствуясь правилом: число электронов, отданных восстановителем, должно равняться числу электронов, присоединенных окислителем. Для составления уравнения надо знать формулы реагирующих веществ и продуктов реакции. Последние определяются либо опытным путем, либо на основе известных свойств элементов. Рассмотрим применение этого метода на примерах.
Пример 1. Составление уравнения реакции меди с раствором нитрата палладия (II). Запишем формулы исходных и конечных веществ реакции и покажем изменения степеней окисления:
Медь, образуя ион меди, отдает два электрона, ее степень окисления повышается от 0 до +2. Медь — восстановитель. Ион палладия, присоединяя два электрона, изменяет степень окисления от +2 до 0. Нитрат палладия (II) — окислитель. Эти изменения можно выразить электронными уравнениями
из которых следует, что при восстановителе и окислителе коэффициенты равны 1. Окончательное уравнение реакции:
Как видно, в суммарном уравнении реакции электроны не фигурируют.
Чтобы проверить правильность составленного уравнения, подсчитываем число атомов каждого элемента в его правой и левой частях. Например, в правой части 6 атомов кислорода, в левой также 6 атомов; палладия 1 и 1; меди тоже 1 и 1. Значит, уравнение составлено правильно.
Переписываем это уравнение в ионной форме:
И после сокращения одинаковых ионов получим
Пример 2. Составление уравнения реакции взаимодействия оксида марганца (IV) с концентрированной соляной кислотой (с помощью этой реакции в лабораторных условиях получают хлор). Запишем формулы исходных и конечных веществ реакции:
Покажем изменение степеней окисления атомов до и после реакции:
Эта реакция окислительно-восстановительная, так как изменяются степени окисления атомов хлора и марганца. HCl — восстановитель, МnO2 — окислитель. Составляем электронные уравнения:
и находим коэффициенты при восстановителе и окислителе. Они соответственно равны 2 и 1. Коэффициент 2 (а не 1) ставится потому, что 2 атома хлора со степенью окисления — 1 отдают 2 электрона. Этот коэффициент уже стоит в электронном уравнении:
Находим коэффициенты для других реагирующих веществ. Из электронных уравнений видно, что на 2 моль НСl приходится 1 моль МnО2. Однако, учитывая, что для связывания образующегося двухзарядного иона марганца нужно еще 2 моль кислоты, перед восстановителем следует поставить коэффициент 4. Тогда воды получится 2 моль. Окончательное уравнение имеет вид
Проверку правильности написания уравнения можно ограничить подсчетом числа атомов одного какого-либо элемента, например хлора: в левой части 4 и в правой 2+2=4.
Поскольку в методе электронного баланса изображаются уравнения реакций в молекулярной форме, то после составления и проверки их следует написать в ионной форме. Перепишем составленное уравнение в ионной форме:
и после сокращения одинаковых ионов в обеих частях уравнения (они подчеркнуты) получим
Пример 3. Составление уравнения реакции взаимодействия сероводорода с подкисленным раствором перманганата калия. Напишем схему реакции — формулы исходных и полученных веществ:
Затем покажем изменение степеней окисления атомов до и после реакции:
Изменяются степени окисления у атомов серы и марганца (H2S — восстановитель, КMnO4 — окислитель). Составляем электронные уравнения, т. е. изображаем процессы отдачи и присоединения электронов:
И наконец, находим коэффициенты при окислителе и восстановителе, а затем при других реагирующих веществах. Из электронных уравнений видно, что надо взять 5 моль H2S и 2 моль КMnO4, тогда получим 5 моль атомов S и 2 моль КMnO4. Кроме того, из сопоставления атомов в левой и правой частях уравнения, найдем, что образуется также 1 моль K2SO4 и 8 моль воды.
Окончательное уравнение реакции будет иметь вид
Правильность написания уравнения подтверждается подсчетом атомов одного элемента, например кислорода; в левой части их 2 


Переписываем уравнение в ионной форме:
Известно, что правильно написанное уравнение реакции является выражением закона сохранения массы веществ. Поэтому число одних и тех же атомов в исходных веществах и продуктах реакции должно быть одинаковым. Должны сохраняться и заряды. Сумма зарядов исходных веществ всегда должна быть равна сумме зарядов продуктов реакции.
Метод полуреакций, или ионно-электронный метод
Как показывает само название, этот метод основан на составлении ионных уравнений для процесса окисления и процесса восстановления с последующим суммированием их в общее уравнение. В качестве примера составим уравнение той же реакции, которую использовали при объяснении метода электронного баланса (см. пример 3). При пропускании сероводорода H2S через подкисленный раствор перманганата калия КMnO4 малиновая окраска исчезает и раствор мутнеет. Опыт показывает, что помутнение раствора происходит в результате образования элементарной серы, т. е. протекания процесса:
Эта схема уравнена по числу атомов. Для уравнивания по числу зарядов надо от левой части схемы отнять два электрона, после чего можно стрелку заменить на знак равенства:
Это первая полуреакция — процесс окисления восстановителя H2S.
Обесцвечивание раствора связано с переходом иона 
В кислом растворе кислород, входящий в состав ионов МnO4, вместе с ионами водорода в конечном итоге образует воду. Поэтому процесс перехода записываем так:
Чтобы стрелку заменить на знак равенства, надо уравнять и заряды. Поскольку исходные вещества имеют семь положительных зарядов (7+), а конечные —два положительных (2+), то для выполнения условия сохранения зарядов надо к левой части схемы прибавить пять электронов:
Для составления общего уравнения реакции надо уравнения полуреакций почленно сложить, предварительно уравняв числа отданных и полученных электронов. В этом случае по правилам нахождения наименьшего кратного определяют соответствующие множители, на которые умножаются уравнения полуреакций. Сокращенно запись проводится так:
Проверяем правильность составленного в ионной форме уравнения: число атомов кислорода в левой части 8, в правой 8; число зарядов; в левой части (2-)+(6+)=4+, в правой 2(2+)=4+. Уравнение составлено правильно, так как атомы и заряды уравнены.
Методом полуреакций составляется уравнение реакции в ионной форме. Чтобы от него перейти к уравнению в молекулярной форме, поступаем так: в левой части конного уравнения к каждому аниону подбираем соответствующий катион, а к каждому катиону — анион. Затем те же ионы в таком же числе записываем в правую часть уравнения, после чего ноны объединяем в молекулы:
Таким образом, составление уравнений окислительно-восстановительных реакций с помощью метода полуреакций приводит к тому же результату, что и метод электронного баланса.
Сопоставим оба метода. Достоинство метода полуреакций по сравнению с методом электронного баланса в том, что в нем применяются не гипотетические ионы, а реально существующие. В самом деле, в растворе нет ионов 

Влияние среды на характер протекания реакций
Обычно для создания в растворе кислой среды используют серную кислоту. Азотную и соляную кислоту применяют редко: первая сама является окислителем, вторая способна окисляться. Для создания щелочной среды применяются растворы гидроксидов калия или натрия.
Руководствуясь приведенной схемой, составим методом полуреакций уравнения реакции взаимодействия сульфита натрия Na2SO3 (восстановитель) с перманганатом калия КМnO4 (окислитель) в различных средах (примеры 1—3).
Пример 1. В кислой среде:
Пример 2. В нейтральной или слабощелочной среде:
Пример 3. В сильнощелочной среде:

или
Пероксид водорода в зависимости от среды восстанавливается согласно схеме:
Здесь Н2O2 выступает как окислитель. Например:
Однако, встречаясь с очень сильным окислителем, таким, как КMnO4, пероксид водорода выступает как восстановитель. Например:
Классификация окислительно-восстановительных реакций
Обычно различают три типа окислительно-восстановительных реакций: межмолекулярные, внутримолекулярные и реакции диспропорционирования.
К межмолекулярным относятся реакции, в которых окислитель и восстанови!ель находятся в разных веществах. Рассмотренные в § 7.3 и § 7.4 реакции относятся к этому типу. Сюда же следует отнести и реакции между разными веществами, в которых атомы одного и того же элемента имеют различные степени окисления:
К внутримолекулярным относятся такие реакции, в которых окислитель и восстановитель находятся в одном и том же веществе. В этом случае атом с более положительной степенью окисления окисляет атом с меньшей степенью окисления. Такими реакциями являются реакции термического разложения. Например:
Сюда же следует отнести и разложение веществ, в которых атомы одного и того же элемента имеют разные степени окисления:
Протекание реакций диспропорционирования сопровождается одновременным увеличением и уменьшением степени окисления атомов одного и того же элемента. При этом исходное вещество образует соединения, одно из которых содержит атомы с более высокой, а другое с более низкой степенями окисления. Очевидно, эти реакции возможны для веществ, содержащих атомы с промежуточной степенью окисления. Примером может служить превращение манганата калия 

К реакциям диспропорционирования относятся и такие часто встречающиеся реакции, как
Раньше реакции диспропорционирования называли реакциями самоокисления — самовосстановления, сейчас это название почти не употребляется.
Сущность электролиза
В итоге на катоде выделяется металлический натрий, а на аноде хлор.
Если теперь почленно сложить уравнения этих двух электродных реакций (предварительно умножив первое на 2), то получим общее, пли суммарное, уравнение электролиза хлорида натрия:
Рис. 7.2. Схема электролиза расплава NaCl
Эта реакция является окислительно-восстановительной: на аноде протекает процесс окисления, на катоде — процесс восстановления.
Электролизом называется окислительно-восстановительный процесс, протекающий на электродах при прохождении электрического тока через расплав или раствор электролита.
Сущность электролиза состоит в осуществлении за счет электрической энергии химических реакций — восстановления на катоде и окисления на аноде. При этом катод отдает электроны катионам, а анод принимает электроны от анионов.
Сущность электролиза удобно изображать с помощью схемы, которая показывает диссоциацию электролита, направление движения ионов, процессы на электродах и выделяющиеся вещества. Схема электролиза расплава хлорида натрия выглядит так:
Для проведения электролиза электроды погружают в расплав или раствор электролита и соединяют их с источником постоянного тока. Прибор, в котором проводят электролиз, называют электролизером или электролитической ванной (рис. 7.2),
Электролиз водных растворов электролитов
Надо различать электролиз расплавленных электролитов и их растворов. В последнем случае в процессах могут участвовать молекулы воды.
а на аноде окисляются хлорид-ионы:
или в молекулярной форме:
Катодные и анодные процессы
Как же протекает восстановительный процесс на катоде в водных растворах?
Ответ можно получить с помощью ряда стандартных электродных потенциалов (см. табл. 12.1). Здесь возможны три случая:
1) катионы металлов, имеющих больший стандартный электродный потенциал, чем у водорода (от Сu 2+ до Аl 3+ ), при электролизе практически полностью восстанавливаются на катоде;
2) катионы металлов, имеющих малый стандартный электродный потенциал (от Li + до Аl 3+ включительно), не восстанавливаются на катоде, а вместо них восстанавливаются молекулы воды;
3) катионы металлов, имеющих стандартный электродный потенциал, меньший, чем у водорода, но больший, чем у алюминия (от Аl 3+ до Н + ), при электролизе на катоде восстанавливаются одновременно о молекулами воды.
Характер реакций, протекающий на аноде, зависит как от присутствия молекул воды, так и от вещества, из которого сделан анод. Обычно аноды подразделяют на нерастворимые и растворимые. Первые изготавливаются из угля, графита, платины, иридия; вторые — из меди, серебра, цинка, кадмия, никеля и других металлов.
Растворимый анод при электролизе сам подвергается окислению, т. е. посылает электроны во внешнюю цепь. При отдаче электронов смещается равновесие между электродом и раствором;
и анод растворяется.
Примеры электролиза водных растворов электролитов приведены в § 7.9.
Применение электролиза
Электролиз находит весьма широкое применение. Для защиты металлических изделий от коррозии на их поверхность наносится тончайший слой другого металла — хрома, серебра, золота, меди, никеля и т. д. Иногда применяют многослойное покрытие. Например, внешние детали автомобиля сначала покрывают тонким слоем меди, на медь наносят тончайший слой никеля, а на него — слой хрома.
Нанесенные на металлы электролизом покрытия получаются ровными по толщине, прочными, служат долго, и, кроме того, таким способом можно покрывать изделия любой формы. Эту отрасль прикладной электрохимии называют гальваностегией. Кроме защиты от коррозии, гальванические покрытия иногда придают красивый декоративный вид предметам.
Другая отрасль электрохимии, близкая по принципу к гальваностегии, названа гальванопластикой. Это получение точных металлических копий о различных предметов. Предмет, с которого хотят изготовить копию, покрывают воском, дают воску застыть и получают восковую матрицу, на которой все углубления копируемого предмета будут выпуклостями. Внутреннюю поверхность матрицы покрывают тонким слоем графита, проводящим электрический ток. Этот графитовый катод опускают в ванну с раствором сульфата меди; анодом служит медь. При электролизе модный анод растворяется, а на катоде осаждается медь. Таким образом получается точная медная копия предмета. С помощью гальванопластики изготовляют клише для печати, грампластинки, металлизируют различные предметы. Гальванопластика открыта русским ученым Б. С. Якоби (1838).
Электролиз используется для получения многих металлов — щелочных, щелочноземельных, алюминия, лантаноидов и др., а также для очистки некоторых металлов от примесей.
В дальнейшем при изучении химии вы встретитесь с другими важными применениями электролиза в технике, в искусстве и быту.
Окислительно- востановительные реакции кратко и подробно
ОВР – реакции, протекающие с изменением степеней окисления элементов, образующих молекулы реагирующих веществ.
Степень окисления
Степень окисления атома относится к основным понятиям химии. Она введена для характеристики состояния атома в соединениях.
Степень окисления — условный заряд атома в соединении, вычисленный исходя
из предположения, что он состоит только из ионов.
Если атом отдает электроны, то он получает положительную степень окисления; если атом принимает электроны, то он получает отрицательный заряд. У простых веществ степень окисления равна 0 (нуль).
Положительную степень окисления в соединениях всегда имеют металлы 

Если при написании требуется показать заряд несвязанного иона (например, находящегося в растворе), то знак 

Если необходимо составить формулу бинарного соединения по степени окисления, то поступают следующим образом:
1) пишут химические знаки элементов в том порядке, в котором элементы следуют друг за другом в ряду электроотрицательности (на первом месте знак элемента, отдающего электроны), например, 
2) исходя из строения атомов, записывают над знаками степени окисления: 
3) проставляют индексы так, чтобы число положительного заряда
было равно числу отрицательного заряда:
В случае, если следует определить степень окисления элементов в предложенной формуле, поступают следующим образом:
1. Как правило, на первом месте записывают элементы с положительными степенями окисления, а на втором — элемент с отрицательной степенью окисления.
Устанавливают, какой из двух элементов получил электроны. Например, в соединении 
2. Определяют, сколько электронов получил кислород. Так как кислород находится в 
Поскольку атомов у кислорода пять, то общий заряд кислорода
3. На атоме фосфора, следовательно, общий положительный заряд (+10), а на один атом приходится (+5).
Итак, результат:
4. Предлагаемое соединение прочитывается слева направо, а название вещества, наоборот, — справа налево.
К первому слогу латинского названия кислорода — оксигениум — добавляют суффикс «ид’: оксид фосфора
В случае более сложных соединений, например 
1) проставляют степень окисления кислороду (-2) и водороду (+1).
2) подсчитывают заряд серы так:
3) если формула содержит скобки, то действуют похожим образом, например:
Существуют формулы и более сложного состава, но учиться считать их степень окисления вы будете позднее. Изменение степени окисления элементов в Периодической системе можно проследить по таблице 13.
Пользуясь алгоритмом, выведем формулы кислородных и водородных соединений рассмотренных элементов (табл. 14, 15), имея в виду, что у кислорода в них степень окисления (-2), а водорода (+1). Мы получим:
1) два ряда кислородных соединений (табл. 14):
2) ряд водородных соединений (табл. 15):
Степень окисления любого элемента в простом веществе равна 0.
Сумма степеней окисление всех атомов в составе нейтральной молекулы равна 0.
Если соединение обрадовано двумя элементами, то у элемента с большей электроотрицательностью степень окисления меньше нуля, а у элемента с меньшей электроотрицательностью — больше нуля.
Максимальная положительная степень окисления любого элемента главной пол группы равна номеру группы в Периодической системе элементов, а минимальная степень окисления для металлов равна 0, а для неметаллов равна N-8, где N — номер группы.
ОВР и химия
Кроме известных вам типов химических реакций: соединения, разложения, замещения, обмена — существуют и другие классификации химических реакций. Рассмотрим реакции, расставим в них степень окисления элементов:
В уравнении (1) ни один из элементов не меняет степень окисления.
В уравнении (2) степень окисления меняется у цинка и водорода.
Реакции, идущие без изменения степени окисления элементов» называются неокислительно-восстановительными. Такими всегда бывают реакции обмена.
Реакции, идущие с изменением степени окисления элементов, называются окислительно-восстановительными. Такими реакциями всегда являются реакции замещения. Реакции соединения и разложения могут быть двух типов.
Рассмотрим основные положения теории окислительно-восстановительных реакций:
1. Окислением называется процесс отдачи электронов атомом, молекулой или ионом. Например:
2. Восстановлением называется процесс присоединения электронов атомом, молекулой или ионом. Например:
При окислении степень окисления элемента повышается, а при восстановлении степень окисления понижается (рис. 25).
3. Атомы, молекулы или ионы, отдающие электроны, называются восстановителями. Во время реакций они окисляются.
4. Атомы, молекулы или ионы, присоединяющие электроны, называются окислителями. Во время реакций они восстанавливаются.
Так как атомы, молекулы, ионы входят в состав определенных веществ, то эти вещества соответственно называются восстановителями или окислителями.
5. Окисление всегда сопровождается восстановлением, и наоборот.
6. Число электронов, отданных восстановителем, равно числу электронов, присоединенных окислителем.
Рассмотрим механизм окислительно-восстановительной реакции подробнее. Например, взаимодействие кальция и фосфора. Кальций как металл отдает свои внешние электроны, а фосфор принимает недостающие электроны:
Затем найденное число электронов вынесем за черту, после этого находим общее кратное между числами отданных и принятых электронов:
Найденные числа последнего столбца называются основными коэффициентами, их расставляют к элементам с нулевой степенью окисления или наименьшей, если нулевой нет:
Такой подбор коэффициентов называется методом электронного баланса.
Рассмотрим данный метод подбора коэффициентов на более сложном примере. Такая реакция происходит при зажигании спичек:
Этапы подбора коэффициентов:
1) расставляем степень окисления у каждого элемента:
2) определяем, какие элементы изменили степень окисления. Это фосфор и хлор;
3) составляем две полуреакции для фосфора и хлора:
4) записываем найденные числа электронов за черту, находим общее кратное:
5) выставляются полученные основные коэффициенты: 
Для простых веществ: 
Если затрудняетесь определить, отдает или принимает элемент электроны, используйте схему 4:
Например, для полуреакции:
Окислительно-воссталовительные реакции — это самые распространенные реакции (рис. 26). Они играют важную роль в природе и технике, являются основой жизнедеятельности. С ними связаны дыхание, обмен веществ в живых организмах, гниение, брожение, фотосинтез. Их можно наблюдать при горении топлива, получении чугуна и стали и т. д. Они лежат в основе круговорота элементов в природе, с их помощью получают многие ценные продукты.
Окисление — процесс отдачи электронов, который сопровождается повышением степени окисление элемента. Вещество, отдающее электроны, называется восстановителем. Восстановление — процесс присоединения электронов, который сопровождается понижением степени окисления элемента. Вещество, принимающее электроны, является окислителем.
Окисление всегда сопровождается восстановлением, и наоборот. Число отданных электронов восстановителем равно числу электронов, присоединенных окислителем.
Окисленность элементов
Когда элемент находится в свободном состоянии — образует простое вещество, тогда движение электронов около всех атомов этого вещества происходит одинаково. Это справедливо для всех простых веществ, независимо от их структуры. Например, в молекуле водорода электроны в равной мере движутся около обоих атомов: молекула 
Иначе обстоит дело в сложных веществах. Химические связи между атомами различных элементов несимметричны; в молекулах сложных веществ осуществляются, как правило, полярные ко-валентные связи. В ионных соединениях эта неравномерность распределения электронов максимальна — при образовании веществ с ионной связью валентные электроны практически полностью переходят от атома одного элемента к атому другого.
Неравномерность распределения электронов между атомами в соединениях получила название окисленности. При этом элемент, электроны которого смещаются к атомам другого элемента (полностью в случае ионной связи или частично в случае полярной), проявляет положительную окисленность. Элемент, к атомам которого смещаются электроны атома другого элемента, проявляет отрицательную окисленность.
Число электронов, смешенных от одного атома данного элемента (при положительной окисленности) или к одному атому данного элемента (при отрицательной окисленности), называется степенью окисленности элемента*.
* Эту величину называют также степенью окисления или окислительным числом элемента.
В простых веществах степень окисленности элемента всегда равна нулю. В соединениях некоторые элементы проявляют всегда одну и ту же степень окисленности, но для большинства элементов она в различных соединениях различна.
Постоянную степень окисленности имеют щелочные металлы 









Определим в качестве примера степень окисленности углерода в 


Для установления степени окисленности элементов в соединениях можно пользоваться таблицей электроотрицательностей элементов (табл. 6). При этом следует иметь в виду, что при образовании химической связи электроны смещаются к атому более электроотрицательного элемента. Так, относительная электроотрицательность фосфора равна 2,2, а иода 2,6. Поэтому в соединении 





Окислительно-восстановительные реакции и их определения
Все химические реакции можно разбить на две группы. В реакциях первой группы окисленность всех элементов, входящих в состав реагирующих веществ, остается неизменной, а в реакциях второй группы окисленность одного или нескольких элементов изменяется.
В качестве примера реакций первой группы можно привести реакцию нейтрализации:
Примером реакции второй группы может служить взаимодействие металла с кислотой:
Если при реакции нейтрализации ни один элемент не изменяет степень своей окисленности, то во втором примере степень окисленности цинка изменяется от 0 до +2, а водорода—от +1 до 0.
Реакции, в результате которых изменяются степени окисленности элементов, называются окислительно восстановительными,
Окислительно-восстановительные реакции имеют очень большое значение в биологических системах. Фотосинтез, дыхание, пищеварение —все это цепи окислительно-восстановительных ре-акций. В технике значение окислительно-восстановительных реакций также очень велико. Так, вся металлургическая промышленность основана на окислительно-восстановительных процессах в ходе которых металлы выделяются из природных соединений.’
Простым примером окислительно-восстановительной реакции может служить реакция образования ионного соединения из простых веществ, например, взаимодействие натрия с хлором:
Эта реакция, как всякая гетерогенная реакция, протекает в несколько стадий. В ходе одной из них атомы натрия превращаются в положительно заряженные ионы; степень окисленности натрия изменяется от 0 до +1:
Такой процесс — отдача электронов, сопровождающаяся повышением степени окисленности элемента,— называется окислением.
Электроны, отдаваемые натрием, принимаются атомами хлора, которые превращаются при этом в отрицательно заряженные ионы; степень окисленности хлора изменяется от 0 до —1:
Присоединение электронов, сопровождающееся понижением степени окисленности элемента, называется восстановлением.
Таким образом, в рассматриваемой реакции натрий окисляется, а хлор восстанавливается.
Вещество, в состав которого входит окисляющийся элемент, называется восстановителем, а вещество, содержащее восстанавливающийся элемент, окислителем. Следовательно, в данном примере натрий — восстановитель, а хлор — окислитель.
Из уравнений процессов восстановления и окисления видно, что одна молекула хлора, восстанавливаясь, присоединяет два электрона, а окисление одного атома натрия сопровождается отдачей одного электрона. Общее число электронов в системе при химических реакциях не изменяется: число электронов, отдаваемых молекулами (атомами, ионами) восстановителя, равно числу электронов, присоединяемых молекулами (атомами, ионами) окислителя. Поэтому одна молекула хлора может окислить два атома натрия.
Составление уравнений окислительно-восстановительных реакций
Мы рассмотрели простейший пример окислительно-восстановительной реакции — образование соединения из двух простых веществ. Обычно уравнения окислительно-восстановительных реакций носят более сложный характер и расстановка коэффициентов в них часто представляет довольно трудную задачу; приведем несколько примеров.
Пример 1. Взаимодействие между иодоводородом и концентрированной серной кислотой. Эта реакция протекает согласно схеме:
Если мы подсчитаем степень окисленности каждого элемента в исходных веществах и в продуктах реакции, то увидим, что она изменяется у иода и у серы. У иода в 


Уравнение процесса окисления иода имеет простой вид:
Уравнение восстановления серы более сложно, так как и исходное вещество 



Четыре атома кислорода, высвобождающиеся при этом процессе, должны связаться в четыре молекулы воды. Для этого понадобятся восемь ионов водорода. Кроме того, два иона водорода необходимы для образования молекулы 

Суммарный заряд ионов, находящихся в левой части этой схемы, равен восьми элементарным положительным зарядам, а в правой ее части имеются лишь незаряженные частицы. Поскольку суммарный заряд в ходе процесса не изменяется, то, следовательно, в процессе восстановления принимают участие также восемь электронов:
В рассматриваемом примере отношение числа электронов, принимаемых в процессе восстановления, к числу электронов, высвобождающихся- при окислении, равно 4: 1. Для получения суммарного уравнения реакции надо, складывая уравнения процессов восстановления и окисления, учесть это соотношение — умножить уравнение восстановления на 4. При этом в записи обычно справа от вертикальной черты проставляются необходимые множители;
Полученное уравнение реакции может быть представлено и в молекулярной форме:
Пример 2. Взаимодействие алюминия с нитратом калия в щелочной среде. Схема реакции:
Здесь степень окисленности изменяется у азота и алюминия. Металлический алюминий (степень окисленности равна 0) превращается в ион 
В щелочной среде источником кислорода, необходимого для протекания этого процесса, служат ионы 

В левой части схемы имеются четыре отрицательных заряда, а в правой — один. Следовательно, в ходе процесса отдаются три электрона:
Для получения уравнения восстановления будем исходить из схемы:
Здесь в ходе процесса атомы азота лишаются атомов кислорода и связываются с атомами водорода. В щелочной среде это возможно при участии молекул воды. Три молекулы воды понадобятся для связывания трех атомов кислорода и еще три молекулы воды — для образования молекулы 
Суммарный заряд правой части схемы равен девяти отрицательным зарядам, а левой — одному. Следовательно, в процессе принимают участие восемь электронов:
Отношение числа электронов, высвобождающихся в процессе окисления, к числу электронов, принимаемых при восстановлении, в данном примере равно 3:8. Следовательно, для получения суммарного уравнения реакции необходимо сложить уравнения процессов окисления и восстановления, умножив первое из них на 8, а второе на 3
или в молекулярной форме:
Пример 3. Каталитическое окисление аммиака. Этой реакцией пользуются в производстве азотной кислоты (см. 

При 
Согласно схеме реакции, степень окисленности изменяется у азота и у кислорода. У азота она возрастает от —3 до +2, а у кислорода уменьшается от 0 до —2. Запишем эти изменения в виде схем, отмечая степени окисленности элементов над их символами. Во избежание путаницы с зарядом иона, будем при этом пользоваться римскими цифрами:
Отношение числа электронов, принимаемых при восстановлении, к числу электронов, высвобождающихся при окислении, равно 4:5. Следовательно, пять молекул кислорода могут окислить четыре молекулы аммиака:
Составление уравнений реакций в трех рассмотренных примеpax проведено в определенном порядке. Его можно придерживаться и в других случаях при составлении уравнений окислительно-восстановительных реакций. Последовательность действий при этом следующая:
1. Составить схему реакции с указанием исходных и образующихся веществ.
2. Определить степень окисленности элементов в веществах правой и левой части схемы; отметить элементы, степень окисленности которых изменяется.
3. Составить уравнения процессов восстановления и окисления; найти отношение числа электронов, принимаемых при восстановлении и отдаваемых при окислении.
4. Сложить уравнения окисления и восстановления с учетом найденного отношения числа электронов (п. 3).
Важнейшие окислители и восстановители
Какие вещества могут проявлять свойства окислителей, а какие — восстановителей? Как уже говорилось, окислитель содержит в своем составе элемент, понижающий степень своей окисленности, а восстановитель содержит элемент, степень окисленности которого повышается в ходе реакции. Следовательно, окислителями могут быть прежде всего соединения высших, а восстановителями — низших степенен окисленности, присущих данному элементу.
Металлы проявляют в своих соединениях только положительную окисленность, и низшая их степень окисленности равна нулю. Иначе говоря, низшей степенью окисленности они обладают только в свободном состоянии. Действительно, все свободные металлы способны, хотя и в различной степени, проявлять только восстановительные свойства. На практике в качестве восстановителей применяют алюминий, магний, натрий, калий, цинк и некоторые другие металлы. Если металлу присущи несколько степеней окисленности, то те его соединения, в которых он проявляет низшую из них, также обычно являются восстановителями, например, соединения железа(II), олова(II), хрома(II), меди(I).
Окислителями могут быть те соединения металлов, в которых степень окисленности металла велика — равна номеру группы, в которой находится металл, или близка к нему. На практике применяют, в частности: аммиачный раствор оксида серебра, аммиачный раствор сульфата меди(II), хлорид ртути(II), диоксид свинца 




Неметаллы проявляют как положительную, так и отрицательную окисленность. Естественно, что соединения, содержащие неметаллы в высших положительных степенях окисленности, могут быть окислителями, а соединения, в которых неметалл проявляет отрицательную окисленность, — восстановителями.
К широко применяемым в промышленности восстановителям относятся водород, углерод (в виде угля или кокса) и монооксид углерода 
К сильным окислителям принадлежат неметаллы верхней части VI и VII групп периодической системы. Сильные окислительные свойства этих веществ объясняются большой электроотрицательностью их атомов. Сильнее всего окислительные свойства выражены у фтора, но в практике чаще пользуются в качестве окислителей кислородом, хлором и бромом.
К соединениям, применяемым в качестве окислителей, относятся также кислоты. Наибольшее практическое значение имеют соляная, серная и азотная кислоты. При этом элементом окислителем в соляной кислоте является водород, в азотной — азот, в разбавленной серной — водород, в концентрированной — сера. Поэтому уравнение процесса восстановления соляной и разбавленной серной кислот имеет вид:
Азотная кислота, в зависимости от ее концентрации, температуры и природы восстановителя, может восстанавливаться до различных степеней окисленности азота (см. 

При восстановлении концентрированной серной кислоты также могут образовываться различные продукты (см. 
Из других соединений неметаллов, применяемых в качестве окислителей, можно указать на пероксид водорода, соли кислот, в которых кислотообразующий элемент проявляет высокую степень окисленности — хлораты 

Окислительно-восстановительная двойственность
Внутримолекулярное окисление-восстановление. Соединения высшей степени окисленности, присущей данному элементу, могут в окислительно-восстановительных реакциях выступать только в качестве окислителей, степень окисленности элемента может в этом случае только понижаться. Соединения низшей степени окисленности могут быть, наоборот, только восстановителями; здесь степень окисленности элемента может только повышаться. Если же элемент находится в промежуточной степени окисленности, то его атомы могут, в зависимости от условий, как принимать, так и отдавать электроны. В первом случае степень окисленности элемента будет понижаться, во втором — повышаться. Поэтому соединения, содержащие элементы в промежуточных степенях окисленности, обладают окислительно-восстановительной двойственностью — способностью вступать в реакции как с окислителями, так и с восстановителями. ‘
Так, азот образует соединения, в которых степень его окисленности изменяется от —3 (аммиак и соли аммония) до +5 (азотная кислота и ее соли). Азот, входящий в состав аммиака, может выступать только в качестве восстановителя, азот азотной кислоты— только в качестве окислителя. Азотистая же кислота 


В качестве примеров окислительно-восстановительной двойственности азотистой кислоты можно привести реакции:
Кроме азотистой кислоты окислительно-восстановительной двойственностью обладают сера, иод, пероксид водорода и ряд других веществ.
Здесь и окисление, и восстановление претерпевает хлор;
Самоокисление-самовосстановление называют также диспропорционированием.
Некоторые сложные вещества в определенных условиях (обычно при нагревании) претерпевают внутримолекулярное окисление-восстановление. При этом процессе одна составная часть вещества служит окислителем, а другая — восстановителем. Примерами внутримолекулярного окисления-восстановления могут служить многие процессы термической диссоциации. Так, в ходе термической диссоциации водяного пара
кислород окисляется (его степень окисленности возрастает от —2 до 0), а водород восстанавливается (его степень окисленности уменьшается от +1 до 0).
Другим примером может служить реакция разложения нитрита аммония, применяемая в лабораторной практике для получения чистого азота:
Здесь ион 
Химические источники электрической энергии
Мы уже знаем, что при любой окислительно-восстановительной реакции происходит переход электронов от восстановителя к окислителю.
Так, при опускании цинковой пластинки в раствор сульфата меди происходит реакция
Здесь восстановитель — цинк — отдает электроны. Эта полуреакция выражается уравнением:
Окислитель — ион меди — принимает электроны. Уравнение этой полуреакции имеет вид:
В рассматриваемом примере обе полуреакции протекают в месте соприкосновения цинка с раствором, так что электроны непосредственно переходят от атомов цинка к ионам меди. Можно, однако, осуществить эту реакцию таким способом, что окислительная и восстановительная полуреакции окажутся пространственно разделенными, а электроны будут переходить от восстановителя к окислителю не непосредственно, а по проводнику электрического тока — по внешней цепи. Этот направленный поток электронов представляет собою электрический ток. При таком осуществлении окислительно-восстановительной реакции ее энергия будет превращена в электрическую энергию, которую можно использовать, включив во внешнюю цепь устройство, потребляющее электрическую энергию (например, электронагревательный прибор, электрическую лампу и т. п.).
Устройства, которые применяют для непосредственного преобразования энергии химической реакции в электрическую энергию, называются гальваническими элементами. Их называют также химическими источниками электрической энергии (сокращенно ХИЭЭ) или химическими источниками тока.
В технике гальваническими элементами принято называть только ХИЭЭ, в которых протекают практически необратимые реакции. Такие ХИЭЭ обычно нельзя перезаряжать: они предназначены для однократного использования (в одни или несколько приемов). ХИЭЭ, в которых протекают практически обратимые реакции, называют аккумуляторами: их можно перезаряжать и использовать многократно.
Действие любого гальванического элемента основано на протекании в нем окислительно-восстановительной реакции. В простейшем случае гальванический элемент состоит из двух пластин или стержней, изготовленных из различных металлов и погруженных в раствор электролита. Такая система делает возможным пространственное разделение окислительно-восстановительной реакции: окисление протекает на одном металле, а восстановление — на другом. Таким образом, электроны передаются от восстановителя к окислителю по внешней цепи.
Рассмотрим в качестве примера медно-цинковый гальванический элемент, работающий за счет энергии приведенной выше реакции между цинком и сульфатом меди (рис. 82). Этот элемент (элемент Якоби —Даниэля) состоит из медной пластины, погруженной в раствор сульфата меди (медный электрод), и цинковой пластины, погруженной в раствор сульфата цинка (цинковый электрод). Оба раствора соприкасаются друг с другом, но для предупреждения смешивания они разделены перегородкой, изготовленной из пористого материала.
При работе элемента, т. е. при замкнутой цепи, цинк окисляется: на поверхности его соприкосновения с раствором атомы цинка превращаются в ионы и, гидратируясь, переходят в раствор. Высвобождающиеся при этом электроны движутся по внешней цепи к медному электроду. Вся совокупность этих процессов схематически изображается уравнением полуреакции, или электрохимическим уравнением:
На медном электроде протекает восстановление ионов меди. Электроны, приходящие сюда от цинкового электрода, соединяются с выходящими из раствора дегидратирующимися нонами меди; образуются атомы меди, выделяющиеся в виде металла. Соответствующее электрохимическое уравнение имеет вид:
Суммарное уравнение реакции, протекающей в элементе, получится при сложении уравнений обеих полуреакций. Таким образом, при работе гальванического элемента электроны от восстановителя переходят к окислителю по внешней цепи, на электродах идут электрохимические процессы, в растворе наблюдается направленное движение ионов.
Направление движения ионов в растворе обусловлено протекающими у электродов электрохимическими процессами. Как уже сказано, у цинкового электрода катионы выходят в раствор, создавая в нем избыточный положительный заряд, а у медного электрода раствор, наоборот, все время обедняется катионами, так что здесь раствор заряжается отрицательно. В результате этого создается электрическое поле, в котором катионы, находящиеся в растворе 

Электрод, на котором протекает окисление, называется анодом. Электрод, на котором протекает восстановление, называется катодом. В медно-цинковом элементе цинковый электрод является анодом, а медный — катодом.
Рис. 82. Схема медно-цинкогово гальванического элемента.
Рис. 83. Схема движения ионов и электронов при работе медно-цинкового гальванического элемента.
Протекающая в гальваническом элементе окислительно-восстановительная реакция представляет собой сложный процесс. Она включает собственно электрохимические стадии (превращения атомов, ионов или молекул на электродах), перенос электронов, перенос ионов. Все эти стадии сопряжены между собой и протекают с одной и той же скоростью; число электронов, которые за единицу времени отдает цинк, равно числу электронов, принимаемых за это же время ионами меди. Поэтому скорость реакции, протекающей в гальваническом элементе, пропорциональна количеству электричества, перенесенного по цепи в единицу времени, т. е. силе тока в цепи.
Электрический ток, протекающий по внешней цепи гальванического элемента, может производить полезную работу. Но работа, которую можно выполнить за счет энергии химической реакции, зависит от ее скорости: она максимальна при бесконечно медленном— обратимом — проведении реакции (см. § 67). Следовательно, работа, которую можно произвести за счет реакции, протекающей в гальваническом элементе, зависит от величины отбираемого от него тока. Если, увеличивая сопротивление внешней цепи, уменьшать ток до бесконечно малого значения, то и скорость реакции в элементе тоже будет бесконечно малой, а работа — максимальной. Теплота, выделяемая во внутренней цепи элемента, будет при этом, наоборот, минимальна.
Работа электрического тока выражается произведением количества прошедшего по цепи электричества на напряжение. В медно-цинковом элементе при окислении одного эквивалента цинка и Одновременном восстановлении одного эквивалента ионов меди по цепи пройдет количество электричества, численно равное одному фарадею 

где 
Но поскольку эта работа зависит от силы тока, то и напряжение между полюсами элемента тоже зависит от силы тока ( 
Для этого предельного случая полезная работа, производимая электрическим током в медно-цинковом элементе при взаимодействии одного эквивалента цинка с одним эквивалентом ионов меди, выразится уравнением
где 
Ясно, что при взаимодействии одного моля атомов цинка с одним молем ионов меди уравнение примет вид:
В общем случае при растворении (или выделении) одного моля вещества, ионы которого имеют заряд, равный 
При постоянных температуре и давлении максимальная полезная работа реакции равна взятому с обратным знаком изменению энергии Гиббса 
Если концентрации (точнее говоря, активности) веществ, участвующих в реакции, равны единице, т. е. если соблюдаются стандартные условия, то э.д.с. элемента называется его стандартной электродвижущей силой и обозначается 
Учитывая, что стандартное изменение энергии Гиббса реакции связано с ее константой равновесия (см. § 68) соотношением
получим уравнение, связывающее стандартную э. д. с. с константой равновесия реакции, протекающей в гальваническом элементе:
Измерения электродвижущих сил можно производить с высокой точностью. Эти измерения представляют собой один из наиболее точных методов определения стандартных энергии Гиббса, а следовательно, и констант равновесия окислительно-восстановительных реакций в растворах.
Прямые опыты с применением радиоактивных индикаторов Показывают, что если привести металл 

При этом металлический электрод оказывается заряженным отрицательно, а раствор — положительно. Если при установлении контакта металл — раствор скорость перехода катионов из металла в раствор была меньше, чем скорость их перехода в обратном направлении, то между электродом и раствором также устанавливается равновесие; но в этом случае электрод заряжается положительно, а раствор — отрицательно.
а также между медным электродом и раствором сульфата меди;
В этом элементе имеются еще две границы раздела фаз: между растворами сульфатов цинка и меди, а также медью и цинком (см. рис. 82). Граница между растворами не оказывает существенного влияния ни на величину э. д. е., ни на протекание реакции при работе элемента. Что же касается границы между металлами, то через нее могут проходить не ионы, как в случае границы металл— раствор, а электроны*. И здесь вследствие неодинакового энергетического состояния электронов в меди и в цинке первоначальные скорости перехода электронов из одного металла в другой и в обратном направлении различны. Однако и в этом случае быстро устанавливается равновесие, при котором металлы также приобретают заряды противоположного знака:
* Диффузия атомов и ионов из металла в металл происходит много медленнее и практически не влияет на установление равновесия на границе между металлами.
Таким образом, при разомкнутой цепи на трех имеющихся в элементе Якоби— Даниэля границах раздела фаз устанавливаются равновесия, причем фазы заряжаются. В результате энергетическое состояние электронов на концах разомкнутой цеп» оказывается неодинаковым: на том медном проводнике, который соприкасается с цинковым электродом, энергия Гиббса электронов выше, а на том, который соединен с медным электродом, — ниже. Разность энергий Гиббса электронов на концах цепи и определяет; э.д. с. данного элемента.
При замыкании внешней цепи электроны перемешаются от цинкового электрода к медному. Поэтому равновесия на фазовых границах нарушаются; происходит направленный переход ионов цинка из металла в раствор, ионов меди — из раствора в металл, электронов— от цинка к меди: протекает окислительно-восстановительная реакция.
В принципе электрическую энергию может дать любая окислительно-восстановительная реакция. Однако число реакций, практически используемых в химических источниках электрической энергии, невелико. Это связано с тем, что не всякая окислительно-восстановительная реакция позволяет создать гальванический элемент, обладающий технически ценными свойствами (высокая и практически постоянная э.д.е., возможность отбирания больших токов, длительная сохранность и др.). Кроме того, многие окислительно-восстановительные реакции требуют расхода дорогостоящих веществ.
В отличие от медно-цинкового элемента, во всех современных гальванических элементах и аккумуляторах используют не два, а один электролит; такие источники тока значительно удобнее в эксплуатации. Например, в свинцовых аккумуляторах (см. § 189) электролитом служит раствор серной кислоты.
Почти во всех выпускаемых в настоящее время гальванических элементах анод изготовляется из цинка, а в качестве вещества для катода обычно применяются оксиды менее активных металлов. Описание важнейших гальванических элементов см. § 214, аккумуляторов—§§ 189, 201, 244.
Химические источники электрической энергии применяются в различных отраслях техники. В средствах связи (радио, телефон, телеграф) и в электроизмерительной аппаратуре они служат источниками электропитания, на автомобилях, самолетах, тракторах применяются для приведения в действие стартеров и других устройств, на транспорте, в переносных фонарях с их помощью производится освещение.
Все обычные ХИЭЭ не свободны от двух недостатков. Во-первых, стоимость веществ, необходимых для их работы (например, свинца, кадмия), высока. Во-вторых, отношение количества энергии, которую может отдать элемент, к его массе мало. На протяжении последних десятилетий ведутся исследования, направленные на создание элементов, при работе которых расходовались бы дешевые вещества с малой плотностью, подобные жидкому или газообразному топливу (природный газ, керосин, водород и др.). Такие гальванические элементы называются топливными. Проблеме топливного элемента уделяется в настоящее время большое внимание и можно полагать, что в ближайшем будущем топливные элементы найдут широкое применение.
Электродные потенциалы
Каждая окислительно-восстановительная реакция слагается из полуреакций окисления и восстановления. Когда реакция протекает в гальваническом элементе или осуществляется путем электролиза, то каждая полуреакция протекает на соответствующем электроде; поэтому полуреакции называют также электродными процессами.
В § 98 было показано, что протекающей в гальваническом элементе окислительно-восстановительной реакции соответствует е.д. с. этого элемента 

В соответствии с разделением окислительно-восстановительной реакции на две полуреакции, электродвижущие силы также принято представлять в виде разности двух величии, каждая из которых отвечает данной полуреакции. Эти величины называются электродными потенциалами.
Для медно-цинкового элемента реакция, протекающая при его работе
разбивается на полуреакции;
Соответственно э.д. с. этого элемента 



При этом изменение энергии Гиббса 
а изменение энергии Гиббса 
В общем случае любому электродному процессу
соответствует электродный потенциал 

Здесь 

В дальнейшем, говоря об электродных процессах, мы будем записывать их уравнения в сторону восстановления (за исключением, конечно, тех случаев, когда речь будет идти именно об окислении).
В результате изучения потенциалов различных электродных процессов установлено, что их величины зависят от следующих трех факторов: 1) от природы веществ — участников электродного процесса, 2) от соотношения между концентрациями* этих веществ и 3) от температуры системы. Эта зависимость выражается уравнением:
* Строго говоря, величина электродного потенциала зависит от соотношения не концентраций, а активностей (см. § 86) веществ; во всех рассматриваемых далее уравнениях вместо концентрации должна стоять активность. Но при невысоких концентрациях растворов погрешность, вносимая заменой активности на концентрацию, невелика.
Здесь 








Физический смысл величины 

Таким образом, в уравнении электродного потенциала первое слагаемое 

Для обычной при электрохимических измерениях стандартной температуры 

Для построения численной шкалы электродных потенциалов нужно потенциал какого-либо электродного процесса принять равным нулю. В качестве эталона для создания такой шкалы принят электродный процесс
Изменение энергии Гиббса, связанное с протеканием этой полуреакции при стандартных условиях, принимается равным нулю. В соответствии с этим и стандартный потенциал данного электродного процесса принят равным нулю. Все электродные потенциалы, приводимые в настоящей книге, а также в большинстве других современных изданий, выражены по этой, так называемой водородной шкале.
Рис. 84. водородный электрод.
Рис. 85. Цепь для измерения электродного потенциала: слева — электрод, потенциал которого нужно измерить; справа — каломельный электрод; в середине — соединительный сосуд.
Приведенный выше электродный процесс осуществляется на водородном электроде. Последний представляет собой платиновую пластинку, электролитически покрытую губчатой платиной и погруженную в раствор кислоты, через который пропускается водород (рис. 84). Водород хорошо растворяется в платине; при этом молекулы водорода частично распадаются на атомы (пластина катализирует этот распад). На поверхности соприкосновения платины с раствором кислоты может протекать, окисление атомов или восстановление ионов водорода. Платина при этом практически не принимает участия в электродных реакциях и играет как бы роль губки, пропитанной атомарным водородом.
Потенциал водородного электрода воспроизводится с очень высокой точностью. Поэтому водородный электрод и принят в качестве эталона при создании шкалы электродных потенциалов.
Установим, какой вид принимает общее уравнение электродного потенциала для водородного электрода. В соответствии с уравнением электродного процесса (см. стр. 271) 


где 

Обычно парциальное давление водорода 

Поскольку стандартный потенциал рассматриваемого процесса принят равным нулю, то
или, учитывая, что 
Для определения потенциала того или иного электродного процесса нужно составить гальванический элемент из испытуемого и стандартного водородного электродов и измерить его э. д. с. Поскольку потенциал стандартного водородного электрода равен нулю, то измеренная э. д. с будет представлять собою потенциал данного электродного процесса.
Практически при измерениях потенциалов в качестве электрода сравнения пользуются не стандартным водородным, а другими электродами, более удобными в обращении, потенциалы которых но отношению к стандартному водородному электроду известны. При этом необходимо рассчитать э. д. с. элемента согласно уравнению:
Здесь 


Решая уравнение относительно 
В качестве электродов сравнения чаще всего применяют хлор-серебряный и каломельный электроды. Хлорсеребряный электрод— это серебряная проволочка, покрытая слоем 
Каломельный электрод представляет собой ртуть, покрытую взвесью каломели 

Для того чтобы найти значение электродного потенциала, необходимо измерить не напряжение работающего элемента, а именно его э. д. с. При измерениях э. д. с. сопротивление внешней цепи (т. е. измерительного устройства) очень велико. Реакция в элементе при этом практически не протекает. Таким образом, электродные потенциалы отвечают обратимому протеканию процессов или, что то же самое, состоянию электрохимического равновесия на электродах. Поэтому электродные потенциалы часто называют равновесными электродными потенциалами или просто равновесными потенциалами.
Рассмотрим теперь, какой вид принимает общее уравнение электродного потенциала в важнейших случаях.
1. Электродный процесс выражается уравнением
где 


К этому случаю относятся оба электрода медно-цинкового элемента и вообще любой металлический электрод в растворе соли этого же металла. Здесь окисленной формой металла являются его ионы, а восстановленной — атомы. Следовательно, 


Например, для процесса
а для процесса
2. Электродный процесс выражается уравнением:
В этом случае и окисленная 

Например, для процесса 
В этом и в рассматриваемых ниже случаях электрод, на котором протекает электродный процесс, изготовляется из инертного материала. Чаще всего в качестве такого материала применяют платину.
Мы рассмотрели примеры, когда в электродных процессах принимали участие только ионы, состоящие из одного элемента. Однако часто окисляющееся или восстанавливающееся вещество состоит не из одного, а из двух или большего числа элементов. Чаще всего в составе окислителя содержится кислород; при этом в электродном процессе обычно принимают участие также вода и продукты ее диссоциации — ионы водорода (в кислой среде) или гидроксид-ионы (в щелочной среде). Рассмотрим, как будут выглядеть в таких случаях уравнения потенциалов электродных процессов.
3. Электродный процесс выражается уравнением:
Эта полуреакция (при протекании ее в сторону восстановления) играет очень большую роль при коррозии металлов (см. § 196). Кислород — самый распространенный окислитель, вызывающий коррозию металлов в водных средах.
В рассматриваемом электродном процессе в результате восстановления кислорода, протекающего с участием ионов водорода, образуется вода. Следовательно, 



Для рассматриваемого процесса 
При парциальном давлении кислорода, равном нормальному атмосферному давлению (которое условно принимается равным единице), 
4. Для электродных процессов, записываемых более сложными уравнениями, в выражениях для потенциалов содержится большее число переменных концентраций. Рассмотрим, например, электродный процесс:
Эта полуреакция протекает (в сторону восстановления) при взаимодействии перманганата калия с большинством восстановителей в кислой среде.
Концентрации всех веществ, участвующих в рассматриваемом электродном процессе, кроме воды, — величины переменные. Для этого процесса 
Примеры 3 и 4 показывают, что в случае электрохимических процессов, протекающих с участием воды, концентрация ионов водорода входит в числитель логарифмического члена уравнения потенциала. Поэтому электродные потенциалы таких процессов зависят от 
Таблица 18. Электродные потенциалы в водных растворах при 25 °С н при парциальном давлении газов, равном нормальному атмосферному давлению
Продолжение табл. 18
Как уже сказано, зависимость электродного потенциала от природы веществ — участников электродного процесса учитывается величиной 

Положение той или иной электрохимической системы в этом ряду характеризует ее окислительно-восстановительную способность. Под электрохимической системой здесь подразумевается совокупность всех веществ — участников данного электродного процесса.
Окислительно-восстановительная способность представляет собою понятие, характеризующее именно электрохимическую систему, но часто говорят и об окислительно-восстановительной способности того или иного вещества (или иона). При этом следует, однако, иметь в виду, что многие вещества могут окисляться или восстанавливаться до различных продуктов. Например, перманганат калия 




Соответствующие электродные процессы выражаются уравнениями:
Поскольку стандартные потенциалы этих трех электродных процессов различны (см. табл. 18), то различно и положение этих трех систем в ряду 

Элементы, проявляющие в своих соединениях только одну степень окисленности, имеют простые окислительно-восстановительные характеристики и занимают в ряду стандартных потенцпалоз мало мест. К их числу относятся в основном металлы главных подгрупп I-III групп периодической системы. Много же мест в ряду занимают те элементы, которые образуют соединения различных степеней окисленности — неметаллы и многие металлы побочных подгрупп периодической системы.
Ряд стандартных электродных потенциалов позволяет решать вопрос о направлении самопроизвольного протекания окислительно-восстановительных реакций. Как и в общем случае любой химической реакции, определяющим фактором служит здесь знак изменения энергии Гиббса реакции. Если из двух электрохимических систем составить гальванический элемент, то при его работе электроны будут самопроизвольно переходить от отрицательного полюса элемента к положительному, т. е. от электрохимической системы с более низким значением электродного потенциала к системе с более высоким его значением. Но это означает, что первая из этих систем будет выступать в качестве восстановителя, а вторая—в качестве окислителя. Следовательно, в гальваническом элементе окислительно-восстановительная реакция может самопроизвольно протекать в таком направлении, при котором электрохимическая система с более высоким значением электродного потенциала выступает в качестве окислителя, т. е. восстанавливается. При непосредственном взаимодействии веществ возможное направление реакции будет, конечно, таким же, как и при ее осуществлении в гальваническом элементе.
Если окислитель и восстановитель расположены далеко друг от друга в ряду 


может самопроизвольно идти как слева направо, так и справа налево. Направление ее протекания определяется концентрациями ионов железа и ртути. В этой реакции участвуют две электрохимические системы:
Соответствующим электродным процессам отвечают потенциалы:
Подсчитаем величины 



Таким образом, при взятом соотношении концентраций 
Теперь подсчитаем 

Следовательно, при этих концентрациях 
Если окислительно-восстановительная реакция протекает с участием воды и ионов водорода или гидроксид-ионов, то необходимо учитывать также величину 
В табл. 18 включено 39 полуреакций; комбинируя их друг с другом, можно решить вопрос о направлении самопроизвольного протекания 
Пример. Установить, направление возможного протекания реакции:
Запишем уравнение реакции в иоино-молекулярной форме: 2Вг
+ РЬ02 + 4Н+ = РЬ2+ + Вг2 + 2НгО
В табл. 18 находим стандартные электродные потенциалы электрохимических систем, участвующих в реакции:
Окислителем всегда служит электрохимическая система с более высоким значением электродного потенциала. Поскольку здесь 

Чем дальше находится та или иная система в ряду стандартных потенциалов, т. е. чем больше ее стандартный потенциал, тем более сильным окислителем является ее окисленная форма. И, наоборот, чем раньше расположена система в ряду, т. е. чем меньше значение 

При протекании окислительно-восстановительных реакций концентрации исходных веществ падают, а продуктов реакции — возрастают. Это приводит к изменению величин потенциалов обеих полуреакций: электродный потенциал окислителя падает, а электродный потенциал восстановителя возрастает. Когда потенциалы обоих процессов становятся равными друг другу, реакция заканчивается— наступает состояние химического равновесия.
Ряд напряжений металлов
Если из всего ряда стандартных электродных потенциалов выделить только те электродные процессы, которые отвечают общему уравнению
то получим ряд напряжений металлов. В этот ряд всегда помешают, кроме металлов, также водород, что позволяет видеть, какие металлы способны вытеснять водород из водных растворов кислот. Ряд напряжений для важнейших металлов приведен в табл. 19. Положение того или иного металла в ряду напряжений характеризует его способность к окислительно-восстановительным взаимодействиям в водных растворах при стандартных условиях. Ионы металлов являются окислителями, а металлы в виде простых веществ — восстановителями. При этом, чем дальше расположен металл в ряду напряжений, тем более сильным окислителем в водном растворе являются его ионы, и наоборот, чем ближе металл к началу ряда, тем более сильные восстановительные свойства проявляет простое вещество — металл.
Таблица 19. Ряд напряжений металлов
Потенциал электродного процесса
в нейтральной среде 


* Потенциалы металлов в воде, конечно, отличны от их потенциалов в стандартных условиях; в большинстве случаев они имеют более отрицательное значение. Но, как правило, это не сказывается на правильности выводов о способности металлов вытеснять водород из воды.
Металлы, расположенные между магнием и водородом, вытесняют водород из растворов кислот. При этом на поверхности некоторых металлов также образуются защитные пленки, тормозящие реакцию. Так, оксидная пленка на алюминии делает этот металл стойким не только в воде, но и в растворах некоторых кислот. Свинец не растворяется в серной кислоте при ее концентрации ниже 80%, так как образующаяся при взаимодействии свинца с серной кислотой соль 
Металлы способны вытеснять друг друга из растворов солей. Направление реакции определяется при этом их взаимным положением в ряду напряжений. Рассматривая конкретные случаи таких реакций, следует помнить, что активные металлы вытесняют водород не только из воды, но и из любого водного раствора. Поэтому взаимное вытеснение металлов из растворов их солей практически происходит лишь в случае металлов, расположенных в ряду после магния.
Вытеснение металлов из их соединений другими металлами г.лервые подробно изучал Бекетов *. В результате своих работ он расположил металлы по их химической активности в «вытеснитель-ный ряд», являющийся прототипом ряда напряжений металлов.
* Николай Николаевич Бекетов (1826—1911) — крупный русский ученый — физико-химик. Выдающимся трудом Бекетова являются его «Исследования над явлениями вытеснения одних элементов другими», опубликованные в 1865 г. Ои открыл свойство алюминия вытеснять при высокой температуре металлы из их оксидов. Это открытие впоследствии легло в основу металлотермии (см. § 192), получившей широкое применение в металлургии. Бекетов осуществил многочисленные термохимические измерения. Ои впервые (с 1865 г.) ввел преподавание физической химии как учебной дисциплины.
Взаимное положение некоторых металлов в ряду напряжений н в периодической системе на первый взгляд не соответствует друг другу. Например, согласно положению в периодической системе химическая активность калия должна быть больше, чем натрия, а натрия — больше, чем лития. В ряду же напряжений наиболее активным оказывается литий, а калий занимает среднее положение между литием и натрием. Цинк и медь по их положению в периодической системе должны иметь приблизительно равную химическую активность, но в ряду напряжений цинк расположен значительно раньше меди. Причина такого рода несоответствий состоит в следующем.
При сравнении металлов, занимающих то или иное положение в периодической системе, за меру их химической активности — восстановительной способности — принимается величина энергии ионизации свободных атомов. Действительно, при переходе, например, сверху вниз по главной подгруппе I группы периодической системы энергия ионизации атомов уменьшается, что связано с увеличением их радиусов (т. е. с большим удалением внешних электронов от ядра) и с возрастающим экранированием положительного заряда ядра промежуточными электронными слоями (см. § 31). Поэтому атомы калия проявляют большую химическую активность — обладают более сильными восстановительными свойствами,—чем атомы натрия, а атомы натрия — большую активность, чем атомы лития.
При сравнении же металлов в ряду напряжений за меру химической активности принимается работа превращения металла, находящегося в твердом состоянии, в гидратированные ионы в водном растворе. Эту работу можно представить как сумму трех слагаемых: энергии атомизации — превращения кристалла металла в изолированные атомы, энергии ионизации свободных атомов металла и энергии гидратации образующихся ионов. Энергия атомизации характеризует прочность кристаллической решетки данного металла. Энергия ионизации атомов — отрыва от них валентных электронов — непосредственно определяется положением металла в периодической системе. Энергия, выделяющаяся при гидратации, зависит от электронной структуры иона, его заряда и радиуса. Ионы лития и калия, имеющие одинаковый заряд, но различные радиусы, будут создавать около себя неодинаковые электрические поля. Поле, возникающее вблизи маленьких ионов лития, будет более сильным, чем поле около больших ионов калия. Отсюда ясно, что ионы лития будут гидратироваться с выделением большей энергии, чем ионы калия.
Таким образом, в ходе рассматриваемого превращения затрачивается энергия на атомизацию и ионизацию и выделяется энергия при гидратации. Чем меньше будет суммарная затрата энергии, тем легче будет осуществляться весь процесс и тем ближе к началу ряда напряжений будет располагаться данный металл. Но из трех слагаемых общего баланса энергии только одно — энергия ионизации—непосредственно определяется положением металла в периодической системе. Следовательно, нет оснований ожидать, что взаимное положение тех или иных металлов в ряду напряжений всегда будет соответствовать их положению в периодической системе. Так, для лития суммарная затрата энергии оказывается меньшей, чем для калия, в соответствии с чем литий стоит в ряду напряжений раньше калия.
Для меди и цинка затрата энергии на ионизацию свободных атомов и выигрыш ее при гидратации ионов близки. Но металлическая медь образует более прочную кристаллическую решетку, чем цинк, что видно из сопоставления температур плавления этих металлов: цинк плавится при 

При переходе от воды к неводным растворителям взаимное положение металлов в ряду напряжений может изменяться. Причина этого лежит в том, что энергия сольватации ионов различных металлов по-разному изменяется при переходе от одного растворителя к другому.
В частности, ион меди весьма энергично сольватируется в некоторых органических растворителях; это приводит к тому, что в таких растворителях медь располагается в ряду напряжений до водорода и вытесняет его из растворов кислот.
Таким образом, в отличие от периодической системы элементов, ряд напряжений металлов не является отражением общей Закономерности, на основе которой можно давать разностороннюю Характеристику химических свойств металлов. Ряд напряжений характеризует лишь окислительно-восстановительную способность электрохимической системы «металл — ион металла» в строго определенных условиях: приведенные в нем величины относятся К водному раствору, температуре 
Электролиз
Электролизом называется совокупность процессов, происходящих при прохождении постоянного электрического тока через электрохимическую систему, состоящую из двух электродов и расплава или раствора электролита.
Примером электролиза может служить электролиз расплава хлорида магния. При прохождении тока через расплав 
Анионы хлора перемещаются к положительному электроду и, отдавая избыточные электроны, окисляются. При этом первичным процессом является собственно электрохимическая стадия — окисление ионов хлора
а вторичным — связывание образующихся атомов хлора в молекулы:
Складывая уравнения процессов, протекающих у электродов, получим суммарное уравнение окислительно-восстановительной реакции, происходящей при электролизе расплава 
Эта реакция не может протекать самопроизвольно; энергия, необходимая для ее осуществления, поступает от внешнего источника тока.
Как и в случае химического источника электрической энергии, электрод, на котором происходит восстановление, называется катодом; электрод, на котором происходит окисление, называется анодом. Но при электролизе катод заряжен отрицательно, а анод— положительно, т. е. распределение знаков заряда электродов противоположно тому, которое имеется при работе гальванического элемента. Причина этого заключается в том, что процессы, протекающие при электролизе, в принципе обратны процессам, идущим при работе гальванического элемента. При электролизе химическая реакция осуществляется за счет энергии электрического тока, подводимой извне, в то время как при работе гальванического элемента энергия самопроизвольно протекающей в нем химической реакции превращается в электрическую энергию.
При рассмотрении электролиза водных растворов нельзя упускать из виду, что, кроме ионов электролита, во всяком водном растворе имеются еще ионы, являющиеся продуктами диссоциации воды — 


Какие именно электрохимические процессы будут протекать у электродов при электролизе, прежде всего будет зависеть от относительных значений электродных потенциалов соответствующих электрохимических систем. Из нескольких возможных процессов будет протекать тот, осуществление которого сопряжено с минимальной затратой энергии. Это означает, что на катоде будут восстанавливаться окисленные формы электрохимических систем, имеющих наибольший электродный потенциал, а на аноде будут окисляться восстановленные формы систем с наименьшим электродным потенциалом. На протекание некоторых электрохимических процессов оказывает тормозящее действие материал электрода; такие случаи оговорены ниже.
Рассматривая катодные процессы, протекающие при электролизе водных растворов, ограничимся важнейшим случаем— катодным восстановлением, приводящим к выделению элементов в свободном состоянии. Здесь нужно учитывать величину потенциала процесса восстановления ионов водорода. Этот потенциал зависит от концентрации ионов водорода (см. стр. 273) и в случае нейтральных растворов 





* К важнейшим условиям электролиза относятся плотность тока, температура, состав раствора. Плотностью тока называется отношение силы тока к рабочей площади электрода.
Электрохимическое выделение водорода из кислых растворов происходит вследствие разряда ионов водорода. В случае же нейтральных или щелочных сред оно является результатом электрохимического восстановления воды:
Таким образом, характер катодного процесса при электролизе водных растворов определяется прежде всего положением соответствующего металла в ряду напряженнй. В ряде случаев большое значение имеют 
При рассмотрении анодных процессов следует иметь в виду, что материал анода в ходе электролиза может окисляться. В связи с этим различают электролиз с инертным анодом и электролиз с активным анодом. Инертным называется анод, материал которого не претерпевает окисления в ходе электролиза. Активным называется анод, материал которого может окисляться в ходе электролиза. В качестве материалов для инертных анодов чаще всего применяют графит, уголь, платину.
На инертном аноде при электролизе водных растворов щелочей, кислородсодержащих кислот и их солей, а также фторо-водорода и фторидов происходит электрохимическое окисление воды с выделением кислорода. В зависимости от 
а в кислой или нейтральной:
В рассматриваемых случаях электрохимическое окисление воды является энергетически наиболее выгодным процессом. Кислородсодержащие анионы или не способны окисляться, или их окисление происходит при очень высоких потенциалах. Например, стандартный потенциал окисления иона
равен 



При электролизе водных растворов бескислородных кислот и их солей (кроме 


в ряду стандартных электродных потенциалов. Эта аномалия связана со значительным перенапряжением (см. § 104) второго и этих двух электродных процессов — материал анода оказывает тормозящее действие на процесс выделения кислорода.
В случае активного анода число конкурирующих окислительных процессов возрастает до трех: электрохимическое окисление воды с выделением кислорода, разряд аниона (т. е. его окисление) и электрохимическое окисление металла анода (так называемое анодное растворение металла).Из этих возможных процессов будет идти тот, который энергетически наиболее выгоден. Если металл анода расположен в ряду стандартных потенциалов раньше обеих других электрохимических систем, то будет наблюдаться анодное растворение металла. В противном случае будет идти выделение кислорода или разряд аниона.
Рассмотрим несколько типичных случаев электролиза водных растворов.
Электролиз раствора 

Схема электролиза* раствора хлорида меди(II):
* На этой и на последующих схемах в рамки заключены формулы веществ, являющихся конечными продуктами электролиза.
Электролиз раствора 




Схема электролиза раствора сульфата калия:
Рис. 86. Схема установки, закон Фарадея.
Электролиз раствора 





Схема электролиза раствора сульфата никеля:
Этот процесс применяется для электрической очистки никеля (так называемое электролитическое рафинирование, см. § 103).
Законы электролиза
С количественной стороны процесс электролиза впервые был изучен в 30-х годах XIX века выдающимся английским физиком Фарадеем *, который в результате своих исследований установил следующие законы электролиза:
* Майкл Фарадей (1791—1867)—один из крупнейших английских физиков и химиков. Большая часть его работ относится к области электричества. Он установил законы электролиза, открыл явление электромагнитной индукции. Впервые получил в жидком виде ряд газов (хлор, аммиак и др.), Открыл бензол и изобутилен.
1. Масса образующегося при электролизе вещества пропорциональна количеству прошедшего через раствор электричества.
Этот закон вытекает из сущности электролиза. Как уже говорилось, в месте соприкосновения металла с раствором происходит электрохимический процесс — взаимодействие ионов или молекул электролита с электронами металла, так что электролитическое образование вещества является результатом этого процесса. Ясно, что количество вещества, получающегося у электрода, всегда будет пропорционально числу прошедших по цепи электронов, т. е. количеству электричества.
2. При электролизе различных химических соединений равные количества электричества приводят к электрохимическому превращению эквивалентных количеств веществ.
Пусть, например, электрический ток последовательно проходит через растворы соляной кислоты, нитрата серебра, хлорида меди(II) и хлорида олова(IV) (рис. 86). Через некоторое время определяют количества выделившихся продуктов электролиза. Оказывается, что за время, в течение которого из раствора соляной кислоты выделяется 1 г водорода, т. е. 1 моль атомов, из остальных растворов выделяются указанные ниже массы металлов:
Сопоставляя выделившиеся массы металлов с атомными массами тех же металлов, находим, что выделяется 1 моль атомов серебра, 

Рассматривая второй закон электролиза с точки зрения электронной теории, нетрудно понять, почему при электролизе вещества выделяются в химически эквивалентных количествах. Обратимся, например, к электролизу хлорида меди(II). При выделении меди из раствора каждый ион меди получает от катода два электрона, и в то же время два хлорид-иона отдают электроны аноду, превращаясь в атомы хлора. Следовательно, число выделившихся атомов меди всегда будет вдвое меньше числа выделившихся атомов хлора, т. е, массы меди и хлора будут относиться друг к другу, как их эквивалентные массы.
Измерениями установлено, что количество электричества, обусловливающее электрохимическое превращение одного эквивалента вещества, равно 96485 (округленно 96 500) кулонам. Величина 

Второй закон электролиза дает прямой метод определения эквивалентов различных элементов. На этом же законе основаны расчеты, связанные с электрохимическими производствами.
Законы электролиза относятся к электролизу растворов, расплавов и твердых электролитов с чисто ионной проводимостью.
Электролиз в промышленности
Важнейшее применение электролиз находит в металлургической и химической промышленности и в гальванотехнике.
В металлургической промышленности электролизом расплавленных соединений и водных растворов получают металлы, а также производят электролитическое рафинирование — очистку металлов от вредных примесей и извлечение ценных компонентов.
Электролизом расплавов получают металлы, имеющие сильно отрицательные электродные потенциалы, и некоторые их сплавы.
При высокой температуре электролит и продукты электролиза могут вступать во взаимодействие друг с другом, с воздухом, а также с материалами электродов и электролизера. В результате этого простая, в принципе, схема электролиза (например, электролиз 
Электролитом обычно служат не индивидуальные расплавленные соединения, а их смеси. Важнейшим преимуществом смесей является их относительная легкоплавкость, позволяющая проводить электролиз при более низкой температуре.
В настоящее время электролизом расплавов получают алюминий, магний, натрий, литий, бериллий и кальций. Для получения калия, бария, рубидия и цезия электролиз расплавов практически не применяется из-за высокой химической активности этих металлов и большой их растворимости в расплавленных солях. В последние годы электролизом расплавленных сред получают некоторые тугоплавкие металлы.
Электролитическое выделение металла из раствора называется электроэкстракцией. Руда или обогащенная руда—концентрат (см. § 192)—подвергается обработке определенными реагентами, в результате которой металл переходит в раствор. После очистки от примесей раствор направляют на электролиз. Металл выделяется на катоде и в большинстве случаев характеризуется высокой чистотой. Этим методом получают главным образом цинк, медь и кадмий.
Электролитическому рафинированию металлы подвергают для удаления из них примесей и для перевода содержащихся в них компонентов в удобные для переработки продукты. Из металла, подлежащего очистке, отливают пластины и помещают их в качестве анодов в электролизер. При прохождении тока металл подвергается анодному растворению — переходит в виде катионов в раствор. Далее катионы металла разряжаются на катоде, образуя компактный осадок чистого металла. Содержащиеся в аноде примеси либо остаются нерастворенными, выпадая в виде анодного шлама, либо переходят в электролит, откуда периодически или непрерывно удаляются..
Рассмотрим в качестве примера электрорафинирование меди, основным компонентом раствора служит сульфат меди — наиболее распространенная и дешевая соль этого металла. Но раствор 
Металлические примеси, содержащиеся в неочищенной («черновой») меди, можно разделить на две группы:
1) 
2) 

Электролитическому рафинированию подвергают медь, никель, свинец, олово, серебро, золото.
К гальванотехнике относятся гальваностегия и гальванопластика. Процессы гальваностегии представляют собой нанесение путем электролиза на поверхность металлических изделий слоев других металлов для предохранения этих изделий от коррозии, для придания их поверхности твердости, а также в декоративных целях. Из многочисленных применяемых в технике гальванотехнических процессов важнейшими являются хромирование, цинкование и никелирование.
Сущность гальванического нанесения покрытий состоит в следующем. Хорошо очищенную и обезжиренную деталь, подлежащую защите, погружают в раствор, содержащий соль того металла, которым ее необходимо покрыть, и присоединяют в качестве катода к цепи постоянного тока; при пропускании тока на детали осаждается слой защищающего металла. Наилучшая защита обеспечивается мелкокристаллическими плотными осадками. Такие осадки обладают, кроме того, лучшими механическими свойствами.
Гальванопластикой называются процессы получения точных металлических копий с рельефных предметов электроосажденнем металла. Путем гальванопластики изготовляют матрицы для прессования различных изделий (граммофонных пластинок, пуговиц и др.), матрицы для тиснения кожи и бумаги, печатные радиотехнические схемы, типографские клише. Гальванопластику открыл русский академик Б. С. Якоби (1801—1874) в тридцатых годах XIX века.
К гальванотехнике относятся также другие виды электрохимической обработки поверхности металлов: электрополирование стали, оксидирование алюминия, магния. Последнее представляет собой анодную обработку металла, в ходе которой определенным образом изменяется структура оксидной пленки на его поверхности. Это приводит к повышению коррозионной стойкости металла. Кроме того, металл приобретает при этом красивый внешний вид.
В химической промышленности методом электролиза получают различные продукты; к числу их относятся фтор, хлор, едкий натр, водород высокой степени чистоты, многие окислители, в частности пероксид водорода.
Электрохимическая поляризация. Перенапряжение
Когда электрод находится при потенциале, равном равновесному, на нем устанавливается электрохимическое равновесие:
Прн смещении потенциала электрода в положительную или в отрицательную сторону на нем начинают протекать процессы окисления или восстановления. Отклонение потенциала электрода от его равновесного значения называется электрохимической поляризацией или просто поляризацией.
Поляризацию можно осуществить включением электрода в цепь постоянного тока. Для этого необходимо составить электролитическую ячейку из электролита и двух электродов—изучаемого и вспомогательного. Включая ее в цепь постоянного тока, можно сделать изучаемый электрод катодом или (при обратном включении ячейки) анодом. Такой способ поляризации называется поляризацией от внешнего источника электрической энергии.
Рассмотрим простой пример поляризации. Пусть медный электрод находится в 0,1 

а на границе металла с раствором установится электрохимическое равновесие:
Подключим электрод к отрицательному полюсу источника тока — сделаем его катодом. Избыток электронов, который появится теперь на электроде, сдвинет потенциал электрода в отрицательную сторону и одновременно нарушит равновесие. Электроны будут притягивать катионы меди из раствора — пойдет процесс восстановления;
Если подключить электрод не к отрицательному, а к положительному полюсу источника тока — сделать его анодом, то вследствие удаления части электронов потенциал электрода сместится в положительную сторону и равновесие также нарушится. Но теперь на электроде будет протекать процесс окисления, так кай в ходе этого процесса высвобождаются электроны:
Таким образом, поляризация электрода в отрицательную сторону связана с протеканием процесса восстановления, а поляризация в положительную сторону — с протеканием процесса окисления. Процесс восстановления иначе называют катодным процессом, а процесс окисления — анодным. В связи с этим поляризация в отрицательную сторону называется катодной поляризацией, а в положительную — анодной.
Другой способ поляризации электрода—это контакт его с электрохимической системой, электродный потенциал которой имеет более положительное или более отрицательное значение, чем потенциал рассматриваемого электрода.
Рассмотрим работу медно-цинкового гальванического элемента. При разомкнутой цепи как на медном, так и на цинковом электродах устанавливаются электрохимические равновесия. Но электродные потенциалы, отвечающие этим равновесиям, различны. В случае 0,1 
При замыкании цепи оба электрода оказывают друг на друга поляризующее действие: потенциал медного электрода под влиянием контакта с цинком сдвигается в отрицательную сторону, а потенциал цинкового электрода под влиянием контакта с медью — в положительную. Иначе говоря, медный электрод поляризуется катодно, а цинковый — анодно. Одновременно на обоих электродах нарушаются электрохимические равновесия и начинают протекать электрохимические процессы: катодный процесс на медном электроде и анодный — на цинковом:
Поляризация электрода — необходимое условие протекания электродного процесса. Кроме того, от ее величины зависит скорость электродного процесса; чем сильнее поляризован электрод, тем с большей скоростью протекает на нем соответствующая полуреакция.
Кроме величины поляризации на скорость электродных процессов влияют некоторые другие факторы. Рассмотрим катодное восстановление ионов водорода. Если катод изготовлен из платины, то для выделения водорода с заданной скоростью необходима определенная величина катодной поляризации. При замене платинового электрода на серебряный (при неизменных прочих условиях) для получения водорода с прежней скоростью понадобится большая поляризация. При замене катода на свинцовый поляризация потребуется еще большая. Следовательно, различные металлы обладают различной каталитической активностью по отношению к процессу восстановления ионов водорода. Величина поляризации, необходимая для протекания данного электродного процесса с определенной скоростью, называется перенапряжением данного электродного процесса. Таким образом, перенапряжение выделения водорода на различных металлах различно.
В табл. 20 приведены для 1 н. растворов величины катодной поляризации, которую необходимо осуществить на электроде для выделения на нем водорода со скоростью 0,1 мл в минуту с 
Таблица 20. Перенапряжение выделения водорода на различных металлах
Выяснение связи между величиной поляризации и скоростью электродного процесса является важнейшим методом изучения электрохимических процессов. При этом результаты измерений обычно представляют в виде поляризационных кривых — кривых зависимости плотности тока на электроде от величины поляризации. Вид поляризационной кривой того или иного электродного процесса отражает особенности его протекания. Методом поляризационных кривых изучают кинетику и механизм окислительно-восстановительных реакций, работу гальванических элементов, явления коррозии и пассивности металлов, различные случаи электролиза.
Большой вклад в развитие кинетики электродных процессов и теории перенапряжения внес советский ученый А. Н Фрумкин*.
* Александр Наумович Фрумкин (!895—1976) — крупнейший советский электрохимик, академик, лауреат Ленинской и Государственной премий. Разработал количественную теорию влияния электрического поля на адсорбцию молекул, развил учение о строении границы металл — раствор, внес значительный вклад в теорию э. д. с. гальванического элемента.
Услуги по химии:
Лекции по химии:
Лекции по неорганической химии:
Лекции по органической химии: