Как лечат инфаркт
Как лечат инфаркт
Инфаркт: Симптомы, лечение, последствия и профилактика
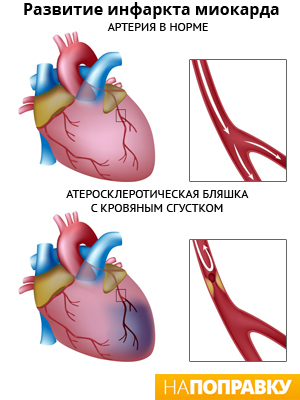
Основная и самая распространенная причина возникновения инфаркта миокарда – это нарушение кровотока в коронарных артериях, которые снабжают сердечную мышцу кровью, а соответственно, кислородом. Чаще всего это нарушение возникает на фоне атеросклероза артерий, при котором происходит образование атеросклеротических бляшек на стенках сосудов. Эти бляшки сужают просвет коронарных артерий, а также могут способствовать разрушению стенок сосудов, что создает дополнительные условия для образования тромбов и стеноза артерий.
Факторы риска инфаркта миокарда
Выделяют ряд факторов, которые значительно повышают риск развития этого острого состояния:
Это острое состояние имеет довольно специфичные симптомы, причем они обычно настолько выражены, что не могут остаться незамеченными. Тем не менее следует помнить, что встречаются и атипичные формы этого заболевания.
В подавляющем большинстве случаев у больных возникает типичная болевая форма инфаркта миокарда, благодаря чему у врача есть возможность правильно диагностировать заболевание и немедленно начать его лечение.
Основной симптом заболевания – это сильная боль. Боль, возникающая при инфаркте миокарда, локализуется за грудиной, она жгучая, кинжальная, некоторые больные характеризуют ее как «раздирающую». Боль может отдавать в левую руку, нижнюю челюсть, межлопаточную область. Возникновению этого симптома не всегда предшествует физическая нагрузка, нередко болевой синдром возникает в состоянии покоя или в ночное время. Описанные характеристики болевого синдрома схожи с таковыми при приступе стенокардии, тем не менее у них есть четкие различия.
В отличие от приступа стенокардии, болевой синдром при инфаркте миокарда сохраняется более 30 минут и не купируется в покое или повторным приемом нитроглицерина. Следует отметить, что даже в тех случаях, когда болевой приступ длится более 15 минут, а принимаемые меры неэффективны, необходимо немедленно вызвать бригаду скорой медицинской помощи.
Атипичные формы инфаркта миокарда
Инфаркт миокарда, протекающий в атипичной форме, может вызвать затруднения у врача при постановке диагноза.
Гастритический вариант. Болевой синдром, возникающий при этой форме заболевания, напоминает боль при обострении гастрита и локализуется в надчревной области. При осмотре может наблюдаться напряжение мышц передней брюшной стенки. Обычно такая форма инфаркта миокарда возникает при поражении нижних отделов левого желудочка, которые прилегают к диафрагме.
Астматический вариант. Напоминает тяжелый приступ бронхиальной астмы. У больного возникает удушье, кашель с пенистой мокротой (но может быть и сухим), при этом типичный болевой синдром отсутствует или выражен слабо. В тяжелых случаях может развиться отек легких. При осмотре может выявляться нарушение сердечного ритма, снижение артериального давления, хрипы в легких. Чаще всего астматическая форма заболевания возникает при повторных инфарктах миокарда, а также на фоне тяжелого кардиосклероза.
Аритмический вариант. Эта форма инфаркта миокарда проявляется в виде различных аритмий (экстрасистолия, мерцательная аритмия или пароксизмальная тахикардия) или атриовентрикулярных блокад различной степени. Из-за нарушения сердечного ритма может маскироваться картина инфаркта миокарда на электрокардиограмме.
Церебральный вариант. Характеризуется нарушением кровообращения в сосудах головного мозга. Больные могут жаловаться на головокружение, головную боль, тошноту и рвоту, слабость в конечностях, сознание может быть спутанным.
Безболевой вариант (стертая форма). Эта форма инфаркта миокарда вызывает наибольшие трудности в диагностике. Болевой синдром может полностью отсутствовать, пациенты жалуются на неопределенный дискомфорт в грудной клетке, повышенное потоотделение. Чаще всего такая стертая форма заболевания развивается у больных сахарным диабетом и протекает очень тяжело.
Иногда в клинической картине инфаркта миокарда могут присутствовать симптомы разных вариантов заболевания, прогноз в таких случаях, к сожалению, неблагоприятный.
Лечение инфаркта миокарда При появлении сильной жгучей боли в сердце больному следует принять получидячее положение и рассосать под языком таблетку нитроглицерина.
У больного можно заподозрить инфаркт миокарда, если:
При подозрении на инфаркт миокарда необходимо немедленно вызвать бригаду скорой помощи и начать оказывать помощь больному. Чем раньше больному будет оказана первая помощь, тем благоприятнее прогноз.
Необходимо снизить нагрузку на сердце, для этого больного нужно уложить с приподнятым изголовьем. Нужно обеспечить приток свежего воздуха и постараться успокоить пациента, можно дать успокоительные препараты,
Следует дать больному под язык (можно предварительно измельчить) таблетку нитроглицерина и разжевать одну таблетку аспирина.
Если под рукой есть препараты из группы бета-блокаторов (Атенолол, Метапролол), то необходимо дать больному разжевать 1 таблетку. Если больной постоянно принимает эти лекарственные средства, то нужно принять внеочередную дозу лекарства.
Дополнительно пациент может принять таблетку панангина или 60 капель корвалола.
При подозрении на остановку сердца (потеря сознания, остановка дыхания, отсутствие пульса и реакции на внешние раздражители) необходимо немедленно начинать реанимационные мероприятия (непрямой массаж сердца и искусственное дыхание). Если больной не приходит в сознание, то продолжать их нужно до приезда врачей.
Квалифицированная помощь при инфаркте миокарда на догоспитальном этапе
Основная задача в лечении пациентов с инфарктом миокарда – это как можно более быстрое возобновление и поддержание кровообращения в пораженном участке миокарда. Здоровье и жизнь больных во многом зависит от оказания помощи на догоспитальном этапе.
Восстановление коронарного кровотока – не менее важная задача для врачей при лечении пациента с инфарктом миокарда. При отсутствии противопоказаний врач может начать проводить тромболизис в машине скорой помощи. Эта процедура показана не всем больным с инфарктом миокарда, показания к ней определяет врач, исходя из результатов электрокардиограммы. Эффективность тромболизиса напрямую зависит от сроков его начала, при введении тромболитических препаратов в первые часы после начала сердечно-сосудистой катастрофы вероятность восстановления кровотока в миокарде достаточно высока.
Решение о проведении тромболизиса на этапе транспортировки в стационар зависит от временного фактора. Введение препаратов начинает врач бригады скорой медицинской помощи, если время транспортировки больного в стационар превышает 30 минут.
Лечение инфаркта миокарда в стационаре
При появлении симптомов инфаркта миокарда больной в короткий срок должен быть госпитализирован в стационар.
Лучший метод восстановления кровотока и проходимости коронарных артерий – немедленная операция ангиопластики сосуда, в ходе которой в артерию устанавливается стент. Стентирование также необходимо провести в первые часы от начала инфаркта миокарда. В некоторых случаях единственным способом спасения сердечной мышцы является срочная операция аортокоронарного шунтирования.
Пациента с инфарктом миокарда госпитализируют в блок интенсивной терапии, а при необходимости – в реанимационное отделение, где при помощи специальных аппаратов врачи могут постоянно наблюдать за состоянием больного.
В терапии этого заболевания может применяться большое количество групп препаратов, ведь при лечении инфаркта миокарда необходимо выполнять сразу несколько задач:
Перечислены далеко не все группы препаратов, которые могут применяться для лечения инфаркта миокарда. Лечебная тактика зависит от общего состояния пациента, наличия сопутствующих заболеваний почек, печени и других органов, а также от многих других факторов. Поэтому лечение этого тяжелого заболевания должен проводить только квалифицированный врач, самолечение недопустимо и может привести к гибели больного.
Последствия инфаркта миокарда всегда негативно отражаются на состоянии всего организма. Конечно, это зависит от того, насколько обширно поражение миокарда. У больных, перенесших инфаркт миокарда, нередко развиваются нарушения ритма сердца. Из-за омертвения участка миокарда и формирования рубца снижается сократительная функция сердца, в результате чего развивается сердечная недостаточность.
В результате обширного инфаркта и формирования большого рубца может возникнуть аневризма сердца – состояние, угрожающее жизни больного и требующее оперативного лечения. Аневризма не только ухудшает работу сердца, но и повышает вероятность образования тромбов в ней, также велик риск ее разрыва.
Профилактика инфаркта миокарда
Профилактика этого заболевания подразделяется на первичную и вторичную. Первичная направлена на то, чтобы не допустить возникновение инфаркта миокарда, а вторичная – на предупреждение повторения сердечно-сосудистой катастрофы у тех, кто ее уже перенес. Профилактика необходима не только пациентам, страдающим сердечно-сосудистыми заболеваниями, но и здоровым людям, и сводится к устранению факторов, повышающих риск возникновения сердечно-сосудистых катастроф.
При симптомах, напоминающих инфаркт миокарда, следует вызвать «Скорую помощь». Лечение больного с инфарктом проводит врач-кардиолог, он же осуществляет реабилитацию и диспансерное наблюдение после перенесенного заболевания. При необходимости стентирования или шунтирования их выполняет кардиохирург.
Инфаркт миокарда
Авторы: врач, к. м. н., Юдинцева М. С., m.yudintseva@vidal.ru
врач, к. м. н., Толмачева Е. А., e.tolmacheva@vidal.ru
врач, научный директор АО «Видаль Рус», Жучкова Т. В., t.zhutchkova@vidal.ru
Как показывают статистические исследования, инфаркт миокарда чаще развивается у мужчин в возрасте от 40 до 60 лет. У женщин это заболевание встречается примерно в полтора-два раза реже.
Инфаркт миокарда возникает у больных ишемической болезнью сердца (ИБС), при атеросклерозе, артериальной гипертонии. К факторам риска развития инфаркта миокарда относится курение (т.к. оно вызывает сужение коронарных сосудов сердца и снижает снабжение сердечной мышцы кровью), ожирение, недостаток двигательной активности.
В то же время инфаркт миокарда может стать первым проявлением ИБС.
К сожалению, инфаркт миокарда является сейчас одной из основных причин инвалидности во взрослом возрасте, а смертность среди всех заболевших составляет 10-12%.
Причины инфаркта миокарда
Кислород и питательные вещества к клеткам сердечной мышцы доставляет специальная разветвленная сеть сосудов, которые называются коронарными. При инфаркте миокарда происходит закупорка одного из таких сосудов тромбом (в 95% случаев тромб коронарной артерии образуется в области атеросклеротической бляшки). Запаса кислорода клеткам сердечной мышцы, которые питала перекрытая артерия, хватит на 10 секунд. Еще около 30 минут сердечная мышца остается жизнеспособной. Потом начинается процесс необратимых изменений в клетках и к третьему-шестому часу от начала окклюзии мышца сердца на этом участке погибает. В зависимости от размера погибшего участка выделяют крупно и мелкоочаговый инфаркт. Если некроз захватывает всю толщу миокарда, его называют трансмуральным.
Клиническая картина инфаркта миокарда отличается многообразием, что затрудняет постановку правильного диагноза в максимально короткий срок.
Диагноз устанавливается на основании трех критериев:
В сомнительных случаях врачи используют дополнительные исследования, например радиоизотопные методы выявления очага некроза миокарда.
Симптомы инфаркта миокарда
Обычно при инфаркте миокарда выявляются следующие признаки:
Далеко не всегда болезнь проявляется такой классической картиной. Человек может ощущать лишь дискомфорт в груди или перебои в работе сердца. В ряде случаев боль вообще отсутствует. Кроме того, встречаются нетипичные случаи инфаркта миокарда, когда заболевание проявляется затруднением дыхания с одышкой или болью в животе. Такие случаи особенно трудны в диагностике.
Осложнения инфаркта миокарда
При отсутствии своевременного лечения инфаркт миокарда может привести к острой сердечной недостаточности, кардиогенному шоку, разрыву сердца, нарушениям сердечного ритма и другим опасным состояниям.
Осложнения, связанные с инфарктом миокарда, требуют неотложной медицинской помощи.
Что можете сделать Вы
Лечение
Что может сделать врач
Во избежание ошибок при малейшем подозрении на инфаркт пациента как можно скорее доставляют в больницу. Лечение инфаркта миокарда обязательно проводится в реанимационном отделении стационара.
Терапия включает обезболивающие, препараты, способствующие растворению образовавшегося тромба, лекарства, снижающие артериальное давление, уменьшающие объем циркулирующей крови, снижающие частоту сердцебиений. Эффективность лечения зависит от времени, прошедшего с момента начала заболевания до попадания в больницу.
После стационара начинается необыкновенно важный период реабилитации, который длится до 6 месяцев. Врач назначит вам необходимую терапию. Некоторые лекарства предстоит принимать всю оставшуюся жизнь. Однако при выполнении назначений, отказе от курения и соблюдении диеты люди после инфаркта миокарда еще долгие годы живут полноценной здоровой жизнью.
Профилактика инфаркта
Профилактикой инфаркта миокарда является ежегодная диспансеризация и своевременная адекватная терапия хронических заболеваний, таких как ишемическая болезнь сердца, гипертоническая болезнь, атеросклероз и др.
Диагностика и лечение инфаркта миокарда на догоспитальном этапе
Как проводится купирование болевого приступа? В каких случаях показана тромболитическая терапия, а в каких — антикоагулянтная? Как проводится тромболитическая терапия? Что важно уточнить перед проведением тромболитической терапии? Инфаркт миокарда —
Как проводится купирование болевого приступа?
В каких случаях показана тромболитическая терапия, а в каких — антикоагулянтная?
Как проводится тромболитическая терапия? Что важно уточнить перед проведением тромболитической терапии?
Инфаркт миокарда — неотложное клиническое состояние, обусловленное некрозом участка сердечной мышцы, развившимся в результате нарушения ее кровоснабжения. Поскольку в первые часы (а иногда и сутки) от начала заболевания бывает сложно дифференцировать острый инфаркт миокарда и нестабильную стенокардию, для обозначения периода обострения ишемической болезни сердца (ИБС) в последнее время пользуются термином «острый коронарный синдром», под которым понимают любую группу клинических признаков, позволяющих заподозрить инфаркт миокарда или нестабильную стенокардию. Острый коронарный синдром может рассматриваться как первичный диагноз; он диагностируется на основании болевого синдрома (затяжной ангинозный приступ, впервые возникшая, прогрессирующая стенокардия) и изменений ЭКГ. Различают острый коронарный синдром с подъемом сегмента ST или остро возникшей полной блокадой левой ножки пучка Гиса (состояние, требующее проведения тромболизиса, а при наличии технических возможностей — ангиопластики) и без подъема сегмента ST — с его депрессией сегмента ST, инверсией, сглаженностью псевдонормализацией зубца Т, или вообще без изменений на ЭКГ (тромболитическая терапия не показана). Таким образом, диагноз «острый коронарный синдром» позволяет оперативно оценить объем необходимой неотложной помощи и выбрать адекватную тактику ведения пациентов.
С точки зрения определения объема необходимой лекарственной терапии и оценки прогноза представляют интерес три классификации. По глубине поражения (на основе данных электрокардиографического исследования) различают трансмуральный и крупноочаговый («Q-инфаркт» с подъемом сегмента ST в первые часы заболевания и формированием зубца Q в последующем) и мелкоочаговый («не Q-инфаркт», не сопровождающийся формированием зубца Q, а проявляющийся отрицательными зубцами Т); по клиническому течению — неосложненный и осложненный инфаркт миокарда; по локализации — инфаркт левого желудочка (передний, задний или нижний, перегородочный) и инфаркт правого желудочка.
Диагностика инфаркта миокарда на догоспитальном этапе
Наиболее типичным проявлением инфаркта миокарда является приступ боли в грудной клетке. Диагностически значимы такие параметры, как интенсивность болевого синдрома (если аналогичные боли возникали ранее, то при инфаркте они бывают необычно интенсивными), его продолжительность (необычно длительный приступ, продолжающийся более 15-20 мин), неэффективность сублингвального приема нитратов. При анализе клинической картины необходимо получить ответы на следующие вопросы:
По симптоматике острейшей фазы инфаркта миокарда, помимо болевого, выделяют и другие клинические варианты инфаркта миокарда (см. таблицу).
Данные физикального обследования (гипергидроз, резкая общая слабость, бледность кожных покровов, признаки острой сердечной недостаточности) при любом клиническом варианте инфаркта миокарда имеют только вспомогательное диагностическое значение.
Электрокардиографическими критериями инфаркта миокарда являются изменения, служащие признаками:
При инфаркте передней стенки подобные изменения выявляются в I и II стандартных отведениях, усиленном отведении от левой руки (aVL) и соответствующих грудных отведениях (V1, 2, 3, 4, 5, 6). При высоком боковом инфаркте миокарда изменения могут регистрироваться только в отведении aVL, и для подтверждения диагноза необходимо снять высокие грудные отведения. При инфаркте задней стенки (нижнем, диафрагмальном) эти изменения обнаруживаются во II, III стандартном и усиленном отведении от правой ноги (aVF). При инфаркте миокарда высоких отделов задней стенки левого желудочка (заднебазальном) изменения в стандартных отведениях не регистрируются, диагноз ставится на основании реципрокных изменений — высоких зубцов R и Т в отведениях V1-V2.
Кроме того, косвенным признаком инфаркта миокарда, не позволяющим определить фазу и глубину процесса, является остро возникшая блокада ножек пучка Гиса (при наличии соответствующей клиники).
Наибольшей достоверностью обладают электрокардиографические данные в динамике, поэтому электрокардиограммы по возможности должны сравниваться с предыдущими.
Таким образом, на догоспитальном этапе оказания медицинской помощи диагноз острого инфаркта миокарда ставится на основании клинической картины и изменений электрокардиограммы. В дальнейшем диагноз уточняется в стационаре после определения уровня маркеров некроза миокарда в крови и на основании динамики ЭКГ. В большинстве случаев острого коронарного синдрома с подъемом сегмента ST формируется инфаркт миокарда с зубцом Q; при остром коронарном синдроме без подъема сегмента ST при повышении уровня маркеров некроза диагностируется инфаркт миокарда без зубца Q, а при нормальном их уровне — нестабильная стенокардия.
Ведение больных на догоспитальном этапе
Для купирования тошноты и рвоты рекомендуют в/в введение 10-20 мг метоклопрамида (церукала, реглана). При выраженной брадикардии показано использование атропина в дозе 0,5 мг (0,5 мл 0,1%-ного раствора) в/в; терапия артериальной гипотензии проводится по общим принципам коррекции гипотензии при инфаркте миокарда.
Недостаточная эффективность обезболивания наркотическими анальгетиками служит показанием к в/в инфузии нитратов (см. ниже). При низкой эффективности нитратов в сочетании с тахикардией дополнительный обезболивающий эффект может быть получен благодаря введению бета-адреноблокаторов (см. ниже). Боль может быть купирована в результате эффективного тромболизиса (см. ниже).
Продолжающиеся интенсивные ангинозные боли служат показанием к применению масочного наркоза закисью азота (обладающей седативным и анальгезирующим действием) в смеси с кислородом. Начинают с ингаляции кислорода в течение 1-3 мин, затем используют закись азота (20 %) с кислородом (80 %) с постепенным повышением концентрации закиси азота до 80 %; после засыпания больного переходят на поддерживающую концентрацию газов — 50:50. Закись азота не снижает выброса левого желудочка. Возникновение побочных эффектов (тошноты, рвоты, возбуждения или спутанности сознания) является показанием для уменьшения концентрации закиси азота или отмены ингаляции. При выходе из наркоза ингалируют чистый кислород в течение 10 мин для предупреждения артериальной гипоксемии.
А. Показаниями к проведению тромболизиса служит подъем сегмента ST более чем на 0,1 мВ по крайней мере в двух стандартных отведениях ЭКГ и более чем на 0,2 мВ в двух смежных грудных отведениях или остро возникшая полная блокада левой ножки пучка Гиса в период от 30 мин до 12 ч от начала заболевания. Применение тромболитических средств возможно и позднее, если сохраняется подъем ST на ЭКГ, продолжается болевой приступ и/или наблюдается нестабильная гемодинамика.
В отличие от внутрикоронарного системный тромболизис (осуществляется внутривенным введением тромболитических средств) не требует каких-либо сложных манипуляций и специального оборудования. При этом он достаточно эффективен, если проводится в первые часы развития инфаркта миокарда (оптимально — на догоспитальном этапе), поскольку сокращение летальности напрямую зависит от сроков достижения реперфузии.
При отсутствии противопоказаний решение вопроса о проведении тромболизиса принимается на основании анализа фактора времени: при транспортировке более 30 мин или при отсрочке внутрибольничного проведения тромболизиса более чем на 60 мин введение тромболитических средств должно осуществляться на догоспитальном этапе. Во всех остальных случаях оно должно быть отложено до стационара.
Наиболее часто для проведения тромболизиса используется стрептокиназа внутривенно только через периферические вены, попытки катетеризации центральных вен недопустимы; перед инфузией возможно внутривенное введение 5-6 мл 25%-ного магния сульфата либо 10 мл кормагнезина-200 в/в струйно, медленно (за 5 мин); «нагрузочная» доза аспирина (250-300 мг разжевать) дается всегда, за исключением случаев, когда аспирин противопоказан (аллергические и псевдоаллергические реакции); 1 500 000 Ед стрептокиназы разводятся в 100 мл изотонического раствора хлорида натрия и вводятся внутривенно за 30 мин.
Одновременного назначения гепарина при использовании стрептокиназы не требуется — предполагают, что стрептокиназа сама обладает антикоагуляционными и антиагрегационными свойствами. Показано, что внутривенное введение гепарина не снижает летальности и частоты рецидивов инфаркта миокарда, а эффективность подкожного введения препарата сомнительна. Если гепарин по каким-либо причинам был введен ранее, это не является препятствием к проведению тромболизиса. Рекомендуется назначение гепарина через 12 ч после прекращения инфузии стрептокиназы. Практиковавшееся ранее использование гидрокортизона для профилактики анафилаксии признано не только малоэффективным, но и небезопасным в острейшей стадии инфаркта миокарда (глюкокортикоиды увеличивают риск разрыва миокарда).
Основные осложнения тромболизиса:
Клинические признаки восстановления коронарного кровотока: прекращение ангинозных приступов через 30-60 мин после введения тромболитика, стабилизация гемодинамики, исчезновение признаков левожелудочковой недостаточности, быстрая (в течение 2-3 ч) динамика ЭКГ с приближением сегмента ST к изолинии на 50% от исходного уровня подъема и ранним формированием патологического зубца Q и/или отрицательного зубца Т, появление реперфузионных аритмий (ускоренного идиовентрикулярного ритма, желудочковой экстрасистолии и др.), быстрая динамика МВ-КФК.
Для решения вопроса о возможности использования тромболитических средств следует уточнить ряд моментов:
Следует также обратить внимание на другие состояния, чреватые развитием геморрагических осложнений и служащие относительными противопоказаниями к проведению системного тромболизиса: тяжелые заболевания печени и почек; подозрение на хроническую аневризму сердца, перикардит, инфекционный миокардит, тромб в сердечных полостях; тромбофлебит и флеботромбоз; варикозное расширение вен пищевода; язвенная болезнь в стадии обострения; беременность.
В сомнительных случаях проведение тромболитической терапии должно быть отложено до поступления больного в стационар (при атипичном развитии заболевания, неспецифических изменениях ЭКГ, давно существующей блокаде ножки пучка Гиса или ЭКГ-признаках несомненного предшествующего инфаркта миокарда, маскирующих типичные изменения).
Б. При отсутствии показаний к тромболитической терапии (поздние сроки, так называемый мелкоочаговый или «не-Q-инфаркт») проводится антикоагулянтная терапия. Ее цель заключается в предупреждении или ограничении тромбоза венечных артерий, а также в профилактике тромбоэмболических осложнений (особенно часто развивающихся у больных передним инфарктом миокарда, при низком сердечном выбросе, мерцательной аритмии). Для этого на догоспитальном этапе внутривенно болюсно вводится гепарин в дозе до 5000 МЕ. Если в условиях стационара не проводится тромболитическая терапия, то начинается длительная внутривенная инфузия гепарина со скоростью 800-1000 МЕ/ч под контролем активированного частичного тромбопластинового времени. Альтернативой может, по-видимому, служить подкожное введение низкомолекулярного гепарина в «лечебной» дозе. Введение гепарина на догоспитальном этапе не препятствует проведению тромболизиса в стационаре.
В. С первых минут от начала развития инфаркта миокарда всем больным при отсутствии противопоказаний следует назначать малые дозы ацетилсалициловой кислоты (аспирина). Антитромбоцитарный эффект препарата максимально проявляется уже через 30 мин, а своевременное начало применения аспирина позволяет существенно снизить летальность. Назначение ацетилсалициловой кислоты перед проведением тромболизиса дает наибольший клинический эффект. Доза для первого приема на догоспитальном этапе составляет 160-325 мг (разжевать). На стационарном этапе препарат назначается 1 раз в сутки по 100-125 мг.
А. Внутривенное введение нитратов при остром инфаркте миокарда способствует купированию болевого синдрома, гемодинамической разгрузке левого желудочка, снижает АД. Растворы нитратов для внутривенного введения готовят ex tempore: каждые 10 мг нитроглицерина (например, 10 мл 0,1%-ного раствора в виде препарата перлинганит) или изосорбида динитрата (например, 10 мл 0,1%-ного раствора в виде препарата изокет) разводят в 100 мл физиологического раствора (20 мг препарата — в 200 мл физиологического раствора и т. д.); таким образом, 1 мл приготовленного раствора содержит 100 мкг препарата. Нитраты вводят капельно под постоянным контролем АД и ЧСС с начальной скоростью 5-10 мкг/мин и последующим увеличением скорости на 20 мкг/мин каждые 5 мин до достижения желаемого эффекта или максимальной скорости введения — 400 мкг/мин. Обычно эффект достигается при скорости инфузии 50-100 мкг/мин. При отсутствии дозатора приготовленный раствор, содержащий в 1 мл 100 мкг нитрата, вводят при тщательном контроле (см. выше) с начальной скоростью 2-4 капли в минуту, при условии стабильной гемодинамики и сохранения болевого синдрома скорость может постепенно увеличиваться вплоть до максимальной — 30 капель в минуту. Введение нитратов начинают как линейные, так и специализированные бригады СиНМП и продолжают в стационаре. Продолжительность внутривенного введения нитратов — 24 ч и более; за 2-3 ч до окончания инфузии назначается первая доза нитратов внутрь. Передозировка нитратов, вызывающая падение сердечного выброса и снижение САД ниже 80 мм рт. ст., может привести к ухудшению коронарной перфузии и к увеличению размеров инфаркта миокарда.
Б. Внутривенное введение бета-адреноблокаторов, так же как и применение нитратов, способствует купированию болевого синдрома. Ослабляя симпатические влияния на сердце (усиливающиеся в первые 48 ч от начала развития инфаркта миокарда как вследствие самого заболевания, так и в качестве реакции на боль) и снижая потребность миокарда в кислороде, они способствуют уменьшению размеров инфаркта миокарда, подавляют желудочковые аритмии, уменьшают риск разрыва миокарда и повышают таким образом выживаемость пациентов. Очень важно, что, согласно экспериментальным данным, бета-адреноблокаторы позволяют отсрочить гибель ишемизированных кардиомиоцитов (они увеличивают время, в течение которого эффективна реперфузионная терапия).
При отсутствии противопоказаний бета-адреноблокаторы назначаются всем больным острым инфарктом миокарда. На догоспитальном этапе показаниями к их внутривенному введению для линейной бригады служат соответствующие нарушения ритма, а для специализированной — упорный болевой синдром, тахикардия, артериальная гипертензия. В первые часы заболевания показано дробное внутривенное введение пропранолола (обзидана) по 1 мг в минуту каждые 3-5 мин под контролем АД и ЭКГ до достижения ЧСС 55-60 в минуту или до достижения общей дозы 0,1 мг на кг массы тела пациента. При брадикардии, признаках сердечной недостаточности, AV-блокаде и снижении САД менее 100 мм рт. ст. пропранолол не назначается, а при развитии указанных изменений на фоне его применения введение препарата прекращается.
Отсутствие осложнений терапии бета-адреноблокаторами на догоспитальном этапе служит показанием для обязательного ее продолжения в условиях стационара с переходом на прием пропранолола внутрь в суточной дозе 40-320 мг в 4 приема (первый прием — спустя 1 ч после внутривенного введения).
В. Внутривенная инфузия магния сульфата проводится у больных с доказанной или вероятной гипомагнезиемией или при синдроме удлиненного QT, а также в случае осложнения инфаркта миокарда некоторыми вариантами аритмий. При отсутствии противопоказаний магния сульфат может служить определенной альтернативой применению нитратов и бета-адреноблокаторов, если их введение по какой-то причине невозможно (из-за противопоказаний или отсутствия препаратов). Согласно результатам ряда исследований, он снижает летальность при остром инфаркте миокарда, а также предотвращает развитие аритмий (в том числе реперфузионных при проведении системного тромболизиса) и постинфарктной сердечной недостаточности.
Этой же цели служит оксигенотерапия, показанная при остром инфаркте миокарда всем больным в связи с частым развитием гипоксемии даже при неосложненном течении заболевания. Ингаляция увлажненным кислородом проводится (если это не причиняет чрезмерных неудобств) с помощью маски или через носовой катетер со скоростью 3-5 л/мин и целесообразна в течение первых 24-48 ч от начала заболевания (начинается на догоспитальном этапе и продолжается в стационаре).
Тактика ведения больного с различными вариантами инфаркта миокарда на догоспитальном этапе представлена на рис. 1 и рис. 2.
Острый инфаркт миокарда является прямым показанием к госпитализации в отделение (блок) интенсивной терапии или кардиореанимации. Транспортировка больного осуществляется на носилках.
А. Л. Верткин, доктор медицинских наук, профессор
В. В. Городецкий, кандидат медицинских наук
О. Б. Талибов, кандидат медицинских наук
Современные подходы к лечению острого инфаркта миокарда
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Российский кардиологический научно-производственный комплекс Минздрава РФ, Москва
Сегодня инфаркт миокарда (ИМ) остается таким же серьезным заболеванием, как и несколько десятилетий назад. Вот только один из примеров, доказывающих тяжесть этой болезни: около 50% больных умирают до того, как успевают встретиться с врачом. Вместе с тем совершенно очевидно, что риск ИМ для жизни и здоровья стал значительно ниже. После того, как 35 лет назад были разработаны основные принципы палат интенсивного наблюдения за коронарными больными и эти палаты начали реально работать в практике здравоохранения, существенно повысилась эффективность лечения и профилактики нарушений ритма и проводимости сердца больных ИМ и снизилась госпитальная летальность. В 70-е годы она составляла более 20%, однако в последние 15 лет, после того как была доказана роль тромбоза в патогенезе острого ИМ и показано благоприятное влияние тромболитической терапии, в целом ряде клиник летальность сократилась в 2 раза и более. Надо сказать, что основные принципы и рекомендации по лечению острого ИМ, впрочем, как и для большинства других серьезных патологий, основываются не только на опыте и знаниях отдельных клиник, направлений, школ, но и на результатах крупных многоцентровых исследований, подчас проводящихся одновременно во многих сотнях больниц в разных странах мира. Конечно, это позволяет врачу в стандартных клинических ситуациях быстрее находить правильное решение.
Основными задачами лечения острого ИМ можно назвать следующие: купирование болевого приступа, ограничение размеров первичного очага поражения миокарда и, наконец, профилактика и лечение осложнений. Типичный ангинозный приступ, развивающийся у подавляющего числа больных при ИМ, связан с ишемией миокарда и продолжается до тех пор, пока не происходит некроз тех кардимиоцитов, которые должны погибнуть. Одним из доказательств именно этого происхождения боли служит быстрое ее исчезновение, при восстановлении коронарного кровотока (например, на фоне тромболитической терапии).
Купирование болевого приступа
Сама по себе боль, воздействуя на симпатическую нервную систему, может существенно увеличивать частоту сердечных сокращений, артериальное давление (АД), а также работу сердца. Именно эти факторы обусловливают необходимость как можно быстрее купировать болевой приступ. Целесообразно дать больному нитроглицерин под язык. Это может ослабить боль в том случае, если больной не получал ранее нитроглицерин в связи с этим приступом. Нитроглицерин может быть в форме таблеток или аэрозоля. Не нужно прибегать к его применению при систолическом АД ниже 90 мм рт.ст.
Основным патогенетическим методом лечения ИМ является восстановление проходимости окклюзированной коронарной артерии. Чаще всего для достижения этого используют либо тромболитическую терапию, либо механическое разрушение тромба при транслюминальной коронарной ангиопластике. Для большинства клиник нашей страны наиболее реалистично сегодня применение первого способа.
Процесс некроза развивается у человека крайне быстро и в основном заканчивается, как правило, уже через 6–12 ч от начала ангинозного приступа, поэтому чем быстрее и полноценнее удается восстановить кровоток по тромбированной артерии, тем более сохранной будет функциональная способность миокарда левого желудочка и в конечном итоге меньше летальность. Оптимальным считается начало введения тромболитических препаратов через 2–4 ч от начала болезни. Успех лечения будет большим, если удастся сократить промежуток времени до начала тромболитической терапии, что может быть осуществлено двумя путями: первый – раннее выявление и госпитализация больных в стационар и быстрое принятие решения о соответствующем лечении, второй – начало терапии на догоспитальном этапе. В наших исследованиях показано, что начало тромболитической терапии на догоспитальном этапе позволяет добиться выигрыша во времени, в среднем около 2,5 ч. Такой способ тромболитической терапии, если он проводится врачами специализированной бригады кардиологической помощи, является относительно безопасным. При отсутствии противопоказаний тромболитическую терапию целесообразно проводить всем больным в первые 12 ч болезни. Эффективность тромболитической терапии выше (снижение летальности на 42–47%), если она начата в течение 1-го часа болезни. При сроках более 12 ч применение тромболитических препаратов проблематично и должно решаться с учетом реальной клинической ситуации. Особенно показана тромболитическая терапия пожилым людям, пациентам с передним ИМ, а также в тех случаях, когда ее начинают достаточно рано. Обязательное условие для начала тромболитической терапии – наличие элеваций сегмента ST на ЭКГ или признаков блокады ножек пучка Гиса. Тромболитическая терапия не показана, если элевации сегмента ST отсутствуют, независимо от того, как выглядит конечная фаза QRS на ЭКГ – депрессии, отрицательные Т или отсутствие каких-либо изменений. Раннее начало терапии тромболитиками позволяет спасти до 30 больных из 1000 леченых.
Сегодня основным путем введения тромболитических препаратов является внутривенный. Все используемые препараты, тромболитики первого поколения, такие как стрептокиназа (1 500 000 ЕД в течение 1 ч) – урокиназа (3 000 000 ЕД в течение 1 ч), второго поколения – тканевой активатор плазминогена (100 мг болюсом плюс инфузия), проурокиназа (80 мг болюсос плюс инфузия 1 ч) – являются высокоэффективными тромболитиками.
Риск терапии тромболитиками общеизвестен – это возникновение кровотечений, из наиболее опасных – кровоизлияние в мозг. Частота геморрагических осложнений невелика, например количество инсультов при применении стрептокиназы не превышает 0,5%, а при использовании тканевого активатора плазминогена – 0,7–0,8%. Как правило, в случае серьезных геморрагий вводят свежезамороженную плазму и, конечно, прекращают введение тромболитика. Стрептокиназа может вызывать аллергические реакции, которые, как правило, удается предотвратить профилактическим введением кортикостероидов – преднизолона или гидрокортизона. Другое осложнение – гипотония, которая чаще наблюдается при использовании препаратов, созданных на основе стрептокиназы, нередко она сопровождается брадикардией. Обычно это осложнение удается купировать после прекращения инфузии тромболитика и введения атропина и адреналина, иногда требуется применение плазмозаменителей и инотропных средств. Сегодня абсолютными противопоказаниями к тромболитической терапии считаются подозрение на расслоение аорты, активное кровотечение и предшествующий геморрагический инсульт.
В среднем тромболитические препараты получает всего лишь одна треть больных ИМ, а в нашей стране эта цифра существенно ниже. Тромболитики не вводят в основном в связи с поздним поступлением больных, наличием противопоказаний или неопределенностью изменений на ЭКГ. Летальность среди больных, не получающих тромболитики, остается по-прежнему высокой и составляет от 15 до 30%.
В 1-е сутки после ИМ повышается симпатическая активность, поэтому использование b-адреноблокаторов, которые снижают потребление кислорода миокардом, уменьшают работу сердца и напряжение стенки желудочка, стало обоснованием их применения у этой категории больных. Ряд крупных многоцентровых исследований, в которых изучалась эффективность внутривенного введения b-блокаторов в 1-е сутки ИМ, показал, что они снижают летальность за 1-ю неделю примерно на 13–15%. Эффект несколько выше, если лечение начинается в первые часы болезни, и отсутствует, если использовать эти препараты со 2–3-го дня заболевания. b-блокаторы уменьшают и количество повторных инфарктов в среднем на 15–18%. Механизм влияния b-блокаторов на летальность – это уменьшение случаев фибрилляции желудочков и разрывов сердца.
Лечение b-блокаторами начинают с внутривенного введения (метопролол, атенолол, пропранолол) – 2–3 раза или столько, сколько потребуется, чтобы оптимально снизить частоту сердечных сокращений. В последующем переходят на прием препаратов внутрь: метопролол 50 мг каждые 6 ч в первые 2 сут, атенолол по 50 мг каждые 12 ч в течение суток, а затем подбирают дозу индивидуально для каждого больного. Основные показания к применению b-блокаторов – признаки симпатической гиперактивности, такие как тахикардия при отсутствии признаков сердечной недостаточности, гипертония, болевой синдром, наличие ишемии миокарда. b-Блокаторы, несмотря на наличие противопоказаний к их применению, например брадикардии (число сердечных сокращений меньше 50 в 1 мин), гипотонии (систолическое АД ниже 100 мм рт.ст.), наличие блокад сердца и отека легких, а также бронхоспазма, применяются тем не менее у подавляющего числа больных ИМ. Однако способность препаратов уменьшать летальность не распространяется на группу b-блокаторов с собственной симпатомиметической активностью. Если больной начал лечиться b-блокаторами, прием препарата следует продолжать до тех пор, пока не появятся серьезные противопоказания.
Применение антиагрегантов и антикоагулянтов
Применение при остром ИМ дезагрегантов, в частности ацетилсалициловой кислоты, способствует уменьшению тромбоза, причем максимальный эффект препарата достигается достаточно быстро после приема первоначальной дозы 300 мг и стабильно поддерживается при ежедневном приеме ацетилсалициловой кислоты в небольших дозах – от 100 до 250 мг/сут. При исследованиях, проведенных у многих тысяч больных оказалось, что применение ацетилсалициловой кислоты снижает 35-дневную летальность на 23%. Противопоказана ацетилсалициловая кислота при обострении язвенной болезни, при его непереносимости, а также при бронхиальной астме, провоцируемой этим препаратом. Длительное применение препарата существенно снижает частоту повторныех инфарктов – до 25%, поэтому прием ацетилсалициловой кислоты рекомендуется на неопределенно долгое время.
Еще одна группа препаратов, воздействующих на тромбоциты, это блокаторы гликопротеина IIВ/IIIА тромбоцитов. В настоящее время известна и доказана эффективность применения двух представителей данного класса – это абсиксимаб и тирофебан. По механизму действия эти препараты выгодно отличаются от ацетилсалициловой кислоты, так как блокируют большинство известных путей активации тромбоцитов. Препараты препятствуют образованию первичного тромбоцитарного тромба, причем действие их иногда бывает достаточно продолжительным – до полугода. Мировой опыт пока еще невелик, в нашей стране работа с этими препаратами только начинается. Из антитромботических препаратов по-прежнему широко используется антикоагулянт гепарин, который в основном назначают для профилактики повторных инфарктов, для предупреждения тромбозов и тромбоэмболий. Схемы и дозы введения его хорошо известны. Дозу подбирают так, чтобы частичное тромбопластиновое время увеличилось в 2 раза по сравнению с нормой. Средняя доза – это 1000 ЕД/ч в течение 2–3 дней, подкожное введение гепарина рекомендуется при медленной активизации пациентов.
В настоящее время имеются данные об использовании низкомолекулярных гепаринов, в частности эноксипарина и фрагмина. Основные их преимущества состоят в том, что они фактически не требуют лабораторного контроля за показателями свертываемости крови и специальной аппаратуры, например инфузионных насосов, для их введения, а главное – они существенно эффективнее чем нефракционированные гепарины. Не потеряло своей значимости применение непрямых антикоагулянтов, особенно при венозных тромбозах, выраженной сердечной недостаточности, наличии тромба в левом желудочке.
В качестве стандартной терапии ИМ антагонисты кальция в настоящее время фактически не используются, так как не оказывают благоприятного влияния на прогноз, а применение их с научной точки зрения малообоснованно.
Внутривенное введение нитратов при ИМ в первые 12 ч заболевания уменьшает размер очага некроза, влияет на основные осложнения ИМ, включая летальные исходы и частоту развития кардиогенного шока. Применение их снижает летальность до 30% в первые 7 дней болезни, это наиболее очевидно при инфарктах передней локализации. Прием нитратов внутрь начиная с 1-х суток заболевания не приводит ни к улучшению, ни к ухудшению прогноза к 30-му дню болезни. Внутривенное введение нитратов должно быть стандартной терапией для всех пациентов, поступивших в первые часы болезни, с передним ИМ и систолическим АД выше 100 мм рт.ст. Начинают введение нитроглицерина с невысокой скоростью, например 5 мкг/мин, постепенно увеличивают ее, достигая уменьшения систолического давления на 15 мм рт.ст. У больных с артериальной гипертонией снижение АД возможно до 130–140 мм рт.ст. Как правило, терапию нитратами проводят в течение 24 ч, если не появляется необходимости продолжения этой терапии, в частности при сохраняющихся болях, связанных с ишемией миокарда, или признаках сердечной недостаточности.
В последнее десятилетие в лечении больных ИМ прочно заняла свое место большая группа ингибиторов ангиотензинпревращающего фермента (иАПФ). Это в первую очередь определяется тем, что данные препараты способны приостанавливать расширение, дилатацию левого желудочка, истончение миокарда, т.е. воздействовать на процессы, приводящие к ремоделированию миокарда левого желудочка и сопровождающиеся серьезным ухудшением сократительной функции миокарда и прогноза. Как правило, лечение иАПФ начинают через 24–48 ч от момента развития ИМ, чтобы снизить вероятность артериальной гипертонии. В зависимости от исходно нарушенной функции левого желудочка терапия может продолжаться от нескольких месяцев до многих лет. Установлено, что лечение каптоприлом в дозе 150 мг/сут у пациентов без клинических признаков недостаточности кровообращения, но при наличии фракции выброса ниже 40% существенно улучшало прогноз. В группе леченых смертность была ниже на 19%, на 22% было меньше случаев сердечной недостаточности, требовавшей лечения в условиях стационара. Таким образом, АПФ (каптоприл 150 мг/сут, рамиприл 10 мг/сут, лизиноприл 10 мг/сут и др.) целесообразно назначать большинству больных ИМ, независимо от его локализации и наличия или отсутствия сердечной недостаточности. Однако эта терапия более эффективна при сочетании клинических признаков сердечной недостаточности и данных инструментальных исследований (низкая фракция выброса). В этом случае риск летального исхода снижается на 27%, т.е. это предотвращает смертельные исходы у каждых 40 из 1000 леченых больных в течение года.
Уже во время пребывания больного в стационаре целесообразно детально исследовать его липидный спектр. Сам по себе острый ИМ несколько уменьшает содержание свободного холестерина в крови. При наличии данных о существенных изменениях этого показателя, например при уровне общего холестерина выше 5,5 ммоль/л, целесообразно рекомендовать больному не только гиполипидемическую диету, но и прием препаратов, в первую очередь статинов.
Таким образом, в настоящее время врач располагает значительным арсеналом средств, позволяющих помочь больному ИМ и свести к минимуму риск возникновения осложнений. Конечно, основной путь достижения этой цели – применение тромболитических препаратов, но вместе с тем использование b-блокаторов, аспирина, АПФ и нитратов может существенным образом повлиять на прогноз и исход заболевания.
Инфаркт миокарда
Обзор
Инфаркт миокарда (сердечный приступ) — это тяжелое неотложное состояние, при котором внезапно нарушается кровообращение сердца, обычно из-за кровяного сгустка (тромба). Недостаток притока крови к сердцу может серьезно повредить сердечную мышцу.
Позвоните по телефону скорой помощи — 03 со стационарного телефона, 112 или 911 — с мобильного, если вы подозреваете у себя или кого-либо другого инфаркт миокарда.
До приезда скорой помощи вы можете принять аспирин, если у вас нет на него аллергии. Аспирин разжижает кровь и помогает восстановить поступление крови к сердцу. Чаще аспирин выпускается в таблетках по 500 мг. Примите половину таблетки (250 мг), разжевав ее перед проглатыванием.
Лечение инфаркта миокарда зависит от степени его тяжести. С помощью лекарственных препаратов или хирургической операции можно уничтожить тромб и восстановить кровообращение сердечной мышцы, тем самым сохранить ее жизнеспособность.
Время, требующееся для восстановления после инфаркта, зависит от величины повреждения миокарда. Некоторые люди приступают к работе уже спустя несколько недель после случившегося, другим требуется несколько месяцев.
Инфаркт миокарда — это одна из самых частых причин для вызова скорой помощи. По данным официальной статистики, в России в последние годы острый инфаркт миокарда бывает у немногим более чем 150 тысяч человек в год. Чаще всего инфаркт миокарда случается у людей старше 45 лет. У мужчин вероятность возникновения инфаркта миокарда в два-три раза выше, чем у женщин.
Медицинский прогноз для человека, перенесшего инфаркт миокарда зависит от:
В целом, в результате инфаркта миокарда умирает примерно треть перенесших его людей. Чаще всего это происходит до попадания в больницу либо же в течение 28 дней после приступа. Если человек выживает в течение 28 дней после инфаркта, медицинский прогноз для него резко улучшается, и большинство таких людей выписываются и живут еще многие годы.
Симптомы инфаркта миокарда
Симптомы включают в себя:
Интенсивность боли значительно различается от человека к человеку. Для многих боль настолько сильна, что они описывают её как «слона, сидящего на моей груди».
Необходимо подчеркнуть, что не все испытывают сильную боль. Часто при инфаркте боль может быть незначительной и даже ошибочно принята за несварение желудка. Именно сочетание перечисленных симптомов говорит о наличии у вас сердечного приступа, а не только сильная боль. У больных диабетом, некоторых женщин и пожилых людей инфаркт может развиваться совсем без боли. Тогда заподозрить его можно по сочетанию остальных значимых симптомов.
Если вы подозреваете у себя или другого человека инфаркт (даже, если не уверены в этом), обязательно вызовите скорую помощь, позвонив — 03 со стационарного телефона, 112 или 911 — с мобильного. Сделать это нужно при первых симптомах, как можно быстрее, не теряя времени на сомнения и раздумья. Лучше врачи исключат инфаркт миокарда и скажут, что вы ошиблись, чем приедут тогда, когда время для спасения жизни будет уже упущено.
Совет для людей со стенокардией
Стенокардия — это заболевание, связанное с нарушением поступления к сердца крови, богатой кислородом. Проявления стенокардии во многом похожи на инфаркт миокарда, но обычно проходят в течение нескольких минут. Тем не менее, иногда у людей со стенокардией может случиться инфаркт миокарда. Важно уметь различать симптомы стенокардии и инфаркта миокарда.
Симптомы стенокардии, как правило, полностью снимает прием лекарственных препаратов. При инфаркте миокарда боль в груди или одышка сохраняются, даже после применения привычных лекарств, которые ранее приносили облегчение.
Если у вас стенокардия, вам могли быть назначены препараты, быстро облегчающие симптомы, например, нитроглицерин. Если первая доза препарата не действует, примите еще одну через пять минут и третью дозу, спустя еще пять минут. Если боль или другие симптомы сохраняется в течение 15 минут, несмотря на три принятые дозы нитроглицерина, вызовите скорую помощь (03 со стационарного телефона, 112 или 911 — с мобильного).
В ожидании бригады скорой помощи
До приезда скорой помощи вы можете принять аспирин, если у вас нет на него аллергии. Аспирин разжижает кровь и помогает восстановить поступление крови к сердцу. Чаще аспирин выпускается в таблетках по 500 мг. Примите половину таблетки (250 мг), разжевав ее перед проглатыванием.
В некоторых случаях инфаркт миокарда может осложниться внезапной остановкой сердца. При остановке сердца человек:
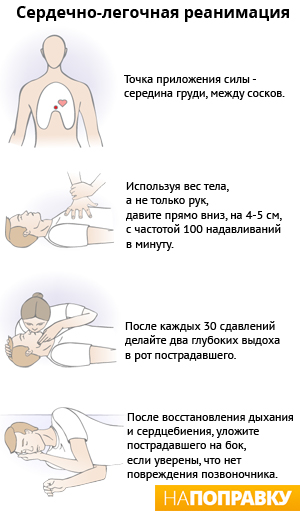
Если вы предполагаете, что у кого-то случилась остановка сердца, вам следует выполнить непрямой массаж сердца, так как он помогает восстановить работу сердца.
Чтобы провести непрямой массаж сердца, положите свою ладонь на центр груди, между сосков. Положите вторую ладонь поверх первой и сцепите пальцы. Используя вес тела (а не только ваших рук), давите прямо вниз (на 4-5 см) на его грудь. Стремитесь делать массаж сердца с частотой 100 надавливаний в минуту.
Эти рекомендации применимы только для взрослых. Прочитайте подробнее о том, как оказать первую помощь ребенку.
Причины инфаркта миокарда
Сердце, как и другие органы нашего тела, нуждается в непрерывном поступлении насыщенной кислородом крови. Если приток крови к сердцу внезапно прерывается, сердечная мышца повреждается и может погибнуть.
Если вовремя не начато лечение, в мышце сердца (миокарде) развиваются необратимые повреждения (некроз — гибель тканей). Если погибла значительная часть миокарда, сердце перестает биться, что приводит к смерти.
Ишемическая болезнь сердца (ИБС)
Ишемическая болезнь сердца (ИБС) — это самая распространенная причина инфаркта миокарда. ИБС — это заболевание, при котором коронарные артерии (крупные кровеносные сосуды, доставляющие кровь к сердцу) забиваются отложениями холестерина. Эти отложения называются атеросклеротическими бляшками.
Во время инфаркта миокарда оболочка одной из бляшек разрывается, что приводит к образованию кровяного сгустка (тромба) в месте разрыва. Тромб может затем перекрыть поступление крови, текущей по коронарной артерии к сердцу, провоцируя инфаркт миокарда. Ниже описаны факторы риска ишемической болезни сердца, многие из которых взаимосвязаны.
Курение. Токсины, содержащиеся в табачном дыму, сужают и повреждают коронарные артерии. Это делает курильщиков более уязвимыми для ИБС. По сравнению с некурящими, у людей, выкуривающих 20 и более сигарет в день, риск развития ИБС и инфаркта миокарда на 60-90% больше. Даже малые дозы табака могут быть опасны. Выкуривая всего лишь одну сигарету в день, вы тем не менее имеете на 30% больше шансов развития ИБС по сравнению с некурящими. Прочитайте подробнее о том, как бросить курить.
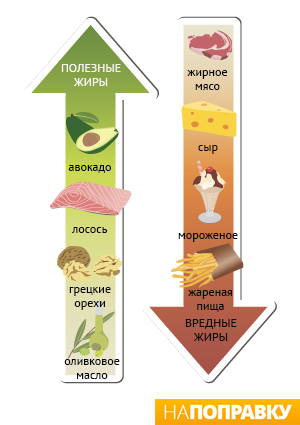
Питание. Если вы едите пищу, богатую насыщенными жирами, уровень холестерина в крови будет расти. Это приводит к увеличению риска ИБС и инфаркта миокарда. Некоторые продукты, например, жирная рыба, могут снижать уровень холестерина в крови. Прочитайте подробнее о том, как правильно питаться.
Частое повышение кровяного давления выше нормы (гипертензия), может приводить к ослаблению коронарных артерий, делая их уязвимыми для ИБС. Чем выше кровяное давление, тем больше риск ИБС и инфаркта миокарда.
Сахарный диабет. Повышенный уровень глюкозы в крови, связанный с наличием диабета 1 типа или 2 типа может вызвать повреждение коронарных артерий. Установлено, что люди с сахарным диабетом, заболевают ИБС в 2-5 раз чаще, чем остальные.
Полнота и ожирение не ведут к прямому повышению риска ИБС, но приводят к развитию связанных с ними факторов риска ИБС. В частности, полные и страдающие ожирением люди:
Недостаток физической активности не связан напрямую с повышенным риском ИБС и инфаркта миокарда. Однако, малоподвижный образ жизни способствует появлению лишнего веса и ожирения, а также — гипертонии.
Избыточное потребление алкоголя способствует повышению кровяного давления (гипертензии) и росту уровня холестерина в крови, повышая риск возникновения ИБС. Также много пьющие люди склонны к нездоровому образу жизни, в том числе — курению, потреблению жирной пищи и недостаточной физической активности.
Возраст и пол. Чем старше вы становитесь, тем выше вероятность развития ИБС. Вероятность инфаркта миокарда у мужчин в два-три раза выше, чем у женщин. Для объяснения этого явления был предложен ряд медицинских обоснований:
Наследственная предрасположенность. Если у вас имеются родственники первого уровня (родители, братья или сестры) с сердечнососудистыми заболеваниями, такими как стенокардия, инфаркт миокарда или инсульт, то у вас в 2 раза увеличивается вероятность развития таких же заболеваний по сравнению с другими людьми.
Загрязнение воздуха. Недавние исследования обнаружили, что воздействие загрязненного воздуха (в особенностями выхлопных газов), повышает риск развития ИБС и инфаркта миокарда. В исследовании, проведенном в 2011 году, установлено, 1 из 13 случаев инфаркта связан с загрязнением воздуха.
Менее распространенные причины инфаркта
Недостаток кислорода в крови (гипоксия). При снижении содержания кислорода в крови, из-за отравления угарным газом или плохой работы легких, к сердцу поступает кровь с пониженным содержанием кислорода. В результате это может привести к повреждению сердечной мышцы — инфаркту миокарда.
Аневризма — это выпячивание стенки кровеносного сосуда. Если стенка кровеносного сосуда истончается до определенной степени, она больше не может выдерживать давление крови, текущей по этому сосуду, и разрывается.
Иногда аневризма может развиться в коронарной артерии, хотя это намного менее распространено, чем другие виды аневризмы. Если разорвется аневризма коронарной артерии, поступление крови к сердцу прекратится, что вызовет инфаркт миокарда.
Диагностика инфаркта миокарда
При подозрении на инфаркт миокарда необходима немедленная госпитализация в больницу, в отделение реанимации и интенсивной терапии, где будет проведена диагностика и начато лечение.
Электрокардиография — это важный метод диагностики инфаркта миокарда. ЭКГ записывает врач или фельдшер скорой помощи, приехавшей к вам по вызову, а затем, в случае госпитализации, повторяют в больнице. ЭКГ измеряет электрическую активность вашего сердца. Каждый раз, когда сердце сокращается, оно вырабатывает слабые электрические импульсы. Аппарат для снятия электрокардиограммы записывает эти импульсы на бумагу, позволяя врачу увидеть, насколько хорошо функционирует ваше сердце.
ЭКГ — безболезненный метод, занимающий не более 5 минут. Во время процедуры электроды (плоские металлические диски) прислоняют к вашим рукам, ногам и грудной клетке. Провода от электродов идут к аппарату ЭКГ, записывающему электрические импульсы. Существует две причины, по которым проведение ЭКГ так важно:
Диагностика вида инфаркта миокарда
Тип инфаркта миокарда можно определить с помощью такого показателя электрокардиограммы как сегмент ST. Сегмент ST — характеризует состояние сердечной мышцы и уровень её повреждения. Чем выше сегмент ST, тем больше вероятный объем повреждения.
Острый коронарный синдром (ОКС) возникает при нарушении коронарного кровообращения (кровотока в сердечной мышце). Инфаркт миокарда — это один из видов острого коронарного синдрома. Существует три основных вида ОКС:
Инфаркт миокарда с подъемом сегмента ST (ИМП ST) — это самый серьезный вид инфаркта миокарда. При этом виде инфаркта миокарда продолжительное нарушение поступления крови вследствие полной закупорки коронарной артерии может привести к повреждению обширной области сердца. ИМП ST — это то, о чем в первую очередь подумают люди, когда они услышат об инфаркте миокарда.
Инфаркт миокарда без подъема сегмента ST (ИМБП ST) может быть менее тяжелым по сравнению с ИМП ST, так как поступление крови к сердцу заблокировано лишь частично. В результате, поврежденной оказывается меньшая область сердца.
Нестабильная стенокардия — это вид острого коронарного синдрома, при котором тоже нарушается кровоснабжение сердца, но необратимое повреждение миокарда (некроз) развиться не успевает. Нестабильная стенокардия может в любой момент перейти в инфаркт миокарда, поэтому рассматривается как неотложное медицинское состояние. При нестабильной стенокардии сердечная мышца сохраняет свою функцию.
Другие виды обследования
Для оценки состояния вашего сердца и проверки наличия возможных осложнений могут быть использованы дополнительные виды обследования. Тем не менее, так как инфаркт миокарда — это неотложное состояние, дополнительные виды обследования обычно проводятся тогда, когда первоначальное лечение уже началось и ваше состояние стабилизировалось.
Анализ крови. Повреждение сердца в результате инфаркта вызывает повышение в крови уровня особых белков — ферментов. Ферменты — это специфические белковые соединения, регулирующие химические процессы, происходящие в вашем организме.
При подозрении на инфаркт миокарда у вас возьмут анализ крови и оценят уровень ферментов — кардиомаркеров, которые выделяются в кровь при повреждении миокарда. Уровень белков будут измерять повторно, в течении нескольких дней. Это позволит оценить степень повреждения сердца и проследить за эффектом от лечения.
Рентген грудной клетки может оказаться полезным, если диагноз инфаркт миокарда остается под вопросом, и имеются другие возможные причины ваших симптомов, например, скоплением воздуха между стенкой грудной клетки и легкими (пневмоторакс). Рентген грудной клетки также позволяет провести диагностику осложнений инфаркта миокарда, таких как скопление жидкости в легких (отек легких).
Эхокардиография — вид ультразвукового обследования, использующего звуковые волны для построения изображения тканей и сосудов сердца. Данный метод может использоваться, чтобы точно установить, какие области сердца были повреждены и как эти повреждения повлияли на работу сердца.
Ангиография коронарных артерий помогает найти место закупорки или сужения коронарных артерий, если оно имеется. Во время процедуры в кровяной сосуд предплечья или бедра вводится тонкая трубка, или катетер. Катетер направляется в коронарные артерии под контролем рентгеновских лучей.
Специальная жидкость — контрастное вещество, поступает через катетер. Эта жидкость хорошо различима на рентгеновских снимках. Анализ того, как эта жидкость проходит по сосудам, снабжающим сердце кровью, помогает выявить все закупоренные или суженные участки сосудов. Коронароангиографию часто проводят непосредственно перед хирургической операцией, потому что ее результаты помогают верно спланировать действия хирурга.
Лечение инфаркта миокарда
Инфаркт миокардаявляется неотложным медицинским состоянием. Позвоните по телефону скорой помощи — 03 со стационарного телефона, 112 или 911 — с мобильного, если вы подозреваете, что у вас или кого-то другого инфаркт миокарда.
До приезда скорой помощи вы можете принять аспирин, если у вас нет на него аллергии. Аспирин разжижает кровь и помогает восстановить поступление крови к сердцу. Чаще аспирин выпускается в таблетках по 500 мг. Примите половину таблетки (250 мг), разжевав ее перед проглатыванием.
Лечение инфаркта миокарда зависит от степени его тяжести. Имеется два основных метода лечения самой тяжелой формы инфаркта — инфаркта миокарда с подъемом сегмента ST (ИМП ST):
Ангиопластика или тромболизис?
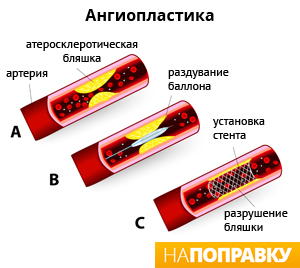
Тем не менее, ангиопластика коронарных артерий — это очень сложный вид хирургического лечения, для проведения которого необходимы квалифицированные специалисты и особое оборудование. Как правило, ангиопластика проводится на базе центров сердечно-сосудистой хирургии (кардиохирургии), которые есть далеко не во всех больницах. Если нет возможности доставить пациента с инфарктом в такую больницу в течение 150 минут, в качестве альтернативы используют тромболизис.
Если результаты ЭКГ показывают, что у вас «менее серьезный» вид инфаркта — инфаркт миокарда без подъема сегмента ST (ИМБП ST) или нестабильная стенокардия, тогда обычно рекомендуются препараты, понижающие свертываемость крови, включая аспирин.
В некоторых случаях, при инфаркте миокарда без подъема сегмента ST или нестабильной стенокардии после первоначального лечения такими препаратами может быть рекомендовано дальнейшее лечение с помощью коронарной ангиопластики или аортокоронарного шунтирования (смотрите ниже).
Коронарная ангиопластика. Во время коронарной ангиопластики в крупную артерию в паху или на руке вводится тонкая трубка, или катетер с раздувающимся баллоном на конце. До места сужения коронарной артерии катетер проводится под контролем рентгеновских лучей. На месте сужения сосуда баллон раздувается, расширяя просвет артерии. Внутрь сосуда обычно устанавливается стент — гибкая металлическая сетка, не дающая артерии сузиться.
Тромболизис — это внутривенное введение лекарственного препарата, называемого тромболитиком. Цель тромболизиса — это разрушение фибрина. Фибрин — плотный белок, который формирует кровяной сгусток, создавая своего рода сетку волокон — основу тромба.
Для лечения инфаркта миокарда используются тромболитики: ретеплазу, альтеплазу и стрептокиназу. Также вам может быть прописана комбинация препаратов, разжижающих кровь, таких как аспирин в низких дозах, гепарин, фондапаринукс, эноксапарин, клопидогрел, прасугрел или тикагрелор, для профилактики повторного образования тромбов.
Если у вас аллергия на аспирин, могут быть использованы такие альтернативы как клопидогрел, прасугрел или тикагрелор. Также вам могут прописать дополнительные препараты — ингибиторы гликопротеина IIb/IIIa, в случае если считается, что имеется повышенный риск повторного инфаркта в ближайшем будущем. Ингибиторы гликопротеина IIb/IIIa не разрушают тромбы,, но предотвращают их рост. Таким образом, они являются методом профилактики повторных сердечных приступов.
Аортокоронарное шунтирование
Иногда техническая возможность проведения коронарной ангиопластики отсутствует из-за особой анатомии ваших артерий. Это может быть в случае, если количество суженых или закупоренных сосудов слишком велико или, если имеется много ответвлений от ваших артерий, которые также закупорены.
Альтернативой ангиопластике в подобной ситуации является проведение аортокоронарного шунтирования (АКШ). Для проведения АКШ выделяют отрезок кровеносного сосуда из другой части тела, обычно из ноги или грудной клетки, для использования в качестве шунта (трансплантанта). Шунты устанавливают вместо закупоренных или суженных артерий. Хирург присоединяет новый кровяной сосуд выше и ниже заменяемого участка артерии.
Осложнения инфаркта миокарда
Потенциальные осложнения, возникающие в результате инфаркта миокарда могут широко варьировать от легких до угрожающих жизни. Многие люди внезапно умирают от осложнений инфаркта миокарда, не успев добраться до больницы.
Мелкоочаговый инфаркт миокарда редко сопровождается осложнениями (однако, также являющийся очень тяжелым состоянием). Крупноочаговый инфаркт миокарда связан с высоким риском осложнений и требует серьезного лечения.
Осложнения инфаркта миокарда могут быть опасными для жизни, это:
Аритмия — это нарушение ритма сердечных сокращений: учащение (тахикардия), урежение (брадикардия) или неритмичное сердцебиение (например, мерцательная аритмия).
Повреждённые во время инфаркта мышцы сердца неправильно проводят электрические импульсы, которые необходимы для правильной работы сердца, что становится причиной аритмии. Некоторые виды аритмии, например, тахикардия, — относительно безопасны и вызывают такие симптомы как:
Другие виды аритмии могут угрожать вашей жизни:
Опасные для жизни виды аритмии являются одной из основных причин смерти в течение 24 часов после инфаркта. Однако, выживаемость пациентов с аритмией значительно повысилась с изобретением автоматического наружного дефибриллятора (АНД) — переносного электронного устройства, посылающего электрические разряды к сердцу и восстанавливающего нормальный ритм сокращений.
Обычно легкие аритмии проходят под действием лекарственных препаратов, например, бета-блокаторов. При более тяжелых аритмиях, вызывающих повторяющиеся и продолжительные симптомы, может потребоваться имплантация электрокардиостимулятора (пейсмейкера).
Электрокардиостимулятор — это электронный прибор для регуляции сердечного ритма. Его имплантируют в грудную клетку во время хирургической операции.
При сердечной недостаточности сердце неспособно эффективно прокачивать кровь по всему организму. Она может развиться после инфаркта миокарда, если мышцы сердца значительно повреждены. Обычно она затрагивает левую половину сердца (левый желудочек). Основные симптомы сердечной недостаточности:
Кардиогенный шок похож на сердечную недостаточность, но является более тяжелым осложнением инфаркта миокарда. Он развивается внезапно, в тех случаях, когда повреждённое сердце не способно эффективно нагнетать кровь в сосуды и снабжать ею жизненно важные органы.
Основные симптомы кардиогенного шока:
Кардиогенный шок лечат с помощью вазопрессоров. Это тип лекарств, которые сокращают сосуды, что приводит к повышению кровяного давления и улучшению циркуляции крови. Кроме того, могут использоваться препараты, разжижающие кровь и облегчающие её перекачивание по организму.
Когда состояние больного кардиогенным шоком стабилизировано, может понадобиться хирургическая операция для улучшения насосной функции сердца. Один из вариантов — имплантировать маленький аппарат — насос, это называется внутриаортальной баллонной контрпульсацией. Такая операция помогает сердцу нагнетать кровь в сосуды.
Другой вариант лечения — проведение аортокоронарного шунтирования (установка шунта из сосуда, взятого из другой части вашего тела, для обхода закупоренного участка).
Разрыв сердца — это тяжелое и относительно распространенное осложнение инфаркта миокарда, возникающее приблизительно в одном из десяти случаев. Разрыв сердца происходит, когда разрываются мышцы, перегородки или клапаны сердца. Разрыв может произойти, если сердце значительно повреждено во время инфаркта миокарда. Обычно он случается в период от одного до пяти дней после инфаркта миокарда.
Симптомы такие же, как и при кардиогенном шоке. Обычно для устранения полученного повреждения необходима операция на открытом сердце. Медицинский прогноз для пациентов с разрывом сердца неблагоприятен и предположительно половина людей умирает в течение пяти дней после того, как они перенесли разрыв сердца.
Реабилитация после инфаркта
Большинство людей могут вернуться на работу после перенесенного инфаркта миокарда, но сроки реабилитации зависят от индивидуальных особенностей организма, состояния сердца и характера работы, которую вы выполняете. Некоторым требуется всего лишь две недели, чтобы вернуться на работу. Другим людям на восстановление понадобится несколько месяцев. Очень важно не форсировать реабилитацию, а восстанавливать силы постепенно.
Во время реабилитации вам будут оказывать помощь разные медицинские работники, в том числе:
Эти специалисты окажут вам лечебную и психологическую поддержку, чтобы обеспечить правильную организацию и безопасность процесса восстановления. Реабилитация начинается уже в больнице, где за вашим состоянием будут внимательно наблюдать и смогут оценить, в чем вы будете нуждаться в дальнейшем. После выписки вы можете продолжить процесс восстановления в домашних условиях. Существует две важные цели реабилитационного процесса:
Сердечная реабилитация
Программа сердечной реабилитации начинается в больнице. Врач, занимающийся вашей реабилитацией, подробно расскажет вам о:
При возвращении домой обычно рекомендуют отдыхать и выполнять только легкие упражнения, такие как подъем и спуск по лестнице два-три раза в день или короткая прогулка. В течение нескольких недель, изо дня в день, постепенно увеличивайте уровень своей нагрузки. То, как быстро вы сможете увеличивать уровень нагрузки, будет зависеть от состояния сердца и общего состояния вашего здоровья. Врач может дать вам разъяснения по предлагаемой программе повышения уровня вашей активности.
Лечащий врач в поликлинике может назначить вам курс лечебной физкультуры. Это комплекс специальных физических упражнений, которые регулярно выполняются под контролем врача-физиотерапевта. Лечебная физкультура является важной частью реабилитации и помогает восстановить работу сердца.
Виды упражнений могут быть разными в зависимости от конкретной программы, но они должны быть в основном аэробными. Аэробные упражнения разработаны для усиления сердечных мышц, улучшения кровообращения и уменьшения кровяного давления. Примерами аэробных упражнений являются занятия на велотренажере, ходьба на беговой дорожке, плавание.
Возвращение на работу
Большинство людей могут вернуться к работе после инфаркта миокарда, но как быстро — будет зависеть от состояния здоровья и вашего сердца, а также характера работы, которую вы выполняете. Если работа не связана с тяжелой нагрузкой, например, работа в офисе, вы, возможно, будете способны вернуться на работу всего через две недели.
Однако, если ваша работа требует применения физической силы, или ваше сердце было значительно повреждено, то может пройти несколько месяцев, прежде чем вы вернетесь на работу. Более конкретный трудовой прогноз вам даст лечащий врач.
Секс после инфаркта
Согласно зарубежным исследованиям, занятия сексом не будут представлять угрозы вашему здоровью, как только вы сможете без боли и одышки подниматься на второй этаж по лестнице. Обычно такого состояния можно достичь примерно через 4 недели после инфаркта миокарда. Тогда занятия сексом не повысят риск нового инфаркта. Прочитайте подробнее о сексе после инфаркта миокарда.
Приблизительно у одного из трех мужчин, перенесших инфаркт миокарда, имеется нарушение потенции, которое может создавать трудности для занятий сексом. Чаще всего это является результатом чувства тревоги и эмоционального стресса, связанных с перенесенным инфарктом миокарда. Реже нарушение потенции возникает как побочный эффект приема бета-блокаторов.
Если вы испытываете нарушение потенции, обратитесь к врачу, который порекомендует вам подходящее лечение. Например, вам могут прописать препарат, стимулирующий приток крови к половому члену и облегчающий возникновение эрекции.
Вождение автомобиля после инфаркта
Весьма рекомендуется воздержаться от вождения автомобиля в течение как минимум 4 недель после инфаркта миокарда. После этого вы можете сесть за руль, если только у вас не будет других заболеваний или осложнений, при которых противопоказано вождение автомобиля.
Депрессия после инфаркта
Инфаркт является пугающим и травмирующим событием, после которого часто появляется чувство тревоги. У многих людей перенесенный эмоциональный стресс вызывает подавленное состояние и уныние в первые недели после выписки. Если состояние депрессии не проходит, обратитесь к своему врачу, возможно вам потребуется дополнительное лечение, чтобы избавиться от нервного напряжения. Депрессия ухудшает процесс восстановления после инфаркта.
Снижение риска повторного инфаркта миокарда
Снижение риска повторного инфаркта миокарда включает в себя коррекцию образа жизни и долгосрочное лечение различными препаратами.
Рекомендуется съедать от двух до четырех порций жирной рыбы в неделю. Жирная рыба содержит жирную кислоту омега-3. Омега-3 способствует снижению уровня холестерина в крови. Источники омега-3 кислот:
Вместо рыбы врач может порекомендовать вам пищевые добавки или лекарственные препараты, содержащие омега-3 кислоты. Никогда не принимайте пищевые добавки, не проконсультировавшись со своим лечащим врачом. Некоторые добавки, такие как бета-каротин, могут быть потенциально вредными для вашего организма.
Также вам рекомендуется придерживаться средиземноморской диеты: есть больше хлеба, фруктов, овощей, рыбы, и меньше мяса. Замените сливочное масло и сыр на продукты, содержащие в своей основе растительное масло, например, оливковое масло.
Если вы курите, вам строго рекомендуется бросить курить как можно скорее.
Если вы принимаете алкоголь, не превышайте рекомендованных дневных норм потребления. Мужчинам рекомендуется не употреблять более 2-4 порций алкоголя в день регулярно, а женщинам — более 2-3. Под регулярным употреблением понимается каждый день или большую часть дней недели. 1 порция алкоголя примерно соответствует рюмке водки, половине бокала вина или половине кружки пива.
Регулярное превышение рекомендованных норм потребления алкоголя приведет к повышению у вас кровяного давления и уровня холестерина, следовательно и риска повторного инфаркта миокарда. Избегайте пьянства (потребления более трех порций алкоголя в течение одного-двух часов). Это вызывает резкое и значительное повышение кровяного давления, что может оказаться опасным.
В исследованиях доказано, что люди, злоупотребляющие алкоголем после инфаркта в 2 раза чаще умирают от повторного инфаркта или инсульта. Если человек, перенёсший инфаркт бросил пить, риск смерти снижается.
Людям с лишним весом или ожирением рекомендуется похудеть и поддерживать вес в норме с помощью низкокалорийной диеты и физических упражнений.
Как только вы полностью восстановитесь после инфаркта (смотрите выше в разделе о сердечной реабилитации, сколько времени это обычно занимает), вам будут необходимы регулярные физические нагрузки. Взрослым следует тратить на аэробную нагрузку умеренной интенсивности (например, катание на велосипеде или быструю ходьбу) не менее 150 минут (2,5 часа) каждую неделю.
Уровень нагрузки должен быть таковым, чтобы вы слегка запыхались. Если вам трудно довести уровень своей нагрузки до 150 минут в неделю, начните с комфортного для вас уровня нагрузки (например, 5-10 минут легких упражнений в день). По мере улучшения физической формы вы сможете повысить интенсивность своих занятий до должного уровня.
Лекарственная профилактика инфаркта миокарда
В настоящее время для сокращения риска инфаркта миокарда широко применяются четыре вида лекарственных средств:
Ингибиторы АПФ часто используются для снижения кровяного давления. Ингибиторы АПФ уменьшают активность гормона, влияющего на давление. В результате происходит расширение сосудов, уменьшается количество жидкости в организме и снижается давление.
Ингибиторы АПФ противопоказаны людям с некоторыми заболеваниями почек, поэтому врач может назначить вам анализы крови и мочи, чтобы убедиться в отсутствии противопоказаний. При длительном приёме иАПФ, анализы крови и мочи нужно повторять ежегодно. Возможные побочные эффекты ингибиторов АПФ:
Наиболее стойким эффектом является кашель, остальные нежелательные реакции обычно проходят за считанные дни. При приеме ингибиторов АПФ совместно с другими лекарственными препаратами, включая безрецептурные препараты, могут возникнуть непредсказуемые побочные эффекты.
Таким образом, не принимайте никаких препаратов в комбинации с назначенными ингибиторами ИПФ, не проконсультировавшись с врачом. Обычно рекомендуется начать прием ингибиторов АПФ сразу же после инфаркта и, в большинстве случаев, продолжать прием этих препаратов всю жизнь. В случае индивидуальной непереносимости ингибиторов АПФ, может быть предписан альтернативный вид препаратов — блокаторы ангиотензиновых рецепторов.
Антиагреганты и антикоагулянты — это группы препаратов, предназначенные для предупреждения тромбообразования. Они действуют, снижая «липкость» тромбоцитов и разрушая основу тромба из нитей фибрина (белка крови). Тромбоциты — это очень маленькие клеточные образования в крови, которые способствуют образованию в ней тромбов.
Чаще всего, перенёсшим инфаркт людям, для разжижения крови назначается аспирин (который часто используется в качестве болеутоляющего при других заболеваниях). Вам могут также прописать прием дополнительных антиагрегантов, таких как клопидогрел или тикагрелор. Эти препараты также используются при аллергии на аспирин.
Возможные побочные эффекты:
Аналогично ингибиторам АПФ, лечение антиагрегантами начинается сразу после инфаркта миокарда. Срок, на который назначаются антиагреганты, варьирует от 4 недель до 12 месяцев, и зависит от вида перенесенного вами инфаркта миокарда и остального лечения, которое вы получаете.
Обычно рекомендуется применять аспирин пожизненно. Если вы испытываете причиняющие вам беспокойство побочные эффекты аспирина, проконсультируйтесь со своим врачом, но не прекращайте прием аспирина, так как резкая отмена препарата повышает риск развития повторного инфаркта миокарда.
Иногда вам также могут прописать прием варфарина. Обычно его выписывают в случае нерегулярного сердечного ритма (мерцательной аритмии) или тяжелого повреждения сердца.
Обширные кровотечения — это самый опасный побочный эффект от приема варфарина. Немедленно обратитесь к врачу и срочно сдайте анализ крови, если вы испытываете какие-либо из следующих побочных эффектов:
Если вы принимаете препараты от тромбообразования, вызовите скорую помощь, если:
Бета-блокаторы — это вид препаратов, применяемых для защиты сердца от дальнейшего повреждения после инфаркта миокарда. Они способствуют расслаблению сердечных мышц, в результате чего сердце бьется медленнее и снижается кровяное давление, что приводит к снижению нагрузки на сердце.
Обычно рекомендуется начать применение бета-блокаторов после стабилизации вашего состояния и продолжать прием бессрочно. Довольно распространенные побочные эффекты бета-блокаторов включают:
Менее распространенные побочные эффекты включают:
Бета-блокаторы могут также взаимодействовать с другими лекарствами, вызывая негативные побочные эффекты. Поэтому проконсультируйтесь с врачом или фармацевтов перед приемом других препаратов, включая безрецептурные препараты, одновременно с бета-блокаторами.
Статины — это группа препаратов, которые снижают уровень холестерина в крови. Статины назначают, чтобы предупредить закупорку артерий холестериновыми бляшками и снизить риск повторного инфаркта.
Статины блокируют действие в печени фермента, называемого ГМГ-КоА-редуктаза, который задействован в выработке холестерина. Статины иногда имеют незначительные побочные эффекты, в том числе:
Иногда статины могут вызвать мышечные боли, слабость и повышенную чувствительность. Обратитесь к врачу, если вы испытываете такие симптомы, возможно, вам требуется коррекция дозы препаратов. Как правило, статины рекомендуется принимать бессрочно.
Профилактика инфаркта миокарда
Коррекция образа жизни — это самый эффективный способ предупредить инфаркт миокарда (или возникновение повторного инфаркта миокарда).
Для предупреждения инфаркта миокарда (также как и инсульта) следует соблюдать три основных правила:
Потребление нездоровой пищи с высоким содержанием жиров усиливает атеросклероз (уплотнение стенок артерий) и повышает риск инфаркта миокарда. Продолжение потребления жирных продуктов приведет к росту атеросклеротических бляшек на стенках артерий, потому что жирная пища содержит холестерин. Выделяют два основных вида холестерина:
Имеется также два вида жиров, насыщенные и ненасыщенные. Избегайте продуктов, содержащих много насыщенных жиров, поскольку они увеличивают уровень плохого холестерина в крови. Продукты, богатые насыщенными жирами:
Употребление в пищу небольшого количества ненасыщенных жиров повышает уровень хорошего холестерина и уменьшает отложения на стенках артерий. Среди продуктов с высоким содержанием ненасыщенных жиров:
Кроме того, сократите количество соли в вашем рационе и ешьте много фруктов и овощей. Соль повышает артериальное давление. Чем больше соли вы употребляете в пищу, тем выше ваше кровяное давление. Вы должны стремиться съедать менее 6 грамм соли в день, что примерно равно одной чайной ложке.
Доказано, что потреблении пищи с низким содержанием жиров (в том числе пищи с высоким содержанием клетчатки, такой как цельнозерновой рис, хлеб и макароны, а также — фруктов и овощей) способствует снижению кровяного давления. Вам надо стремиться каждый день съедать пять порций фруктов и овощей по 80 грамм.
Регулярное потребление алкоголя выше допустимых норм приведет к повышению кровяного давления. Помимо этого, алкоголь является высококалорийным продуктом, поэтому регулярно употребляя алкоголь, вы наберете лишний вес. Наличие лишнего веса также приводит к повышению уровня кровяного давления.
Физические упражнения и активный образ жизни приводят к снижению кровяного давление за счет поддержания сердца и кровеносных сосудов в хорошем состоянии. Регулярные физические упражнения могут также помочь вам снизить вес, что также поможет снизить кровяное давление.
Рекомендуются упражнения с невысокой нагрузкой, такие как ходьба, плавание или езда на велосипеде или велотренажере. Занятия с более интенсивной нагрузкой, такие как игра в футбол или теннис, могут навредить вашему здоровью. Посоветуйтесь с лечащим врачом, перед тем, как приступить к занятиям любым видом спорта.
К какому врачу обратиться после инфаркта?
С помощью сервиса НаПоправку выберите хорошего кардиолога. Этот врач занимается лечением и реабилитацией больных после инфаркта. Если вам требуется плановая госпитализация, найдите хорошую кардиологическую клинику на нашем сайте.
Ишемическая болезнь сердца: терапия инфаркта и стенокардии
обзор ЛС, использующихся при лечении стенокардии, инфаркта миокарда
1.Предынфарктный — учащение и усиление приступов стенокардии (от нескольких часов до нескольких недель);
2.Острейший — от момента появления ишемии до развития миокарда (от 30 минут до 2 часов);
3.Острый — от образования некроза до ферментативного расплавления некротизированной мышечной ткани (от 2 часов до 10 суток);
4.Подострый — начальные процессы организации рубца, развитие грануляционной ткани на месте некротической (до 5 недель);
5.Постинфарктный — адаптация миокарда к новым условиям функционирования (до 6 месяцев).
ОИМ имеет различные варианты течения (см.таблицу 1).
Общая летальность при ОИМ составляет 30–35 %. Большая часть смертей приходится на первые двое суток, поэтому основные лечебные мероприятия проводят именно в этот период в специализированных отделениях интенсивной терапии.
В последние несколько лет достаточно широко в клиническую практику вошел новый термин — острый коронарный синдром (ОКС), промежуточный диагноз между нестабильной стенокардией и ОИМ. ОКС — предварительный диагноз, позволяющий врачу определить неотложные лечебные и организационные мероприятия. Выделяют ОКС с подъемом и без подъема сегмента ST при ЭКГ исследовании.
Инфаркт миокарда: клиника, диагностика, лечение
Острый инфаркт миокарда (ИМ) — клинический синдром, возникающий в результате повреждения сердечной мышцы при несоответствии между потребностью миокарда в кислороде и возможностью его доставки. При этом возникает некроз кардиомиоцитов в зоне поврежде
Острый инфаркт миокарда (ИМ) — клинический синдром, возникающий в результате повреждения сердечной мышцы при несоответствии между потребностью миокарда в кислороде и возможностью его доставки. При этом возникает некроз кардиомиоцитов в зоне повреждения одновременно, что отличает данный процесс от других форм миокардиального повреждения.
Этилогия и патофизиология. Факторами риска являются гиперхолестеринемия, сахарный диабет, артериальная гипертензия, малоподвижный образ жизни, семейный анамнез, табакокурение и другие.
Основным в процессе принято считать атеросклероз коронарных артерий, включающий в себя разрыв или деэндотелизацию атеросклеротической бляшки, тромбоз, вазоконстрикцию, часто на фоне воспаления. Важную роль также играет нарушение свертываемости крови, уменьшение коронарного кровотока и недостаточная его компенсация коллатеральным кровообращением, нарушение обмена простагландинов, функции калликреин-кининовой системы, иммунологические нарушения. Независимо от причины, ИМ характеризуется наступлением необратимой гибели клеток миокарда. Зона инфаркта, которая изначально охватывает субэндокардиальный слой миокарда, начинает распространяться на более глубокие слои, направляясь к эпикарду. Даже при тотальной окклюзии коронарного сосуда, снабжающего зону инфаркта, наблюдается некоторый антеградный кровоток, что может позволить сохраниться в зоне поражения жизнеспособным кардиомиоцитам, поэтому считается, что существует временной период до 6–12 часов, когда возможно повлиять на размер зоны некроза путем увеличения кровотока в поврежденном участке.
У более 50% больных тотальная коронарная окклюзия развивается в области ранее существующей атеросклеротической бляшки. Тотальная окклюзия чаще развивается в проксимальных сегментах крупных артерий, что впоследствии на ЭКГ проявляется патологическими зубцами Q. При отсутствии тотальной тромботической окклюзии коронарного сосуда чаще возникает Q-необразующий ИМ (по ЭКГ).
Развитие ИМ сопровождается нарушением систолической и диастолической функции и ремоделированием левого желудочка (ЛЖ). Нарушение систолической функции обусловлено тем, что некротизированный участок миокарда не участвует в сокращении сердца, тогда как в неповрежденной ближайшей зоне имеется компенсаторная гиперкинезия. Диастолическая дисфункция связана со снижением эластичности и растяжимости миокарда. В результате диастола ЛЖ неполноценна, миокард недостаточно релаксируется, повышается конечное диастолическое давление. Данные нарушения возникают при поражении менее 10% массы миокарда левого желудочка. Ремоделирование ЛЖ обусловлено истончением миокарда и снижением тонуса миокарда в области некроза, компенсаторным расширением полости ЛЖ, развитием состояния гибернации в периинфарктной зоне, активизацией циркулирующей и местной ренин-ангиотензиновой и симпатоадреналовой системы, гиперпродукцией эндотелина. Ремоделирование сердца после ИМ может носить адаптивный и дезадаптивный характер. Адаптивный характер проявляется в уменьшении размеров ЛЖ, поддержании удовлетворительной сократительной способности ЛЖ, стабилизации миокардиального стресса. Сохраняется гемодинамически выгодная форма ЛЖ, поддерживается удовлетворительная сократительная способность ЛЖ и стабилизация миокардиального стресса. Дезадаптивный характер процесса ремоделирования ЛЖ заключается в прогрессированной дилатации ЛЖ с переходом к гемодинамически невыгодной сферической форме сердца, что приводит к развитию рестриктивного типа диастолического наполнения ЛЖ. Этот тип дисфункции является мощным предиктором сердечно-сосудистой смертности.
Клиническая картина. Проявления ИМ имеют множество вариантов. От бессимптомного течения и эпизодического дискомфорта в области сердца до развернутого болевого приступа с различными нарушениями ритма и проводимости. Чаще описываются ощущения «давления», «тяжести» и «жжения» в центральной части грудной клетки с иррадиацией в плечевой пояс, руку, челюсть, эпигастральную область. Больной беспокоен, прикладывает руку к грудине (симптом Левайна). Для пожилого больного с множественной сопутствующей патологией ИМ часто проявляется в признаках сердечной недостаточности (нарастание одышки, отеков, появление сердцебиения, атипичность стенокардитической боли).
Физикальные исследования варьируют от полной нормы до выраженных отклонений (расширение верхушечного толчка, появление 3 и 4 тона, ослабление тонов, появление влажных хрипов в легких и др.). Ни один из этих признаков не подтверждает, но и не исключает наличие ИМ. Диагностика ИМ основана на выявлении маркеров повреждения сердечной мышцы.
Маркеры повреждения кардиомиоцитов. В настоящее время наиболее убедительным маркером является тропонин. Он имеет более высокую чувствительность к ИМ, чем МВ-фракции креатинфосфокиназы (МВ-КФК). Современные методы анализа позволяют наделять тропонин практически абсолютной кардиоспецифичностью, но, учитывая это качество, тропонин может быть повышен и при неишемическом повреждении миокарда. Поэтому только комплексный подход (клинические данные, эхокардиографические и др.) позволяют доказать острую ишемию миокарда и развитие ИМ. Уровень тропонина повышается в первые 4–6 часов и держится повышенным в пределах 8–12 дней. Длительность выявления маркера позволяет диагностировать ИМ в поздние сроки, без исследования лактатдегидрогеназы (ЛДГ). Для более точного ориентирования в сроках ИМ целесообразно исследовать «короткоживущие» маркеры некроза. «Ранним» маркером некроза миокарда является повышение активности МВ-КФК. Активность МВ-КФК повышается в первые часы повреждения миокарда и превышает нормальные показатели между 6–12 часами болезни, достигая пика к 18–24 часу заболевания, а к 48 часу показатели маркера возвращаются к нормальным. Необходимо помнить о других причинах повышения МВ-КФК: повреждение скелетной мускулатуры, хронические миопатии, почечная недостаточность, гипотиреоз за счет снижения клиренса, а также то, что соотношение МВ-КФК и общей КФК не считается критерием диагностики ИМ.
Электрокардиография. Наиболее значимыми признаками ИМ являются изменения сегмента ST (подъем с выпуклостью вверх). При нижней локализации ИМ следует фиксировать ЭКГ на правой половине грудной клетки в отведениях V3R или V4R. Для огибающей окклюзии характерны изменения в так называемых задних отведениях (V7–V9), чаще в виде появления патологического зубца Q. При этом вышеуказанные признаки нельзя считать 100% обязательными. В большинстве случаев типичные изменения ЭКГ отсутствуют, что может быть обусловлено наличием нарушения внутрижелудочковой проводимости или изолированной депрессией сегмента ST.
Эхокардиография (ЭхоКГ). Диагностическая точность ЭхоКГ зависит от качества получаемого изображения. Отсутствие патологии при ЭхоКГ не может служить основанием для исключения ишемической болезни сердца или некроза сердечной мышцы. ЭхоКГ не позволяет отличить свежий очаг асинергии от зоны постинфарктного кардиосклероза. Исследование незаменимо для исключения осложнений ИМ и сопутствующей патологии.
Лечение. Для достижения максимального положительного результата лечение должно начинаться как можно раньше, начиная с первого часа заболевания, что позволит иметь значительно лучший прогноз. Как можно раньше должна быть проведена реперфузионная терапия путем тромболизиса или первичной ангиопластики. Доказано, что рано начатое лечение приводит к существенному снижению смертности при всех формах ИМ. Первичная ангиопластика на инфаркт-ассоциированной артерии в первый час заболевания позволяет восстановить естественную перфузию миокарда в зоне повреждения Чем позже проведена реперфузия, тем выше смертность. В настоящее время доступность ангиопластики остается невысокой.
В 1996 году Европейским обществом кардиологов и Американской коллегией предложены рекомендации по лечению больных острым инфарктом миокарда, состоящие из ряда принципиальных позиций.
Большим достижением в обезболивании некупирующегося ангинозного приступа стала эпидуральная блокада. Широкое применение затруднено из-за развития специфических осложнений и наличия технических трудностей при ее выполнении.
Применение ингаляционных средств наркоза в настоящее время используется редко, только по определенным показаниям (проведение кардиоверсии, искусственная вентиляция легких, выполнение болезненных манипуляций).
2. Восстановление кровотока (реканализация) по инфаркт-ассоциированной артерии существенно уменьшает размеры зоны поражения миокарда. Эффективность тромболитической терапии (ТЛТ) прямо зависит от времени начала лечения. Желательно, чтобы время обращения за помощью и начало ТЛТ не превышало 90 минут. Показанием к ТЛТ считается наличие смещения сегмента ST вверх от изоэлектрической линии более 0,1 мВ не менее чем в двух смежных отведениях ЭКГ или блокады ножки пучка Гиса у больных, поступивших в первые 12 часов после появления симптомов ИМ. Однако при сохранении боли и указанных выше изменений на ЭКГ считается целесообразным проведение ТЛТ и в более поздние сроки (вплоть до 24 часов после начала заболевания). Под блокадой ножки пучка Гиса подразумевается вновь возникшая или предположительно вновь возникшая полная блокада левой ножки пучка Гиса, затрудняющая интерпретацию ЭКГ. Наиболее доступным с доказанной эффективностью считается препарат стрептокиназа. Препарат активизирует плазминоген непрямым способом. Препарат не следует назначать пациентам, которые перенесли ранее тяжелую стрептококковую инфекцию или которым данный препарат вводился в течение последних 5–6 месяцев. Быстрое введение стрептокиназы может вызывать резкое снижение артериального давления. Рекомендуемая доза стрептокиназы составляет 1500000 ЕД в течение часа.
Урокиназа является прямым активатором плазминогена, имеет короткий период полувыведения, вызывает более быстрое восстановление проходимости инфаркт-ассоциированной артерии, чем эквивалентная доза стрептокиназы. Рекомендуемая доза 2000000 ЕД болюсно и 3000000 ЕД в/в капельно в течение 90 минут.
Тканевой активатор плазминогена (ТАП) считается фибрин-специфичным активатором плазминогена. По сравнению со стрептокиназой и урокиназой ТАП способствует более раннему восстановлению проходимости инфаркт-ассоциированной артерии, возможно, именно этот фактор обусловлено снижает смертность при его использовании. Режим назначения ТАП 100 мг в/в в течение 3 часов: 10 мг болюсно, далее 50 мг в течение первого часа и еще 40 мг в течение последующих 2 часов. При массе тела пациента менее 65 кг назначается препарат в дозе 1,25 мг/кг (за 3 часа), при этом 10% от общей дозы должны быть введены в виде первичного болюса. Применение более высоких доз (больше 100 мг) ТАП ассоциировано с риском внутричерепного кровотечения.
С течением времени были синтезированы и другие ТАП с несколько иным молекулярным строением: ретеплаза, тенектеплаза.
Противопоказания к применению ТЛТ определяются риском возникновения серьезных кровотечений, в особенности внутричерепных. Существуют абсолютные противопоказания: активное внутреннее кровотечение, любой сосудистый эпизод в течение последних 2 месяцев, новообразование центральной нервной системы, тяжелая травма, хирургическое вмешательство в течение 3 месяцев, беременность, тяжелая артериальная гипертензия. К относительным противопоказаниям относят подозрение на расслоение аорты, сердечно-сосудистую реанимацию в течение 2 недель, злокачественные новообразования, язвенную болезнь в стадии обострения, нарушения гемостаза, системные заболевания, эндокардит и ряд других заболеваний. Следует индивидуально решать вопрос по проведению ТЛТ у больных старшего возраста, в связи с наличием большого количества сопутствующей патологии.
Сопутствующее лечение
Аспирин необходимо назначать всем больным с подозрением на ИМ, при отсутствии противопоказаний. Его положительное влияние на выживаемость, частоту реинфарктов и ишемических инсультов продемонстрировано как при проведении ТЛТ, так и в ее отсутствие. При сочетании Аспирина с ТЛТ эффективность последней значительно возрастает. Доказано, что Аспирин ингибирует агрегацию тромбоцитов и ускоряет фибринолиз. Поэтому всем больным ИМ следует назначать Аспирин немедленно в дозе 160–325 мг (разжевывать).
Гепарин при внутривенном введении совместно с активаторами плазминогена способствует ускорению проходимости инфаркт-ассоциированной артерии, особенно при использовании ТАП. При использовании стрептокиназы внутривенная инфузия гепарина не является столь необходимой. Стандартная схема гепаринтерапии предлагает первоначальное болюсное введение 5000 ЕД нефракционированного гепарина, а затем инфузию со скоростью 1000 ЕД/час, пока активированное частичное тромбопластиновое время (АЧТВ) не увеличится в 1,5–2 раза по сравнению с исходным. В связи с трудностями точной титрации данной формы гепарина, рекомендуется использовать низкомолекулярные гепарины (НМГ) с расчетом дозы на кг веса пациента.
β-блокаторы снижают риск повторного ИМ у больных, пролеченных тромболитической терапией. β-блокаторы снижают риск смерти, модулируют нейрогуморальные и гормональные системы, замедляют ремоделирование сердечно-сосудистой системы, вызывают нормализацию функционального состояния тромбоцитов. Рекомендуется применять препараты данной группы в первые 12 часов после начала ИМ у всех больных, не имеющих противопоказаний (бронхиальная астма, сахарный диабет, брадикардия, гипотония). Используются суточные доза метопролола, пропранолола.
Ингибиторы ангиотензин-превращающего фермента (иАПФ). Сердечная недостаточность (СН) является частым осложнением и одной из основных причин смертности в острый период ИМ и в отдаленные сроки после его развития. Возникновение и прогрессирование СН у больных, перенесших ИМ, связано с процессом ремоделирования миокарда ЛЖ, патофизиологический процесс которого запускается уже в первые часы заболевания. Повреждение клеточных и структурных компонентов миокарда и расширение зоны инфаркта предрасполагает к дилатации и дисфункции ЛЖ, которая определяет высокую смертность больных ИМ. Изменения в структуре ЛЖ в первые 3 дня, а в последующем пролиферация фибробластов и синтез коллагена приводят к прогрессированию ремоделирования сердца. Активным участником этих процессов являетcя ангиотензин II, вызывающий спазм коронарных артерий, увеличение работы сердца, повышение потребления миокардом кислорода, а в последующем пролиферацию фибробластов. Таким образом, появились теоретические основания для использования иАПФ при ИМ. Ингибиторы АПФ, уменьшая синтез ангиотензина II, вызывающего вазоконстрикцию как артериального, так и венозного сосудистого русла, способствуют нормализации центральной и периферической гемодинамики, тем самым предотвращают развитие кардиогенного шока, снижая нагрузку на сердце существенно, подавляют процесс ремоделирования ЛЖ. Однако применение иАПФ в остром периоде ИМ ограничивается риском снижения системного артериального давления (АД). В связи с этим, несмотря на доказанную эффективность иАПФ, не утратил своей актуальности поиск безопасных препаратов данной группы, пригодных для применения с первых суток ИМ в сочетании с ТЛТ. К препаратам, не вызывающим резкого снижения АД, относится лизиноприл (Диротон). Эффективность Диротона как средства, препятствующего ремоделированию ЛЖ и развитию СН, а также уменьшающего риск смерти после развития ИМ, показана в условиях эксперимента и клиники. В отличие от большинства иАПФ Диротон не нуждается в биотрансформации в печени для образования активных метаболитов, а также не содержит сульфгидрофильной группы, являющейся причиной ряда побочных эффектов. Отсутствие печеночного метаболизма у Диротона позволяет рекомендовать его больным с патологией печени. Диротон уменьшает риск взаимодействия с другими лекарственными препаратами, которые подвергаются биотрансформации в печени. Исследование эффективности Диротона у пациентов с ИМ и в раннем постинфарктном периоде показало снижение смертности, уменьшение СН. Диротон доказал свою эффективность также у больных пожилого возраста.
Антиаритмические препараты. Обычно речь идет о применении Лидокаина, который ранее назначался всем с профилактической целью купирования желудочковых нарушений ритма. Впоследствии оказалось, что реканализация инфаркт-ассоциированной артерии уменьшает вероятность развития таких аритмий, и доказано, что рутинное применение препарата способствует увеличению смертности. Лидокаин следует назначать только при желудочковой тахикардии или фибрилляции желудочков.
Магния сульфат (магнезия сульфат) может применяется при наличии лабораторно доказанной гипомагнемии или других специфических показаний (например, полиморфная желудочковая тахикардия).
Н. В. Журавлева, кандидат медицинских наук
О. А. Поворинская
РНИИ геронтологии, Москва