Как вылечить ревматоидный артрит
Как вылечить ревматоидный артрит
Ревматоидный артрит причины, симптомы, методы лечения и профилактики
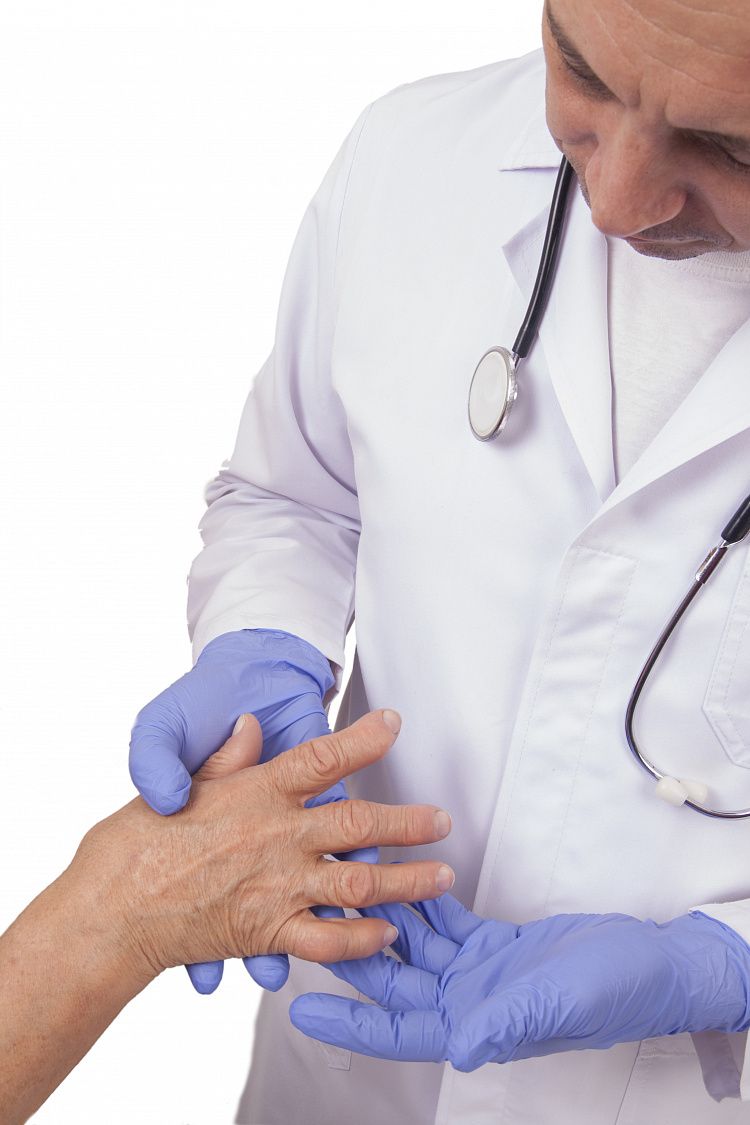
Ревматоидный артрит — заболевание системного характера. Сопровождается поражением соединительной ткани, чаще развивается в суставах. Прогрессирует деформация, формируются анкилозы. Двигательная активность сустава уменьшается и полностью утрачивается. Для предотвращения инвалидности требуется записаться на прием к травматологу и пройти лечение.
Клиники ЦМРТ более 10 лет специализируются на консервативном лечении ревматоидного артрита. Центры оснащены современным экспертным оборудованием для точной диагностики, эффективного лечения и реабилитации. Опытные специалисты применяют индивидуальный подход, составляя комплекс лечебных мероприятий, направленных на борьбу с патологией на всех стадиях.
Запишитесь на прием к ортопеду-травматологу
Поставить точный диагноз, определив причины и характер заболевания, назначить эффективное лечение может только квалифицированный врач на очном приеме.
Запишитесь к врачу через онлайн-форму на сайте или по телефону
Ортопед • Хирург • Флеболог
стаж 9 лет
Ортопед • Травматолог
стаж 8 лет
Ортопед • Травматолог
стаж 41 год
Адреса лечебных клиник в Москве
Симптомы ревматоидного артрита
Выделяют следующие признаки болезни:
Тяжелые стадии характеризуются следующими признаками:
Статью проверил
Дата публикации: 24 Марта 2021 года
Дата проверки: 24 Марта 2021 года
Дата обновления: 19 Августа 2022 года
Содержание статьи
Причины
Точные причины прогрессирования ревматоидного артрита установить не удается. Однако установлены факторы, повышающие вероятность возникновения недуга:
Заболевание чаще диагностируется у представительниц женского пола, объясняется гормональными перестройками организма.
Стадии развития ревматоидного артрита
Выделяют 4 стадии прогрессирования заболевания.
Разновидности
Выделяют несколько видов ревматоидного артрита:
Серопозитивный ревматоидный артрит. Характеризуется присутствием в кровеносной системе ревматоидного фактора. Организмом вещество воспринимается, как антиген.
Серонегативный ревматоидный артрит. Отличается отсутствием ревматоидного фактора. Характеризуется неяркой симптоматикой. Болезнь развивается медленнее, в сравнении с серопозитивной формой, прогноз благоприятнее.
Ювенальный ревматоидный артрит. Диагностируется в возрасте до 16 лет. Характеризуется поражением сердечной, почечной, дыхательной системы. Остальные симптомы аналогичные. Болезнь отличается агрессивных характером, быстро развивается на крупные суставные ткани.
Системный ревматоидный артрит. Отличается наличием внесуставной симптоматики. Характеризуется поражением почечной и сердечной системы. Встречается реже остальных.
Диагностика
Чтобы поставить диагноз, врач оценивает клинические признаки заболевания. Ревматоидный артрит подтверждают, если:
Чтобы подтвердить диагноз, пациенту назначают лабораторные анализы:
Дополнительно назначают биопсию поражённых суставов и исследуют синовиальную жидкость. Из инструментальной диагностики назначают рентген: исследование позволяет оценить степень деформации суставов.
Ревматоидный артрит: новые подходы к старой проблеме
Р. М. Балабанова, профессор, доктор медицинских наук, руководитель отдела изучения и коррекции аутоиммунных нарушений ГУ Института ревматологии РАМН
Е. В. Шекшина, кандидат медицинских наук, младший научный сотрудник
Хроническое системное иммуноопосредованное воспалительное заболевание с преимущественным поражением периферических (синовиальных) суставов по типу симметричного эрозивнодеструктивного полиартрита, сопровождающегося пролиферацией синовиоцитов и ангиогенезом (что сближает его с онкологическими заболеваниями), называют РЕВМАТОИДНЫМ АРТРИТОМ (РА).
Распространенность РА среди взрослого населения различных климато-географичеcких зон – в среднем 0,6–1,3%. Ежегодная заболеваемость за последние годы сохраняется на высоком уровне – 0,02%. Для РА характерен половой диморфизм: женщины болеют в 3–4 раза чаще, чем мужчины. Во время беременности нередко развивается ремиссия. У женщин пик заболеваемости РА приходится на 35–55 лет, у мужчин – на 40–60 лет.
Этиология и патогенез заболевания
До настоящего времени причина возникновения РА не уточнена. В его развитии равнозначна роль как генетических, так и внешнесредовых факторов, среди которых предполагается участие инфекции, иммунизации, питания, переливания крови, курения, УФО-облучения и др.
О генетической предрасположенности к заболеванию свидетельствует его высокая агрегация в семьях больных РА. Заболеваемость им в раннем возрастезначительно чаще встречается в семьях, где были родственники с РА. Роль генетической предрасположенности к этому заболеванию подтверждена и его более высокой частотой среди монозиготных близнецов (12–32%) по сравнению с дизиготными (3,5–9%).
Из эндогенных факторов в развитии РА определенную роль играют половые гормоны, что подтверждается большой частотой заболевания среди женщин, а также положительным влиянием беременности на течение РА и его обострением после родоразрешения или ее прерывания. У женщин, больных РА, выявлен дефицит андрогенов – тестостерона и дегидроэпиандростерона, у мужчин также низок уровень тестостерона.
Участие половых гормонов в развитии РА подтверждает влияние экзогенных эстрогенов (оральных контрацептивов), снижающих риск развития РА.
Среди внешнесредовых факторов возникновения этого заболевания в первую очередь предполагается роль инфекции. Классических эпидемиологических доказательств инфекционной этиологии РА нет, но это не исключает ее участия в генетически предрасположенном организме, о чем свидетельствуют результаты исследований на животных.
Специфический (инфекционный) триггер РА не установлен, но есть много претендентов: микоплазма, парвовирус В19, цитомегаловирус (ЦМВ), вирус простого герпеса 6-го типа, Эпстайна – Барр вирус (ЭБВ). Один из механизмов развития так называемых аутоиммунных заболеваний, к которым относится и РА, – “молекулярная мимикрия”. Микробы и вирусы могут содержать белковые структуры (аминокислотные последовательности), сходные с белками хозяина. Иммунный ответ на патоген с целью его элиминации может “изменить направление”, в результате чего возникает перекрестная реакция с собственными антигенами, структурно схожими с чужеродными.
В сыворотке больных РА содержатся в повышенных титрах антитела к латентному или репликативному антигену ЭБВ. Тлимфоциты периферической крови больных РА не способны контролировать ЭБВ-позитивные В-лимфобластоподобные линии, и это объясняет частоту ЭБВ-инфицированных периферических В-лимфоцитов при РА в сравнении с контролем. Длительная экспозиция одного или нескольких вирусов, что нередко имеет место при РА, может играть триггерную роль в инициации иммунного воспаления, так как антигены вируса не только перекрестно реагируют с антигенами хозяина, но и выполняют адъювантный эффект.
Патогенез
ЭФ РА(?) > Трансформация IgG в АутоАГ > IgM,A,G-ревматоидные факторы + АутоАГ = ЦИК > синовиальная ткань > повышение активности медиаторов воспаления, проницаемости микрососудов, хемотаксис лейкоцитов, фагоцитоз ЦИК > повреждение лизосом лейкоцитов и макрофагов > высвобождение лизосомальных ферментов > повреждение клеточных структур > образование новых АутоАГ > цепная реакция
Неизвестный этиологический фактор ревматоидного артрита вызывает первичную иммунную реакцию в виде образования антител в виде IgG. По неизвестной причине они трансформируются и превращаются в аутоантигены, которые в условиях иммунодефицита по Тсупрессорам инициируют выработку В-лимфоцитами антител групп Ig M, A, G (ревматоидные факторы). Они образуют с аутоантигеном циркулирующие иммунные комплексы (ЦИК), оседающие главным образом в синовиальной оболочке суставов и вызывающие повышение активности медиаторов воспаления, нарушение микроциркуляции, активацию хемотаксиса лейкоцитов.
В процессе фагоцитоза повреждаются лизосомы нейтрофилов и макрофагов, высвобождаются лизосомальные ферменты, повреждающие клеточные структуры. Образуются новые аутоантигены, новые аутоантитела, и патологический процесс приобретает характер цепной реакции. На какое-то время она может затихать, но затем вновь возобновляется под влиянием специфических и неспецифических факторов.
Исход воспалительного процесса характеризуется редукцией, а затем и прекращением миграции клеток в воспаленную ткань с последующим повышением апоптоза клеток и восстановлением тканей. Постоянная активация моноцитов и макрофагов приводит к неспособности их блокировать эти процессы, что способствует переходу острого воспаления в хроническое.
Важную роль в патогенезе РА играют простагландины.
Другой механизм, участвующий в воспалении и деструкции хряща, – усиление новообразования сосудов. Этот ангиогенез в синовии связывают с действием провоспалительных цитокинов, который приводит к усилению проникновения воспалительных клеток в ткани сустава, что обеспечивает поступление питательных веществ, необходимых для нормального функционирования воспалительных и пролиферирующих клеток. Важная роль отводится нейтрофилам, увеличение количества которых в синовиальной жидкости приводит к гиперпродукции хемоаттрактантов. Дегрануляция нейтрофилов сопровождается высвобождением протеиназ, реактивных форм кислорода, продуктов метаболизма арахидоновой кислоты.
Процессы, происходящие в синовии при РА, напоминают локальное злокачественное новообразование. Масса вновь образованных клеток и соединительной ткани во много раз превышает массу нормальной синовиальной оболочки. Образующийся при РА паннус обладает способностью к инвазии и деструкции хряща, субхондральной кости и связочного аппарата. Синовиоциты больных РА обладают фенотипическими свойствами трансформированных опухолевых клеток. В синовиальной жидкости и тканях обнаружено увеличение уровня факторов роста – тромбоцитарного и фибробластного. Сходство ревматоидного синовита и локализованного злокачественного новообразования проявляется и на молекулярном уровне. Ряд цитокинов обладает способностью вызвать длительно сохраняющиеся фенотипические изменения клеток.
Патологический процесс при РА в первую очередь развивается в суставах и околосуставных тканях и имеет свои особенности в зависимости от стадии заболевания.
Синовит выявляется рано, даже в клинически неизмененном суставе. Нарушения в синовиальной мембране обусловлены иммунологическими процессами. В начальных стадиях процесса строма скудно инфильтрирована лимфоцитами, плазматическими клетками, лаброцитами (тучными клетками) и макрофагами. Т-лимфоциты имеют морфологические и иммунологические характеристики антигензависимых клеток. В-лимфоциты как предшественники плазматических клеток и сами плазматические клетки синтезируют иммуноглобулины in situ.
На ранней стадии имеет место пролиферация кроющих синовиоцитов типа В, имеющих морфологическое сходство с фибробластами. Клетки формируют несколько слоев с очаговым “частоколом”. Встречаются капилляриты и продуктивные васкулиты. На этой стадии выявляется преобладание экссудативных и альтернативных процессов в синовиальной мембране – отек, полнокровие и очаги фибриноидных изменений.
Для развернутой стадии характерна картина хронического пролиферативного процесса. При этом отмечаются выраженная гиперплазия и гипертрофия ворсинок. Становится более очевидной пролиферация кроющих синовиоцитов с формированием нескольких слоев и наличием гигантских клеток.
В морфогенезе ревматоидного синовита важное место занимает поражение сосудов микроциркуляторного русла – васкулиты и ангиоматоз. В стенках сосудов выявляются отложения иммуноглобулинов. На этой стадии в синовиальной мембране могут формироваться ревматоидные узелки, а в случае присоединения амилоидоза – амилоидные массы.
Особенность позднего периода – выраженный ангиоматоз, сочетающийся с продуктивными васкулитами и тромбозами. Волнообразное течение болезни находит отражение и в морфологии синовиальной мембраны.
Под ней в перихондральной ее части формируется синовиальный паннус – сосудистая и фиброзная ткань. В процессе развития он врастает в хрящ, разрушая его.
Специфический морфологический признак при РА – ревматоидный узелок. Его можно увидеть в различных органах и тканях, но наиболее частая локализация – кожа и синовиальная мембрана. Узелок представлен очагом фибриноидного некроза, окруженного палисадообразно расположенными макрофагами, лимфоцитами и плазматическими клетками. Нередко в нем видны гигантские многоядерные клетки. С помощью моноклональных антител удалось подтвердить участие иммунопатологических реакций в развитии ревматоидных узелков.
Особое место в прогрессировании ревматоидного процесса занимают васкулиты, которые выявляютсяво всех органах, но не имеют специфических морфологических признаков. Исследование сосудов кожи у больных РА с признаками кожного васкулита показало, что изменения микроциркуляторного русла носят генерализованный характер.
При этом заболевании обнаруживают продуктивные, деструктивные и деструктивно-продуктивные васкулиты. Сосуды поражены генерализованно и полиморфно – от умеренной пролиферации эндотелия и инфильтрации наружной оболочки до некроза средней оболочки стенки сосуда. Преобладают поражения сосудов мелкого калибра – кожи, скелетной мускулатуры, внутренних органов. Наиболее типичны продуктивные васкулиты и тромбоваскулиты, реже встречается панваскулит типа узелкового полиартериита с очаговым или тотальным некрозом средней оболочки.
Изменения в сосудах крупного и среднего калибра могут быть обусловлены поражением vasa vasorum и развивающейся в связи с этим ишемией сосудистой стенки. Иногда наблюдается картина аортита с последующим склерозом и расширением устья аорты.
Поражение серозных оболочек проявляется чаще всего сухим плевритом с незначительным фибринозным выпотом, что ведет к образованию спаек. В легочной ткани процесс развивается по типу хронической межуточной пневмонии, очагового или диффузного пневмосклероза с образованием ревматоидных узелков.
Поражение почек обусловлено гломерулонефритом (мембранозным или мембранозно-пролиферативным), нефроангиосклерозом, хроническим интерстициальным нефритом, ангиитом. Часто нефропатия обусловлена отложением амилоидных масс. В латентной стадии амилоид обнаруживают периваскулярно в ткани пирамид и некоторых артериолах клубочков, в нефротической стадии в большинстве клубочков, стенках сосудов, пирамидах отложения амилоида массивные.
В желудочно-кишечном тракте выявляют признаки гастрита, энтерита, колита, которые достаточно часто обусловлены иммунокомплексным процессом, что подтверждается обнаружением в подслизистой основе иммуноглобулинов, фибрина. Наиболее тяжелые изменения желудочно-кишечного тракта связаны с отложением амилоидных масс в слизистой оболочке, стенке сосудов с развитием лимфоидно-плазмоцитарной инфильтрации, атрофией слизистой оболочки и подслизистой основы.
В биоптатах печени отмечают изменения в портальной соединительной ткани с продуктивными васкулитами, лимфоидно-гистиоцитарной или плазмоцитарной инфильтрацией, склеротические изменения, а также дистрофию, некроз гепатоцитов. При амилоидном поражении отложения амилоида наблюдают в ретикулярной строме долек печени по ходу внутридольковых капилляров, в стенке сосудов. Амилоид нередко замещает большую часть паренхимы.
В селезенке выявляют гиперплазию и плазматизацию лимфоидной ткани, пролиферацию эндотелия синусов, отложения белковых преципитатов.
При РА поражаются различные отделы нервной системы и ее элементы (сосуды, соединительная ткань, нервные волокна). Периферическая система в основном поражена за счет vasa nervorum. В соединительной ткани нервной системы выявляют фибриноидные изменения, лимфоидные и плазмоклеточные инфильтраты, а также отложения амилоида, микронекрозы.
Клиническая картина РА
Суставной синдром – ведущий в клинической картине РА. Начало заболевания чаще всего подострое (55–70%), как правило, спровоцированное перенесенной острой инфекцией или обострением хронической, охлаждением, травмой, стрессовой ситуацией.
Развитию артрита за несколько недель или месяцев предшествует продромальный период, признаки которого – усталость, похудание, периодически возникающая боль в суставах (часто на изменение атмосферного давления), снижение аппетита, повышенная потливость, субфебрильная температура, небольшая анемия, увеличение СОЭ.
По данным В. А. Насоновой и М. Г. Астапенко (1989), в продромальном периоде у 32% больных развивается утренняя скованность, особенно в суставах конечностей, которая при активном движении проходит. Среди причин возникновения этого симптома – нарушение нормального ритма выработки гормонов надпочечниками со смещением на более поздний период суток, а также аккумуляция цитокинов в отечной жидкости воспаленных суставов во время сна.
В начальном периоде РА у 1/3 больных отмечают артралгии, усиливающиеся при движении, у 2/3 – симметричный артрит мелких суставов кистей и стоп. Боль и скованность наибольшие в утренние часы, постепенно убывающие к вечеру. Интенсивность и длительность этих проявлений коррелирует с прогрессивностью болезни, сохраняясь при выраженной активности до обеда, а у отдельных больных проходит только к вечеру.
У 8–15% страдающих РА заболевание начинается остро в течение нескольких дней. При этом пациент может указать время и движение, спровоцировавшее боль. Артралгии могут сопровождаться такой же резкой болью в мышцах, длительной утренней скованностью, лихорадкой, что приводит больного к обездвиженности.
В 15–20% случаев РА начинается незаметно с медленным прогрессированием артрита без повышения температуры тела, ограничения движений.
Поражение суставов в ранней стадии РА может быть нестойким и самопроизвольно исчезать на несколько месяцев и даже лет. Стойкий полиартрит с прогрессированием воспалительного процесса отмечен у 70% больных. Первыми, как правило, при РА вовлекаются вторые-третьи пястно-фаланговые, проксимальные межфаланговые и суставы запястья, реже – плюсне-фаланговые. Затем по частоте поражения следуют коленные, локтевые, голеностопные. Позднее вовлечение крупных суставов некоторые авторы объясняют более высоким соотношением поверхности синовиальной мембраны к суставному хрящу. По нашим данным, у 87% заболевших все началось с поражения мелких суставов кистей, у 9,7% – крупных (коленные, плечевые). Стойкий прогрессирующий полиартрит имел место у 43%, у 57% больных он носил волнообразное течение с периодами ремиссии. У 20,4% пациентов развился ишемический некроз головок бедренных костей.
Некоторые суставы в дебюте болезни остаются интактными (“суставы исключения”) – дистальные межфаланговые, первый пястнофаланговый сустав большого пальца кисти, проксимальный межфаланговый мизинца.
Ранняя фаза РА характеризуется преобладанием экссудативных явлений симметрично пораженных суставов кистей с наличием выпота, определяемого по симптому флюктуации, воспалительному отеку периартикулярных тканей, резкой болезненности при пальпации, положительному симптому сжатиякисти.
Над мелкими суставами может быть слегка гиперемирована кожа, а над крупными – повышенная температура. Вследствие воспаления суставных тканей и рефлекторного спазма мышц резко ограничивается движение в пораженных суставах, что ведет к развитию мышечной атрофии. Артрит сопровождается воспалительным поражением влагалищ сухожилий, чаще разгибателей, реже – сгибателей кисти и стопы.
У 15–20% заболевших в первый год болезни может произойти спонтанное затухание симптомов артрита и развиться ремиссия болезни. Но у большей части больных процесс принимает прогрессирующий характер с переходом в экссудативно-пролиферативную фазу.
Наряду с общими симптомами (слабость, астения, похудание, ухудшение сна, аппетита, субфебрильная температура) прогрессирует суставной синдром. Преобладание пролиферативных процессов в суставных тканях приводит к их утолщению, стойкой плотной или пружинящей припухлости периартикулярных тканей, что вызывает изменение конфигурации суставов, в первую очередь мелких – кистей и стоп, запястья, лучезапястных, коленных, локтевых. Плечевые, тазобедренные суставы поражаются при РА редко, еще реже вовлекаются суставы позвоночника.
Классификация РА
Первая была предложена А. И. Нестеровым в 1961 году, после чего неоднократно уточнялась в связи с появлением новых данных о клинике и вариантах течения РА. Последний был одобрен на I Всероссийском конгрессе ревматологов в 2003 году.
Выделено 2 клинико-иммунологических варианта: серопозитивный и серонегативный РА. Полиартрит как основное проявление этого заболевания включает в себя оба варианта. Внесуставные проявления в основном отнесены к серопозитивному варианту и представлены лишь там, где ревматоидная принадлежность не вызывает сомнений. Сюда же отнесена особая форма РА – синдром Фелти. Серонегативный вариант РА имеет свои клинико-лабораторные особенности, к нему отнесен и синдром Стилла взрослых.
Характеризуя активность заболевания, выделяют 4 степени: 0 – ремиссия, 1 – низкая, 2 – средняя, 3 – высокая. Определение активности базируется на наиболее лабильных клинических и лабораторных признаках:
Определение СРБ в нашей стране не стандартизировано, поэтому мы взяли за исходное значение норму, а далее – ее 2–3- и более кратное превышение.
Зарубежными ревматологами предложено для оценки активности РА применять DAS (счет активности болезни).
По МКБ Х принята такая классификация РА: Воспалительные полиартропатии
Ревматоидная болезнь легкого
Лекарства последнего поколения для лечения ревматоидного артрита
Лекарства последнего поколения, разработанные по современным технологиям фармацевтики, облегчают страдания человека, снижают риск дальнейших осложнений. Что же такое ревматоидный артрит, каковы причины, симптомы, какие методы лечения возможны?
Что собой представляет болезнь?
Это системная неврологическая патология, связанная с воспалением хрящевой ткани в суставном сочленении. Причинно-следственные связи клинического состояния различны. Однако все они обусловлены проблемами в работе защитной иммунной организации человека. Наиболее вероятный провоцирующий фактор – инфекционное поражение.
Реакция на воспалительный процесс инфицирования – это медленное разрушение соединительных тканей, связанное с их дегенеративно-дистрофической реорганизацией.
Если вовремя не провести адекватное лечение, то следующим этапом дегенерации станет деформация суставной поверхности. Это влечет значительное ограничение подвижности костно-суставных сегментов ОДА нижней конечности.
Возможные причины возникновения неврологической патологии:
При ревматоидном артрите симптомы заболевания без медикаментозной терапии могут сохраняться длительное время и выражаться в следующих проявлениях:
Такие симптоматические признаки возможны при любых воспалительных реакциях. Поэтому перед тем как проводить лечение ревматоидного артрита, необходимо идентифицировать диагностические признаки заболевания.
Человеку необходимо обратиться к врачу, который на основе собранного анамнеза, диагностического лабораторного исследования (УЗИ, рентген, МРТ, КТ), других уточняющих процедур диагностики определит степень выраженности неврологической патологии. Он установит причинно-следственную связь воспалительной реакции, назначит медикаментозное лечение.
При лечении обязательна двигательная активность суставных сегментов. С этой целью консультирующий специалист назначает физиотерапевтические процедуры, лечебный массаж, гимнастические упражнения, мануальные методы воздействия на суставную патологию.
Подробное видео о природе заболевания:
Системная медикаментозная терапия
Лечебная терапевтическая реакция предусматривает применение пяти групп фармакологических лекарственных средств.
| № п/п | Фармакологические комбинации | Назначение лекарственных средств |
| 1 | Нестероидные противовоспалительные (НПВП) | Устранение симптомов |
| 2 | Базисные противоревматические группы | Уменьшение воспалительной активности, смягчение костно-суставной деструкции |
| 3 | Глюкокортикостероиды | Нормализация обменных функций, восстановление активного кровообращения |
| 4 | Биологические средства лечения | Устранение ферментативного разрушения близлежащих тканевых соединений суставной поверхности |
| 5 | Миорелаксанты | Для расслабления скелетной мускулатуры при значительном снижении двигательной активности |
Нестероидные противовоспалительные
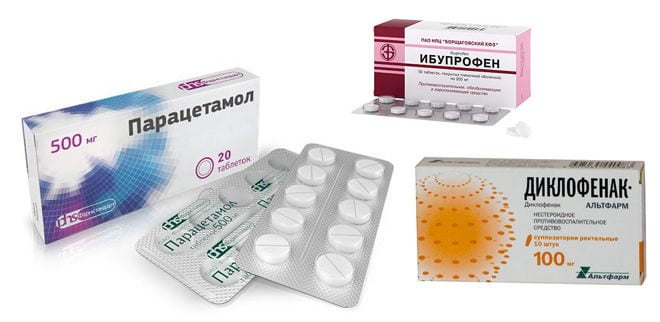
При обезболивании и устранении воспалительной реакции врачи назначают наиболее известные препараты нестероидной противовоспалительной активности – Диклофенак®, Ибупрофен® или Парацетамол®.
Однако существуют более действенные средства лечения из нестероидной противовоспалительной группы с наименьшим эффектом побочного воздействия, связанным с органами мочеполовой, желудочно-кишечной систем.
Среди нестероидных противовоспалительных комбинаций выделяется Дексалгин® 25 немецкого производителя – компании BERLIN-CHEMIE/MENARINI PHARMA GmbH. Выпускается в виде таблеток с активным действующим веществом декскетопрофеном, отпускаемый в аптечной сети только по рецептурному назначению врача. Благодаря активному компоненту и вспомогательным веществам (кукурузный крахмал, микрокристаллическая целлюлоза и т. д.) нестероидная лекарственная форма оказывает анальгезирующее, противовоспалительное и жаропонижающее действие.
После приема фармацевтического средства основные симптомы ревматоидного артрита — боль, отечность, покраснение – исчезают через 30-40 минут. Однако длительность обезболивания составляет 4-5 часов – и наступает новый виток болевых приступов. Дозировка и курс лечения определяется лечащим специалистом с учетом возрастных, половых, индивидуальных особенностей пациента.
Препарат не назначается беременным женщинам, детям до 12 лет, больным людям с хроническими дыхательными патологиями, почечной и печеночной недостаточностью. Лекарство не предназначено для длительного применения. Курс лечения не должен превышать 5-7 дней.
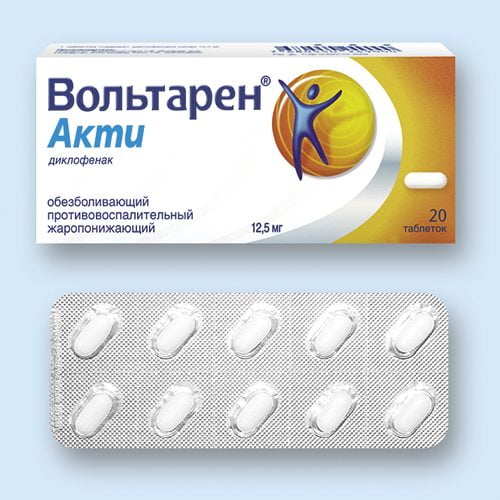
Следующий нестероидный противовоспалительный препарат нового (последнего) поколения – это Вольтарен® акти российского производителя АО «ГлаксоСмитКляйн Хелскер». Лекарство выпускается в виде таблеток белого цвета. Основное действующее вещество – диклофенак натрия.
Вольтарен® акти обладает всеми свойствами фармакологических средств нестероидной противовоспалительной активности – жаропонижающим, болеутоляющим. Лечебный эффект наступает после 15-20 минут, что делает эффективным применение препарата для скорейшего купирования болевого приступа и урегулирования температурного режима. Курс лечения лекарственным средством не должен превышать 5 дней. Противопоказания: язвенная болезнь желудка, дети до 14 лет, почечная, печеночная или сердечная недостаточность. Принимать его не рекомендуют людям с хронической патологией органов дыхания.
Среди новинок фармацевтической промышленности для наружного применения – противовоспалительный анальгезирующий крем Аэртал® испанской фирмы «ALMIRALL S.A.».
Благодаря активному действующему веществу – ацеклофенаку — применение лекарственной формы целесообразно при воспалении в суставе, других костно-мышечных, суставных сегментах опорно-двигательного аппарата.
Исключения – заболевания кожного покрова в месте предполагаемого проведения терапевтических действий, индивидуальная непереносимость фармакологического продукта.
Базисные противоревматические препараты
Среди интересных модифицирующих антиревматических продуктов фармацевтического рынка:
Как и чем лечить болезнь, решает лечащий врач. Данная группа лекарственных препаратов обладает очень медленным терапевтическим эффектом. Рекомендуется применять базисные средства лечения совместно с прочими фармакологическими группами – нестероидными противовоспалительными препаратами, глюкокортикостероидами.
Глюкокортикостероиды
Этот вид фармакологических препаратов представляет собой стероидный гормон, синтезируемый корой надпочечников, обладающий разносторонним физиологическим действием:
Среди назначаемых фармакологических средств последнего поколения наиболее эффективны:
Являясь мощнейшим контринсулярным гормоном, глюкокортикостероиды практически не назначаются пациентам с сахарным диабетом.
Биологические средства лечения
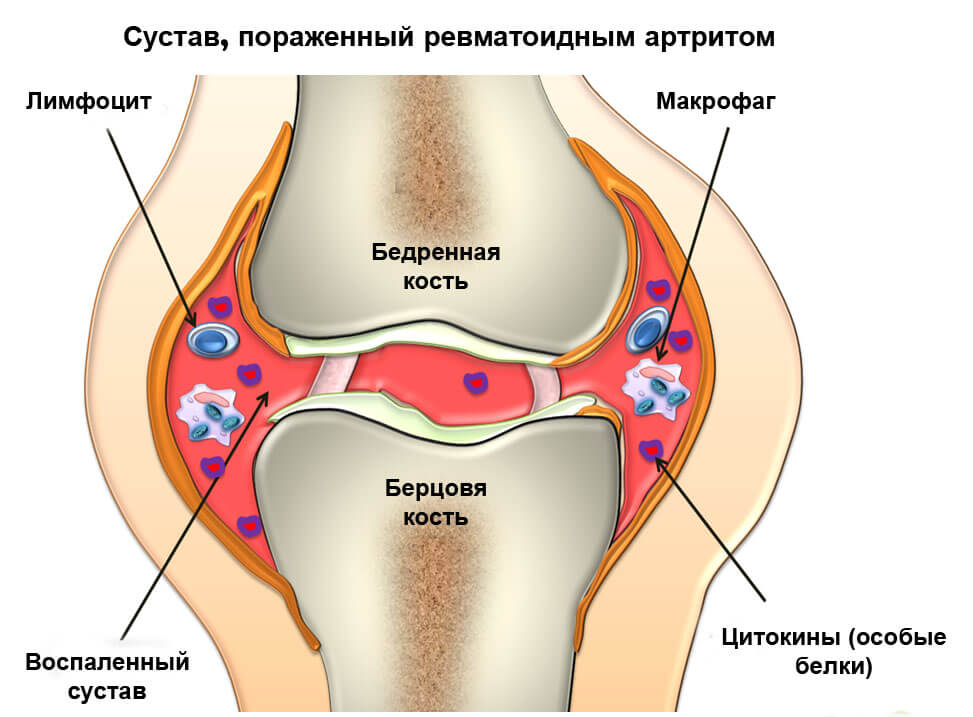
При ревматоидном артрите происходит ферментация синовиальной оболочки в суставной полости, которая приводит к разрушению дисульфидных связок в близлежащих костно-суставных тканях и хрящах. Это влечет каскадную реакцию, усугубляет клиническую симптоматику неврологического заболевания. Организм отвечает воспалительной реакцией, сопровождающейся выработкой цитокинов, наиболее опасен ФНО – фактор некроза опухоли. Такое состояние может обеспечить пациенту значительное снижение подвижной активности суставов и физическую нетрудоспособность.
Поэтому в комплексное лечение вводятся специальные блокаторы (ингибиторы ФНО) или антицитоновые препараты:
Миорелаксанты
Медицинский термин происходит от латинского myorelaxantia, где myo – это мускул, relaxantis – расслабляющий. Цель их назначения – это снижение мышечного тонуса в зоне неврологического повреждения. Классифицируется лекарственная форма следующим образом (смотреть таблицу).
| Деполяризующие миорелаксанты | Не деполяризующие миорелаксанты | ||
| Ультракороткого действия | Короткого действия | Среднего действия | Длительного действия |
| Дитилин® – деполяризующий миорелаксант короткого действия | Мивакрон® – для кратковременного угнетения нервно-мышечной передачи | Тракриум® – лекарственная форма периферического действия конкурентного типа. Основной компонент – атрикурия безилат снижает чувствительность холинорецепторов, обеспечивая невозможность возбуждения и сокращения мышечного волокна | Павулон® – недеполяризующий миорелаксант продолжительной активности, обеспечивающий релаксацию скелетной мускулатуры |
Доклад на тему медикаментозного лечения:
Прогноз
Обязательным условием для скорейшего выздоровления является не только применение медикаментозных фармацевтических комбинаций. В комплексную терапию необходимо включать физиотерапевтические процедуры, специальные упражнения, лечебный массаж, санаторно-курортное оздоровление.
В случае неэффективности перечисленных методов терапии или при прогрессировании болевой симптоматики в костно-суставном сегменте предусмотрено хирургическое вмешательство:
Медицинские эксперты отмечают, что продолжительность жизни пациентов с ревматоидной патологией сокращает жизнь человека в среднем на 5-10 лет.
По лабораторным исследованиям американской Клиники Мэйо (США, Миннесота), проведенным в 2005 году, риск сердечно-сосудистых патологий в 2 раза выше у пациентов, страдающих ревматическими и артрологическими заболеваниями. Эта неутешительная статистика в наибольшей степени объясняется хронической стадией ревматоидного артрита опорно-двигательной системы.Уменьшить риск хронических патологий и увеличить продолжительность жизни поможет назначение биофармацевтических средств лечения. Они активно воздействуют на жизненно важные биологические объекты – кровь, клеточную структуру и соединительные ткани.
Ревматоидный артрит: симптомы, лечение, диагностика
Ревматоидный артрит — хроническое аутоиммунное заболевание. В результате нарушения работы иммунной системы клетки организма начинают воспринимать собственные ткани как чужеродные. Ревматоидный артрит может поразить любые суставы. Чаще всего патология локализуется в суставах запястья, пальцев, пяток или коленей.
Ревматоидный артрит в МКБ 10
Ревматоидный артрит является хроническим системным заболеванием соединительной ткани с преимущественным поражением периферических (синовиальных) суставов по типу деструктивно–эрозивного полиартрита. Серонегативный ревматоидный артрит имеет код по МКБ № М05.8, ревматоидный артрит серонегативный – М06.0. Вероятный ревматоидный артрит в МКБ определён с кодом М05.9, М06.4, М06.9.
Кто страдает от заболевания
До настоящего времени не удалось установить точных причин развития ревматоидного артрита. Существуют теории, согласно которым среди этиологических факторов выделяют генетическую предрасположенность, экологическое воздействие и гормональные нарушения. Согласно статистическим данным женщины в 3 раза чаще страдают от ревматоидного артрита, чем мужчины. Средний возраст дебюта заболевания составля ет 40-60 лет.
Физические симптомы ревматоидного артрита
На начальных стадиях развития ревматоидного артрита могут поражаться суставы пальцев рук, стоп, коленные суставы, лодыжки. По мере прогрессирования патологического процесса увеличивается площадь поражения. Основными клиническими симптомами ревматоидного артрита являются:
Эмоциональные симптомы ревматоидного артрита
Помимо физических симптомов, пациенты с ревматоидным артритом страдают от эмоциональных переживаний. Сопутствующими признаками могут быть:
Эмоциональное напряжение усиливается по мере прогрессирования заболевания. Данное состояния негативно сказывается как на работоспособности, так и на взаимоотношениях в семье. Важно вовремя обратиться за помощью и соблюдать врачебные рекомендации.
Причины и факторы риска РА
Среди основных предрасполагающих факторов к развитию ревматоидного артрита выделяют:
Генетическая предрасположенность
HLA-DR4 — специфический антиген, который выявляется у большинства больных ревматоидным артритом. Его обнаружение не гарантирует, что у человека разовьется заболевание. Тем не менее, наличие антигена повышает риск возникновения ревматоидного артрита.
Факторы окружающей среды и образа жизни
Врачи выделяют предрасполагающие факторы риска, наличие которых повышает риск развития ревматоидного артрита. К ним относятся:
Нарушение гормонального баланса
Имеется связь между гормональным фоном и периодами обострения ревматоидного артрита. Это подтверждает тот факт, что женщины чаще мужчин страдают от данного заболевания.
Инфекции и микробиом
Существует теория о связи инфекционных заболеваний с развитием ревматоидного артрита. Кроме того, прорабатывается предположение о том, что микробиом человека может провоцировать дебют ревматоидного артрита. Микробиом — совокупность всех условно-патогенных микробов, заселяющих человеческий организм. Считается, что их деятельность может негативно сказываться на многих процессах, в том числе на иммунной системе. Несмотря на подобное предположение, точных доказательств, указывающих на связь между инфекциями и ревматоидным артритом, до сих пор не выявлено
Диагностика
Диагностика ревматоидного артрита включает в себя комплексное исследование. Оно состоит из лабораторных и инструментальных методов. Обследование направлено на выяснение локализации патологического процесса и степени его распространенности. В состав диагностических мероприятий входят:
Отек суставов
Синовит — воспалительное состояние, при котором наблюдается отечность сустава, покраснение кожи в области поражения. На фоне патологического процесса повышается температура тела и возникает болевой синдром, усиливающийся при движении. На фоне ревматоидного артрита синовит поражает, как правило, несколько суставов.
Анализ крови
Определить точный перечень лабораторных исследований, который позволит диагностировать ревматоидный артрит, сложно. Врачи выделяют несколько показателей, повышение которых заставляет заподозрить развитие заболевания. Среди них:
Данные исследования крови не являются специфичными. Поэтому для интерпретации полученных результатов необходимо обратиться к врачу.
Визуализирующие методы исследования
Инструментальные методы исследования позволяют определить стадию заболевания, если лабораторные способы диагностики дали недостаточно информации. К основным визуализирующим методам обследования при ревматоидном артрите относятся:
Физический осмотр и история болезни пациента
Диагностика ревматоидного артрита не обходится без физического осмотра пациента и выяснения его истории болезни. Врач внимательно осматривает кожные покровы, изучает подвижность суставов. На консультации необходимо дать ответы на следующие вопросы:
Для уточнения диагноза и определения дальнейшей тактики лечения уточняются сопутствующие заболевания, применяемая терапия. Важен момент выяснения наследственной отягощенности.
Лечение ревматоидного артрита
Для лечения ревматоидного артрита применяется комбинированная терапия. Для этого используются лекарственные средства, диетическое питание, физические упражнения и оперативное вмешательство. Основными задачами оказываемого лечения являются:
Лечение РА лекарственными препаратами
Ревматоидный артрит относится к числу заболеваний, трудно поддающихся лечению. Хроническое течение патологии характеризуется периодическими рецидивами и ремиссиями. Основными задачами медикаментозной терапии являются купирование обострения, уменьшение скорости прогрессирования заболевания. При неэффективности лекарственных средств применяется оперативное вмешательство. Рассмотрим основные группы препаратов, назначаемых при ревматоидном артрите:
Современные подходы к терапии ревматоидного артрита
Лекарственное средство хумира выпускается в стеклянных шприцах, в которых находится одна доза раствора для подкожного введения. Один шприц содержит 40мг основного действующего вещества адалимумаб и вспомогательные ингредиенты:
Раствор лекарственного средства хумира слегка окрашен, опалесцирующий. Препарат оказывает иммунодепрессивное действие. Адалимумаб представляет собой рекомбинантное моноклональное антитело, пептидная последовательность которого идентична lgG1 человека. Он селективно связывается с фактором некроза опухоли, который играет важную роль в развитии патологического воспаления и разрушения суставной ткани, и нейтрализует его биологические функции.
Показания и противопоказания к применению препарата хумира
Ревматологи Юсуповской больницы назначают препарат хумира пациентам, страдающим следующими заболеваниями:
В первых двух случаях хумира применяется в режиме монотерапии или в сочетании с метотрексатом или иными базисными противовоспалительными препаратами. Отзывы при псориазе хорошие.
Противопоказанием к применению лекарственного средства хумира является повышенная чувствительность к адалимумабу или любым вспомогательным компонентам лекарственного средства, инфекционные заболевания, в том числе туберкулёз, беременность и период грудного вскармливания. Препарат не назначают детям и подросткам до 16 лет. С осторожностью препарат при демиелинизирующих заболеваниях. Врачи рекомендуют женщинам репродуктивного возраста избегать зачатия во время лечения хумирой. Если существует необходимость в лечении препаратом хумира женщин, которые кормят грудью, на время всего курса терапии малыша переводят на искусственное вскармливание.
Побочные эффекты препарата хумира
Во время проведения клинических исследований по безопасности применения препарата хумира установлено, что во время лечения лекарственным средством у пациентов очень часто возникали инфекционные заболевания верхних дыхательных путей. Часто развивалась инфекция нижних дыхательных путей, включая бронхит и пневмонию, органов мочевыделительной системы, герпетическая инфекция (включая простой и опоясывающий герпес). При применении препарата хумира у пациентов повышается риск заболевания гриппом, поверхностной грибковой инфекцией, включая поражения кожи и ногтей.
Возможны следующие осложнения со стороны системы кроветворения:
Иногда у пациентов увеличиваются лимфатические узлы. Редко возникают реакции повышенной чувствительности. При применении препарата хумира нечасто развиваются нежелательные реакции со стороны обмена веществ: гиперхолестеринемия, гиперурикемия, снижение аппетита, анорексия, гипергликемия, снижение или повышение массы тела.
У некоторых пациентов возникают реакции со стороны следующих систем организма:
У пациентов во время лечения препаратом хумира может возникнуть сыпь на коже, кожный зуд, выпадение волос. Редко возникают язвы на коже, ангионевротический отёк, шелушение кожи, реакции фотосенсибилизации. Пациентов может беспокоить боль в суставах, мышцах, плечевом поясе и спине. Редко возникают мышечные судороги, бурсит, синовит, тендинит. Со стороны мочеполовой системы возможны следующие нежелательные реакции:
У женщин может нарушиться менструальный цикл. Иногда у пациентов повышается утомляемость, повышается температура тела. Их беспокоит чувство жара, озноб, боль в грудной клетке. Может ухудшаться заживление ран.
Физические упражнения и поддержание здорового веса
Лечение ревматоидного артрита не обходится без нормализации веса. Для этого необходимо изменить образ жизни. Пациентам с диагностированным ревматоидным артритом требуется подобрать нагрузку, которая будет положительно воздействовать на суставы, не перегружая их. Врачебные рекомендации по изменению образа жизни заключаются в следующем:
Диета
Врачи разработали 5 основных правил питания, которых необходимо придерживаться при диагностированном ревматоидном артрите. К ним относятся:
Хирургия при РА
Показанием для выполнения оперативного вмешательства при ревматоидном артрите является неэффективность медикаментозного лечения. Современная хирургия предлагает несколько видов операций, облегчающих состояние пациентов. Вмешательства различаются в зависимости от возраста больного, локализации патологического процесса, а также степени тяжести заболевания. Основными формами операций при ревматоидном артрите являются:
Эндопротезирование
Эндопротезирование считается наиболее эффективным методом лечения пораженных суставов. Суть операции заключается в замене суставных компонентов на имплантаты. Подобным образом оперируются плечевые, тазобедренные, коленные суставы, а также суставы пальцев рук и ног.
Артродез
Артродез — операция, заключающаяся в сращивании суставов. Подобным образом удается увеличить нагрузку, которую выдерживают пораженные суставы. Кроме того, артродез позволяет уменьшить выраженность болевого синдрома.
Синовэктомия
Синовэктомия — оперативное вмешательство, чаще выполняемое на ранних стадиях развития ревматоидного артрита. Данный вид операций проводится на коленных суставах и суставах пальцев. Суть вмешательства заключается в удалении воспаленной синовиальной оболочки. Синовэктомия не способна полностью избавить от заболевания. Однако, после операции отмечается облегчение состояния.
Опытные врачи Юсуповской больницы проводят полный курс диагностики и лечения ревматоидного артрита. Для этого используются современные аппараты, отвечающие требованиям безопасности и качества. Запись на консультацию к врачу производится по телефону.
Ревматоидный артрит
Ревматоидный артрит – тяжелое, с трудом поддающееся лечению заболевание. Причины развития его установлены не полностью, тем не менее, при проведении правильно назначенного комплексного лечения качество жизни пациента может быть вполне удовлетворительным. Но это при условии неукоснительного выполнения больным всех рекомендаций лечащего врача.
Специалисты клиники «Парамита» в Москве имеют большой опыт в лечении ревматоидного артрита.
Что такое ревматоидный артрит
Ревматоидный артрит (РА) – хроническое системное прогрессирующее заболевание, проявляющееся в виде воспаления в основном мелких суставов. Связано оно не с инфекцией, а с поломкой иммунной системы. Поражается соединительная ткань, поэтому данное заболевание называется системным. Патологический процесс часто распространяется и внутренние органы (сердце, сосуды, почки) – это внесуставные проявления болезни.
Всего в мире ревматоидным артритом болеет около 1% населения. Заболеть можно в любом возрасте, но чаще это случается в 35 – 55 лет у женщин и немного позже (в 40 – 60 лет) у мужчин. Ревматоидный артрит у женщины диагностируют в три раза чаще, чем мужчины.
Причины
Точные причины начала данного заболевания не установлены. Но известны основные причинные факторы:
В результате целого комплекса причин клетки синовиальной оболочки начинают выделять воспалительные цитокины – белковые молекулы, инициирующие и поддерживающие воспаление. Развивается длительно протекающий воспалительный процесс, происходит разрушение хрящевой и костной суставной ткани, деформация конечности. Хрящевая ткань заменяется соединительной, появляются костные разрастания, нарушается функция сустава. Очень часто причиной развивающегося аутоиммунного поражения суставов является герпетическая инфекция – вирусы простого герпеса 1, 2 типа, цитомегаловирус, вирус Эпштейна – Барр (вызывает мононуклеоз) и другие возбудители, например, микоплазмы.
Предрасполагающие (запускающие, триггерные) факторы:
Симптомы
Заболевание протекает волнообразно, в виде периодов обострений (рецидивов) и ремиссий.
Как начинается ревматоидный артрит
Начало в большинстве случаев подострое и имеет связь с перенесенной инфекцией, переохлаждением, травмой или нервным перенапряжением, беременностью, родами.
В большинстве случаев при ревматоидном артрите поражается сначала небольшое количество суставов стоп и кистей. На ранней стадии могут также поражаться коленные суставы. Поражения симметричны. При подостром течении первые признаки нарушений появляются через несколько недель, при медленном, хроническом – через несколько месяцев.
Острое начало, высокая активность патологического процесса и системные проявления характерны для ювенильного ревматоидного артрита у детей и подростков. Он может начинаться с высокой температуры, изначального поражения сразу нескольких суставов и признаков поражения внутренних органов.
Симптомы разгара заболевания
Ревматоидный артрит сопровождается признаками общей интоксикации. Это слабость, недомогание, небольшое повышение температуры тела, головные боли. Нарушается аппетит, больной теряет массу тела.
Суставной синдром. Поражаются сначала мелкие суставы кисти (число их увеличивается), а затем и крупные суставы (плечевые, коленные). Они опухают, становятся очень болезненными, постепенно теряют свою функцию, обездвиживаются. Длительное обездвиживание приводит к выраженной атрофии (уменьшению в объеме) мышц. Ревматоидный артрит характеризуется также тем, что поражения разных суставов могут быть неодинаковыми: в одних могут преобладать признаки воспаления (отек), в других – пролиферации (разрастания соединительной ткани с деформацией и нарушением функции).
Появляются подкожные ревматоидные узелки – небольшие, умеренно плотные, безболезненные образования, располагающиеся на поверхности тела, чаще всего на коже локтей.
Поражается периферическая нервная система. Из-за поражения нервов больные ощущают онемение, жжение, зябкость в конечностях.
При ревматоидном васкулите происходит поражение различных мелких и частично средних кровеносных сосудов. Часто это проявляется в виде точечных очагов некроза в области ногтей или безболезненных язв в области голени. Иногда васкулит может проявляться в виде микроинфарктов.
Когда нужно срочно обращаться за медицинской помощью
К врачу следует обращаться при появлении следующих симптомов:
Локализации процесса
При ревматоидном артрите вначале обычно поражаются мелкие суставы кистей, пальцев рук и стоп. Внешний вид верхних х конечностей:
Подробнее про артрит суставов пальцев читайте здесь.
Лечение ревматоидного артрита
Методы лечения ревматоидного артрита: базисная терапия, противовоспалительные средства разных групп, методы физического и механического воздействия на иммунную систему, местное лечение, физиотерапевтическое лечение, диета.
Основным средством лечения ревматоидного артрита считаются так называемые базисные препараты. Поэтому именно с базисных препаратов мы начнем наш разговор о методах лечения артрита. 
Считается, что базисные препараты воздействуют на основание болезни, ее «базис». Применяются эти средства с прицелом на будущее, в расчете на их способность прерывать развитие заболевания. Но нужно иметь в виду, что в отличие от противовоспалительных средств и гормонов, базисные препараты не дают сиюминутного положительного эффекта, то есть они не устраняют симптомов болезни в первые дни и недели их применения. Как правило, базисные препараты способны подействовать не раньше, чем через месяц, — и в этом их существенный недостаток.
Кроме того, практически ни один базисный препарат не способен дать гарантированного стопроцентного результата. То есть притормаживают развитие артрита и со временем дают улучшение многие из базисных препаратов, но насколько выраженным будет это улучшение, не сможет заранее предсказать ни один, даже самый многоопытный ревматолог. Потому правильный подбор базисной терапии во многом зависит не только от опыта врача, но и от его интуиции. Тем не менее свои характерные достоинства и недостатки есть у любого базисного препарата, и о них мы сейчас побеседуем.
Базисная терапия ревматоидного артрита
В настоящее время в качестве базисной терапии используют чаще всего препараты трёх групп: соли золота, антималярийные лекарства, и антимикробный препарат сульфасалазин.
1. Цитостатики (иммунодепрессанты).
Цитостатические препараты, или так называемые иммунодепрессанты (метотрексат, арава, ремикейд, азатиоприн, циклофосфан, хлорбутин, циклоспорин, и другие), были заимствованы ревматологами у онкологов. По мнению большинства современных ревматологов цитостатики — лучшая группа базисных препаратов для лечения не только ревматоидного, но и псориатического артрита.
В онкологии эти препараты применяются для торможения деления клеток, в том числе раковых. Причем онкологическим больным цитостатики назначаются в огромных дозах, что приводит к большому количеству осложнений. В связи с этим и врачи, и больные очень настороженно относятся к применению цитостатиков, опасаясь тяжелых побочных эффектов.
Однако когда речь идет о применении этих препаратов в лечении артрита, опасность явно преувеличивается, ведь в артрологии цитостатики используются в значительно меньших дозах, чем в онкологии. Дозы цитостатиков при лечении артритов примерно в 5-20 раз меньше доз, используемых при лечении опухолей!
Такие небольшие количества иммунодепрессантов редко вызывают побочное действие, а вот терапевтический эффект чаще всего бывает значительным. Использование цитостатиков помогает, как минимум, 70-80% больных, причем наибольшую пользу лекарства приносят страдающим быстро прогрессирующей тяжелой формой ревматоидного артрита.
Побочные явления возможны у 15-20% пациентов и редко бывают тяжелыми. Чаще всего это аллергические сыпи, ощущение «мурашек» на коже, расстройство стула и умеренные нарушения мочеиспускания. Все эти проявления обычно исчезают сразу после отмены препаратов. Другие побочные эффекты, о которых можно узнать из аннотации к препаратам, случаются при приеме «противоартритных доз» цитостатиков нечасто.
Тем не менее, во избежание осложнений, необходимо контролировать состояние больного, принимающего иммунодепрессанты. Раз в месяц нужно исследовать мочу, и главное — раз в две недели делать анализ крови, взятой из пальца, чтобы вовремя заметить возможное угнетение кроветворения. Раз в три месяца необходимо проверять «печеночные показатели» в крови, взятой из вены. Если же все в порядке и пациент легко переносит цитостатическую терапию, можно ждать явного улучшения самочувствия уже через 2–4 недели после начала лечения.
В настоящее время ревматологи чаще всего используют для лечения ревматоидного артрита 3 цитостатических препарата:
Метотрексат — пожалуй, лучший из лучших базисных препаратов для лечения ревматоидного и псориатического артритов. На сегодняшний день он считается «препаратом выбора» при этих заболеваниях. Для базисного лечения ревматоидного артрита метотрексат принимают только 1 раз (по 10-20 мг) в неделю.
В первый раз выбирают конкретный день, скажем, понедельник, и с этих пор на протяжении всего курса лечения метотрексат принимают только по понедельникам. Терапевтический эффект обычно проявляется через 5-6 недель от начала приема метотрексата и достигает максимума обычно за полгода-год.
Внимание! В день приема метотрексата желательно обойтись без употребления нестероидных противовоспалительных препаратов. Во все остальные дни противовоспалительные препараты можно использовать смело.
Арава, или лефлуномид. Считается, что по эффективности и переносимости арава не уступает метотрексату и сульфасалазину. Хотя по моим наблюдениям, она все-таки переносится несколько хуже метотрексата.
В целом арава рекомендуется больным, у которых артрит протекает очень активно, и тем, кто плохо переносит метотрексат. А еще араву иногда назначают тем пациентам, которым метотрексат помогает слабо — поскольку бывает так, что порой арава помогает больным, для которых метотрексат оказался неэффективным (и наоборот, часто бывает так, что метотрексат пациенту помогает хорошо, а арава — нет).
Терапевтический эффект обычно проявляется через 4-6 недель от начала приема аравы и может нарастать в течение 4-6 месяцев.
Ремикейд, он же инфликсимаб, и препараты схожего действия. Новый быстродействующий и довольно эффективный базисный препарат.
Его применяют в тех случаях, когда другие базисные препараты, в частности метотрексат, не дают должного эффекта. А еще ремикейд применяют в тех случаях, когда необходимо снизить дозу принимаемых кортикостероидных гормонов, или при очень высокой активности артрита.
К сожалению, ремикейд пока весьма дорого стоит. Тем не менее, несмотря на высокую стоимость, применение ремикейда потихоньку набирает обороты — в силу того, что ремикейд действует быстрее многих других базисных препаратов.
Однако применять ремикейд надо с большой осторожностью. Очень часто он переносится больными тяжелее, чем арава или метотрексат, и чаще дает побочные эффекты.
До начала лечения ремикейдом необходимо выявить и пролечить все имеющиеся у пациента инфекции, в том числе скрытые, и пролечить все абсцессы. Ведь если этого не сделать, применение ремикейда может спровоцировать сильнейшее обострение недолеченных инфекционных процессов вплоть до развития сепсиса.
Кроме того, во время лечения ремикейдом рекомендуется применять антиаллергические препараты, чтобы предотвратить возможные аллергические реакции (они бывают довольно часто).
Еще во время лечения необходимо использовать надежные методы контрацепции, чтобы не допустить возникновения беременности — ремикейд категорически противопоказан беременным, а также кормящим матерям (на время терапии следует воздержаться от кормления грудью). Грудное вскармливание разрешается не ранее, чем через 6 месяцев после окончания лечения ремикейдом!
Другие цитостатические препараты, такие как азатиоприн (имуран), хлорбутин, циклофосфан (эндоксан) и циклоспорин (имуспорин, консупрен, сандиммун, экорал), при ревматоидном артрите применяются редко, поскольку они переносятся пациентами гораздо тяжелее, чем метотрексат, арава и ремикейд и гораздо чаще дают различные побочные эффекты. Из-за «тяжести» перечисленных препаратов, из-за их плохой переносимости и высокой частоты побочных эффектов, эти лекарства применяют только в крайних случаях, при неэффективности остальных базисных препаратов.
2. Антималярийные препараты (делагил и плаквенил).
Антималярийные препараты делагил (он же хлорохин, резохин, хингамин) и плаквенил (он же гидроксихлорохин, гидрохлорин) с давних пор использовались инфекционистами для лечения тропической лихорадки (малярии).
Однако в XX в. на них обратили внимание и ревматологи. Они заметили, что при очень длительном применении делагил и плаквенил способны влиять на активность ревматоидного процесса, постепенно уменьшая воспаление в суставах.
К сожалению, со временем выяснилось, что эти препараты действуют очень медленно: лечебный эффект развивается только спустя полгода — год непрерывного приема лекарства. Эффективность делагила и плаквенила тоже оказалась невысокой. Это одни из самых слабых из всех современных базисных препаратов.
Но у них есть важное достоинство — хорошая переносимость и малое количество побочных эффектов.
Хотя эффективность этих препаратов не очень велика и действуют они медленно, мы вынуждены использовать их и поныне, поскольку ощущаем относительный дефицит антиревматоидных средств.
Ведь иногда возникают ситуации, когда другие базисные средства безуспешно перепробованы и отменены из-за неэффективности или выраженного побочного действия. Тогда-то и приходится использовать пусть слабые, но все же обладающие специфическим антиартритным действием делагил и плаквенил.
По мнению большинства ведущих современных ревматологов, базисную терапию нужно начинать с антималярийных средств только тогда, когда ревматоидный артрит протекает очень мягко, и нет необходимости в более сильных лекарствах, обладающих лучшим лечебным действием, но способных провоцировать многочисленные побочные эффекты.
Ведь в отличие от них антималярийные препараты практически безвредны. Лишь в редких случаях при длительном применении делагил или плаквенил могут провоцировать развитие побочных реакций.
3. Сульфаниламиды (сульфасалазин и салазопиридазин).
Сульфасалазин и салазопиридазин — антимикробные препараты, успешно применяемые в базисной терапии ревматоидного артрита. По силе лечебного действия сульфаниламиды совсем немного уступают препаратам золота и метотрексату, вполне сопоставимы по эффективности с Д-пеницилламином, и явно превосходят по силе действия такие препараты, как делагил и плаквенил.
Главным преимуществом сульфаниламидов перед остальными базисными препаратами является их хорошая переносимость — сульфасалазин и салазопиридазин почти не дают осложнений даже при долгом применении.
При длительном приеме побочные эффекты развиваются только у 10-20% больных, и эти побочные эффекты практически никогда не бывают тяжелыми.
Умаляет достоинства сульфаниламидных препаратов лишь медленное развитие их лечебного эффекта. Некоторое улучшение состояния при лечении сульфаниламидами обычно отмечается лишь после трех месяцев терапии, а «пик формы» достигается спустя 6-12 месяцев от начала лечения.
Итак, существует 3 основных группы базисных препаратов для борьбы с ревматоидным артритом. Все они имеют свои достоинства, и, к сожалению, свои недостатки, которые мы только что рассмотрели. Самый частый вопрос, который задают пациенты по поводу базисной терапии и который нередко обсуждается больными в Интернете, касается потенциальной вредности базисных препаратов.
Так, один из самодеятельных «специалистов», явно не разбирающийся в проблеме, с возмущением заявил на одном из Интернет-форумов: «Что же за лекарства такие назначают врачи, если они имеют столько побочных эффектов — одно лечат, другое калечат?»
Вот уж действительно, до чего велико желание некоторых недалеких людей видеть во всем чуть ли не заговор врачей. Но может они правы, и нам действительно не нужно назначать пациенту никаких лекарств вообще, и базисных препаратов в частности? Пусть себе болеет и мучается?
Если отбросить досужие измышления недалеких критиков, факты выглядят так: по многочисленным наблюдениям ученых и врачей (и по моим наблюдениям тоже), чем позже больному назначают базисную терапию, тем для него хуже — болезнь протекает гораздо тяжелее, с многочисленными осложнениями, и чаще заканчивается фатальным исходом. И наоборот, если базисные препараты назначены пациенту вовремя, в первые месяцы болезни, нам часто удается добиться существенного улучшения самочувствия больного, а иногда получается даже и вовсе прервать развитие болезни.
Хотя, безусловно, подбор базисной терапии — дело серьезное. И мы обязаны учитывать возможность развития побочных эффектов. А потому лечащий врач, как говорится, должен постоянно держать «руку на пульсе» и регулярно контролировать состояние пациента.
Еще желательно, чтобы пациент был максимально информирован о том, какие осложнения может вызвать принимаемое лекарство, и сообщал врачу о любых настораживающих реакциях. Именно с целью дать вам максимум информации о принимаемых лекарствах и их возможных побочных реакциях я и писал эту главу.
Но все же: какой базисный препарат предпочесть в каждом конкретном случае? Вот на этот вопрос может ответить только ваш лечащий ревматолог. Только он знает (во всяком случае, должен знать), когда и какое базисное средство следует применить для того или иного пациента.
Хотя недостаток базисных средств как раз в том и состоит, что врачам бывает трудно со стопроцентной вероятностью угадать, даст ли лекарство должный терапевтический эффект. Ответ на этот вопрос можно получить только через месяц-другой от начала применения препарата. И если препарат не действует, то приходится его менять и снова пару месяцев ждать результата.
Таким образом, на подбор базисной терапии порой уходит от 4 до 6 месяцев. Срок, безусловно, чрезвычайно долгий для болеющего человека, но приходится смиряться — другого выбора у нас нет. Но мы можем попытаться улучшить состояние пациента на этот «срок ожидания» с помощью методов физического и механического воздействия на иммунную систему, с помощью противовоспалительных средств, и с помощью местного воздействия на суставы. О них разговор пойдет дальше.
Противовоспалительные средства разных групп
1. Нестероидные противовоспалительные препараты (НПВП).
Как средство первой помощи при суставных болях чаще всего используют «классические» нестероидные противовоспалительные препараты — диклофенак, ибупрофен, кетопрофен, пироксикам, индометацин, мовалис, бутадион и др. Нестероидные противовоспалительные препараты при ревматоидном артрите эффективно снижают воспаление в суставах и уменьшают болевые ощущения.
Без сомнения, эти препараты способны существенно облегчить жизнь больного, но вылечить ревматоидный артрит с помощью нестероидных противовоспалительных препаратов невозможно. Их применяют не для того, чтобы вылечить артрит, а для временного снижения воспаления и боли в суставе.
То есть они не могут остановить развитие болезни, а применяются исключительно симптоматически. И как только пациент прекращает их принимать, болезнь постепенно возвращается.
Тем не менее, поскольку человеку, болеющему ревматоидным артритом, очень трудно обойтись без нестероидных противовоспалительных препаратов, и принимать НПВП при артрите приходится долго, поговорим о том, как их лучше использовать.
Начинать лечение следует с наименее токсичных препаратов. То есть с тех, которые быстро всасываются и легко выводятся из организма. К таким препаратам относятся диклофенак, ибупрофен, кетопрофен и их производные, а также селективный противовоспалительный препарат мовалис.
Индометацин, пироксикам, кеторолак и их аналоги выводятся из организма дольше, считаются более «тяжелыми» препаратами, поэтому их стараются назначать реже, в основном тем пациентам, у которых меньше риск развития побочных эффектов со стороны почек, сердечно-сосудистой системы и желудка. Кроме того, учитывая, что у пожилых людей индометацин может вызывать развитие психических нарушений, его назначают, как правило, только пациентам молодого или среднего возраста.
Второй критерий выбора — эффективность препарата. Обычно лечебный эффект от применения нестероидных противовоспалительных средств развивается быстро, в течение первых трех — семи дней лечения. Если за это время улучшения от приема используемого противовоспалительного препарата не наступило, его надо поменять на другой.
При этом одним из самых эффективных противовоспалительных препаратов считается диклофенак. Правда, многих пациентов, да и врачей, отпугивает чересчур подробная аннотация к препарату. Особенно та ее часть, где пунктуально перечислены все возможные осложнения и побочные эффекты к лекарству. Большинство людей, прочитавших аннотацию, думают, что у них обязательно возникнут все перечисленные осложнения.
Между тем, диклофенак ничуть не вреднее аспирина, который многие пьют не задумываясь. Просто аннотация к диклофенаку написана честнее и подробнее. А перечисленные побочные эффекты возникают далеко не у всех людей, даже годами принимающих диклофенак или его аналоги.
2. Кортикостероидные гормональные препараты (кортикостероиды).
Для оказания быстрой помощи страдающим ревматоидным артритом многие врачи, особенно зарубежные, помимо нестероидных противовоспалительных препаратов, не задумываясь назначают противовоспалительные кортикостероидные гормоны: преднизолон (он же медопред), триамцинолол (он же кеналог, полькортолон, триамсинолол, кенакорт), дексаметазон, метилпреднизолон (он же метипред, медрол, депо-медрол), бетаметазон (он же дипроспан, флостерон, целестон).
Среди наших врачей бытует два полярно разных взгляда на использование гормональных кортикостероидных препаратов. Одни врачи однозначно приветствуют их использование в лечебных целях, а другие полностью отвергают и игнорируют. В результате пациенты, старающиеся быть в курсе веяний «медицинской моды», находятся в полном недоумении: полезны такие гормоны при артрите или вредны, можно их использовать или нет? Что же, давайте порассуждаем вместе.
С одной стороны, применение таких гормонов почти всегда способствует явному улучшению состояния пациента. Сразу уменьшается боль в суставах, исчезает утренняя скованность, пропадают или уменьшаются слабость и ознобы. Естественно, такой быстрый результат вызывает у любого пациента чувство благодарности к врачу. А в условиях платной медицины эта благодарность часто подкрепляется материально — за такое облегчение пациент готов платить деньги, причем немалые, — что является главным стимулом западной и современной платной медицины.
Вы спросите: может быть, тогда стоит не отменять гормоны, а продолжать принимать их постоянно? Нет, это не выход. То, что со временем кортикостероиды перестают так же хорошо снимать боль, как в начале их применения, это полбеды. Хуже всего, что постепенно «накапливаются» побочные эффекты от их использования.
Таких побочных эффектов немало — кортикостероиды способствуют развитию симптомокомплекса Иценко-Кушинга, при котором происходит задержка натрия и воды в организме с возможным появлением отеков и повышением артериального давления. Кроме того, такие гормоны повышают уровень сахара в крови вплоть до развития сахарного диабета, способствуют увеличению веса тела, снижают иммунитет, провоцируют у некоторых пациентов появление язвы желудка и двенадцатиперстной кишки, повышают риск образования тромбов.
При длительном приеме кортикостероидов могут произойти появление угрей, лунообразного лица, нарушения менструального цикла, развитие геморрагического панкреатита. У некоторых пациентов развиваются реакции со стороны нервной системы: появляются бессонница, эйфория, возбуждение (в некоторых случаях даже с развитием психозов), судороги по типу эпилепсии. К тому же при длительном применении лекарственные кортикостероиды подавляют выработку организмом своих естественных гормонов.
В результате рано или поздно наступает момент, когда из-за побочных эффектов пациент вынужден отказаться от приема кортикостероидных гормонов. Но сделать это не так-то просто. Организм уже не может обойтись без поступления кортикостероидов извне, и быстрое снижение их дозы приводит к резкому ухудшению самочувствия и обострению суставных болей.
Поэтому уменьшать дозы потребляемых гормонов приходится постепенно, по несколько миллиграмм в неделю. И окончательная их отмена отдаляется на несколько месяцев. Но даже при таком постепенном уменьшении дозы гормонов процесс редко проходит безболезненно для организма.
Так что, прежде чем назначить пациенту гормонотерапию, врач должен трижды взвесить, чего будет больше от такого лечения — вреда или пользы. С моей точки зрения, гормоны следует назначать только при высокой активности артрита, при «зашкаливании» в анализах воспалительных показателей (например, повышении СОЭ, или РОЭ, выше 40 мм/час, при сильном повышении уровней С-реактивного белка, серомукоида и других показателей), особенно если воспаление не сбивается нестероидными противовоспалительными препаратами, и сопровождается сильнейшими болями и слабостью заболевшего.
Так что, прежде чем назначить пациенту гормонотерапию, врач должен трижды взвесить, чего будет больше от такого лечения — вреда или пользы. С моей точки зрения, гормоны следует назначать только при высокой активности артрита, при «зашкаливании» в анализах воспалительных показателей (например, повышении СОЭ, или РОЭ, выше 40 мм/час, при сильном повышении уровней С-реактивного белка, серомукоида и других показателей), особенно если воспаление не сбивается нестероидными противовоспалительными препаратами, и сопровождается сильнейшими болями и слабостью заболевшего.
И, конечно, гормоны однозначно следует назначать при развитии ряда так называемых системных осложнений артрита — синдроме Фелти, синдроме Стилла, ревматической полимиалгии и др. То есть, с одной стороны, врач не имеет права назначать гормоны всем подряд, но и не должен отказываться от их применения в тех случаях, когда они действительно необходимы.
Ведь в некоторых ситуациях применение гормонов может, без преувеличения, спасти пациенту жизнь. Поэтому подходить к вопросу об их применении нужно крайне взвешенно, и, естественно, необходимо учитывать еще и наличие противопоказаний к гормональному лечению.
Местное лечение
1. Внутрисуставное введение кортикостероидных гормонов
Чаще всего в сустав при артритах вводят препараты кортикостероидных гормонов: кеналог, дипроспан, гидрокортизон, флостерон, целестон, метипред, депо-медрол. Кортикостероиды хороши тем, что они быстро и эффективно подавляют боль и воспаление при отеке и припухании сустава. Именно быстрота, с какой достигается лечебный эффект, — причина того, что кортикостероидные инъекции завоевали особую популярность среди врачей.
Введение кортикостероидных гормонов в сустав помогает больному пережить период особо острого воспаления отдельных суставов. Такие внутрисуставные инъекции могут существенно облегчить жизнь больному даже в особо тяжелых случаях ревматоидного артрита. Но обычно лечебного эффекта от инъекции хватает всего на 3-4 недели. Затем воспаление вновь начинает понемногу нарастать.
То есть такие инъекции ни в коей мере не являются панацеей. Тем более, что их нельзя делать слишком часто — иначе гормоны начнут оказывать отрицательное воздействие на весь организм.
Поэтому интервалы между такими процедурами должны быть не меньше 7-10 дней. А в один сустав в сумме, даже с большими интервалами, нежелательно делать больше 5-8 гормональных уколов. Ведь слишком частые введения гормонов провоцируют нарушение структуры связок сустава и окружающих его мышц, постепенно вызывая «разболтанность» сустава и деструкцию хряща.
2. Лазерная терапия
Этот метод оказывает при ревматоидном артрите мягкий противовоспалительный эффект. Применяется лазеротерапия и как отдельный метод лечения ревматоидного артрита, и в сочетании с базисной терапией.
Существуют два способа воздействия лазерным излучением на организм больного. В острой фазе ревматоидного артрита лазером облучают не суставы пациента, а область локтевой вены — то есть излучение воздействует на кровь, циркулирующую внутри организма. Считается, что после облучения крови лазером в организме происходят разнообразные положительные сдвиги: нормализуется иммунитет, улучшается кровоснабжение органов и тканей, уменьшается любое воспаление и подавляются очаги инфекции.
В хронической фазе болезни (при нормализации анализов и температуры тела) лазером воздействуют непосредственно на суставы больного ревматоидным артритом. Делается это при условии, что у пациента нормальные анализы и температура тела. Улучшение после лазеротерапии отмечается у 80% больных, хотя в начале курса лечения происходит кратковременное обострение заболевания.
В целом наиболее благоприятные результаты отмечаются у пациентов с вялотекущей, мягкой формой ревматоидного артрита. При тяжелых формах болезни лазер малоэффективен. Курс лечения состоит из 15-20 процедур, проводимых через день.
Противопоказаниями к применению лазера являются опухолевые заболевания, болезни крови, гиперфункция щитовидной железы, инфекционные заболевания, физическое истощение, кровотечения, инфаркт миокарда, инсульт, туберкулез, цирроз печени, гипертонический криз.
3. Криотерапия — воздействие местным охлаждением
Криотерапия является одним из лучших местных методов лечения ревматоидного, псориатического и реактивного артритов, а также болезни Бехтерева. Криотерапия с успехом применяется как в острой, так и в хронической фазе ревматоидного артрита. Лечение это практически безвредное и почти не имеет противопоказаний, но требует регулярности. Улучшение после криотерапии отмечается более чем у 80% больных ревматоидным артритом.
Существуют два основных аппаратных метода криотерапии: сухая криотерапия (воздействие воздухом сверхнизкой температуры, в частности применение криосаун), и «жидкая криотерапия» — воздействие на организм струей жидкого азота.
При «жидкой криотерапии» на пораженные суставы или спину направляют струю жидкого азота под давлением, азот моментально испаряется и быстро охлаждает место воздействия. В результате такой процедуры удается добиться выраженной ответной реакции со стороны организма и пораженных суставов — уменьшается воспаление и отечность суставов, улучшается кровообращение и обмен веществ, снижаются болевые ощущения. Курс лечения включает 8-12 процедур, проводимых ежедневно или через день.
При правильном воздействии криотерапия жидким азотом почти не имеет противопоказаний и может быть использована даже для лечения пожилых, ослабленных больных. Ее нельзя применять лишь при синдроме Рейно, некоторых аритмиях, и непосредственно сразу после инфаркта или инсульта.
Во время сухой криотерапии раздетого пациента на очень короткое время помещают в специальное помещение — криосауну, куда подается очень холодный воздух. Сухая криотерапия оказывает меньшее локальное воздействие на отдельные воспаленные суставы пациента, но, равно жидкой криотерапии, хорошо действует на общее состояние больных ревматоидным артритом — особенно в том случае, когда у пациента воспалена сразу большая группа суставов.
Однако, при прочих равных условиях, сухая криотерапия в коммерческих медицинских центрах стоит, как правило, значительно дороже жидкой криотерапии, поскольку требует более сложного и дорогостоящего оборудования.
4. Лечебные мази и кремы
Лечебные мази и кремы часто рекламируются как средства, гарантирующие исцеление от суставных заболеваний. Однако при артрите лечебные мази способны принести больному лишь небольшое облегчение.
Обычно при ревматоидном артрите используют мази на основе нестероидных противовоспалительных веществ (индометациновая, бутадионовая, долгит, вольтарен-гель, фастум-гель и др.). К сожалению, они действуют не так эффективно, как хотелось бы — ведь кожа пропускает не более 5-7% действующего вещества, а этого явно недостаточно для развития полноценного противовоспалительного эффекта.
Но зато эти мази почти никогда не вызывают тех побочных эффектов, которые случаются от внутреннего применения нестероидных противовоспалительных средств. То есть они практически безвредны.
Физиотерапевтическое лечение ревматоидного артрита
Массаж и любые физиотерапевтические процедуры, за исключением криотерапии и лазера, при ревматоидном артрите проводятся только тогда, когда минует обострение артрита, и показатели крови придут в норму. Ведь физиопроцедуры и массаж оказывают стимулирующее действие на организм, которое полезно при артрозах, но при артритах способно усиливать воспаление суставов.
Поэтому физиотерапию и массаж делают исключительно при нормальной температуре тела, хороших анализах крови и при отсутствии покраснения и отека суставов (покраснение и отек указывают на скопление в суставе патологической «воспалительной» жидкости).
Еще раз подчеркну: массаж и практически любые физиотерапевтические процедуры, за исключением криотерапии и лазера, абсолютно противопоказаны при средней и высокой активности ревматоидного артрита, пока продолжается заметное воспаление суставов!
И только после ликвидации обострения можно переходить к мягкому массажу и физиотерапии, чтобы добиться улучшения кровообращения больных суставов, уменьшения их деформации и увеличения их подвижности.
С этой целью применяют инфракрасные облучения, диатермию, УВЧ, аппликации парафина, озокерита и лечебных грязей. Эти виды физиотерапии способствуют мышечной релаксации и устранению контрактуры суставов, улучшают питание больных суставов. С успехом применяется также фонофорез с лекарственными препаратами (например, с гидрокортизоном). Фонофорез оказывает на суставы больного мягкое противовоспалительное действие.
Несколько реже при ревматоидном артрите используется рентгенотерапия. Метод заключается в воздействии на пораженные суставы небольших доз рентгеновских лучей. Малые дозы облучения оказывают выраженное обезболивающее и противовоспалительное действие и не вызывают серьезных осложнений. Иногда рентгенотерапию применяют для усиления противовоспалительного эффекта базисных препаратов, даже при активном ревматоидном артрите.
Диета при ревматоидном артрите
Диета при ревматоидном артрите — одна из важных составляющих лечения. У некоторых больных проявляется четкая взаимосвязь между активностью воспаления и переносимостью определенных продуктов питания.
Обострение артрита наступает при употреблении в пищу продуктов, «аллергизирующих» организм, а их отмена приводит к улучшению состояния. Наиболее часто, по мнению ряда ученых, обострению воспалительного процесса при ревматоидном артрите способствует употребление в пищу кукурузы, пшеницы, свинины, цитрусовых, овсянки, ржи, молока и молочных продуктов.
Значит, все эти продукты необходимо по возможности ограничить или исключить из рациона больного ревматоидным артритом. Рекомендуется употребление рыбы, рыбьего жира и других морепродуктов, а также овощей, фруктов, куриных яиц, перловой и гречневой круп. Питание должно быть дробным и частым, 5-6 раз в день.
Готовить еду желательно на пару. Постарайтесь сократить употребление поваренной соли и как можно меньше есть жареную или копченую пищу. Некоторые ученые рекомендуют пациентам, болеющим ревматоидным артритом, вообще перейти на диету № 10 (см. 1-ю главу).
Статья доктора Евдокименко© для книги «Артрит», опубликована в 2003 году.
Отредактирована в 2011г. Все права защищены.
Современная медикаментозная терапия ревматоидного артрита
Ревматоидный артрит — это заболевание, находящееся в фокусе внимания ревматологов всего мира в течение десятилетий. Это связано с большим медицинским и социальным значением этой болезни. Ее распространенность достигает
Ревматоидный артрит — это заболевание, находящееся в фокусе внимания ревматологов всего мира в течение десятилетий. Это связано с большим медицинским и социальным значением этой болезни. Ее распространенность достигает 0,5–2% от общей численности населения в промышленно развитых странах [1, 2]. У больных ревматоидным артритом наблюдается уменьшение продолжительности жизни по сравнению с общей популяцией на 3–7 лет [3]. Трудно переоценить колоссальный ущерб, наносимый этим заболеванием обществу за счет ранней инвалидизации пациентов, которая при отсутствии своевременно начатой активной терапии может наступать в первые 5 лет от дебюта болезни.
Ревматоидный артрит — хроническое воспалительное заболевание неясной этиологии, для которого характерно поражение периферических синовиальных суставов и периартикулярных тканей, сопровождающееся аутоиммунными нарушениями и способное приводить к деструкции суставного хряща и кости, а также к системным воспалительным изменениям.
Патогенез заболевания весьма сложен и во многом недостаточно изучен. Несмотря на это, к настоящему времени хорошо известны некоторые ключевые моменты в развитии ревматоидного воспаления, которые определяют основные методы лечебного воздействия на него (рис. 1). Развитие хронического воспаления в данном случае связано с активацией и пролиферацией иммунокомпетентных клеток (макрофагов, Т- и В-лимфоцитов), что сопровождается выделением клеточных медиаторов — цитокинов, факторов роста, молекул адгезии, а также синтезом аутоантител (например, антицитруллиновых антител) и формированием иммунных комплексов (ревматоидные факторы). Эти процессы ведут к формированию новых капиллярных сосудов (ангиогенез) и разрастанию соединительной ткани в синовиальной оболочке, к активации циклооксигеназы-2 (ЦОГ-2) с повышением синтеза простагландинов и развитием воспалительной реакции, к выделению протеолитических ферментов, активации остеокластов, а в результате — к деструкции нормальных тканей суставов и возникновению деформаций.
Лечение ревматоидного артрита
Исходя из патогенеза заболевания, становится очевидным, что эффективно воздействовать на развитие заболевания можно на двух уровнях:
Поскольку, помимо собственно воспаления, активация иммунной системы сопровождается многими другими патологическими процессами, воздействие на первом уровне является существенно более глубоким и эффективным, нежели на втором. Медикаментозная иммуносупрессия представляет собой основу лечения ревматоидного артрита. К иммуносупрессорам, применяющимся для лечения данного заболевания, относятся базисные противовоспалительные препараты (БПВП), биологические препараты и глюкокортикостероиды. На втором уровне действуют нестероидные противовоспалительные препараты (НПВП) и глюкокортикостероиды.
В целом иммуносупрессивная терапия сопровождается более медленным развитием клинического эффекта (в широких рамках — от нескольких дней в случае биологической терапии до нескольких месяцев в случае применения некоторых БПВП), который в то же время бывает очень выраженным (вплоть до развития клинической ремиссии) и стойким, а также характеризуется торможением деструкции суставов.
Собственно противовоспалительная терапия (НПВП) может давать клинический эффект (обезболивание, уменьшение скованности) очень быстро — в течение 1–2 ч, однако при помощи такого лечения практически невозможно полностью купировать симптоматику при активном ревматоидном артрите и, по-видимому, оно совсем не влияет на развитие деструктивных процессов в тканях.
Глюкокортикостероиды обладают как иммуносупрессивным, так и непосредственным противовоспалительным эффектом, поэтому клиническое улучшение может развиваться быстро (в течение нескольких часов при внутривенном или внутрисуставном введении). Имеются данные о подавлении прогрессирования эрозивного процесса в суставах при длительной терапии низкими дозами глюкокортикостероидов и о положительном их влиянии на функциональный статус больного. В то же время из практики хорошо известно, что назначение только глюкокортикостероидов, без других иммуносупрессивных средств (БПВП), редко дает возможность достаточно эффективно контролировать течение болезни.
Немедикаментозные способы терапии ревматоидного артрита (физиотерапия, бальнеотерапия, диетотерапия, акупунктура и др.) представляют собой дополнительные методики, с помощью которых можно несколько улучшить самочувствие и функциональный статус пациента, но не купировать симптоматику и достоверно повлиять на деструкцию суставов.
Ортопедическое лечение, включающее ортезирование и хирургическую коррекцию деформаций суставов, а также реабилитационные мероприятия (лечебная физкультура и др.) имеют особое значение преимущественно на поздних стадиях заболевания для поддержания функциональной способности и улучшения качества жизни больного.
Основными целями лечения при РА являются [2, 6]:
Надо иметь в виду, что цели лечения могут существенно изменяться в зависимости от длительности болезни. На ранней стадии болезни, т. е. при длительности болезни 6–12 мес, достижение клинической ремиссии — вполне реальная задача, так же как и торможение развития эрозий в суставах. С помощью современных методов активной медикаментозной терапии удается добиться ремиссии у 40–50% пациентов [4, 5], показано также отсутствие появления новых эрозий по данным рентгенографии [7] и магнитно-резонансной томографии [8] у значительного количества больных при длительности наблюдения 1–2 года.
При длительно текущем ревматоидном артрите, особенно при недостаточно активной терапии в первые годы заболевания, достижение полной ремиссии теоретически тоже возможно, однако вероятность этого значительно ниже. То же самое можно сказать и о возможности остановить прогрессирование деструкции в суставах, уже существенно разрушенных за несколько лет болезни. Поэтому при далеко зашедшем ревматоидном артрите возрастает роль реабилитационных мероприятий, ортопедической хирургии. Кроме того, на поздних стадиях заболевания длительная поддерживающая базисная терапия может использоваться для вторичной профилактики осложнений болезни, таких как системные проявления (васкулит и др.), вторичный амилоидоз.
Базисная терапия ревматоидного артрита. БПВП (синонимы: базисные препараты, болезнь-модифицирующие антиревматические препараты, медленно действующие препараты) являются главным компонентом лечения ревматоидного артрита и при отсутствии противопоказаний должны быть назначены каждому пациенту с этим диагнозом [9]. Особенно важно максимально быстрое назначение БПВП (сразу после установления диагноза) на ранней стадии, когда имеется ограниченный период времени (несколько месяцев от появления симптоматики) для достижения наилучших отдаленных результатов — так называемое «терапевтическое окно» [10].
Классические БПВП обладают следующими свойствами.
БПВП существенно различаются между собой по механизму действия и особенностям применения. Основные параметры, характеризующие БПВП, представлены в таблице 1.
БПВП условно могут быть подразделены на препараты первого и второго ряда. Препараты первого ряда обладают наилучшим соотношением эффективности (достоверно подавляют как клиническую симптоматику, так и прогрессирование эрозивного процесса в суставах) и переносимости, в связи с чем назначаются большинству пациентов.
К БПВП первого ряда относятся следующие.
БПВП второго ряда применяются значительно реже в связи с меньшей клинической эффективностью и/или большей токсичностью. Они назначаются, как правило, при неэффективности или непереносимости БПВП первого ряда.
БПВП способны вызвать значительное улучшение (хороший клинический ответ) приблизительно у 60% пациентов. В связи с медленным развитием клинического эффекта назначение БПВП на сроки менее 6 мес не рекомендуется. Длительность лечения определяется индивидуально, типичная продолжительность «курса» лечения одним препаратом (в случае удовлетворительного ответа на терапию) составляет 2–3 года и более. Большинство клинических рекомендаций подразумевают неопределенно долгое применение поддерживающих дозировок БПВП для сохранения достигнутого улучшения.
При недостаточной эффективности монотерапии каким-либо базисным препаратом может быть избрана схема комбинированной базисной терапии, т. е. сочетания двух-трех БПВП. Наиболее хорошо зарекомендовали себя следующие сочетания:
В комбинированных схемах препараты обычно применяются в средних дозировках. В ряде клинических исследований было продемонстрировано превосходство комбинированной базисной терапии над монотерапией, однако более высокая эффективность комбинированных схем не считается строго доказанной. Комбинация БПВП ассоциирована с умеренным повышением частоты побочных эффектов.
Биологические препараты в лечении ревматоидного артрита. Термин биологические препараты (от англ. biologics) применяется по отношению к лекарственным средствам, производимым с использованием биотехнологий и осуществляющим целенаправленное («точечное») блокирование ключевых моментов воспаления с помощью антител или растворимых рецепторов к цитокинам, а также другим биологически активным молекулам. Таким образом, биологические препараты не имеют никакого отношения к «биологически активным пищевым добавкам». В связи с большим количеством «молекул-мишеней», воздействие на которые потенциально может подавлять иммунное воспаление, разработан целый ряд лекарственных средств из этой группы и еще несколько препаратов проходят клинические испытания.
К основным зарегистрированным в мире для лечения ревматоидного артрита биологическим препаратам относятся:
Для биологических препаратов характерны выраженный клинический эффект и достоверно доказанное торможение деструкции суставов. Эти признаки позволяют относить биологические препараты к группе БПВП. В то же время особенностью группы является быстрое (нередко в течение нескольких дней) развитие яркого улучшения, что объединяет биологическую терапию с методами интенсивной терапии. Характерная черта биологических средств — потенцирование эффекта в сочетании с БПВП, в первую очередь с метотрексатом. В связи с высокой эффективностью при ревматоидном артрите, в том числе у резистентных к обычной терапии пациентов, в настоящее время биологическая терапия выдвинулась на второе по значимости место (после БПВП) в лечении этого заболевания.
К отрицательным сторонам биологической терапии относятся:
Биологические методы терапии показаны, если лечение препаратами из группы БПВП (такими, как метотрексат) не является адекватным вследствие недостаточной эффективности или неудовлетворительной переносимости.
Одной из наиболее важных молекул-мишеней служит ФНО-a, который имеет множество провоспалительных биологических эффектов и способствуют персистенции воспалительного процесса в синовиальной оболочке, деструкции хряща и костной ткани за счет прямого действия на синовиальные фибробласты, хондроциты и остеокласты. Блокаторы ФНО-α являются наиболее широко применяемыми биологическими средствами в мире.
В России зарегистрирован препарат из этой группы инфликсимаб (ремикейд), представляющий собой химерное моноклональное антитело к ФНО-α. Препарат, как правило, назначается в сочетании с метотрексатом. У пациентов с недостаточной эффективностью терапии средними и высокими дозами метотрексата инфликсимаб существенно улучшает ответ на лечение и функциональные показатели, а также приводит к выраженному торможению прогрессирования сужения суставной щели и развития эрозивного процесса.
Показанием к назначению инфликсимаба в комбинации с метотрексатом является неэффективность одного или более БПВП, применявшихся в полной дозе (в первую очередь метотрексата), с сохранением высокой воспалительной активности (пять и более припухших суставов, скорость оседания эритроцитов (СОЭ) более 30 мм/ч, С-реактивный белок (СРБ) более 20 мг/л). При раннем ревматоидном артрите с высокой воспалительной активностью и быстрым нарастанием структурных нарушений в суставах комбинированная терапия метотрексатом и инфликсимабом может быть назначена сразу.
До назначения инфликсимаба требуется провести скрининговое обследование на туберкулез (рентгенография грудной клетки, туберкулиновая проба). Рекомендуемая схема применения: начальная доза 3 мг/кг массы тела больного в/в капельно, затем по 3 мг/кг массы тела через 2, 6 и 8 нед, далее по 3 мг/кг массы тела каждые 8 нед, при недостаточной эффективности доза может повышаться вплоть до 10 мг/кг массы тела. Длительность лечения определяется индивидуально, обычно не менее 1 года. После отмены инфликсимаба поддерживающая терапия метотрексатом продолжается. Следует иметь в виду, что повторное назначение инфликсимаба после окончания курса лечения этим препаратом ассоциировано с повышенной вероятностью реакций гиперчувствительности замедленного типа.
Вторым зарегистрированным в нашей стране препаратом для проведения биологической терапии является ритуксимаб (мабтера). Действие ритуксимаба направлено на подавление В-лимфоцитов, которые не только являются ключевыми клетками, отвечающими за синтез аутоантител, но и выполняют важные регуляторные функции на ранних стадиях иммунных реакций. Препарат обладает выраженной клинической эффективностью, в том числе у больных, недостаточно отвечающих на терапию инфликсимабом.
Для лечения ревматоидного артрита препарат применяется в дозе 2000 мг на курс (две инфузии по 1000 мг, каждая с промежутком в 2 нед). Ритуксимаб вводится внутривенно медленно, рекомендуется проведение инфузии в условиях стационара с возможностью точного контроля за скоростью введения. Для профилактики инфузионных реакций целесообразно предварительное введение метилпреднизолона 100 мг. При необходимости возможно проведение повторного курса инфузий ритуксимаба через 6–12 мес.
Согласно европейским клиническим рекомендациям, ритуксимаб целесообразно назначать в случаях неэффективности или невозможности проведения терапии инфликсимабом. Возможность применения ритуксимаба в качестве первого биологического препарата служит в настоящее время предметом исследований.
Глюкокортикостероиды. Глюкокортикостероиды обладают многогранным противовоспалительным действием, обусловленным блокадой синтеза провоспалительных цитокинов и простагландинов, а также торможением пролиферации за счет воздействия на генетический аппарат клеток. Глюкокортикостероиды оказывают быстрый и ярко выраженный дозозависимый эффект в отношении клинических и лабораторных проявлений воспаления. Применение глюкокортикостероидов чревато развитием нежелательных реакций, частота которых также повышается с увеличением дозы препарата (стероидный остеопороз, медикаментозный синдром Иценко–Кушинга, поражение слизистой ЖКТ). Эти препараты сами по себе в большинстве случаев не могут обеспечить полноценного контроля над течением ревматоидного артрита и должны назначаться вместе с БПВП.
Глюкокортикостероиды при данном заболевании применяются системно и локально. Для системного применения показан основной метод лечения — назначение низких доз внутрь (преднизолон — до 10 мг/сут, метилпреднизолон — до 8 мг/сут) на длительный период при высокой воспалительной активности, полиартикулярном поражении, недостаточной эффективности БПВП.
Средние и высокие дозы глюкокортикостероидов внутрь (15 мг/сут и более, обычно 30–40 мг/сут в пересчете на преднизолон), а также пульс-терапия глюкокортикостероидами — внутривенное введение высоких доз метилпреднизолона (250–1000 мг) или дексаметазона (40–120 мг) могут применяться для лечения тяжелых системных проявлений ревматоидного артрита (выпотной серозит, гемолитическая анемия, кожный васкулит, лихорадка и др.), а также некоторых особых форм болезни. Продолжительность лечения определяется временем, необходимым для купирования симптоматики, и составляет обычно 4–6 нед, после чего осуществляется постепенное ступенчатое снижение дозы с переходом на лечение низкими дозами глюкокортикостероидов.
Глюкокортикостероиды в средних и высоких дозах, пульс-терапия, по-видимому, не обладают самостоятельным влиянием на течение ревматоидного артрита и развитие эрозивного процесса в суставах.
Для локальной терапии применяются препараты в микрокристаллической форме, назначающиеся в виде внутрисуставных и периартикулярных инъекций: бетаметазон, триамсинолон, метилпреднизолон, гидрокортизон.
Глюкокортикостероиды для локального применения обладают ярко выраженным противовоспалительным действием, преимущественно в месте введения, а в ряде случаев — и системным действием. Рекомендуемые суточные дозы составляют: 7 мг — для бетаметазона, 40 мг — для триамсинолона и метилпреднизолона, 125 мг — для гидрокортизона. Эта доза (суммарно) может использоваться для внутрисуставного введения в один крупный (коленный) сустав, два сустава среднего размера (локтевые, голеностопные и др.), 4–5 мелких суставов (пястно-фаланговые и др.), либо для периартикулярного введения препарата в 3–4 точки.
Эффект после однократного введения обычно наступает на протяжении 1–3 дней и сохраняется в течение 2–4 нед при хорошей переносимости.
В связи с этим повторные инъекции глюкокортикостероидов в один сустав нецелесообразно назначать ранее чем через 3–4 недели. Проведение курса из нескольких внутрисуставных инъекций в один и тот же сустав не имеет терапевтического смысла и чревато осложнениями (локальный остеопороз, усиление деструкции хряща, остеонекроз, нагноение). В связи с повышенным риском развития остеонекроза внутрисуставное введение глюкокортикостероидов в тазобедренный сустав в целом не рекомендуется.
Глюкокортикостероиды для локального применения назначаются в качестве дополнительного метода купирования обострений ревматоидного артрита и не могут служить заменой системной терапии.
НПВП. Значение НПВП в лечении ревматоидного артрита за последние годы существенно снизилось в связи с появлением новых эффективных схем патогенетической терапии. Противовоспалительное действие НПВП достигается с помощью подавления активности ЦОГ, или избирательно ЦОГ-2, и тем самым снижается синтез простагландинов. Таким образом НПВП действуют на конечное звено ревматоидного воспаления.
Действие НПВП при ревматоидном артрите — уменьшение выраженности симптомов болезни (боль, скованность, припухлость суставов). НПВП обладают обезболивающим, противовоспалительным, жаропонижающим эффектом, но мало влияют на лабораторные показатели воспаления. В подавляющем большинстве случаев НПВП не способны как-либо заметно изменить течение заболевания. Их назначение в качестве единственного противоревматического средства при достоверном диагнозе ревматоидный артрит в настоящее время считается ошибкой. Тем не менее НПВП являются основным средством симптоматической терапии при данном заболевании и в большинстве случаев назначаются в сочетании с БПВП.
Наряду с лечебным эффектом, все НПВП, включая селективные (ингибиторы ЦОГ-2), способны вызывать эрозивно-язвенное поражение ЖКТ (в первую очередь верхних его отделов — «НПВП-гастропатия») с возможными осложнениями (кровотечения, перфорации и пр.), а также нефротоксические и другие нежелательные реакции.
Основные характерные черты, которые необходимо учитывать при назначении НПВП, следующие.
Существует индивидуальная чувствительность к различным НПВП как в отношении эффективности, так и переносимости лечения. Дозы НПВП при ревматоидном артрите соответствуют стандартным. Продолжительность лечения НПВП определяется индивидуально и зависит от потребности больного в симптоматической терапии. При хорошем ответе на терапию БПВП препарат из группы НПВП может быть отменен.
К наиболее часто применяющимся при ревматоидном артрите НПВП относятся:
Селективные НПВП, по эффективности достоверно не отличаясь от неселективных, реже вызывают НПВП-гастропатии и серьезные нежелательные реакции со стороны ЖКТ, хотя и не исключают развитие этих осложнений. Ряд клинических исследований продемонстрировал повышенную вероятность развития тяжелой сосудистой патологии (инфаркт миокарда, инсульт) у пациентов, получавших препараты из группы коксибов, в связи с чем возможность лечения целекоксибом должна обсуждаться с особой осторожностью у больных с ИБС и другими серьезными кардиоваскулярными патологиями.
Дополнительные медикаментозные методы лечения. В качестве симптоматического анальгетика (или дополнительного анальгетика при недостаточной эффективности НПВП) может использоваться парацетамол (ацетаминофен) в дозе 500–1500 мг/сут, который обладает относительно невысокой токсичностью. Для локальной симптоматической терапии используются НПВП в виде гелей и мазей, а также диметилсульфоксид в виде 30–50% водного раствора в форме аппликаций. При наличии остеопороза показано соответствующее лечение препаратами кальция, витамина Д3, бифосфонатами, кальцитонином.
Общие принципы ведения больных РА
Больному с установленным диагнозом ревматоидный артрит должен быть назначен препарат из группы БПВП, который при хорошем клиническом эффекте может применяться как единственный метод терапии [9]. Другие лечебные средства используются по мере необходимости.
Больной должен быть информирован о характере своего заболевания, течении, прогнозе, необходимости длительного сложного лечения, а также о возможных нежелательных реакциях и схеме контроля за лечением, неблагоприятных сочетаниях с другими препаратами (в частности, алкоголем), возможной активации очагов хронической инфекции на фоне лечения, целесообразности временной отмены иммуносупрессивных препаратов при возникновении острых инфекционных заболеваний, о необходимости контрацепции на фоне лечения.
Терапия ревматоидного артрита должна назначаться врачом-ревматологом и проводиться под его наблюдением. Лечение биологическими препаратами может проводиться только под контролем ревматолога, имеющего достаточные знания и опыт для его проведения. Терапия является длительной и подразумевает периодический контроль активности болезни и оценку ответа на терапию. Упрощенный алгоритм представлен на рисунке 2.
Мониторинг активности болезни и ответа на терапию включает оценку показателей суставного статуса (число болезненных и припухших суставов и др.), острофазовых показателей крови (СОЭ, СРБ), оценку боли и активности болезни по визуальной аналоговой шкале, оценку функциональной активности больного в повседневной деятельности с помощью русского варианта опросника состояния здоровья (HAQ). Существуют признанные международным сообществом ревматологов методики количественной оценки ответа на лечение с помощью рекомендованного Европейской лигой по борьбе с ревматизмом (EULAR) индекса DAS (Disease Activity Score) и критериев Американской коллегии ревматологов (ACR) [1]. Кроме того, должен осуществляться мониторинг безопасности проводимой пациенту терапии (в соответствии и формуляром и существующими клиническими рекомендациями). В связи с тем, что эрозивный процесс может развиваться даже при низкой воспалительной активности, помимо оценки активности болезни и ответа на терапию обязательно применяется рентгенография суставов. Прогрессирование деструктивных изменений в суставах оценивают путем стандартной рентгенографии кистей и стоп с использованием рентгенологической классификации стадий ревматоидного артрита, количественных методик по индексам Sharp и Larsen. С целью мониторинга состояния больного обследование рекомендуется проводить с определенной периодичностью (табл. 2).
Лечение резистентного к терапии РА
Резистентным к лечению целесообразно считать пациента с неэффективностью (отсутствием 20% улучшения по основным показателям) как минимум двух стандартных БПВП в достаточно высоких дозах (метотрексат — 15–20 мг/нед, сульфасалазин — 2000 мг/сут, лефлуномид — 20 мг/сут). Неэффективность может быть первичной и вторичной (возникающей после периода удовлетворительного ответа на терапию либо при повторном назначении препарата). Существуют следующие пути преодоления резистентности к терапии:
С точки зрения отдаленных результатов в отношении функциональных нарушений, качества жизни и ее продолжительности оптимальной стратегией терапии ревматоидного артрита является многолетнее лечение БПВП с планомерной сменой схемы их применения по мере необходимости [11].
Литература
Д. Е. Каратеев, доктор медицинских наук
Институт ревматологии РАМН, Москва