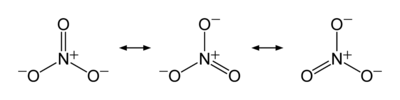
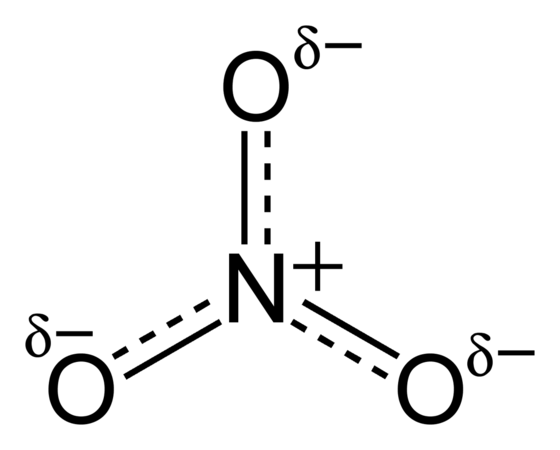
какую форму имеет нитрат ион
НИТРАТЫ НЕОРГАНИЧЕСКИЕ
Безводные нитраты-кристаллич. соед., нитраты d-элементов окрашены. Условно нитраты могут быть разделены на соед. с преим. ковалентным типом связи (соли Be, Cr, Zn, Fe и др. переходных металлов) и с преим. ионным типом связи (соли щелочных и щел.-зем. металлов). Для ионных нитратов характерны более высокая термич. устойчивость, преобладание кристаллич. структур более высокой симметрии (кубич.) и отсутствие расщепления полос нитрат-иона в ИК спектрах. Ковалентные нитраты имеют более высокую р-римость в орг. р-рителях, более низкую термич. устойчивость, их ИК спектры носят более сложный характер; нек-рые ко-валентные нитраты летучи при комнатной т-ре, а при растворении в воде частично разлагаются с выделением оксидов азота.
Нитраты Na, К (натриевая и калиевая селитры) встречаются в виде прир. залежей.
Анализ нитратов на нитрат-ион основан на его восстановлении до NH 3 сплавом Деварда и поглощении NH 3 титрованным р-ром к-ты либо на осаждении в виде нитроннитрата с помощью нитрона.
Н итраты применяют во мн. отраслях пром-сти. Аммония нитрат (аммиачная селитра)-осн. азотсодержащее удобрение; в качестве удобрений используют также нитраты щелочных металлов и Са. Нитраты-компоненты ракетных топлив. пиротехн. составов, травильных р-ров при крашении тканей; их используют для закалки металлов, консервации пищевых продуктов, как лекарственные средства и для получения оксидов металлов. См. также Калия нитрат, Натрия нитрат и др.
Лит.: Addison С. С., Logan N.. Anhydrous metal nitrates, «Advances Inorganic Chemistry and Radiochemistry», 1964, v. 6, p. 72-142. П.М. Чукуров.
Нитрат
 | |||||||||||||||||||||||||||||||||||||||||||
| Имена | |||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Систематическое название ИЮПАК Добавка нитратов дает положительные результаты при тестировании работоспособности при упражнениях на выносливость. [3] Прием больших доз нитрата в форме чистого нитрата натрия или свекольного сока у молодых здоровых людей быстро увеличивает концентрацию нитратов в плазме примерно в 2-3 раза, и эта повышенная концентрация нитратов может сохраняться в течение как минимум 2 недель. Повышенный уровень нитратов в плазме стимулирует выработку оксида азота. Оксид азота является важной физиологической сигнальной молекулой, которая используется, среди прочего, в регуляции кровотока в мышцах и дыхания митохондрий. [4] КолбасыНитраты производятся рядом видов нитрифицирующих бактерий в естественной среде с использованием аммиака или мочевины в качестве источника азота. Нитратные соединения для пороха исторически производились в отсутствие источников минеральных нитратов с помощью различных процессов ферментации с использованием мочи и навоза. МетгемоглобинемияНитраты не действуют на младенцев и беременных женщин. [11] [12] Синдром синего ребенка вызывается рядом других факторов, таких как расстройство желудка, например, диарейная инфекция, непереносимость белков, токсичность тяжелых металлов и т. Д., При этом нитраты играют второстепенную роль. [13] Стандарты питьевой водыВ Законе о безопасной питьевой воде Агентство по охране окружающей среды США установило максимальный уровень загрязнения питьевой водой 10 мг / л или 10 частей на миллион нитратов. [14] Водная токсичностьВ пресноводных или устьевых системах вблизи суши концентрация нитратов может достигать смертельных для рыб концентраций. Хотя нитраты намного менее токсичны, чем аммиак, [16] уровни нитратов более 30 ppm могут подавлять рост, ослаблять иммунную систему и вызывать стресс у некоторых водных видов. [17] Нитратная токсичность остается предметом споров. [18] Симптомы отравления нитратами у домашних животных включают учащенное сердцебиение и учащенное дыхание; в запущенных случаях кровь и ткани могут стать синими или коричневыми. Корм можно проверить на содержание нитратов; обработка состоит из дополнения или замены существующих запасов материалом с более низким содержанием нитратов. Безопасные уровни нитратов для различных видов скота следующие: [19]
Контроль измерений проводят на оборудовании: UNICO 2100. Распространённость: нитраты являются одними из основных соединений азота, который, будучи биогенным элементом, широко распространён в биосфере. Нитраты — это промежуточная стадия трансформации азота, поэтому данные соединения присутствуют во всех природных водах, попадая туда в процессе окисления и трансформации органического вещества. Повышенное содержание нитратов в воде сопряжено с активным применением этой формы азота в качестве минерального удобрения при выращивании практически всех агрономически ценных культур (овощи, зерновые, лен, хлопок и так далее). НормированиеНесмотря на то, что азот сам по себе важен и необходим для любого живого организма, нитратная его форма не играет положительной роли в организме человека. Поэтому в вашей питьевой воде по возможности нитратов быть не должно.
Повышенное содержание нитратов в воде говорит о смещении баланса цикла азота и о возможном развитии процессов эвтрофикации водоёма. Также рост концентрации нитратов служит индикатором снижения содержания в воде растворённого кислорода — это особенно актуально для владельцев аквариумов. Поливная вода, в свою очередь, может (а в некоторых случаях даже должна) содержать в себе нитратный азот для обеспечения роста и развития растений. Предельно допустимая концентрация (ПДК) нитрат-иона в различных водных объектах
Польза и вредОпасность для организма представляют не сами нитраты, а продукты их трансформации: нитриты и нитрозамины. Нитратный азот в пищеварительном тракте и полости рта трансформируется в нитритный под действием фермента нитратредуктазы. В присутствии, например, мяса, активно образуются нитрозамины. Образование продуктов уменьшается при попадании нитратов в организм совместно с веществами, обладающими антиоксидантными свойствами — например, с витамином С. Положительна роль нитратов (спорно)Через нитриты и при поступлении отдельно от мясной пищи: они окисляются до оксида азота, который поступает в кровь, приводит к расширению сосудов и нормализации кровяного давления. Отрицательная роль нитратовПри метаболизме до нитритов: При метаболизме до нитрозаминов: Методы очистки водыИонный обмен. В результате использования ионообменных смол (специфических анионитов) в воде происходит замена нитратов на хлориды. Поскольку нитраты не имеют положительной роли их можно убирать из воды полностью. Этот метод мало распространён, т.е. применяется редко, поскольку аниониты распространены меньше, чем катиониты (смолы для фильтрации катионов). Обратный осмос. Вместе с другими веществами обратный осмос убирает из воды нитраты. Этот метод используется чаще остальных для очистки воды от нитратов. При использовании реминерализатора убедитесь, что соли в нем не содержат нитраты.
Нитраты в воде и методы удаленияНитраты в воде и методы удаления. Нитраты — это соли азотной кислоты, хорошо растворимые в воде. В воде эти соли легко распадаются на ионы (заряженные частицы) и существуют в «свободной» форме: в виде нитрат-ионов NO3—. Заряд у нитрат-ионов отрицательный, поэтому они называются анионы (ионы с отрицательным зарядом). Источники появления нитратов в воде Существуют и другие причины, из-за которых в водоносных горизонтах находится вода с нитратами с превышенным уровнем допустимых норм. Источником заражения выступают: — недопустимо близкое соседство скважины с частным туалетом, септиком, баней или выгребной ямой; — применение бытовой химии, после чего отработанный раствор сливают попадает в грунт без очистки; — обустройство питьевой скважины неподалёку от массовых захоронений, кладбищ; — завышенная концентрация удобрений для роста огородных культур; — городские коммунальные отходы, промышленный мусор. Нитраты входят в 3 класс опасности, по нормам СанПин предел в 45 мг/дм3. Содержание в воде нитратов может колебаться в зависимости от сезона. Ещё большую опасность для здоровья человека представляют производные нитратов – нитриты. Нитриты относится ко 2 классу опасности, уровень содержания примесей по требованиям СанПин не должно превышать 3 мг/дм3 соответственно. Нитраты и нитраты могут накапливаться в организме. Поэтому, с целью обезопасить собственное здоровье, при употреблении воды из скважины лучше придерживаться минимальных значений. Влияние нитратов на организм человека. Находясь в организме, нитраты взаимодействуют с гемоглобином. В результате химической реакции гемоглобин в крови человека замещается метгемоглобином. Новое соединение не способно насытить клетки тела необходимым кислородом, что вызывает ряд негативных последствий. Кислородное голодание сопровождается рядом неприятных симптомов: развивается анемия; человека сопровождает постоянное чувство усталости; длительное воздействие нитратов в дозах, значительно превосходящих нормы, провоцирует обмороки и в крайних случаях заканчивается летальным исходом. Кроме этого, регулярное употребление воды с содержанием нитратов выше установленных значений, может спровоцировать: развитие злокачественных образований; появление аллергических реакций; всевозможные раздражения на поверхности кожи и слизистых оболочках; оказывать угнетающее действие на функционирование щитовидной железы; нарушить работу нервной системы; проблемы с ЖКТ. Методы очистки воды На сегодняшний день широко применяется три метода: 1.- удаление нитратов из воды анионообменными смолами: 2.- удаление нитратов из воды обратным осмосом. 3.- фильтрование воды через цеолит. Применение анионообменных смол Поскольку у частицы есть заряд, то здесь её можно поймать, так как отрицательный заряд притягивается к положительному. Для этого разработаны специальные вещества — нитрат селективные (избирающие нитраты) анионообменные смолы, то есть смолы, которые производят обмен нитрат-анионами. Анионообменная смола — это длинная органическая молекула, на которую «подвешены» активные центры с положительным зарядом, защищённым слабо держащимся ионом с отрицательным зарядом. Сильноосновные аниониты (в хлористой форме) селективны последовательно к: сульфатам→ нитратам → хлоридам → бикарбонатам. При использовании данной загрузки необходимо тщательно контролировать объем воды, который проходит через фильтр с анионитами. Это связано с тем, что со временем в процессе фильтрации накопленные нитраты начинают вытесняться. В итоге концентрация нитратов повышается до уровня исходной воды. То есть, если превысить расчётный объем воды, возможен не только проскок нитратов, но и сброс их из фильтра в воду. Необходимо всегда производить точный расчёт обменной ёмкости, так как от этого зависит качество потребляемой воды и работа всей установки. Регенерацию проводят до того, как начнётся проскок нитратов в фильтрат. Если жёсткость поступающей на установку воды выше 2 мг экв/л, ее необходимо предварительно умягчать, так как сильноосновные аниониты не удаляют ионы кальция и магния. В противном случае при регенерации анионита в его массе будут скапливаться труднорастворимые соединения, что повлечёт за собой снижение ёмкости анионита. Очерёдность фильтров при этом очень важна! Сначала снижаем жёсткость, потом удаляем нитраты. Применение нитратселективных анионитов Желательно использовать такую смолу даже при большом количестве сульфатов в воде, так как она избирательна, прежде всего по отношению к нитратам. Селективность данных анионитов: нитраты→сульфаты→хлориды→бикарбонаты. Объёмная ёмкость данной загрузки ниже стандартной смолы. Нитратселективная также как стандартная смола может вызвать сброс нитратов, если позволить выйти за ее расчётный запас обменной емкости, селективная к нитратам смола может вызвать сброс сульфатов, а позже и нитратов, если вовремя не произвести ее регенерацию. Вывод: тип анионита для очистки воды от нитратов выбирают на основании информации о содержании в исходной воде нитратов и сульфатов: ▫ если содержание сульфатов не превышает содержание нитратов, целесообразно использовать стандартные высокоосновные аниониты; ▫ если концентрация сульфатов превышает концентрацию нитратов, более целесообразно применять нитратселективные аниониты. Определение содержания нитратов и расчеты времени работы сменных картриджей или анионообменной смолы осложняется тем, что их концентрация может меняться, необходимо вовремя отследить увеличение, чтобы продлить ресурс фильтрующей загрузки. Важен постоянный регулярный контроль и соответствующая корректировка работы установки. Применение обратного осмоса Обратный осмос считается одним из наиболее эффективных способов очистки воды не только от нитратных, но и других соединений, которые загрязняют воду. фильтрование воды через цеолит Следующий вариант очистки воды от нитратов предполагает использование в качестве загрузки природных минеральных сорбентов (шунгита) или молекулярных сит (цеолитов). Цеолиты – синтетические или природные адсорбенты с регулярной структурой пор, представляющие собой алюмосиликаты натрия, калия либо иных элементов. В промежутках кристаллического каркаса расположены гидратированные положительные ионы щелочных и щелочно-земельных металлов, компенсирующих заряд каркаса, и молекулы воды. Общая химическая формула цеолитов: Ме2/n[(Аl203) x (Si02)y].Н20, где Me – катион щелочного металла; n – его валентность. В качестве катионов природные цеолиты чаще всего включают натрий, калий, кальций, реже – магний, барий, стронций. Кристаллическая структура цеолитов образована тетраэдрами Si04 и Аl04. Поскольку цеолит обладает способностью поглощать или пропускать через кристаллический каркас молекулы других химических соединений, он играет роль своего рода молекулярного сита. Также цеолиты относят к ионообменникам катионного типа, то есть они могут очищать воду от тяжёлых металлов. И если сравнивать с синтетическими смолами, то этот способ лучше избавляет жидкость от ионов цезия, свинца, кадмия, стронция. При очистке воды от нитратов, например, из скважины, природные цеолиты используются в виде порошков. Отработавший цеолит подвергают неоднократной регенерации при помощи исходный воды либо солевого раствора – выбор зависит от целевого использования. Ниже показана степень эффективности очистки цеолитом от загрязнений. Эффективность водоочистки цеолитом по органическим и неорганическим загрязнителям: № Вредные вещества Степень очистки, % Хлор (хлорид-ион) 91,2 Но не стоит обольщаться, что только при помощи одного цеолита удастся справиться со всеми названными загрязнениями. Причина кроется в том, что структура этого минерала обладает различными пустотами, которые соответствуют разным веществам. Например, цеолит, справляющийся с нефтепродуктами, будет бесполезен при очистке воды от нитратов только из-за различной геометрии веществ. Наука | Научпоп6.1K постов 68.6K подписчика Правила сообществаВНИМАНИЕ! В связи с новой волной пандемии и шумом вокруг вакцинации агрессивные антивакцинаторы банятся без предупреждения, а их особенно мракобесные комментарии — скрываются. Основные условия публикации — Посты должны иметь отношение к науке, актуальным открытиям или жизни научного сообщества и содержать ссылки на авторитетный источник. — Посты должны по возможности избегать кликбейта и броских фраз, вводящих в заблуждение. — Научные статьи должны сопровождаться описанием исследования, доступным на популярном уровне. Слишком профессиональный материал может быть отклонён. — Видеоматериалы должны иметь описание. — Названия должны отражать суть исследования. — Если пост содержит материал, оригинал которого написан или снят на иностранном языке, русская версия должна содержать все основные положения. Не принимаются к публикации — Точные или урезанные копии журнальных и газетных статей. Посты о последних достижениях науки должны содержать ваш разъясняющий комментарий или представлять обзоры нескольких статей. — Юмористические посты, представляющие также точные и урезанные копии из популярных источников, цитаты сборников. Научный юмор приветствуется, но должен публиковаться большими порциями, а не набивать рейтинг единичными цитатами огромного сборника. — Посты с вопросами околонаучного, но базового уровня, просьбы о помощи в решении задач и проведении исследований отправляются в общую ленту. По возможности модерация сообщества даст свой ответ. — Оскорбления, выраженные лично пользователю или категории пользователей. — Попытки использовать сообщество для рекламы. — Многократные попытки публикации материалов, не удовлетворяющих правилам. — Нарушение правил сайта в целом. Окончательное решение по соответствию поста или комментария правилам принимается модерацией сообщества. Просьбы о разбане и жалобы на модерацию принимает администратор сообщества. Жалобы на администратора принимает @SupportComunity и общество пикабу. интересно, а сколько они служат? и как на них можно по считать время регенирации. Подумалось тут.ХедХантер и кладменыМотивации пост. а в пустыне она вообще бесценна. Ответ на пост «Не прокатило»у всех есть такие родственники. есть у меня замечательный дядя, которого я видел последний раз лет в 10. Спустя 20 лет он приехал в гости. По дороге его уставший от жизни жигуль тройка немного рыгнул трамблером. Приехал к нему с подкатом, жигуля погрузили и поехали на место семейной сходки. по приезду дядя очень нахваливал мою машину, а потом, уже за столом, выдал что дарит мне свой жигуль: мол хоть и ломается, но это уже почти ретро и скоро я её смогу продать за все деньги мира. Ну пьяные базары, обычное дело. потому радуйтесь что проебали отношения с таким замечательнейшим родственником 🙂 В свете последних событий.Рамзан Кадыров замечен в сепаратизме?Как все уже знают, Кадыров пригрозил силой отнять у ингушей их земли. Как это: часть страны решила отобрать территорию у другой части этой же страны? Интересно, почему на него не заводят дело за призывы к силовому захвату или отчуждение территории? А ведь это сепаратизм. Развал СССР тоже начался с взаимных претензий его республик. Если какой-то регион России, собирается силой захватить другой регион, то это уже не субьект Российской Федерации. Это самостоятельная государственная единица. Как вы считаете, можно ли расценивать действия Рамзана Кадырова как прямой отказ подчиняться действущему законодательству России и проявлением сепаратизма? Прошу юридической помощи, напали чеченцы в метроНитратыСоли азотной кислоты называют нитратами, которые в основном используются в качестве удобрений в сельском хозяйстве и как окислители, например при производстве фейерверков или в химическом синтезе. Соли азотной кислоты являются ионными соединениями, состоящие из положительно заряженных ионов металлов. Нитраты образуются при взаимодействии металлов, оксидов, карбонатов или гидроксидов металлов с разбавленной азотной кислотой. Свойства и использование нитратовНитраты в основном представляют собой бесцветные кристаллические твердые вещества, которые разлагаются под воздействием термической нагрузки. Нитраты щелочных металлов образуют нитриты и кислород, а нитраты тяжелых металлов превращаются в оксиды. Как в случае нитрата аммония, термическое разложение может происходить со взрывом. Термическое разложение нитратов играет решающую роль в воспламенении фейерверков. Нитраты часто являются хорошими окислителями. В отличие от расплавов, водные растворы не обладают окислительным действием. Удобрения, содержащие нитраты, используются для покрытия азотного дефицита растений. Чтобы предотвратить слишком быстрое вымывание растворимых нитратов из почвы, они используются в соответствующих комбинированных удобрениях, которые выделяют ионы нитрата очень медленно. Важным сырьем для этих удобрений является нитрат натрия, нитрат калия, нитрат кальция и аммиачная селитра. Обнаружение нитрат-ионаНитраты не могут быть обнаружены реакциями осаждения. По этой причине были разработаны тест-полоски, которые вызывают характерные цветовые реакции с нитрат-ионами. Другой простой способ обнаружения нитрат-ионов — это так называемый кольцевой тест. Раствор, который нужно проверить, смешивают с несколькими каплями раствора сульфата железа (II). Раствор покрывают концентрированной серной кислотой (осторожно!). Серная кислота имеет более высокую плотность, чем водный раствор, и оседает на дне пробирки. На границе раздела образуется кольцо коричневого цвета. Нахождение в природе и применениеНитрат калия встречается в природе редко и должен производиться из нитрата натрия. Он также является важным компонентом черного порошка, смеси 10% мелкоизмельченной серы, 15% молотого древесного угля и 75% нитрата калия. Он использовался с XII века в Китае и с XIV века в Европе в качестве взрывчатого вещества и метательного вещества в пушках и мушкетах. Приблизительно 2300 литров газообразных продуктов реакции образуются из одного килограмма черного пороха. Нитрат калия используется в салютах для осветительных приборов и как компонент холодных смесей. Другой важный нитрат — это нитрат серебра, который можно получить путем реакции концентрированной азотной кислоты с серебром. Полученный таким образом нитрат серебра используется для гальванического серебряного покрытия. Он также используется для удаления новообразований и в качестве важного реагента в аналитической химии, например для обнаружения галогенид-ионов (хлорид, бромид, йодид). Реакция обнаружения основана на том, что раствор нитрата серебра добавляют по каплям к кислому раствору пробы. В присутствии упомянутых галогенидов образуется галогенид серебра, который плохо растворяется в воде и выпадает в виде осадка. Хлорид серебра белый, бромид серебра слегка желтый, а йодид серебра интенсивно желтый.
| |||||||||||||||||||||||||||||||||||||||||||