кариотип стертой формы дисгенезии гонад
Публикации в СМИ
Дисгенезия гонад
Дисгенезия гонад — группа наследственных заболеваний с нарушением тканевой структуры половых желёз; в зависимости от хромосомного пола различают XX и XY типы дисгенезии.
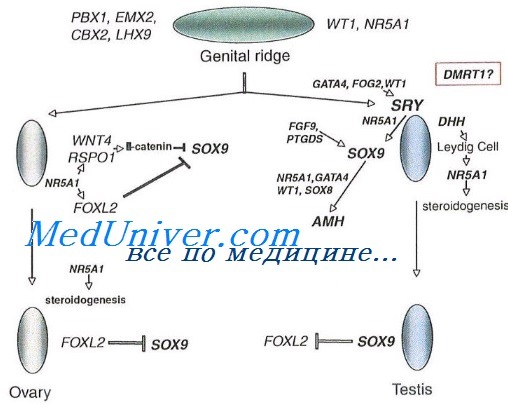
• Дисгенезия гонад, XY тип •• (306100, Xp22.11–p21.2, гены GDXY, TDFX, SRVX, À ), (233420, r ), (233430, r ) — при рождении пациенты с XY женским типом дисгенезии гонад кажутся нормальными девочками, однако у них не развиваются вторичные половые признаки в пубертатном возрасте, отсутствуют менструации, и они имеют гонады в виде полосок. Половой хроматин отрицательный, кариотип 46,XY •• Тип SRY (*480000, Y-сцепленное) — аббревиатура происходит от термина «участок Y-хромосомы, ответственный за формирование пола» (Sex-determining Region Y). Этот участок содержит гены, кодирующие фактор транскрипции, мутации или делеции которых приводят к нарушению половой дифференцировки у мальчиков.
• Дисгенезия гонад, XX тип (дисгенезия яичника гипергонадотропная с нормальным кариотипом, #233300, 2p21–p16, ген рецептора к ФСГ FSHR, ODG1, 136435, r ). Клинически: дисгенезия гонад, первичная аменорея, остеопороз, повышение уровня гонадотропинов. Синдром Перро (*233400, r ): дисгенезия гонад XX типа с глухотой. Клинически: нейросенсорная тугоухость, нистагм, ограничение движений глаз, дисгенезия гонад, первичная аменорея, остеопороз, «полая» стопа, повышение уровня гонадотропинов, атаксическая походка, низкорослость.
МКБ-10 • Q50 Врождённые аномалии [пороки развития] яичников, фаллопиевых труб и широких связок
Код вставки на сайт
Дисгенезия гонад
Дисгенезия гонад — группа наследственных заболеваний с нарушением тканевой структуры половых желёз; в зависимости от хромосомного пола различают XX и XY типы дисгенезии.
• Дисгенезия гонад, XY тип •• (306100, Xp22.11–p21.2, гены GDXY, TDFX, SRVX, À ), (233420, r ), (233430, r ) — при рождении пациенты с XY женским типом дисгенезии гонад кажутся нормальными девочками, однако у них не развиваются вторичные половые признаки в пубертатном возрасте, отсутствуют менструации, и они имеют гонады в виде полосок. Половой хроматин отрицательный, кариотип 46,XY •• Тип SRY (*480000, Y-сцепленное) — аббревиатура происходит от термина «участок Y-хромосомы, ответственный за формирование пола» (Sex-determining Region Y). Этот участок содержит гены, кодирующие фактор транскрипции, мутации или делеции которых приводят к нарушению половой дифференцировки у мальчиков.
• Дисгенезия гонад, XX тип (дисгенезия яичника гипергонадотропная с нормальным кариотипом, #233300, 2p21–p16, ген рецептора к ФСГ FSHR, ODG1, 136435, r ). Клинически: дисгенезия гонад, первичная аменорея, остеопороз, повышение уровня гонадотропинов. Синдром Перро (*233400, r ): дисгенезия гонад XX типа с глухотой. Клинически: нейросенсорная тугоухость, нистагм, ограничение движений глаз, дисгенезия гонад, первичная аменорея, остеопороз, «полая» стопа, повышение уровня гонадотропинов, атаксическая походка, низкорослость.
МКБ-10 • Q50 Врождённые аномалии [пороки развития] яичников, фаллопиевых труб и широких связок
Кариотип стертой формы дисгенезии гонад
Этиологические факторы первичной аменореи достаточно разнообразны. Как было сказано выше, к четырем основным причинам первичной аменореи относятся следующие:
• дисгенезия гонад (почти половина всех случаев);
• мюллерова агенезия (например, врожденное отсутствие матки и влагалища);
• гипоталамические расстройства, в том числе связанные с избыточной физической нагрузкой и нарушениями питания;
• конституциональная задержка полового созревания. К другим, более редким причинам первичной аменореи относятся анатомические особенности (неперфорированная девственная плева или поперечная перегородка влагалища), синдром тестикулярной феминизации, а также врожденные дефекты синтеза гонадотропинов или врожденная резистентность яичников к гонадотропинам. Некоторые из перечисленных нарушений рассмотрены в данной статье.
Дисгенезия гонад как причина первичной аменореи
Термин «дисгенезия гонад» в общем используют для описания всех форм нарушения развития гонад у пациентов с нормальным кариотипом (46ХХ; 46XY), а также ряда аномальных или мозаичных нарушений, наиболее частое из которых — синдром Тернера (45X0). Гонады в таких случаях представляют собой функционирующие фиброзные тяжи.
Чистая форма дисгенезии гонад. Для чистой формы дисгенезии гонад характерны: женский фенотип, наличие гонад в виде фиброзных тканей, наружные половые органы, развитые по женскому типу, нормально развитые мюллеровы структуры и кариотип 46XY (синдром Суайра) или 46ХХ. Это гетерогенное состояние может быть результатом структурных нарушений в Y-хромосоме, мутации гена SRY (мутации в участке Y-хромосомы, при которой происходит нарушение половой дифференцировки у мальчиков) или мутации аутосомного гена.
Смешанная дисгенезия гонад. Смешанная дисгенезия гонад развивается вследствие хромосомного мозаицизма. В кариотипе у таких больных отмечают частичную моносомию по половым хромосомам с отсутствием или аномалией второй половой хромосомы, причем кариотип чаще всего 45X0/46XY.
Фенотипически это могут быть и женщины, и мужчины, и псевдогермафродиты — в зависимости от отношения доли клеток с кариотипом 45X0 к клеткам с нормальным (46ХХ или 46XY) кариотипом в каждой из гонад. У этих пациентов обнаруживают нарушение половой дифференцировки.
Возможны варианты наличия фиброзированной половой железы с одной стороны и недостаточно развитой или нормальной — с другой в сочетании с ипсилатеральным развитием вольфова протока или мюллеровых структур. Большинство таких пациентов имеют низкий рост, а у одной трети выявляют признаки синдрома Тернера.
У большинства пациенток с дисгенезией гонад никогда не бывает менструаций. Эта группа больных составляет около 40% всех случаев первичной аменореи, и у 40% из них обнаруживают аномалии кариотипа. При нарушениях кариотипа синдром Тернера (46,Х0) диагностируют в 50% случаев, мозаичный кариотип X0/XY — в 25%.
Больных с дисгенезией гонад и нормальным кариотипом необходимо также обследовать для исключения нейросенсорной тугоухости и синдрома инактивированной Х-хромосомы. Поиск этих клинических связей особенно важен, если в семейном анамнезе есть случаи преждевременной яичниковой недостаточности (ПЯН).
Лечение дисгенезии гонад
Подростки с дисгенезией гонад нуждаются в гормональной терапии с целью стимуляции роста и своевременного полового развития. В течение первого года применяют эстрогены в низких дозах (0,25-0,3 мг/сут) иногда в сочетании с гормоном роста, чтобы индуцировать нормальное половое развитие, минимизировать эффекты раннего закрытия эпифизов костей и обеспечить нормальный рост. Приблизительно через год терапии эстрогенами подключают препараты прогестерона (например, медроксипрогестерон по 5 мг/сут или иную форму прогестерона), который используют во второй половине месяца.
Дозы эстрогенов постепенно увеличивают, чтобы за 2-3 года больные достигли половой зрелости.
Для поддерживающей терапии используют 2 мг/сут эстрадиола или 1,25 мг/сут конъюгированных эстрогенов. Если назначено лечение гормоном роста, эстрогены можно назначить раньше. Если же гормон роста не используется, начало лечения эстрогенами может быть отсрочено до 14-15 лет, но не позже. Применение этинилэстрадиола повышает риск артериальной гипертензии у больных с синдромом Тернера. Больным с Y-хромосомой с целью предотвращения малигнизации показана гонадэктомия.
Благодаря возможности использования донорской яйцеклетки у больных может наступать беременность. Однако повышенные требования, которые беременность предъявляет к сердечно-сосудистой системе (с учетом того, что распространенность ее аномалий у этих больных достигает 25-50%), становятся у таких больных существенным фактором риска. В докладе ASRM говорится, что риск развития расслаивающей аневризмы аорты и ее разрыва составляет 2% и выше, а риск смерти во время беременности повышается в 100 раз.
Выявление любых тяжелых аномалий сердечно-сосудистой системы необходимо рассматривать как противопоказание для донации ооцитов. Даже при отсутствии подобных аномалий сохраняется риск расслаивающей аневризмы аорты во время беременности.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Нарушения полового развития
Преждевременное половое развитие (ППР)
ППР называют появление вторичных половых признаков и менструаций у девочек в возрасте до 8 лет.
ППР клинически может проявляться в виде изосексуальной формы, т.е., когда у девочек появляются признаки полового развития свойственные ее полу, и в виде гетеросексуальной формы, т.е., когда у девочек возникают признаки, свойственные мужскому половому развитию.
Изосексуальное преждевременное половое развитие может быть истинным и ложным.
Церебральная патология у девочек с ППР может иметь органический и функциональный характер.
Причинами органического поражения центральной нервной системы (ЦНС) являются:
К редким формам органического поражения нервной ткани относятся опухоли мозга. При органическом поражении мозга ППР, как правило, развивается после появления или на фоне церебральной и неврологической симптоматики.
Церебральное ППР протекает в виде полной или неполной формы. Для полной формы характерно развитие вторичных половых признаков и менструации. При этом последовательность появления, развития вторичных половых признаков и наступления менструации не отличается от таковых при физиологическом половом созревании (сначала увеличиваются молочные железы, затем появляется оволосение на лобке и в подмышечных впадинах, и только после этого появляются менструации).
Конституциональная форма истинного преждевременного полового развития. При этой форме ППР не удается выявить неврологической, церебральной патологии. Преждевременным является только возраст, в котором начинается процесс полового созревания. Темп и последовательность этого процесса не нарушаются. Отмечается наследственный характер конституционального ППР.
Яичникова форма (ложная) ППР.
Яичниковая форма ППР обусловлена секрецией половых гормонов опухолевой тканью яичников. При этом гипоталамус и гипофиз остаются незрелыми. Поэтому эта форма ППР называется ложной.
Диагностика преждевременного полового развития не представляет затруднений. Обычно диагноз ставят при объективном осмотре ребенка. Причину, вызвавшую ППР, установить сложнее. Тщательное обследование девочек включает: гинекологическое исследование с подробной регистрацией состояния вульвы, шейки матки, симптома «зрачка», натяжения шеечной слизи, кольпоцитологии. Важное значение для диагностики имеют данные о динамике полового развития.
Девочкам с клиническими проявлениями ППР показано пристальное наблюдение у детских гинекологов для своевременного выявления причин, вызвавших эту патологию развития. К числу обязательных методов обследования относятся:
1. ультразвуковое исследование органов малого таза;
2. лапароскопия при сомнительных данных ультразвукового исследования;
3. неврологическое исследование с применением ЭЭГ и РЭГ;
4. определение уровня половых гормонов в плазме крови;
5. изучение тестов функциональной диагностики в динамике обследования;
6. определение костного возраста (рентгенограмма кистей рук и черепа).
Вопросы терапии ППР имеют два аспекта: лечение патологии, вызвавшей ППР, и торможение процесса ППР.
При церебральной форме ППР, обусловленной последствиями нейроинфекции, родовой травмы, асфиксии, лечение представляет чрезвычайно сложную задачу. Большая роль отводится профилактике асфиксии и родовой травмы. Правильное ведение беременности и родов предотвращает нарушения ЦНС.
Вопрос о торможении процесса ППР возникает в связи с тем, что дети могут быть травмированы своим необычным для данного возраста видом и особым отношением сверстников и взрослых. В подобной ситуации целесообразнее избрать путь немедикаментозного воздействия и постараться отвлечь девочек от сознания своей исключительности беседой, разъяснением, даже временной изоляцией от детского коллектива.
Все вышесказанное относится только к конституциональной и церебральным формам ППР. Опухоли яичников подлежат удалению с последующим тщательным гистологическим исследованием.
Фолликулярную кисту яичников, вызвавшую симптомы ППР, по современным представлениям, удалять не рекомендуется, т.к. они самостоятельно подвергаются обратному развитию.
Обследование и лечение девочек с ППР необходимо проводить в условиях крупных стационаров, оснащенных соответствующим оборудованием и имеющих квалифицированных специалистов.
Гетеросксуальное преждевременное половое развитие.
Гетеросексуальным ППР называют появление признаков полового созревания противоположного (мужского) пола у девочек в первом десятилетии жизни. Наиболее частой клинической формой гетеросексуального ППР является патология, получившая название «адреногенитальный синдром» (АГС), который известен как врожденная гиперплазия надпочечников, ложный женский гермафродитизм или ППР девочек по гетеросексуальному типу.
АГС явуляется следствием врожденного дефицита ферментных систем, участвующих в синтезе стероидных гормонов надпочечников. Этот генетический дефект имеет рецесивный путь наследования, носителями дефектного гена могут быть и мужщины и женщины.
В зависимости от характера дефицита ферментных систем АГС делится на 3 формы, общим симптомом которых является вирилизация.
В первом десятилетии жизни у девочек с врожденной формой АГС развивается картина преждевременного полового развития по гетеросексуальному типу.
Задержка полового развития (ЗПР)
Церебральная форма задержки полового развития.
Клиническая картина. В настоящем разделе описаны церебральные формы ЗПР, при которой основной и порой единственной жалобой является нарушение полового развития. Девушки с ЗПР отличаются от сверстниц не только недостаточным развитием вторичных половых признаков и аменореей, но и отсутствием «феминизации фигуры», т. е. распределением жировой и мышечной ткани по женскому типу и изменений в строении таза. У девушек с ЗПР антропометрическими исследованиями установлено евнухоидное телосложение: удлинение рук и ног, относительно короткое туловище, уменьшение поперечных размеров таза. Рост их обычно выше, чем у сверстниц. Хронологический возраст обычно опережает биологический (костный). Дефицит эстрогенов, играющих важную роль в процессах окостенения, является причиной затягивания у таких девушек периода роста в длину.
Исключение составляют девушки с гиперпролактинемией (пролактинома гипофиза или функциональная гиперпролактинемия). У этих пациенток обычно признаком ЗПР является первичная аменорея в сочетании с нерезко выраженной гипоплазией матки. Телосложение, длина тела соответствует у них соответствуют возрастным нормативам, а молочные железы равиты правильно или слегка гиперплазированы вследсткие гиперпролактинемии.
Яичниковая форма задержки полового развития.
Эта форма наименее изучена, очевдно, в связи с ее редкостью. При ней не установлено хромосомной патологии и изменения содержания полового хроматина. В строении яичников кроме уменьшения фолликулярного аппарата, изменений не выявлено. Подобные яичники являются гипопластическими. Возможно, в патогенезе данной патологии играют определеннную роль детские инфекционные заболевания (коревая краснуха, паротит и др.) или токсические влияния, вызывающие нарушения фолликулярного аппарата или инервации яичников, что приводит к изменению их чувствительности к стимулирующим гормонам гипофиза.
Клиническая картина. Для клинической картины ЗПР при гипопластических яичниках характерны интерсексуальные черты телосложения; несмотря на задержку процессов окостенения эпифизов трубчатых костей, длина тела девочек не превышает обычные возрастные нормативы. Вторичные половые признаки недоразвиты, отмечается также гипоплазия наружных и внутренних половых органов. Характерна первичная аменорея, однако могут быть редкие и скудные менструации.
У больных с ЗПР при подозрении на церебральные формы патологии необходимо неврологическое обследование:
Лечение центральных форм ЗПР является сложной задачей. В разработке комплексного лечения должен участвовать невропатолог. Кроме назначений невропатолога применяется циклическая витаминотерапия, а также, заместительная гормональная терапия, при гипопластических яичниках.
Лечение ЗПР на фоне потере массы тела основано на полноценном питании, в сочетании с психотерапевтическим воздействием, разъяснением вреда «косметической» диеты.
Отсутствие полового развития
СТЕРТАЯ ФОРМА ДИСГЕНЕЗИИ ГОНАД.
В литературе описаны около 60 женщин с мозаичным кариотипом 45,Х/ 46,ХХ, у которых была сохранена репродуктивная функция, однако у 70% из них наступившая беременность закончилась или самопроизвольными выкидышами на разных сроках или рождением детей с пороками развития и хромосомными синдромами.
ЧИСТАЯ ФОРМА ДИСГЕНЕЗИИ ГОНАД.
При этом клиническом варианте дисгенезии гонад соматических уродств и задержки роста нет. Харктерны нормальный рост, отсутствие соматических пороков развития, недоразвитые вторичные половые признаки и выраженный половой инфантилизм. Телосложение варьирует от евнухоидного до интерсексуального. Кариотип больных чаще всего 46,ХХ или 46,ХУ (синдром Свайера). Гонады представляеют собой фиброзные тяжи, в которых иногда имеются элементы стромы.
Причины возникновения чистой формы дисгенезии гонад с кариотипом 46,ХХ не ясны до сих пор.
Диагноз ставят на основании клинической картины заболевания, эхоскопии органов малого таза, определении кариотипа и полового хроматина, лапароскопии.
СМЕШАННАЯ ФОРМА ДИСГЕНЕЗИИ ГОНАД.
Как и при двух описанных выше формах дисгенезии гонад, в диагностике большое значение имеют анамнестические данные и осмотр больных. Обязательными являются определение кариотипа, ультразвуковое исследование половых органов и лапароскопия с биопсией гонад.
Лечение дисгенезии гонад.
Кариотип стертой формы дисгенезии гонад
Отсутствие менархе, развития молочных желез, полового и подмышечного оволосения в возрасте после 16 лет являются симптомами отсутствия полового развития. Причиной данной патологии является аплазия гонад или порок их развития, при которых отсутствует функционально активная гормонопродуцирующая ткань яичников. Половое развитие не наступает у девочек, которым по каким-либо показаниям было произведено удаление яичников в возрасте до 8—10 лет.
Другой причиной отсутствия полового развития является генетически обусловленный порок развития половых желез, называемый дисгенезией гонад.
Дисгенезия гонад — редкая патология, частота ее 1 на 10—12 тыс. новорожденных.
Этиология. Причиной развития дисгенезии гонад являются хромосомные нарушения в виде утраты одной Х хромосомы или ее части. Чаще всего встречаются четыре клинических формы дисгенезии гонад: типичная, или классическая (синдром Шерешевского—Тернера), стертая, чистая и смешанная.
Типичная форма дисгенезии гонад или синдром Шерешевского — Тернера
Для этой формы характерен кариотип 45,Х. Больные отличаются весьма специфической внешностью, которая получила название фенотипа Шерешевского — Тернера. Обязательными симптомами являются низкий рост (до 150 см), короткая широкая шея с низкой линией роста волос, кожные складки, идущие от сосцевидных отростков к акромиальному, высокое небо, низко расположенные ушные раковины, деформация локтевого сустава, широко расставленные соски молочных желез, множественные пигментные пятна на коже. Непостоянными признаками являются аномалии прикуса, косоглазие, третье веко, щитовидная грудная клетка, крыловидные лопатки. У 38% больных встречаются аномалии развития почек и мочеточников, у 16%—пороки развития сердечно-сосудистой системы. Наружные половые органы, также как и внутренние, гипопластичны, имеется выраженный половой инфантилизм. По данным УЗИ, гонады представляют собой тонкие (шириной около 0,3—0,5 см) соединительнотканные тяжи.
Диагностика. Типичные признаки синдрома Шерешевского — Тернера имеются при рождении. Дети, родившиеся в срок, отличающиеся малой массой тела — до 2600—2800 г, своеобразными отеками рук и ног, которые вскоре проходят без лечения. У детей, подростков и взрослых диагноз ставится на основании внешнего вида пациентов, отсутствия полового хроматина.
Стертая форма дисгенезии гонад
Наибольший интерес и сложности в диагностике представляет стертая форма дисгенезии гонад. Само название свидетельствует о значительной вариабельности клинических проявлений этой формы. Причиной заболевания является также наличие хромосомной аномалии в кариотипе больных. Наиболее часто при этом типе дисгенезии гонад имеет мозаичный характер 45,Х/ 46,ХХ. Как правило, тяжесть клинических проявлений зависит от процентного соотношения нормального и аберрантного клеточных клонов. Чем выше процент клона 45,Х, тем ближе больные по внешнему виду и клинической картине заболевания к больным с синдромом Шерешевского—Тернера. Превалирование нормального клеточного клона 46,ХХ сглаживает соматические признаки типичной формы дисгенезии гонад. У больных реже отмечается низкий рост, может наблюдаться недостаточное, но спонтанное развития вторичных половых признаков при наличии первичной аменореи; у 20% больных в нормальные сроки наступает менархе, а у 10% больных отмечают относительно регулярные менструации в течения до 10 лет после менархе, которые затем переходят в олигоменарею и вторичную аменорею. Наружные и внутренние половые органы гипопластичны. При УЗИ и лапароскопии выявляются резко гипопластичные гонады.
В литературе описаны около 60 женщин с мозаичным кариотипом 45,Х/ 46,ХХ, у которых была сохранена репродуктивная функция, однако у 70% из них наступившая беременность закончилась или самопроизвольными выкидышами на разных сроках или рождением детей с пороками развития и хромосомными синдромами.
Чистая форма дисгенезии гонад
При этом клиническом варианте дисгенезии гонад соматических уродств и задержки роста нет. Характерны нормальный рост, отсутствие соматических пороков развития, недоразвитые вторичные половые признаки и выраженный половой инфантилизм. Телосложение варьирует от евнухоидного до интерсексуального. Кариотип больных чаще всего 46,ХХ или 46,ХY (синдром Свайера). Гонады представляют собой фиброзные тяжи, в которых иногда имеются элементы стромы.
Причины возникновения чистой формы дисгенезии гонад с кариотипом 46,ХХ не ясны до сих пор.
Диагноз ставят на основании клинической картины заболевания, эхоскопии органов малого таза, определении кариотипа и полового хроматина, лапароскопии.
При кариотипе 46,ХY отмечается повышенная частота возникновения гормонально—активных опухолей в дисгенетических гонадах.
Смешанная форма дисгенезии гонад
Как и при двух описанных выше формах дисгенезии гонад, в диагностике большое значение имеют анамнестические данные и осмотр больных. Обязательными являются определение кариотипа, ультразвуковое исследование половых органов и лапароскопия с биопсией гонад.

Лечение дисгенезии гонад. Тактика ведения больных зависит от формы дисгенезии гонад и кариотипа больных. В основу терапии должно быть положено правило: наличие кариотипа 46,ХY или мозаицизма с присутствием клеточного клона 46,ХУ либо фрагментов Y—хромосомы является абсолютным показанием к оперативному удалению дисгенетических гонад. Это производится в связи с высоким риском малигнизации при данных формах дисгенезии гонад.
Больным с типичной и чистой формами дисгенезии гонад при кариотипе 46,ХХ проводится заместительная терапия половыми гормонами. Эта терапия необходима для феминизации фигуры, развития молочных желез, полового оволосения, наружных и внутренних половых органов и циклических менструальноподобных выделений. Указанные изменения избавляют девушек от сознания неполноценности и способствуют их социальной адаптации. Но это не единственная причина необходимой подобной терапии. Применение препаратов половых гормонов подавляет выделение гонадотропинов гипофизом и снижает риск развития злокачественного перерождения гонад.
Начало лечения: этинилэстрадиол 0,02-0,1 мг/сут, или конъюгированные эстрогены, 0,3-1,25 мг/сут., назначают внутрь. Лучше начинать с минимальных доз эстрогенов. Чем меньше начальная доза, тем медленнее наступает эффект и тем легче его регулировать. Правильность подбора доз эстрогенов контролируют по уровням ЛГ и ФСГ.
Не позднее, чем через год переходят к заместительной циклической терапии эстрогенами и прогестагенами. Первоначальное лечение эстрогенами и последующее добавление прогестагенов имитируют естественную последовательность событий пубертатного периода. В результате ускоряется наступление вторичных половых признаков и менархе. Если на фоне ежедневного приема эстрогенов появляются маточные кровотечения, циклическую терапию начинают раньше, чем через год.
Схема циклической терапии: эстрогены принимают ежедневно с 1-го по 21-е число каждого календарного месяца. С 12-го или с 15-го числа по 21-е добавляют прогестагены 5-10 мг/сут. внутрь. С 22-го числа до конца месяца прием всех препаратов прекращают, а с 1-го числа следующего календарного месяца цикл лечения повторяют. Вместо отдельных препаратов эстрогенов и прогестагенов можно применять пероральные контрацептивы с низким содержанием эстрогенов. После наступления менархе для поддержания регулярных менструаций переходят на минимальные дозы эстрогенов.