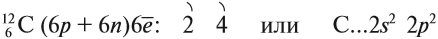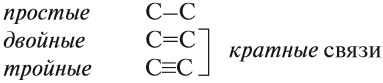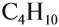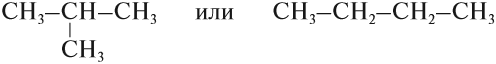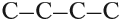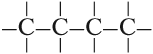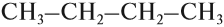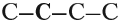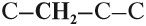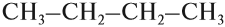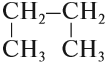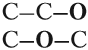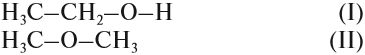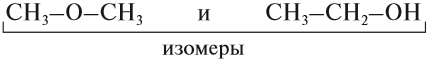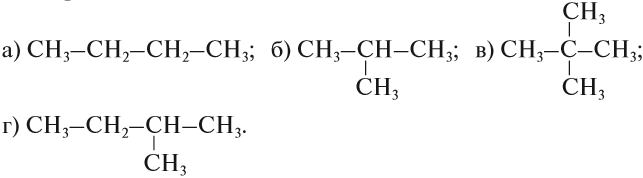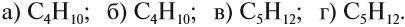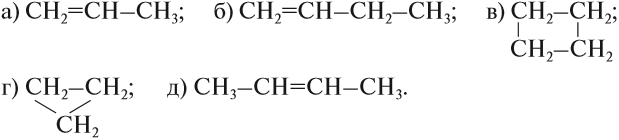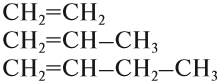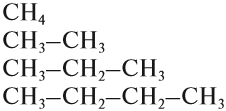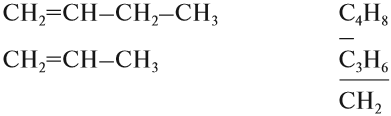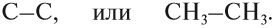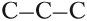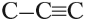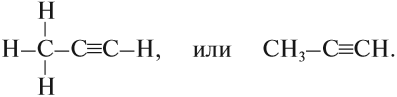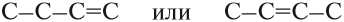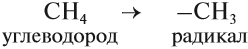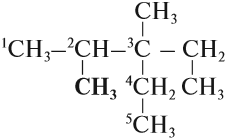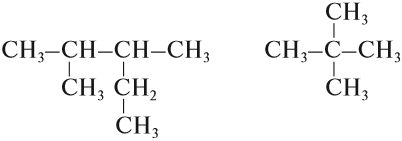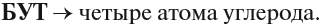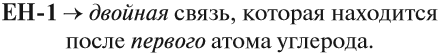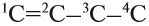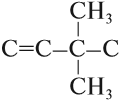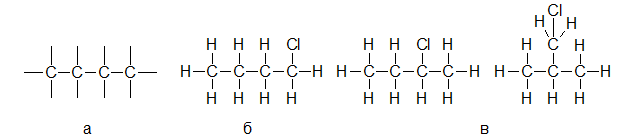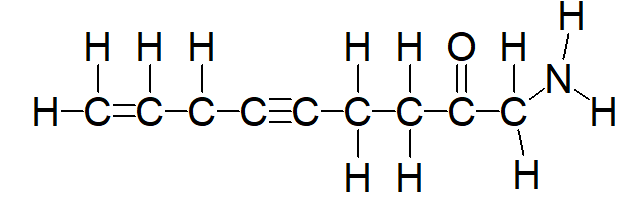Что такое органика
Что такое органика
Неорганические вещества — это химические вещества, которые не являются органическими, то есть они не содержат углерода (кроме карбидов, цианидов, карбонатов, оксидов углерода и некоторых других соединений, которые традиционно относят к неорганическим).
Органические соединения, органические вещества — класс химических соединений, в состав которых входит углерод (за исключением карбидов, угольной кислоты, карбонатов, оксидов углерода и цианидов). Органические соединения, кроме углерода, чаще всего содержат элементы водород, кислород, азот, значительно реже — серу, фосфор, галогены и некоторые металлы (порознь или в различных комбинациях).
Так же под словом органика могут подразумевать
Биопродукты (органические продукты) — продукция сельского хозяйства и пищевой промышленности, изготовленная без использования (либо с меньшим использованием) синтетических пестицидов, синтетических минеральных удобрений, регуляторов роста, искусственных пищевых добавок, а также без использования генетически модифицированных продуктов (ГМО)
Значение слова «органика»
Источник (печатная версия): Словарь русского языка: В 4-х т. / РАН, Ин-т лингвистич. исследований; Под ред. А. П. Евгеньевой. — 4-е изд., стер. — М.: Рус. яз.; Полиграфресурсы, 1999; (электронная версия): Фундаментальная электронная библиотека
орга́ника
1. разг. то же, что органическая химия ◆ Законы органики. Открытия в органике. Экзамен по органике. Энциклопедический словарь, 2009 г. ◆ Итак, органика ― это химия даже не одного элемента, а лишь одного класса соединений этого элемента. В. Станцо, «Углерод», 1969 г. // «Химия и жизнь» (цитата из НКРЯ)
2. органическая материя, органические вещества ◆ Тёплые и богатые органикой воды северо-западной части Южного Каспия захватываются вихрем и перемещаются к северу. Картографирование биологической продуктивности Каспийского моря, 2004 г. // «Геоинформатика» (цитата из НКРЯ) ◆ Под влиянием биохимических и термических процессов органика разлагается и образует нефтяные углеводороды. Андрей Осадчий, «Долгий путь к большой нефти», 2009 г. // «Наука и жизнь» (цитата из НКРЯ)
3. разг. то же, что органическое удобрение (органические удобрения) ◆ Широко применять органику для повышения урожайности свёклы. Удобрять органикой вспаханные земли. Энциклопедический словарь, 2009 г.
4. разг. то же, что органические остатки ◆ Для «скромных» сапрофагов пиршественный стол накрыт щедро: их «меню» — вся отмершая органика. А. Перешкольник, «Солнечная цепь жизни», 1968 г. // «Вокруг света» (цитата из НКРЯ)
5. разг. то же, что ископаемые остатки организмов ◆ В глинистых сланцах Западной Австралии была обнаружена органика, возраст которой составляет 2,7 миллиарда лет. Новости науки, «2009» // «Знание — сила» (цитата из НКРЯ)
6. разг. то же, что живые организмы ◆ Атмосфера планеты раскаляется, вся органика погибает. Сергей Лесков, «Не спасутся даже черти. Создана ещё одна теория о конце света», 2002 г. // «Известия», 2002.06.14 (цитата из НКРЯ)
7. разг. то же, что органичность, естественность ◆ У него уже тогда было то, что нельзя ни сыграть, ни наработать, ни «изобразить» ― какое-то особое «лёгкое дыхание» на сцене и неправдоподобная органика. Парадокс Гвоздицкого, 2003 г. // «Театральная жизнь» (цитата из НКРЯ)
Делаем Карту слов лучше вместе

Спасибо! Я обязательно научусь отличать широко распространённые слова от узкоспециальных.
Насколько понятно значение слова постулированный (прилагательное):
Органика: мифы и реальность
Что такое органика? Внезапная популярность органических продуктов питания, косметики, экодомов и отелей – дань моде или новая философия жизни?
«Органика равно «здоровье». Отсутствие химии», – такие мысли возникают у каждого, кто видит на прилавке продукцию с маркировкой “Organic”.
При изучении темы органики даже сложно было предположить, насколько она связывает воедино сферу жизненных циклов человека и природы.
Органика – это намного больше, чем просто полезные и качественные продукты.
Органическое хозяйство – это целая система производства, способствующая сохранению состояния почвы, экосистем и здоровья людей.
«… Принципы такого хозяйства основаны на экологических процессах, биологическом разнообразии и цикличности, которые адаптированы под местные условия и не терпят использования ресурсов с негативными составляющими. Концепция органического сельского хозяйства заключается в том, чтобы как можно точнее повторить «производство» в естественных экосистемах». В. И. Кочурко, Е. Э. Абарова, В. Н. Зуев «Основы органического земледелия».
Тем не менее, несмотря на конкретное определение, понятие органики «обросло» мифами и теориями, которые нивелируют значимость этого направления в глазах потребителя.
Миф первый и основной: если вырастил сам или приобрел с бабушкиного огорода, значит, продукт чистый и, соответственно, имеет право считаться органическим.
К сожалению, такое утверждение в корне неверно и вот почему: для выращивания органик-продуктов земля не должна обрабатываться минеральными удобрениями и пестицидами минимум 3 года.
Земля должна отдавать витамины и микроэлементы, но после стольких десятилетий бездумного и грубого использования ее плодородный слой попросту истощен, и продукты, произрастающие на такой земле, будут непригодны в пищу, – прямая взаимосвязь между природой и человеком.

Еще одно из главных требований органических стандартов – это чистое соседство. Поясним: даже если бабушка или фермер ухаживают за своим участком в соответствии с правилами органического земледелия, а сосед при этом нещадно удобряет свои владения химией, то у бабушки и фермера земля также становится зараженной! И об органической составляющей на их огородах уже говорить не приходится.
Также важно понимать, что ели коровы, не кормили ли их кормами с вредными примесями/гормонами роста/антибиотиками, в каких условиях они содержатся.
Это лишь малая часть правил для производства органической продукции.
Вывод: то, что выросло у бабушки на огороде, как правило, не является органической продукцией.

Миф второй: маркировочные метки на упаковке, такие как «Экологически чистый», «БИО», «Натуральный продукт», «Органический продукт» – это одно и то же/это маркетинговый ход.
В связи с тем, что нормативно-правовое регулирование в части органической продукции зародилось относительно недавно, возникло множество смешанных понятий, таких как «Эко», «БИО», «Натуральный/фермерский» продукт и т.д., вводящих потребителя в заблуждение и ступор возле прилавка с товарами.
Стоит сразу разграничить эти понятия, чтобы далее вопросов и сомнений в качестве продукции у потребителя не возникало.
Наверное, каждый хоть раз в жизни встречал на упаковке маркировку «экологический/экологически чистый», но мало знает, что такое понятие ничем не подкреплено. Да, продукт, возможно, без ГМО и запрещенных химсоединений, но тогда каждый товар на прилавке был бы удостоен такой маркировки, ведь по законодательству РФ все продукты, допущенные в торговую сеть, прошли проверку соответствующих контрольных органов и являются экологически безопасными. Следовательно, экологически чистое не есть органика.
Дабы приостановить это глобальное «экологическое» веяние, которое вводило в заблуждение людей и создавало конкуренцию настоящим последователям Рудольфа Штайнера (австрийский доктор философии, педагог, лектор и социальный реформатор, также изобрел систему органического земледелия, известную как биодинамическая. – Прим. ред.), в 2005 г. был принят Национальный стандарт Российской Федерации ГОСТ Р 51074-2003 «Продукты пищевые. Информация для потребителей», в пункте 3.5.1.5 которого указано: «Нанесение на пищевую продукцию надписи “Экологически чистый” не допускается». Казалось бы, данный стандарт остановит это злоупотребление маркировками, но не тут-то было: производители прибегли к ухищрениям и стали применять различные приемы для привлечения покупателей, такие как использование в наименованиях продукции приставок или слов «био», «эко», «натуральный» и т. п. Во многих случаях это были маркетинговые приемы, которые не подкреплялись ни новейшими технологиями производства, ни нормативно-правовой базой. Основное заблуждение состоит в том, что если в странах ЕС, в США, Австралии и Новой Зеландии маркировки bio, eco, nature и т.д. законодательно закреплены, то и в РФ эта сертификация действительна. Спешим вас заверить: в России зарубежная сертификация не работает, следовательно, о «био-эко-натуральности» не может быть и речи.
Благо в РФ в 2015 году был введен в действие ГОСТ Р 56508– 2015 «Продукция органического производства. Правила производства, хранения, транспортирования», в котором также указан порядок сертификации и маркировки органической продукции. Следовательно, увидев значок «Органик» с зеленым листиком и наименованием ГОСТа, можете быть уверены: перед вами действительно органический продукт, а не очередная маркетинговая уловка.
Стоит отдельно добавить по поводу органической косметики: на законодательном уровне она не существует, только различные системы добровольной сертификации. Как правило, по евростандартам, таким как «Экосерт» (Ecocert), Институт Этического Сертифицирования (ICEA) и т.д. Но единой системы на все товары нет.
В связи с введенными против РФ санкциями стали развиваться и процветать фермерские хозяйства, и их продукцию все чаще можно встретить на прилавках. Бытует мнение, что качество таких продуктов гораздо лучше, нежели у крупных производителей, антисанитария меньше, а животные – счастливее. В действительности же система реализации не всегда работает на фермера, и ему приходится время от времени прибегать к химии, давать животным больше гормонов роста и антибиотиков, чтобы снизить риски потерь и собственные издержки. Поэтому слово «фермерский» никак нельзя ставить в один ряд с органик-продукцией.
Также нельзя объединять понятия «натуральный» и «органический».
«Натуральный продукт считается таковым, если он произведен природой, а не синтезирован человеком в лаборатории. Но это не означает, что продукт не был выращен и обработан с помощью химических веществ, антибиотиков, гормонов и прочих синтетических препаратов». Сергей Бачин, «Органика. Мифы и реальность».
Поэтому можно сделать вывод, что маркировка “натуральный” к органике абсолютно никакого отношения не имеет.
«На сегодняшний день «органический» — это единственный законодательно закрепленный термин, характеризующий чистую еду, то есть произведенную не в рамках индустриально-химической модели сельского хозяйства». Сергей Бачин, «Органика. Мифы и реальность».
Миф третий: органические продукты стоят дороже обычных.
На данный момент спрос на органические продукты превышает предложение.
Затраты на производство обычно выше, так как используется ручной кропотливый труд.
Вы только представьте, что в цену на органические продукты входят не только затраты на их производство, но и на охрану окружающей среды. На стоимости также отражаются более высокие требования к выращиванию домашнего скота.
Почему при явном обосновании того, что цены на органик-продукцию более высокие, мы отнесли этот пункт к мифам?
Здесь стоит рассуждать таким образом: не органическая еда дорогая, а промышленная – дешевая. Замена сырья на более дешевые синтетические аналоги позволяет продавать продукцию промышленного производства по фактически заниженным ценам. А платить потом все равно придется – правда, уже своим здоровьем.
Дело в понимании, какой жизнью мы хотим жить. Какой уровень жизни для вас является приемлемым? Какова цена вашего здоровья и благополучия? Нельзя отделить себя от окружающего мира – мира природы, частью которого мы являемся.
Это и есть философия жизни. Органика как философия. Она играет двоякую роль в обществе: с одной стороны, органика отвечает запросам потребителей, которые желают быть более здоровыми; с другой стороны, она дает возможность производить товары народного потребления, внося при этом существенный вклад в защиту окружающей среды и благополучие животных.
Это лишь доказывает, что органика – не дань моде, а естественный процесс в цикле самой жизни.
Редакция Porusski благодарит компанию «Углече Поле» за помощь в подготовке материала и организации съемки.
«Органика» — не значит «экологичность»
Тайлер Дерден делает домашний рецепт. Скорее всего, органический, на базе глицерина.
Мы тут запустили линейку экокосметики и занялись экологичностью производства. На самом деле, конечно, началось с того, что мы почти втрое сократили потребление воды за счёт кардинальной переделки линии водоподготовки. Вообще-то мы хотели меньше платить за неё городу, но получилось очень экологично.
Как только мы увидели экономию, стали смотреть на другие экологичные решения. И ещё тренды привели к тому, что в любом случае нужно было производить экокосметику либо вообще органик-косметику. Потому что надпись «эко-» даёт минимум +20 % к цене.
И вот тут-то и началось странное противоречие.
Дело в том, что почти всё то, что называют «органик-» и «эко-», на деле при расчёте потребляемых ресурсов на единицу продукции таковым не является. Приведу пару примеров. Вот когда на полках магазинов начал появляться «органический» салат-латук дороже обычного, я была удивлена. Серьёзно, вы возьмёте салат, обильно удобряемый натуральным навозом с ближайшей фермы, когда есть контролируемые гидропонные линии, где он растёт на чистых растворах? Особенно после 2011 года, когда натуральные удобрения заразили резистентным к антибиотикам штаммом кишечной палочки кучу людей в Германии и убили 48 из них.
Что такое вообще органические продукты?

Эмблема «NationalOrganicProgram» Министерства сельского хозяйства США.
Термин «органический продукт» веселит каждого человека, связанного с химией. Сразу представляется богатый выбор неорганических продуктов из поваренной соли, соды и воды из-под крана. На самом деле это понятие описывает продукты сельского хозяйства, выращенные без применения пестицидов, минеральных удобрений, регуляторов роста и соответствующие ряду других параметров. В целом идея маркировки условной кукурузы, которая выращивалась и обрабатывалась без применения вредных веществ, выглядит довольно неплохо на первый взгляд. Но в итоге всё получилось как всегда.
Тема очень быстро стала модной несмотря на то, что фактически внедрение такого «органического производства» приводит к резкому снижению урожайности и повышению цен. Ладно бы ещё повышенная цена и возврат к древним технологиям времён тяпки и ручного пресса были оправданны качеством продукта. Многие готовы платить больше, чтобы есть более здоровую пищу, богатую витаминами и полезными веществами. Но вот упрямая наука, как всегда, расстраивает своими скучными фактами. Крупный метаанализ в 2009 году показал, что употребление органической пищи не даёт никакого положительного эффекта для здоровья, если сравнивать с аналогичными продуктами питания. Да и каких-то уникальных отличий в витаминах и питательной ценности тоже не обнаружили.
В итоге мы получаем дорогие продукты, которые ещё имеют и кучу проблем с точки зрения их экологичности. Почему-то люди очень часто отождествляют эти термины, а в реальности органическое производство скорее наоборот является проблемным с точки зрения влияния на экосистемы. Вы потратите гораздо больше воды, энергии и других ресурсов, чтобы вырастить то же самое количество урожая, что и при традиционном интенсивном земледелии.
Проще говоря, «органик-» — это созданный неоптимальным образом, часто с большими затратами ресурсов планеты, чем «неорганик-» продукт.
Страшный пропиленгликоль в органической косметике
Если говорить о косметике, которая подойдёт под определение «органик-», то там всё ещё интереснее. Если соблюдать все требования, то продукт получается, мягко говоря, очень дорогим и местами откровенно более низкокачественным. Я лично пробовала в качестве теста делать экстракты из огурца на ручном прессе. Было лёгкое ощущение, что я вступила в общину амишей и вернулась к образу жизни XIX века.
Приведу банальный пример. В органик-косметике запрещено использовать пропиленгликоль для получения экстрактов, и в состав его включать тоже нельзя, при том что тот же пропиленгликоль — это абсолютно разрешённая пищевая добавка E1520. Да, вы можете его спокойно принимать внутрь в разумных количествах. Взрослому человеку потребуется принять примерно полтора килограмма чистого вещества, чтобы отравиться. То есть вещество в 2,8 раза менее токсично, чем этиловый спирт, который вполне себе употребляют внутрь. И в 6,7 раза менее токсично, чем страшная поваренная соль, которую вы кладёте в суп. Но в органик-косметику такой ужас, конечно, класть нельзя. И в качестве растворителя для экстракта разрешено применять сверхкритический CO2 или глицерин. Они часто или дороже для конкретного применения, или не дают нужных параметров экстрагирования. C ними вполне можно работать, но в определённых разумных рамках, где это оправданно с точки зрения здравого смысла.
Теперь давайте перейдём к глицерину, который очень «органик-».
Нефтяной глицерин
Это мой любимый миф про страшный глицерин, который получают из нефти. И вот он-то и сотворит что-то страшное с вашей кожей в отличие от натурального растительного, который просто добро во плоти и совсем не такой. Все, кто хоть немного знаком с химией, знают, что две идентичные молекулы любого вещества имеют совершенно одинаковые свойства. И неважно, из какого сырья они получены, если соблюдается нужная степень чистоты. Поэтому нет смысла говорить о натуральном и химическом витамине C, глицерине или другом веществе.
Есть смысл говорить об очистке. Это боль для производства на самом деле, потому что, например, те же соли гиалуроновой кислоты в России можно достать только трупного происхождения с птицефабрик (это переработанные гребни петухов), но не из биореактора с добрыми пьяными бактериями (как мы заказываем из Европы). В петухах есть их петушиные белки, которые даже после очистки дестабилизируют сырьё и могут вызвать аллергию. Бактерии ничего в рецепт не добавляют. То же самое касается всяких натуральных экстрактов трав: если есть возможность заменить компоненты, то мы обычно покупаем очищенные отдельные вещества, но часто нужно получить именно комплекс веществ, который в десятки или сотни раз проще достать в 20-тонной канистре раствора из ромашки.
Чтобы получить натуральный глицерин, вам достаточно взять любое масло или жир, отщепить от него в щелочной среде жирные кислоты и отделить получившийся глицерин. Всё. Причём неважно, что это был за жир. Подойдут оливковое масло первого отжима, страшноватого вида жмых какой-нибудь масличной культуры и отработанное фритюрное масло из ближайшего фастфуда. Дальше только вопрос качества очистки и производства. Мы, конечно, не используем глицерин, полученный из фритюра, но не из-за каких-то предубеждений, а просто из-за того, что его не обрабатывают до нужной степени чистоты из-за экономической нерентабельности. Такие источники почти полностью идут на производство биодизеля. Зато им вполне успешно выкармливают козлов. Серьёзно.
Тут я даже не знаю, что сказать фанатам органик-косметики. Ну просто глицерин и глицерин. Дальше спор обычно переходит на консерванты.
Не менее страшные консерванты

Кристаллы бензойной кислоты. Один из самых распространённых консервантов.
По сути, органик-косметика подразумевает отсутствие консервантов. Я уже рассказывала раньше, что любые подобные средства без консервантов, по сути, — вкуснейший корм для миллионов бактерий и низших грибов. То есть храниться всё это должно только в холодильнике, а фасовка в баночки просто недопустима. В такое средство нельзя привычно ткнуть пальцем: вы немедленно его контаминируете, и оно очень быстро испортится.
Да, мы стараемся не нагружать нашу продукцию излишним количеством консервантов, но под немного странные требования «органик-» это всё равно не подходит. Решается это правильными флаконами-дозаторами. Всё потому, что мы и так делаем довольно сложные формулы, и вносить туда ещё один агент в большом количестве — так себе идея. Хороший пример — та же бензойная кислота. Пищевая добавка E210 или E211 в виде натриевой соли. Подавляет рост любых плесневых грибов и бактерий. И, конечно, жуткий консервант, который невероятно опасен, по мнению некоторых борцов за чистоту продукта. Предельно допустимые концентрации в пищевых продуктах составляют 0,15–0,25 % от массы продукта. И вот тут опять получается неудобно для ярых поборников концепции «всё только натуральное!». В самой что ни на есть натуральной бруснике содержится до 0,2 % бензойной кислоты. В клюкве поменьше, но тоже весьма много. В итоге свежие ягоды просто не проходили бы стандартов по добавленным консервантам, если бы бензоаты не были продуктом естественного синтеза в самом растении. Кстати, именно поэтому на упаковках морса часто гордо пишут «Без консервантов». Просто там уже такое количество натуральных бензоатов, что можно ничего дополнительно не добавлять.
И да, если говорить про блокирование роста грибов в растворе, то без таких средств это крайне тяжело сделать. В экомарках часто используются консерванты, которые могут противостоять некоторое время бактериям, но не грибку.
Следующий шаг — упаковка
С упаковкой всё достаточно просто: меньше упаковки — лучше экология.
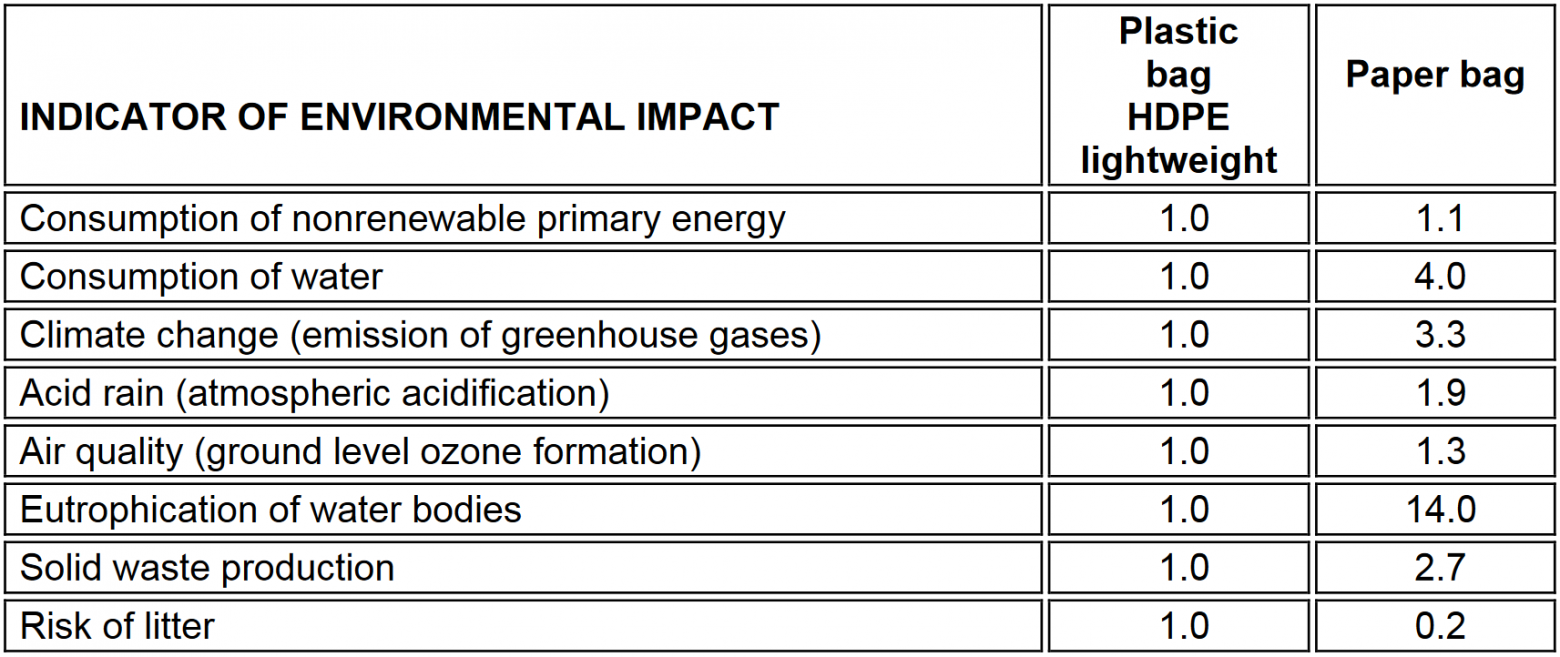
Но вот преимущества картона и бумаги перед пластиком — очень частое заблуждение. Очень часто, когда производитель хочет подчеркнуть свою близость к природе, он использует бумажные пакеты и коробки максимально натурального коричневатого оттенка. И опять упрямые учёные портят весь маркетинг. Вот замечательное и подробное исследование, проведённое в Северной Ирландии:
Исследование очень убедительно показывает, что на производство бумажной упаковки тратится намного больше природных ресурсов. Воды нужно больше, процесс создания более энергоёмкий. Плюс бумага занимает больше объёма и больше весит, а значит, для транспортировки такой упаковки потребуется больше грузовиков, чем для перевозки пластиковой тары. При этом переработка одного килограмма пластика требует на 91 % меньше энергии, чем переработка одного килограмма бумаги.
Но, тем не менее, мы решили убрать лишний картон из своих упаковок: это экологично и даёт оптимизацию себестоимости.
И всё же мы запустили экосерию
Рынок — штука суровая. Если потребителю хочется экологичности — мы стараемся ему в этом помочь. Мы запустили отдельную серию «the U», которая максимально соответствует нашему представлению о таких продуктах.
В смысле что из множества всего, что подпадает под определение «экокосметика», мы выбрали то, что реально даёт хоть какую-то пользу экологии, а не увеличивает вред. Мы не хотим следовать экотрендам курильщика, которые часто абсурдны и делают экосистеме только хуже, а стараемся придерживаться экологичности здорового человека.

Очищающий скраб Your Fresh Head для кожи головы.
Мы постарались убрать избыток того же картона, за который нас многие ругали. Полностью от него избавляться пока не получается, но мы уже перестали изображать матрёшку из множества вложенных друг в друга коробочек. Наш скраб для кожи головы из этой серии фасуется в те же банки, что и наша унипаста для проведения ЭЭГ. Раньше мы вначале фасовали в групповые коробки по шесть штук, которые складывались уже в транспортировочные. Мы исключили из этой цепочки групповые коробки и стали складывать сразу в транспортировочные. Это сэкономило довольно большое количество картона, но нам пришлось доработать контроль вскрытия банки. В случае отсутствия дополнительной упаковки это важно.
Консерванты в этой серии мы подбирали полностью аналогичные тем, что встречаются в растительных источниках. Это уже известная вам бензойная кислота и её соли. А ещё фенилэтиловый спирт. У него, кроме антибактериальной активности, есть один очень важный бонус — он очень вкусно пахнет розами. В промышленности он обычно используется как заменитель натурального розового масла. В природных источниках содержится в розовом, гераниевом, неролиевом и других эфирных маслах. В конечной версии наших продуктов мы решили остановиться на использовании бензилового спирта и эфира глицерина с приятным запахом — этилгексилглицерина. У последнего, помимо антибактериальной активности, есть еще приятный эффект — он работает как эмолиент, снижая потерю влаги кожей. Это весьма приятный бонус для людей с атопическим дерматитом. Но об этом я как-нибудь отдельно расскажу.
Ну и заодно у нас дошли руки до модификации нашей водоподготовки. Для производства наших полимеров нам нужно много высокоочищенной воды после обратноосмотической мембраны. Да, я понимаю, что от снижения потребления воды в засушливых регионах Африки её не прибавится. Но даже в этом случае мы решили, что будет неразумным тратить больше ресурсов, чем необходимо. Во-первых, вода всё же не бесплатная, а во-вторых, даже во влажных регионах инфраструктура не рассчитана на неограниченный рост потребления. Поэтому мы полностью переделали этот узел и значительно снизили количество концентрата с солями, который сбрасывается обратно в канализацию при получении чистой воды. Даже видео на носок сняли. Вертикальное, как вы любите.
А если я за экологию?
Не надо слепо верить маркетологам. В любой непонятной ситуации лучше свериться с научными источниками и исследованиями на эту тему. Весьма часто оказывается, что выводы получаются прямо противоположными.
Если интересно, то заходите к нам в telegram-канал (@geltek_cosmetics) с хрониками нашей уютной лаборатории.
Урок 17. Основные понятия органической химии
Известно, что все сложные вещества условно можно разделить на органические и неорганические.
В состав неорганических веществ может входить любой элемент периодической системы. Основными классами неорганических веществ являются оксиды, кислоты, основания и соли. Свойства этих веществ были рассмотрены в первых двух разделах.
В состав органических веществ обязательно входит атом углерода, который в подавляющем числе органических соединений образует цепи. Эти цепи имеют разную длину и разное строение, поэтому органических соединений теоретически может быть бесчисленное множество.
Основу любого органического соединения составляет углеводородная цепь, которая может соединяться с функциональными группами.
Свойства органического соединения описывают по схеме:
Прочитав очередной урок, попробуйте описать изучаемые соединения на любом примере, используя эту схему. И всё получится!
Предмет органической химии. Теория строения органических веществ
Органические вещества известны людям с давних пор. Ещё в древности люди использовали сахар, животные и растительные жиры, красящие и душистые вещества. Все эти вещества выделялись из живых организмов. Поэтому такие соединения стали называться органическими, а раздел химии, который изучал вещества, образующиеся в результате жизнедеятельности живых организмов, получил название «органическая химия». Это определение было дано шведским учёным Берцелиусом* в 1827 году.
* Берцелиус Йенс Якоб (20.08.1779–7.08.1848) — шведский химик. Проверил и доказал ряд основных законов химии, определил атомные массы 45 химических элементов, ввёл современное обозначение химических элементов (1814) и первые химические формулы, разработал понятия «изомерия», «катализ» и «аллотропия».
Уже первые исследователи органических веществ отмечали особенности этих соединений. Во-первых, все они при сжигании образуют углекислый газ и воду, значит, все они содержат атомы углерода и водорода. Во-вторых, эти соединения имели более сложное строение, чем минеральные (неорганические) вещества. В-третьих, возникали серьёзные затруднения, связанные со способами получения и очистки этих соединений. Полагали даже, что органические соединения невозможно получить без участия «жизненной силы», которая присуща только живым организмам, то есть органические соединения нельзя, казалось, получить искусственно.
И, наконец, были обнаружены соединения одинакового молекулярного состава, но различные по свойствам. Такое явление не было характерно для неорганических веществ. Если для неорганического вещества известен состав, то известны и его свойства.
А химики-органики обнаружили, что вещество состава С2Н6О у одних исследователей является достаточно инертным газом, а у других — жидкостью, активно вступающей в разнообразные реакции. Как это объяснить?
К середине 19-го века было создано немало теорий, авторы которых пытались объяснить эти и другие особенности органических соединений. Одной из таких теорий стала теория химического строения Бутлерова*.
* Бутлеров Александр Михайлович (15.09.1928–17.08.1886) — русский химик. Создал теорию химического строения органических веществ, лежащей в основе современной химии. Предсказал изомерию многих органических соединений, заложил основы учения о таутомерии.
Некоторые её положения были изложены А. М. Бутлеровым в 1861 году на конференции в г. Шпейере, другие были сформулированы позже в научных работах А. М. Бутлерова. В целом, основные положения этой теории в современном изложении можно сформулировать так.
1. Атомы в молекулах располагаются в строгом порядке, согласно их валентности.
2. Атом углерода в органических молекулах всегда имеет валентность равную четырём.
3. Порядок соединений атомов в молекуле и характер химических связей между атомами называется химическим строением.
4. Свойства органических соединений зависят не только от того, какие атомы и в каких количествах входят в состав молекулы, но и от химического строения:
5. Изучая свойства органических соединений, можно сделать вывод о строении данного вещества и описать это строение одной-единственной химической формулой.
6. Атомы в молекуле влияют друг на друга, и это влияние сказывается на свойствах вещества.
При изучении органической химии нужно чаще вспоминать эти положения и, прежде чем описывать свойства какого-либо вещества, следует указать его строение при помощи химической формулы, в которой будет показан порядок соединения атомов в молекуле — графическая формула.
Особенности строения органических соединений
Органическая химия изучает строение молекул и свойства соединений углерода, кроме самых простых (угольная и синильная кислоты и их соли).
В состав неорганических соединений могут входить любые из 114 известных в настоящее время химических элементов. Сейчас известно более 0,5 млн неорганических веществ.
В состав органических молекул обычно входят атомы 6 химических элементов: C, H, O, N, P, S. И тем не менее в настоящее время известно более 20 миллионов органических соединений.
Почему органических веществ так много?
Поскольку в состав любого органического соединения входит атом углерода, попробуем найти ответ на этот вопрос, рассмотрев особенности строения атома углерода.
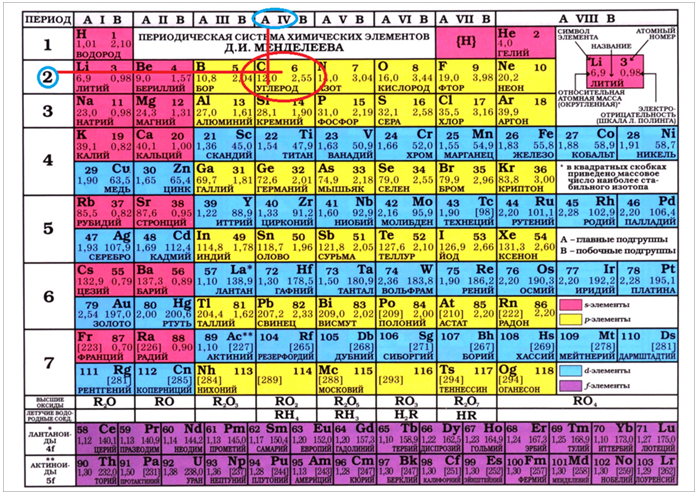
Углерод — химический элемент 2-го периода, IV группы Периодической системы химических элементов Менделеева, следовательно, строение его атома можно изобразить так:
Таким образом, на внешнем уровне атома углерода находится четыре электрона. Являясь неметаллом, атом углерода может и отдавать четыре электрона, и принимать до завершения внешнего уровня также четыре электрона. Поэтому:
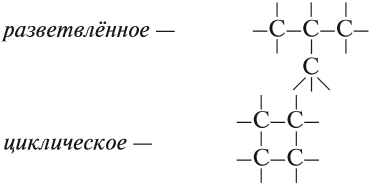
В состав углеродных цепочек может входить разное число атомов углерода: от одного до нескольких тысяч. Кроме того, цепочки могут иметь разное строение:
Между атомами углерода могут возникать химические связи разного типа:
Поэтому всего лишь четыре (!) атома углерода могут образовать более 10 соединений разного строения, даже если в состав таких соединений будут входить только атомы углерода и водорода. Эти соединения будут иметь, например, следующие «углеродные скелеты»:
Задание 17.1. Попробуйте составить сами 2–3 цепочки атомов углерода иного строения из четырёх атомов углерода.
Выводы
Способность атомов углерода образовывать УГЛЕРОДНЫЕ ЦЕПИ разного состава и строения — главная причина многообразия органических соединений.
Классификация органических соединений
Поскольку органических соединений очень много, их классифицируют по разным признакам:
В данном пособии будут рассмотрены свойства соединений различных классов, поэтому определения и примеры будут даны позднее.
Формулы органических соединений
Формулы органических соединений можно изображать по-разному. Состав молекулы отражает молекулярная (эмпирическая) формула:
Но эта формула не показывает расположения атомов в молекуле, т. е. строения молекулы вещества. А в органической химии это понятие — химическое строение молекулы вещества — самое главное! Последовательность соединения атомов в молекуле показывает графическая (структурная) формула. Например, для вещества строения С4Н10 можно написать две такие формулы:
Можно показать все химические связи:
Такие развёрнутые графические формулы наглядно показывают, что атом углерода в органических молекулах четырёхвалентен. При составлении графических формул нужно сначала изобразить углеродную цепь, например:
Затем чёрточками обозначить валентность каждого атома углерода:
У каждого атома углерода должно быть четыре чёрточки!
Затем заполнить «свободные» валентности атомами водорода (или другими одновалентными атомами или группами).
Теперь можно переписать эту формулу в сокращённом виде:
Если вы хотите сразу написать такую формулу для бутана — ничего сложного нет, нужно только считать до четырёх. Изобразив углеродный «скелет», нужно задать себе вопрос: сколько валентностей (чёрточек) имеет данный конкретный атом углерода?
Две. Значит, нужно добавить 2 атома водорода:
Следует помнить, что графические формулы можно записывать по-разному. Например, графическую формулу бутана можно записать так:
Поскольку последовательность расположения атомов не нарушилась, то это формулы одного и того же соединения(!) Проверить себя можно, составив названия этих соединений (см урок 17.7). Если названия веществ совпадают, то это — формулы одного и того же вещества.
Изомерия
К середине 19-го века, когда было получено и изучено достаточно много органических соединений, химики-органики обнаружили непонятное явление: соединения, имеющие одинаковый состав, имели разные свойства! Например, газ, который с трудом вступает в реакции и не реагирует с Nа, имеет состав C2H6O. Но существует жидкость, имеющая тот же состав и очень активная в химическом отношении. В частности, эта жидкость состава C2H6O активно реагировала с Na, выделяя водород. Совершенно разные по физическим и химическим свойствам вещества имеют одинаковую молекулярную формулу! Почему? Ответ на этот вопрос можно получить при помощи теории строения органических соединений Бутлерова, одно из положений которой утверждает: «Свойства органических соединений зависят от химического строения их молекул».
Так как химические свойства рассматриваемых соединений различны, значит, их молекулы имеют разное строение. Попробуем составить графические формулы этих соединений. Для вещества состава C2H6O можно предложить только два вида цепочек:
Заполнив эти «скелеты» атомами водорода, получаем:
Вопрос. Какое из этих соединений способно реагировать с Nа, выделяя водород?
Очевидно, к такому взаимодействию способно только вещество (I), содержащее связь «О–Н», которой нет в молекуле (II). И газ Н2 выделяется потому, что разрушается связь «О–Н». Если бы для образования водорода нужно было бы разрушить связь «С–Н», то поскольку такие связи есть в обоих веществах, газ Н2 выделялся бы в обоих случаях. Таким образом, формула (I) отражает строение молекулы жидкости, а формула (II) — газа.
Существование соединений, которые имеют одинаковый состав, но разное химическое строение, называется изомерией.
ИЗОМЕРЫ — это соединения, которые имеют одинаковый состав, но разное химическое строение, а значит, и разные свойства.
Поэтому молекулы органических соединений следует изображать при помощи графических (структурных) формул, так как в этом случае будет видно строение изучаемого вещества, а значит, будет видно, как и за счёт чего происходит химическая реакция.
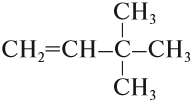
Упражнение 17.1. Среди следующих соединений найдите изомеры:
Решение. Поскольку изомеры имеют одинаковый состав, определим состав (молекулярные формулы) всех этих соединений, то есть пересчитаем число атомов углерода и водорода:
Ответ. Соединения а) и б) изомерны друг другу, так как имеют одинаковый состав C4H10, но различное химическое строение.
Соединения в) и г) изомерны друг другу, так как имеют одинаковый состав C5H12, но различное химическое строение.
Задание 17.2. Среди следующих соединений найдите изомеры:
Гомологи
Из того же положения теории строения органических соединений Бутлерова следует, что вещества, имеющие похожее (сходное) строение молекул, должны иметь и похожие (сходные) свойства. Органические соединения, которые имеют похожее строение, а, значит, и похожие свойства, образуют гомологические ряды.
Например, углеводороды, в составе молекул которых есть только одна двойная связь, образуют гомологический ряд алкенов:
Углеводороды, в молекулах которых имеются только простые связи, образуют гомологический ряд алканов:
Члены любого гомологического ряда называются ГОМОЛОГАМИ.
Гомологи — это органические соединения, которые похожи по химическому строению и, значит, по свойствам. Гомологи отличаются друг от друга по составу на группу СН2 или (СН2)n.
Убедимся в этом на примере гомологического ряда алкенов:
Задание 17.3. Сравните состав членов гомологического ряда алканов (гомологов алканов) и убедитесь, что по составу они отличаются на группу СН2 или (СН2)n.
Выводы
Гомологи похожи по строению, а значит, и по свойствам; гомологи отличаются по составу на группу СН2. Группа СН2 называется гомологической разностью.
Названия углеводородов. Правила международной номенклатуры
Для того чтобы понимать друг друга, нужен язык. Люди говорят на разных языках и не всегда понимают друг друга. Химики же, для того чтобы понимать друг друга, пользуются одним и тем же международным языком. Основу этого языка составляют названия соединений (номенклатура).
Правила номенклатуры (названий) органических соединений были приняты в 1965 году. Они называются правилами ИЮПАК (IUPAC)*.
* IUPAC — International Union of Pure and Applied Chemistry — Международный союз чистой и прикладной химии.
За основу названий органических соединений принимаются названия гомологов-алканов:
** Для этих соединений имеется ввиду, что они имеют линейное строение.
В этих названиях КОРНИ слов (полужирный шрифт) — мет-, эт-, проп- и так далее — указывают на число атомов углерода в цепи:
Задание 17.4. Сколько атомов углерода содержит углеродная цепь соединений:
Суффикс в названии указывает на характер (тип) связей. Так, суффикс -ан- показывает, что все связи между атомами углерода простые.
Задание 17.5. Вспомните, что такое гомологи, и установите, являются ли гомологами алканов следующие вещества:
В названиях могут быть и другие суффиксы:
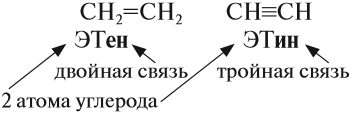
Упражнение 17.2. Попробуйте составить графические формулы ЭТана, ЭТена и ЭТина.
Решение. Все эти вещества имеют корень -ЭТ-, то есть в состав этих веществ входит . атома углерода. В первом веществе имеется . связь, так как суффикс -ан-:
Рассуждая аналогично, Вы получите:
Предположим, нужно изобразить графическую формулу пропина.
1. Корень -проп- указывает, что в цепи 3 атома углерода:
2. Суффикс -ин- указывает, что имеется одна тройная связь:
3. Каждый атом углерода имеет валентность IV. Поэтому допишем недостающие атомы водорода:
Задание 17.6. Составить графическую формулу пропена.
Теперь, предположим, нужно составить графическую формулу бутена. Корень -бут- означает, что в цепи имеется 4 атома углерода, суффикс -ен- указывает, что имеется двойная связь. Но где расположена эта связь? Возможны варианты:
Значит, в этом случае необходимо обозначить место двойной связи. Для этого атомы углерода нумеруют. Нумерацию начинают с того конца углеродной цепи, к которому ближе кратная двойная связь:
Хотя двойная связь в каждом случае соединяет два атома углерода, после суффикса -ен- записывают меньший номер.
Задание 17.7. Составьте графические формулы соединений: а) пентен-2; б) бутин-1.
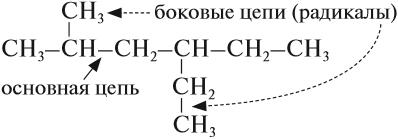
Ранее было сказано, что углеродные цепи могут быть линейными и разветвлёнными. Мы научились составлять названия линейных углеводородов. Теперь рассмотрим правила составления названий разветвлённых углеводородов. Для этого вспомним, что разветвлённые углеводороды имеют ответвления (боковые цепи, радикалы) от основной цепи:
Ответвления от основной (главной) цепи называются радикалами.
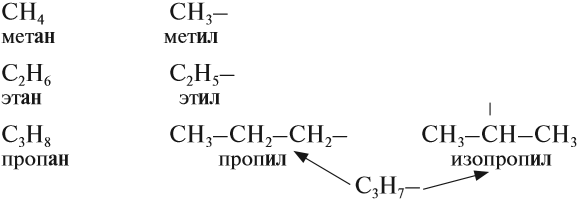
Радикалы по составу отличаются от соответствующего углеводорода на один атом водорода:
Названия радикалов предельных углеводородов имеют суффикс -ил-:
Правила составления названий углеводородов:
1) выбрать главную цепь: она должна быть самой длинной и самой разветвлённой (содержать максимальное число радикалов);
2) атомы углерода, которые не вошли в состав главной цепи, образуют боковые цепи (радикалы);
3) нумерацию атомов главной (основной) цепи начинают с того конца, от которого ближе кратная связь, а для предельных углеводородов — с того конца, к которому ближе радикал. В любом случае сумма номеров, которые появились в названии, должна быть наименьшей;
4) перед названием радикала ставят номер атома углерода (адрес), с которым он соединён;
5) если одинаковых радикалов несколько, то их число обозначают так:
6) затем записывают названия соответствующих радикалов (начиная с самых простых) и в конце названия записывают название углеводорода — основной цепи, указывая тип связи и место положения этой связи.
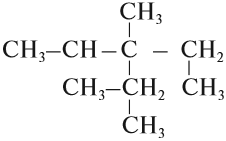
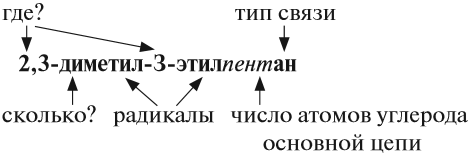
Упражнение 17.3. Назвать углеводород:
1. Выберем самую длинную цепь; в данном случае она содержит 5 атомов углерода: корень — пент.
2. Все связи простые: суффикс -ан-. Получается: пентан.
3. Нумеруем главную цепь слева направо, так как к левому концу ближе радикал «метил-»:
4. У второго атома углерода и у третьего атома углерода имеется по одному радикалу «метил-», то есть всего два радикала «метил-»; обозначим их «ди»; получаем: 2,3-диметил…
5. У третьего атома углерода есть ещё один радикал «этил-», поэтому получаем:
Упражнение 17.4. Назвать:
Пример. Составить графическую формулу углеводорода: 3,3-диметилбутен-1.
1. Определим число атомов углерода в основной цепи:
2. Определим тип химической связи в основной цепи:
3. Составляем «углеродный скелет»:
4. У атома углерода № 3 имеется два (ДИ) радикала «метил», т. е. каждый радикал имеет один атом углерода:
5. Допишем атомы водорода согласно валентности:
Задание 17.8. Составьте структурные (графические) формулы:
Органические вещества
Органические соединения, органические вещества — класс химических соединений, в состав которых входит углерод (за исключением карбидов, угольной кислоты, карбонатов, оксидов углерода и цианидов). [1]
Содержание
История
Название органические вещества появилось на ранней стадии развития химии во время господства виталистических воззрений, продолжавших традицию Аристотеля и Плиния Старшего о разделении мира на живое и неживое. Вещества при этом разделялись на минеральные — принадлежащие царству минералов, и органические — принадлежащие царствам животных и растений. Считалось, что для синтеза органических веществ необходима особая «жизненная сила» (лат. vis vitalis ), присущая только живому, и поэтому синтез органических веществ из неорганических невозможен. Это представление было опровергнуто Фридрихом Вёлером в 1828 году путём синтеза «органической» мочевины из «минерального» цианата аммония, однако деление веществ на органические и неорганические сохранилось в химической терминологии и по сей день.
Количество известных органических соединений составляет почти 27 млн
. Таким образом, органические соединения — самый обширный класс химических соединений. Многообразие органических соединений связано с уникальным свойством углерода образовывать цепочки из атомов, что в свою очередь обусловлено высокой стабильностью (то есть энергией) углерод-углеродной связи. Связь углерод-углерод может быть как одинарной, так и кратной — двойной, тройной. При увеличении кратности углерод-углеродной связи возрастает её энергия, то есть стабильность, а длина уменьшается. Высокая валентность углерода — 4, а также возможность образовывать кратные связи, позволяет образовывать структуры различной размерности (линейные, плоские, объёмные).
Классификация
Основные классы органических соединений биологического происхождения — белки, липиды, углеводы, нуклеиновые кислоты — содержат, помимо углерода, преимущественно водород, азот, кислород, серу и фосфор. Именно поэтому «классические» органические соединения содержат прежде всего водород, кислород, азот и серу — несмотря на то, что элементами, составляющими органические соединения, помимо углерода могут быть практически любые элементы.
Соединения углерода с другими элементами составляют особый класс органических соединений — элементоорганические соединения. Металлоорганические соединения содержат связь металл-углерод и составляют обширный подкласс элементоорганических соединений.
Характерные свойства
Существует несколько важных свойств, которые выделяют органические соединения в отдельный, ни на что не похожий класс химических соединений.
Номенклатура органических соединений
Органическая номенклатура — это система классификации и наименований органических веществ. В настоящее время распространена номенклатура ИЮПАК.
Классификация органических соединений построена на важном принципе, согласно которому физические и химические свойства органического соединения в первом приближении определяются двумя основными критериями — строением углеродного скелета соединения и его функциональными группами.
В зависимости от природы углеродного скелета органические соединения можно разделить на ациклические и циклические. Среди ациклических соединений различают предельные и непредельные. Циклические соединения разделяются на карбоциклические (алициклические и ароматические) и гетероциклические.
Алифатические соединения
Алифатические соединения — органические вещества, не содержащие в структуре ароматических систем.
Ароматические соединения
Ароматические соединения, или арены, — органические вещества, в структуру которых входит одна (или более) ароматическая циклическая система (см. Ароматизация)
Гетероциклические соединения
Гетероциклические соединения — вещества, в молекулярной структуре которых присутствует хотя бы один цикл с одним (или несколькими) гетероатомом
Полимеры
Полимеры представляют собой особый вид веществ, также известный как высокомолекулярные соединения. В их структуру обычно входят многочисленные сегменты (соединения) меньшего размера. Эти сегменты могут быть идентичны, и тогда речь идёт о гомополимере. Полимеры относятся к макромолекулам — классу веществ, состоящих из молекул очень большого размера. Полимеры могут быть органическими (полиэтилен, полипропилен, плексиглас и т. д.) или неорганическими (силикон); синтетическими (поливинилхлорид) или природными (целлюлоза, крахмал).
Структурный анализ органических веществ
В настоящее время существует несколько методов характеристики органических соединений. Кристаллография (рентгеноструктурный анализ) — наиболее точный метод, требующий, однако, наличия высококачественного кристалла достаточного размера для получения высокого разрешения. Поэтому пока этот метод не используется слишком часто.
Элементный анализ — деструктивный метод, использующийся для количественного определения содержания элементов в молекуле вещества.
Инфракрасная спектроскопия (ИК): используется главным образом для доказательства наличия (или отсутствия) определённых функциональных групп.
Масс-спектрометрия: используется для определения молекулярных масс веществ и способов их фрагментации.
Спектроскопия ядерного магнитного резонанса ЯМР.
Ультрафиолетовая спектроскопия (УФ): используется для определения степени сопряжения в системе
Про другие методы смотрите в разделе Аналитическая химия.
Органическая химия для «чайников»: история, понятия
Базовые основы органической химии для чайников
Если вы поступили в университет, но к этому времени так и не разобрались в этой нелегкой науке, мы готовы раскрыть вам несколько секретов и помочь изучить органическую химию с нуля (для «чайников»). Вам же остается только читать и внимать.
Основы органической химии
Органическая химия выделена в отдельный подвид благодаря тому, что объектом ее изучения является все, в составе чего есть углерод.
Органическая химия – раздел химии, который занимается изучением соединения углерода, структуру таких соединений, их свойства и методы соединения.
Органические соединения, количество которых сегодня достигает 20 млн, очень важны для полноценного существования всех живых организмов. Впрочем, никто и не сомневался, иначе человек просто закинул бы изучение этого непознанного в долгий ящик.
Чтобы хотя бы минимально понять органическую химию, приготовьтесь много читать
Цели, методы и теоретические представления органической химии представлены следующим:
Немного из истории органической химии
Вы можете не верить, но еще в далекой древности жители Рима и Египта понимали кое-что в химии.
Как мы знаем, они пользовались натуральными красителями. А нередко им приходилось использовать не готовый естественный краситель, а добывать его, вычленяя из цельного растения (например, содержащиеся в растениях ализарин и индиго).
Органическая химия зародилась давно, просто люди называли это иначе
Можем вспомнить и культуру употребления алкоголя. Секреты производства спиртных напитков известны в каждом народе. Причем многие древние народы знали рецепты приготовления «горячей воды» из крахмал- и сахарсодержащих продуктов.
Так продолжалось долгие, долгие годы, и только в 16-17 веках начались какие-то изменения, небольшие открытия.
В 18 веке некто Шееле научился выделять яблочную, винную, щавелевую, молочную, галловую и лимонную кислоту.
Дальше – интереснее: в 1773 году его коллега по ремеслу Руэль сумел выделить мочевину из человеческой мочи.
Тогда всем стало ясно, что продукты, которые удалось выделить из растительного или животного сырья, имели много общих черт. В то же время они сильно отличались от неорганических соединений. Поэтому служителям науки нужно было срочно выделить их в отдельный класс, так и появился термин «органическая химия».
Несмотря на то, что сама органическая химия как наука появилась лишь в 1828 году (именно тогда господину Вёлеру удалось выделить мочевину путем упаривания цианата аммония), в 1807 году Берцелиус ввел первый термин в номенклатуру в органической химии для чайников:
Раздел химии, который изучает вещества, полученные из организмов.
Следующий важный шаг в развитии органический химии – теория валентности, предложенная в 1857 году Кекуле и Купером, и теория химического строения господина Бутлерова от 1861 года. Уже тогда ученые стали обнаруживать, что углерод – четырехвалентен и способен образовывать цепи.
В общем, с эти самых пор наука регулярно испытывала потрясения и волнения благодаря новым теориям, открытиям цепочкам и соединениям, что позволяло так же активно развиваться органической химии.
У углерода четыре валентности
Но это уже совсем другая история, которую вы можете изучить сами. Далее мы предлагаем вам посмотреть научно-популярное видео про органическую химию для чайников:
Ну а если вам некогда и срочно нужна помощь профессионалов, вы всегда знаете, где их найти.
Наталья – контент-маркетолог и блогер, но все это не мешает ей оставаться адекватным человеком. Верит во все цвета радуги и не верит в теорию всемирного заговора. Увлекается «нейрохиромантией» и тайно мечтает воссоздать дома Александрийскую библиотеку.
Органические соединения
Органические вещества — класс соединений, в состав которых входит углерод (за исключением карбидов, карбонатов, оксидов углерода и цианидов).
Название «органические соединения» появилось на ранней стадии развития химии и говорит само за себя — ученые той эпохи считали, что живые существа состоят из особых органических соединений.
Основные классы соединений биологического происхождения — белки, липиды, углеводы — содержат, помимо углерода, преимущественно водород, азот, кислород и серу. Именно поэтому, несмотря на то, что элементами, составляющими органические соединения, помимо углерода, могут быть практически любые элементы, «классические» органические соединения содержат прежде всего водород, кислород, азот и серу.
Соединения углерода с другими элементами составляют особый класс органических соединений — элементоорганические соединения. Металлоорганические соединения содержат связь металл-углерод и составляют обширный подкласс элементоорганических соединений.
Количество известных органических соединений давно перевалило за 10 млн; таким образом, органические соединения — самый обширный класс химических соединений. Многообразие органических соединений связано с уникальным свойством углерода образовывать цепочки из атомов углерода, что в свою очередь обусловлено высокой стабильностью (то есть энергией) углерод-углеродной связи. Связь углерод-углерод может быть как одинарной, так и кратной: двойной, тройной. При увеличении кратности углерод-углеродной связи возрастает её энергия, т. е. стабильность, а длина уменьшается. Высокая валентность углерода — 4, а также возможность образовывать кратные связи, позволяет образовывать структуры различной размерности (линейные, плоские, объёмные).
Существует несколько важных свойств, которые выделяют органические соединения в отдельный ни на что не похожий класс химических соединений.
Содержание
Органическая номенклатура
Органическая номенклатура —это система классификации и наименований органических веществ.
Классификация
Классификация органических соединений построена на важном принципе, согласно которому физические и химические свойства органического соединения в первом приближении определяются двумя основными критериями — строением углеродного скелета соединения и его функциональными группами. В соответствии с этими критериями построена классификация органических соединений.
Классификация органических веществ.
Алифатические соединения
Алифатические соединения — органические вещества, не содержащие в структуре ароматических систем.
Ароматические соединения
Ароматические соединения или арены — органические вещества, в структуру которых входит одна (или более) ароматическая циклическая система (см. Ароматизация)
Гетероциклические соединения
Гетероциклические соединения — вещества, в молекулярной структуре которых присутствует хотя бы один цикл с одним (или несколькими) гетероатомом
Полимеры
Полимеры представляют собой особый вид веществ, также известный как высокомолекулярные соединения. В их структуру обычно входят многочисленные сегменты меньшего размера. Эти сегменты могут быть идентичны, тогда речь идет о гомополимере. Полимеры относятся к макромолекулам, классу веществ, состоящих из молекул очень большого размера. Полимеры могут быть органическими (полиэтилен, полипропилен, плексиглас и т. д.) или неорганическими (силикон); синтетическими (поливинилхлорид), или природными (целлюлоза, крахмал).
Структурный анализ органических веществ
В настоящее время существует несколько методов характеристики органических соединений. Кристаллография (рентгеноструктурный анализ) — наиболее точный метод, требующий, однако, наличия высококачественного кристалла достаточного размера для получения высокого разрешения. Поэтому пока этот метод не используется слишком часто.
Элементный анализ — деструктивный метод, использующийся для количественного определения содержания элементов в молекуле вещества.
Инфракрасная спектроскопия (ИК): используется главным образом для доказательства наличия (или отсутствия) определенных функциональных групп.
Масс-спектрометрия: используется для определения молекулярных масс веществ и способов их фрагментации.
Спектроскопия ядерного магнитного резонанса ЯМР.
Ультрафиолетовая спектроскопия (УФ): используется для определения степени сопряжения в системе
Про другие методы смотри в разделе Аналитическая химия.
Органическое вещество
Органические вещества — класс соединений, в состав которых входит углерод (за исключением карбидов, карбонатов, оксидов углерода и цианидов).
Название «органические соединения» появилось на ранней стадии развития химии и говорит само за себя — ученые той эпохи считали, что живые существа состоят из особых органических соединений.
Основные классы соединений биологического происхождения — белки, липиды, углеводы — содержат, помимо углерода, преимущественно водород, азот, кислород и серу. Именно поэтому, несмотря на то, что элементами, составляющими органические соединения, помимо углерода, могут быть практически любые элементы, «классические» органические соединения содержат прежде всего водород, кислород, азот и серу.
Соединения углерода с другими элементами составляют особый класс органических соединений — элементоорганические соединения. Металлоорганические соединения содержат связь металл-углерод и составляют обширный подкласс элементоорганических соединений.
Количество известных органических соединений давно перевалило за 10 млн; таким образом, органические соединения — самый обширный класс химических соединений. Многообразие органических соединений связано с уникальным свойством углерода образовывать цепочки из атомов углерода, что в свою очередь обусловлено высокой стабильностью (то есть энергией) углерод-углеродной связи. Связь углерод-углерод может быть как одинарной, так и кратной: двойной, тройной. При увеличении кратности углерод-углеродной связи возрастает её энергия, т. е. стабильность, а длина уменьшается. Высокая валентность углерода — 4, а также возможность образовывать кратные связи, позволяет образовывать структуры различной размерности (линейные, плоские, объёмные).
Существует несколько важных свойств, которые выделяют органические соединения в отдельный ни на что не похожий класс химических соединений.
Содержание
Органическая номенклатура
Органическая номенклатура —это система классификации и наименований органических веществ.
Классификация
Классификация органических соединений построена на важном принципе, согласно которому физические и химические свойства органического соединения в первом приближении определяются двумя основными критериями — строением углеродного скелета соединения и его функциональными группами. В соответствии с этими критериями построена классификация органических соединений.
Классификация органических веществ.
Алифатические соединения
Алифатические соединения — органические вещества, не содержащие в структуре ароматических систем.
Ароматические соединения
Ароматические соединения или арены — органические вещества, в структуру которых входит одна (или более) ароматическая циклическая система (см. Ароматизация)
Гетероциклические соединения
Гетероциклические соединения — вещества, в молекулярной структуре которых присутствует хотя бы один цикл с одним (или несколькими) гетероатомом
Полимеры
Полимеры представляют собой особый вид веществ, также известный как высокомолекулярные соединения. В их структуру обычно входят многочисленные сегменты меньшего размера. Эти сегменты могут быть идентичны, тогда речь идет о гомополимере. Полимеры относятся к макромолекулам, классу веществ, состоящих из молекул очень большого размера. Полимеры могут быть органическими (полиэтилен, полипропилен, плексиглас и т. д.) или неорганическими (силикон); синтетическими (поливинилхлорид), или природными (целлюлоза, крахмал).
Структурный анализ органических веществ
В настоящее время существует несколько методов характеристики органических соединений. Кристаллография (рентгеноструктурный анализ) — наиболее точный метод, требующий, однако, наличия высококачественного кристалла достаточного размера для получения высокого разрешения. Поэтому пока этот метод не используется слишком часто.
Элементный анализ — деструктивный метод, использующийся для количественного определения содержания элементов в молекуле вещества.
Инфракрасная спектроскопия (ИК): используется главным образом для доказательства наличия (или отсутствия) определенных функциональных групп.
Масс-спектрометрия: используется для определения молекулярных масс веществ и способов их фрагментации.
Спектроскопия ядерного магнитного резонанса ЯМР.
Ультрафиолетовая спектроскопия (УФ): используется для определения степени сопряжения в системе
Про другие методы смотри в разделе Аналитическая химия.
Органическая химия
Органи́ческая хи́мия — раздел химии, изучающий соединения углерода, их структуру, свойства, методы синтеза. [1] Органическими называют соединения углерода с другими элементами. Наибольшее количество соединений углерод образует с так называемыми элементами-органогенами: H, N, O, S, P. [2] Способность углерода соединяться с большинством элементов и образовывать молекулы различного состава и строения обусловливает многообразие органических соединений (к концу XX века их число превысило 10 млн, сейчас более 60 млн [источник не указан 472 дня] ). Органические соединения играют ключевую роль в существовании живых организмов.
Предмет органической химии включает следующие цели, экспериментальные методы и теоретические представления:
Содержание
История
Способы получения различных органических веществ были известны ещё с древности. Египтяне и римляне использовали красители индиго и ализарин, содержащиеся в растительных веществах. Многие народы знали секреты производства спиртных напитков и уксуса из сахар- и крахмалсодержащего сырья.
Во времена средневековья к этим знаниям ничего не прибавилось, некоторый прогресс начался только в XVI—XVII в: были получены некоторые вещества, в основном путём перегонки определённых растительных продуктов. В 1769—1785 г. Шееле выделил несколько органических кислот, таких как яблочная, винная, лимонная, галловая, молочная и щавелевая. В 1773 г. Руэль выделил из человеческой мочи мочевину.
Выделенные из животного или растительного сырья продукты имели между собой много общего, но отличались от неорганических соединений. Так возник термин «Органическая химия» — раздел химии, изучающий вещества, выделенные из организмов (определение Берцелиуса, 1807 г.). При этом полагали, что эти вещества могут быть получены только в живых организмах благодаря «жизненной силе».
Как принято считать, органическая химия как наука появилась в 1828 году когда Фридрих Вёлер впервые получил органическое вещество — мочевину — в результате упаривания водного раствора цианата аммония (NH4OCN).
Важным этапом стала разработка теории валентности Купером и Кекуле в 1857 г., а также теории химического строения Бутлеровым в 1861 г. В основу этих теорий были положены четырёхвалентность углерода и его способность к образованию цепей. В 1865 году Кекуле предложил структурную формулу бензола, что стало одним из важнейших открытий в органической химии. В 1875 г. Вант-Гофф и Ле Бель предложили тетраэдрическую модель атома углерода, по которой валентности углерода направлены к вершинам тетраэдра, если атом углерода поместить в центр этого тетраэдра. В 1917 году Льюис предложил рассматривать химическую связь с помощью электронных пар.
В 1931 г. Хюккель применил квантовую теорию для объяснения свойств альтернантных ароматических углеродов, чем основал новое направление в органической химии — квантовую химию. В 1933 г. Ингольд провёл изучение кинетики реакции замещения у насыщенного атома углерода, что привело к масштабному изучению кинетики большинства типов органических реакций.
Историю органической химии принято излагать в связи с открытиями сделанными в области строения органических соединений, однако такое изложение больше связано с историей химии вообще. Гораздо интереснее рассматривать историю органической химии с позиции материальной базы, то есть собственно предмета изучения органической химии.
На заре органической химии предметом изучения были преимущественно субстанции биологического происхождения. Именно этому факту органическая химия обязана своим названием. Научно-технический прогресс не стоял на месте, и со временем основной материальной базой органической химии стала каменноугольная смола, выделяемая при получении кокса прокаливанием каменного угля. Именно на основе переработки каменноугольной смолы в конце XIX века возник основной органический синтез. В 50-60 годах прошлого века произошёл переход основного органического синтеза на новую базу — нефть. Таким образом появилась новая область химии — нефтехимия. Огромный потенциал, который был заложен в новом сырье вызвал бум в органической химии и химии вообще. Появление и интенсивное развитие такой области как химии полимеров обязана прежде всего новой сырьевой базе.
Несмотря на то, что современная органическая химия в качестве материальной базы по прежнему использует сырье биологического происхождения и каменноугольную смолу, объём переработки этих видов химического сырья по сравнению с переработкой нефти мал. Смена материально-сырьевой базы органической химии была вызвана прежде всего возможностями наращивания объёмов производства.
Классификация органических соединений
Правила и особенности классификации
В основе классификации лежит структура органических соединений. Основа описания структуры — структурная формула. Атомы элементов обозначаются латинскими символами, как они обозначены в периодической таблице химических элементов (таблице Менделеева). Водородные и электронодефицитные связи обозначаются пунктирной линией, ионные связи обозначаются указанием зарядов частиц, входящих в состав молекулы. Поскольку в подавляющее большинство органических молекул входит водород, его обычно не обозначают при изображении структуры. Таким образом, если в структуре у одного из атомов изображена недостаточная валентность, значит, возле этого атома расположен один или несколько атомов водорода.
Атомы могут образовывать циклические и ароматические системы.
Основные классы органических соединений
Строение органических молекул
Органические молекулы в основном образованы ковалентными неполярными связями C—C, или ковалентными полярными типа C—O, C—N, C—Hal. Согласно октетной теории Льюиса и Косселя молекула является устойчивой, если внешние орбитали всех атомов полностью заполнены. Для таких элементов как C, N, O, Галогены необходимо 8 электронов, чтобы заполнить внешние валентные орбитали, для водорода необходимо только 2 электрона. Полярность объясняется смещением электронной плотности в сторону более электроотрицательного атома.
Классическая теория валентных связей не в состоянии объяснить все типы связей, существующие в органических соединениях, поэтому современная теория использует методы молекулярных орбиталей и квантовохимические методы.
Строение органического вещества
Свойства органических веществ определяются не только строением их молекул, но и числом и характером их взаимодействий с соседними молекулами, а также взаимным пространственным расположением. Наиболее ярко эти факторы проявляются в различии свойств веществ, находящихся в разных агрегатных состояниях. Так, вещества, легко взаимодействующие в виде газа, могут совершенно не реагировать в твёрдом состоянии, или приводить к другим продуктам.
В твёрдых органических веществах, в которых наиболее ярко проявляются эти факторы, различают органические кристаллы и аморфные тела. Их описанием занимается наука «химия органического твёрдого тела», основание которой связывают с именем советского физика-кристаллографа А. И. Китайгородского. Примеры полезных органических твёрдых тел — органические люминофоры, разнообразные полимеры, сенсоры, катализаторы, электропроводники, магниты и др.
Особенности органических реакций
В неорганических реакциях обычно участвуют ионы, они проходят быстро и до конца при комнатной температуре. В органических реакциях часто происходят разрывы ковалентных связей с образованием новых. Как правило, эти процессы требуют особых условий: определённой температуры, времени реакции, и часто наличия катализатора. Обычно протекает не одна, а сразу несколько реакций, поэтому выход целевого вещества зачастую не превышает 50 %. Поэтому при изображении органических реакций используют не уравнения, а схемы без расчёта стехиометрии.
Реакции классифицируются в зависимости от способов разрыва и образования связей, способов возбуждения реакции, её молекулярности.
Определение структуры органических соединений
За все время существования органической химии как науки важной задачей было определить структуру органических соединений. Это значит узнать, какие атомы входят в состав соединения, в каком порядке эти атомы связаны между собой и как расположены в пространстве.
Существует несколько методов решения этих задач.
Описанных выше методов, как правило, полностью хватает для определения структуры неизвестного вещества.
Химия
Основы органической химии
План урока:
Что такое органическая химия?
Современное определение органической химии:
– это раздел химической науки, который изучает способы получения углеводородов и их производных, а также свойства, полученных веществ.
Не стоит думать, что предмет органической химии очень узкий, раз объект его исследований можно описать только 2 словами, поскольку количество углеводородов и их производных достаточно превышает все неорганические вещества вместе взятые.
История изучения органической химии
Развитие органической химии, как отдельной науки, началось недавно, но с предметом ее исследования люди были знакомы очень давно.
Первые вещества органической химии получались из живых организмов – растений и животных. Например, духи изготавливались из растительных масел, спирт синтезировали благодаря брожению винограда, а красные красители и вовсе из специальных червей. Поскольку получить искусственно такие вещества из неорганических материалов люди не могли, то предположили, что для их создания нужна «живая сила».
В 1827 году понятие органической химии было введено шведским ученым Й.Я. Берцелиусом.
В 1845 году немецким ученым Г. Кольбе было доказано, что органическое вещество можно добыть из неорганических соединений, и в качестве примера он показал получение уксусной кислоты из углерода, воды, серы и хлора.
В мире стал развиваться новый предмет, получивший название «химия органического синтеза».
С помощью химического анализа было показано, что при сжигании любого органического вещества, продуктами будут вода и углекислый газ, а в отдельных случаях чистая сажа или копоть, основу которых составляет уголь.
Современная задача органической химии – изучить вещества, молекулы которых образованы связями атомов углерода.
Характеристика основного элемента органической химии
Чтобы определить свойства и потенциальные возможности вступления в химические превращения какого-либо элемента, необходимо знать особенности его строения. Какие будут образовываться химические связи и каким образом их можно разорвать зависит от элемента.
Общее строение атома углерода
Зная эти основные цифры, можно подробно разобрать схему строения углеродного атома. У него 2 составляющие: ядро,заряженное положительно и электроны, которые заряжены отрицательно и находятся в пространстве вокруг него.
Порядковый номер элемента численно равен заряду ядра и числу в нем электронов. Число нейтронов вычисляется по формуле:
где А – массовое число, Nп – число протонов, Nн – число нейтронов.
Получаем, что количество нейтронов равно: Nн = А – Nп = 12-6 = 6
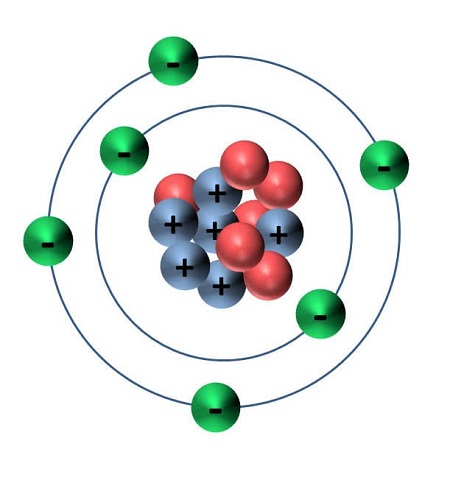
На рисунке 1 видно наглядно, какое строение у атома углерода.
Рисунок 1. – Строение атома углерода
Подробное электронное строение атома углерода
Ядро элемента не несет интереса в описаниях химических реакций, так как связи образуются при объединении электронных оболочек. При их связывании и перераспределении электронной плотности образуются новые молекулы.
Электронная структура
По расположению в ПСХЭ наглядно видно, что углерод имеет:
На первом энергетическом уровне в s-орбитали у всех элементов находятся 2 электрона. (см.рис.1). Второй уровень, он же и внешний для углерода, состоит из одной s и трех p орбиталей, и расположение электронов в них зависит от того, в каком состоянии находится атом.
Основное и возбужденное состояние
В основном состоянии на s и p орбиталях расположено по 2 электрона.
Если электрону, находящемуся на s-орбитали, добавить некоторое количество энергии из вне, то он может «перескочить» в пустую p-орбиталь с большей энергией.
Возбужденное состояние атома углерода представляет собой такую конфигурацию, при которой на внешнем уроне каждая его орбиталь имеет по 1 электрону.
Переход из основного состояния в возбужденное называется активацией.
На рисунке 2 схематически изображен процесс активации.
Рисунок 2. – Переход электрона с 2s-орбитали на 2p-орбиталь под действием дополнительной энергии
Атом углерода образует связи с другими элементами и между собой благодаря объединению неспаренных электронов. Если сравним конфигурацию атома углерода в возбужденном состоянии с конфигурацией в основном, можно сделать вывод о том, что в возбужденном состоянии он способен образовать больше ковалентных связей. В этом состоянии ему нужно быстро находить в окружении себя другие элементы и химически с ними связываться, так как при отсутствии дополнительной энергетической подпитки электрон снова перейдет с p-орбитали на s.
Знание о возбужденном состоянии атома углерода позволило в дальнейшем описывать механизмы реакций, рисовать структурные формулы веществ и описывать расположение молекул в пространстве.Полученные знания в 1861 году обобщил А.М. Бутлеров.
Степень окисления
В любых соединениях степень окисления определяет, какой условный заряд имеет тот или иной элемент в молекуле, если бы все связи были ионные.
Таблица 1. – Постоянные степени окисления элементов
Молекула спирта имеет формулу СH3-CН2-ОН, найдите значения степеней окисления атомов углерода в ней.
Разбиваем молекулу по связям С-С на участки. Получаем частицы СН3— и –СН2OH.
Для тренировки постарайтесь найти степень окисления углерода в соединениях, формулы которых: СH3CH2CH3, CH2CHCOH; CH3C(NH2)CH2CH2OH.
Валентность атома углерода
Под валентностью понимают, что это то количество связей, которые образовывает химический элемент. Один из основополагающих законов органической химии гласит, что в органических соединениях у атома углерода валентность постоянна и равняется 4 (т. к. в возбужденном состоянии у него 4 неспаренных электрона)
Углеродные связи в органических веществах
В ходе протекания химической реакции органические вещества претерпевают изменения, поскольку происходит разрушение старых и образование новых связей. Глядя на молекулу, опытный химик-органик скажет, какая именно связь разрушится, под действием каких факторов и предскажет, какие продукты и какого строения получатся в конце превращения.
Одинарные химические связи углерода
При объединении 2 неспаренных электронов 2 разных элементов, образуется одинарная связь.
Рассмотрим на конкретном примере, каким образом можно изобразить на бумаге структурные формулы веществ,имеющих состав С4H9Cl.
Помня о том, сколько связей может образовывать атом углерода, рисуем углеродный скелет органической молекулы (см. рис.3 а). Связи между атомами углерода ковалентные неполярные, т.к. образованы элементами с одинаковой электроотрицательностью.
Затем добавим к этому углеродному скелету атомы водорода и хлора (см. рис 3 б). Образовавшиеся связи хлор-углерод и углерод-водород – ковалентные полярные, т.к. образованы элементами с разной электроотрицательностью.Кроме изображенной на рисунке структурной формулы, для вещества состава С4H9Cl можно записать и некоторые другие (см. рис. 3 в). Ковалентные связи, образуемые атомом углерода, позволяют создать огромное количество соединений, у которых физические и химические свойства будут уникальны.
Рисунок 3. – Этапы построения органической молекулы
Формулу органического соединения, представленного на рисунке 3 б, можно записать проще, не изображая столько разветвлений.
Кратные связи углерода
В некоторых молекулах атомы углерода могут образовывать двойные и даже тройные связи. Это такой тип связей, на которые стоит обращать внимание, изучая строение веществ, потому что их наличие в молекуле придает соединению определенные свойства. Например, соединения с чередующимися кратными и одинарными связями могут проводить электрический ток.
Помимо кратных связей между собой, атом углерода образует двойные связи и с другими элементами (N, P, O, S). На схеме ниже представлен пример органической молекулы, которая содержит связи разных типов.
Разнообразие органических молекул
Молекулы органических соединений являются «кирпичиками» в построении живой материи и различных веществ. На свойства таких веществ влияет количество атомов в молекуле и их расположение друг относительно друга в пространстве. По строению органических молекул определяют их реакционные способности, цвет и токсичность.
Знание строения материалов позволило выбирать самые качественные для использования в постройке домов, автомобилей, ракет и многих других конструкций.
Одна из задач химиков-органиков получить материалы с определенным порядком расположения молекул.
Форма, объем, а также расположение молекулы в пространстве, зависят от того, в каких направлениях в ней связаны атомы. Это может быть объемная структура, расположение в одной плоскости или линяя.
Если бы мы рассмотрели расположение орбиталей в возбужденном состоянии атома углерода, и присоединили другие элементы к его s и p орбиталям, то все получившиеся молекулы имели бы строго объемное строение, однако на практике это не так. Чтобы объяснить расположение атомов в молекуле и пространстве, было предложено понятие гибридизации.
Гибридизация
Гибридизация – объединение орбиталей атома, которые имеют разные формы (s и p). Объединенные орбитали получаются с одинаковой формой, размером и энергией (рисунок 4).
Объединяться могут не только s и p орбитали, но и d и f, однако в атоме углерода таких нет, поэтому на уроках органической химии их объединения рассматриваться не будут.
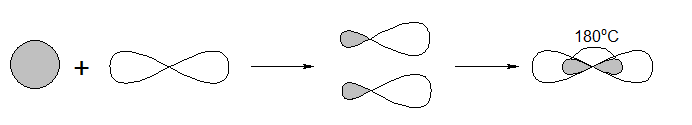
Рисунок 4. – Образование гибридных орбиталей из s и p
Основные типы гибридизации атома углерода в молекулах
Наглядно разберемся, как можно представить объединение орбиталей.
Предположим, что у нас есть синяя краска и белая краска, и мы в палитре их объединяем, т.е. смешиваем. При «смешении» мы получили краску нового голубого цвета. Тоже самое происходит и с орбиталями в атоме, только смешиваются не цвета, а формы и энергии.
Объединение орбиталей в углероде может проходить по 3 путям:
Зная, как гибридизация влияет на взаимное расположение атомов друг относительно друга, можно изобразить схематически строение молекулы любого органического вещества.
Рассмотрим молекулу, в которой есть участки с одинарными, двойными и тройными связями, и изобразим ее в пространстве (см.рис. 5).
Рисунок 5. – Пространственное расположение молекулы, в которой есть одинарные и кратные связи.
Стоит отметить, что представленные типы гибридизаций атомов в молекулах, характерны не только органическим соединением, но многим неорганическим веществам.
Важнейшие представители органических соединений
Соединения, у которых небольшое количество атомов в молекуле, простые структурные формулы и из которых путем последовательных химических реакций можно получить все остальные химические вещества, называют фундаментальными.
Самые простые органические соединения
Вещества, состоящие только из 2 видов атомов, называются простейшими. В органической химии соединения, образованные только атомами углерода и водорода, называют простыми. На их основе можно создавать другие классы органических веществ, путем замены водорода на другие группы, называемые функциональными.
Общая классификация органических молекул
Классификация органических соединений начинается с анализа углеродного скелета молекулы. Он может быть замкнутый в «кольцо» или в виде цепочки (по-научному: циклический и ациклический).
Циклические соединения делятся на те, в которых цикл состоит только из атомов углерода (тогда такие называются карбоциклические) и на те, у которых помимо него есть еще другой элемент (тогда такие соединения называют гетероциклические).
Карбоциклические подразделяются по наличию кратных связей в цикле на ароматические (когда цикл содержит кратные связи) и алициклические (в которых кратных связей не содержится).
Ациклические делятся на соединения, которые состоят только из одинарных связей (такие соединения называются предельными) и те, которые содержат в структуре углеродного скелета кратные связи (такие соединения называют непредельными).
Классификация углеводородов
Углеводороды можно разделить на разные группы по аналогичным признакам классификации органических соединений.По видам связей углеводороды делятся на те, в которых:
Каждый класс соединений вступает в химические реакции по определенным механизмам и будет рассмотрен более подробно на последующих уроках.
Агрегатные состояния простых органических веществ
Органические вещества выпускаются в мире в промышленных масштабах. Поступающие на завод вещества, называются сырьем, а выпускаемые из него – целевым продуктом.
В зависимости от того, какое сырье использует предприятие, его доставка может осуществляться разными способами: трубопроводами или с помощью транспортировочных машин.
Основная сырьевая база для производства сложных веществ и материалов – углеводороды, которые впоследствии претерпевают химические изменения и превращаются в другие вещества, которые используют для создания более сложных продуктов, например лекарств, пластмасс, клеев, пленок и др.
Самыми востребованными веществами из углеводородов являются этен и этин (вещества, в которых содержится только 2 атома углерода, которые соединены двойной и тройной связью).
Газообразные углеводороды
Этен и этин представляют собой газообразные органические вещества и для их транспортировки используют специальные газовые трубопроводы и баллоны, где они хранятся в сжиженном виде.
Изготавливают из них полимеры, например, полиэтиленовые пакеты или реактивы для более узкого органического синтеза.
Обычно, вещества в газообразном состоянии имеют в составе молекул от 1 до 4 углеродных атомов.
Жидкие органические вещества класса углеводородов
Состав таких веществ обычно подразумевает наличие атомов в своем составе больше, чем в молекулах газообразных веществ. Из-за утяжеления молекул их подвижность падает и в них могут образовываться межмолекулярные связи.
Для их транспортировки используют бочки, трубопроводы и цистерны. В составе молекул в жидком состоянии содержится от 5 до 18 атомов углерода.
Твердые углеводороды
Если увеличивать количество углеродных атомов в структуре органической молекулы, то углеводороды будут представлять из себя твердые, но пластичные материалы. Примером такого органического вещества является воск или парафин, в состав которых входят тяжелые углеводороды.
Для их транспортировки используют грузовые машины, а складывают их в коробки или ящики.
Кратко примеры агрегатных состояний органических веществ представлены в таблице 2.
Таблица 2. – Агрегатные состояния органических веществ
Азы органической химии
Определения.
Существуют вещества, в состав молекул которых входят атомы углерода и водорода.
Такие вещества называются органическими.
Все остальные вещества (которые не являются органическими) называются не-органическими.
Раздел химии, который изучает органические вещества, называется органической химией.
Раздел химии, изучающий неорганические вещества, называется неорганической химией.
Второе название органических веществ – угле-водороды, потому что они содержат атомы углерода и водорода.
Органическая химия и химия углеводородов – это одно и то же.
Кроме водорода и углерода, в составе молекул органических веществ могут быть атомы и других химических элементов – например, кислорода, азота, серы, фосфора.
Но главное – углерод и водород.
Почему углеводороды называются органическими?
Потому что в организме обязательно есть органические вещества.
Но при этом органические вещества есть не только в организме.
Органических веществ намного больше, чем неорганических.
***
Как устроены органические вещества.
(Строение органических соединений).
К атому углерода может присоединиться второй атом углерода,
ко второму атому углерода может присоединиться третий атом углерода,
к 3-му – 4-й и т.д.
Такие соединения из атомов углерода называют цепочками атомов углерода.
Их можно сравнить с поездом, в котором вместо вагончиков – атомы углерода.
Если первый атом углерода соединится с последним атомом углерода цепочки, то получится замкнутая цепочка, которую называют циклом. Обычно в циклах 5 или 6 атомов углерода.
Но атомы углерода четырёхрукие (четырёхвалентные).
Поэтому в таких «поездах» из атомов углерода у атомов углерода остаются свободные ручки – незанятые связями с другими атомами ручки.
В самом деле, первый атом углерода использует всего одну руку из четырёх рук, когда соединяется со вторым атомом углерода.
Значит, ещё три руки у первого атома углерода остаются свободными.
Эти сводобные три руки атом углерода «подаёт» трём одноруким атомам ВОДОРОДА (мы же говорили, что органические вещества состоят из атомов углерода и водорода).
В результате первый атом углерода углеродной цепочки соединённе только со вторым атомом углерода, но ещё и с тремя атомами водорода.
Это часто записывают так: CН3–
В этой записи С – это атом углерода, Н3 – это три атома водорода, присоединённые к атому углерода, а черточка «–» – это свободная «рука» (валентность, связь).
То же самое, что и о первом атоме углерода цепочки, можно сказать и о последнем атоме цепочки – в этом смысле концевые атомы углерода цепочки равноценны.
Но у нас есть ещё и второй атом углерода, третий и т.д. (если цепочка длинная – длиннее двух атомов углерода).
Второй атом углерода использует одну из четырёх рук для соединения с первым атомом углерода, а вторую руку – для соединения с третьим атомом углерода, то есть две руки у него заняты связями с соседними атомами углерода.
Значит, у второго атома углерода имеются две свободных руки – свободных от связей с атомами углерода.
И эти две свободных руки второй атом углерода использует для соединения с однорукимм атомами водорода.
Это часто записывают так: –CН2–.
В этой записи С – это атом углерода, Н2 – это два атома углерода, а две чёрточки по сторонам – это связи атома углерода с соседними атомами углерода.
Причём буквы «Н2» здесь ВОЗЛЕ атомы углерода (возлк буквы «С») означают не молекулу водорода, а просто «два атома водорода (Н), соединённые с атомом углерода (С).
Эти два Н между собой вообще не соединены, они соединены только с атомом углерода, с одним и тем же, но не друг с другом.
Это запись показывает только то, что при атоме углерода есть два атома углерода.
Точно такая же ситуация, как у второго атома углерода, имеется и у третьего, и четвёртого и всех остальных, сколько их есть в молекуле, кроме самого последнего – у него ситуация такая, как упервого (см. выше).
Рассмотрим теперь соединения углерода и водорода (углеводороды) по порядку, то есть начиная с соединения, содержащего всего один атомуглерода, затем два и т.д.
**
1С.
Органические молекулы с одним атомом углерода.
Метан и метанОЛ.
Если в молекуле всего один атом углерода, то конечно же цепочки из углеродных атомов в этом случае нет, то всё же такая молекула относится к органическим.
Один атом углерода соединяется с четырьмя атомами водорода, так как у атома С четыре руки, а у атомов водорода по одной руке.
В результате образуется молекула из одного С и четырёх Н, которая обозначается так: СН4.
Буквы С означает атом углерода, буква Н означает атомы водорода, цифра четыре после буквы Н означает, что атомов Н (водорода) четыре штуки.
Вещество, молекулы которого имеют такой состав, называется МЕТАНом (в именительном падеже – метан).
Метан является газом в обычных условиях.
Этот тот самый газ, который иногда взрывается в шахтах, губя шахтёров.
Метан является и основным веществом так называемого болотного газа.
Спирт метанол.
(Не путать с «питьевым спиртом ЭТАнолом
и главное – НЕ ПИТЬ метанол).
Если в молекулу метана добавить всего один атом кислорода (вставив его между атомом углерода и любым из атомов водорода), то молекуле получится такая группа атомов: –С–О–Н.
Такая группа называется спиртовой (если рядом нет такой группы атомов: С=О),
а молекулы с такой группой называются спиртами или алкоголями.
Но не путайте эти спирты и алкоголи с магазинскими алкоголями – в химии это понятие шире, и подробнее об этом рассказано далее.
Метан, в который вставлен один атом кислорода, называется уже иначе – метанОЛом.
Окончание «ол» означает наличие спиртовой группы, то есть атомов О и Н рядом (ОН).
Отступление про метанол токсикологическое…
Обычный спирт называется ЭТАнолом или винным спиртом.
Этанолом тоже можно отправиться, в том числе насмерть.
Но риск отравления этанолом всё же меньше, чем риск отравления метанолом.
Поэтому человек, собирающийся выпить водку, должен знать, что в ней может оказаться метанол.
И у него нет никакой возможности заранее узнать, есть в водке метанол, пока он её не выпьет.
Поэтому человек должен знать, как спастись, если ему станет плохо после водки.
А спастись после отравления метанолом
(или хотя бы уменьшить масштаб поражения организма и уменьшить тяжесть последствий в случае выпивания метанола)
можно, если сразу после метанола (или водки с метанолом) выпить настоящей водки с ЭТАнолом.
Но для этого нужно иметь при себе проверенную водку – проверенную или в лаборатории, или кем-то ранее уже испробованную.
**
2С
Органические молекулы с двумя атомами углерода:
ЭТАН и этанОЛ.
Бывают молекулы, в состав которых входит по два атома углерода.
Один атом углерода держит своей рукой (одной из четырёх) за руку (одну из четырёх) другой атом углерода:
С**С или С–С.
У каждого из этих двух атомов углерода остаётся ЕЩЁ ПО ТРИ свободных руки, то есть всего шесть свободных рук.
Эти шесть сводобных рук два атома углерода протягивают рукам одноруких атомов водорода – конечно же ШЕСТИ атомам водорода.
Один атом углерода протягивает три своих
свободных руки атомам водорода – и второй атом углерода точно так же протягивает три своих свободных руки атомам углерода.
Атом углерода вместе с присоединёнными к нему тремя атомами водорода обозначается
так: СН3–
или так: –СН3,
или так: Н3С–
При этом имеется в виду, что каждый из трёх атомов водорода (Н) присоединён только к атому углерода – между собой напрямую атомы водорода в этом случае не соединены.
В целом молекулу из двух атомов углерода можно показывать так:
Н3С–СН3.
Или так:
СН3–СН3.
В обоих случаях имеется в виду, что два атома углерода (С) соединены между собой, причём напрямую, а не через Н или три Н, а к каждому из обоих атомов углерода присоединены по три атома Н.
А можно написать форумулу этана и так (если «сжать» до простой формулы, показывающей только число атомов разных элементов): С2Н6.
Вещество, молекулы которого имеют такой состав, называется ЭТАНом (этан).
Спирт этанол.
(Тот самый, который в водке или пиве).
Если в молекулу этана добавить всего один атом кислорода (вставив его между атомом углерода и любым из атомов водорода), то в молекуле (теперь уже бывшего) этана получится такая группа атомов: –С–О–Н.
Такая группа (ОН) называется спиртовой (если рядом нет С=О – об этом говориться в разделе про карбоксильную группу), а молекулы с такой группой называются спиртами или алкоголями.
Но не путайте эти спирты и алкоголи с магазинскими алкоголями – в химии это понятие шире, и подробнее об этом рассказано далее.
Атом кислорода вставлен между любым из атомов водорода и соединённым с ним атомом углерода.
Окончание «ол» означает наличие спиртовой (ОН) группы.
Формула этанола выглядит так же, как формула этана (СН3–СН3), но с дополнительной буквой О (означающей наличие атома кислорода):
СН3–СН2ОН.
Или так: С2Н5ОН.
(Это сжатый вариант, показывающий состав молекулы).
Спиртные напитки,
опьянение,
алкоголизм.
Этанол – это тот самый спирт, который употребляют любители спиртных напитков.
Но спирты бывают разными (с разным числом атомов углерода и т.д.), а в спиртных напитках должен быть не какой попало спирт, а именно этанол.
Присутствие в этанол-содержащем спиртном напитке других спиртов (вдобавок к этанолу или вместо этанола) делает спирной напиток (токсичный и сам по себе) особо токсичным.
Пример см. выше в рассказе про метанол.
Подробнее см. о сивушных маслах.
Раствор, а не чистый спирт.
В спиртных напитках этанол обычно присутствует в смеси с водой, то есть спиртные напитки являются водными растворами.
(Причём этанол и вода хорошо растворяются друг в друге в любых пропорциях).
Крепость.
Чем больше этанола и меньше воды – тем более крепким считается спиртной напиток.
Крепость измеряют в градусах.
Выражение 40 градусов напитка означает, что в нём из ста долей напитка 40 долей приходится на этанол, а остальные 60 (100 минус 40) – на воду.
Другими словами, градусы – это просто проценты.
7 градусов – это 7 процентов этанола на остальные 93 (100-7=93) процента воды.
О токсичности этанола.
Не все лично наблюдали или слышали о случаях, когда человек умирал сразу же после первой же рюмки водки.
Но такое бывает.
То, что кто-то такого не видел – не значит, что такого не бывает.
Вопрос:
как узнать заранее, умрёт ли человек от первой рюмки?
Ответ:
никак. Почти.
Обычно заранее это невозможно узнать.
Только после того, как человек выпьет водку или другой крепкий спиртной напиток.
Вопрос:
почему некоторые люди могут пить водку часто и долго, а другие умирают после первой рюмки?
Ответ:
это зависит от особенностей организма.
Некоторые организмы не способны выжить после употребления водки.
Вопрос:
может ли умереть от рюмки водки человек, который ранее уже много раз пил водку?
Ответ:
да, может.
Вопрос:
когда и почему такое может случиться (смерть от рюмки водки у ранее употреблявшего алкоголь человека) и как спасти такого человека?
Ответ:
смерть от рюмки водки может наступить у тех людей, которые:
1) голодные,
2) замёршие,
3) уставшие.
Вот такие люди рискуют умереть от рюмки водки, выпитой в состоянии голода, холода или усталости.
Отсюда и выводы:
1. Пока человек голоден и не наелся – пить водку нельзя.
2. Пока человек не согрелся – пить нельзя.
3. Пока человек не отдохнул – пить водку нельзя.
(Распространённое мнение о том, что водка согревает – миф – есть только ощущение тепла, но реальной нормализации температуры тела после водки не происходит, а то и наоборот).
Про спасение ответ далее.
Вопрос:
что делать, если человеку после рюмки водки стало плохо?
Ответ:
надо срочно дать ему сладкое, пока он не потерял сознание – например, глоток сладкого чая или конфету и т.д.
А если человек уже потерял сознание – спасти его сможет только инъекция глюкозы.
Но обычно никто ведь не держит наготове ни сладкий чай, ни глюкозу.
А зря.
Вопрос:
каково обычное воздействие этанола на состояние организма?
Ответ:
этанол часто оказывает на организм выпившего его (содержащий его напиток) человека опьяняющее действие – то есть опьяняет.
Причём чем выше градус или больше количество выпитого – тем быстрее возникает опьянение иболее продолжительное.
Вопрос:
что меняется в организме опьяневшего человека?
Ответ:
Нарушается координация движений – отсюда знакомая многим шатающаяся походка пьяных людей.
Нарушается речь – в народе об этом говорят «язык заплетается».
Многие люди начинают при опьянении говорить то, что не сказали бы в трезвом состоянии.
«Что у трезвого на уме – то у пьяного на языке».
Многие люди начинают совершать поступки, которые не совершили бы в трезвом состоянии.
Многие пьяные люди беззащитны – нередки случаи нападения на пьяных, ограбления пьяных.
А некоторые пьяные люди просто засыпают на улице и замерзают там или заболевают.
И наоборот – многие пьяные сами становятся агрессивными и нападают на других людей.
Вопрос:
что меняется в настроении опьяневшего человека?
Ответ:
многие опьяневшие люди чувствуют себя более комфортно, более раскрепощённо, более смелыми, более весёлыми, более остроумными (хотя даже они сами в трезвом виде могут посчитать, что ничего остроумного в их словах не было, сказанных в состоянии опьянения), менее напряжёнными.
Ради этого эффекта люди обычно и употребляют спиртные напитки – ради улучшения настроения.
А также ради того, чтобы «забыться» и «расслабиться», «снять стресс».
Вопрос:
какое количество алкоголя способно привести человека в состояние опьянения?
Ответ:
это индивидуально.
Разные люди пьянеют от разных количеств алкоголя.
Некоторые люди от «напёрстка» пьянеют, а другие не пьянеют и от бутылки.
Из этого следует, что выпившие и пьяный – не одно и то же.
Некоторые люди могут остаться трезвыми даже после того как выпили водку.
Но таких людей мало.
Вопрос:
почему от одной и той же дозы алкоголя одни люди пьянеют, а другие нет?
Ответ:
потому что у некоторых людей алкоголь быстро «исчезает» из организма, а у других медленно.
Если выпитый алкоголь (этанол) исчез, то он и не опьяняет человека.
Ещё раз. – В организме некоторых людей этанол быстро «исчезает», поэтому вскоре после употребления спиртных напитков этанола в их организме уже нет.
Вот такие люди и не пьянеют даже после стакана водки или больше.
А если этанол остаётся в организме долго после употребления, то и человек долго будет пьяным.
Вопрос:
почему у некоторых людей этанол быстро исчезает из организма и не делает их пьяными?
Ответ:
потому что у таких людей очень активен тот фермент, который избавляет их от этанола.
А у других людей этот фермент не очень активный.
Активность фермента зависит от генетических особенностей человека.
Остальные люди при долгом употреблении алкоголя тоже могут развить в себе способность не пьянеть от стакана или двух, но цена такой способности – цирроз и другие болезни.
Вопрос:
куда исчезает этанол из организма?
Ответ:
этанол исчезает за счёт превращения в другое вещество – оно называется уксусный альдегидом (или этаналем, или ацет-альдегидом).
Превращение этанола в этаналь происходит благодаря действию фермента – того самого, высокая активность которого даёт человеку способность много выпить, но не захмелеть (не опьянеть), то есть оставаться трезвым.
Название этого фермента – дегидрогеназа алкоголя или АлкДГ – алкоголь-дегидрогеназа.
Слово дегидрогеназа переводится как – отщепляющая водород (дву атома).
Вопрос:
как действует на организм уксусный альдегид?
Ответ:
ужасно. Потому что альдегид этот является сильным ядом для организма человека.
Это то самое вещество, действие которого на организм виновато в страданиях людей при похмелье.
(Оно проявляется в тошноте, рвоте, слабости, сильной жажде и так далее.)
Скорость возникновения похмелья после употребления алкоголя зависит от активности фермента, образующего альдегид из этанола (Алк-ДГ).
А тяжесть зависит от количества альдегида (а значит и употреблённого ранее этанола).
У некоторых людей похмелье наступает через несколько часов после употребления алкоголя, когда они уже успели «побалдеть» от действия этанола.
Такие люди часто решаются страдать снова и снова при похмелье – лишь бы перед этим ощутить опьянение.
Именно такие люди и рискуют приобрести зависимость от алкоголя.
У некоторых людей недомогание возникает очень быстро – когда они ещё не успели прочувствовать опьянение.
Такие люди не очень рискуют стать зависимыми от алкоголя, так как они не успевают почувствовать ничего приятного от его употребления, а вот неприятности чувствуют очень ярко.
А есть люди, которые не страдают от похмелья.
Они не страдают от него потому, что у них просто нет похмелья.
А похмелья у них нет потому, что их организм быстро избавляет их от уксусного альдегида.
Вот они и не страдают от похмелья – для него нет причины в виде альдегида.
Но ядовитый альдегид не только причиняет человеку страдания, но и повреждает все системы организма, что ведёт к развитию заболеваний и раннему старению.
Вопрос:
как организм избавляется от ядовитого альдегида?
Ответ:
с помощью фермента, который превращает (В ПЕЧЕНИ) уксусный альдегид в уксусную кислоту.
В итоге альдегид «исчезает», и симптомы отравления тоже исчезают – человек «выздоравливает» после похмелья, то есть после отравления альдегидом.
Поэтому даже те люди, которые не пьянеют и не страдают от похмелья, страдают от употребления этанола, так как его регулярноне употребление повреждает и их печень тоже.
Другое дело, что эти люди обычно и не имеют особого желания употреблять этанол, раз они не испытывают приятных ощущений от его употребления.
Просто они не должны считать, что не страдают от этанола, раз не испытывают похмелья. И поэтому не должны поддаваться на уговоры выпить лишний раз.
Итак.
Этанол вызывает опьянение и превращается в альдегид, который вызывает похмелье и превращается в уксусную кислоту.
***
С3.
Пропан и пропанол.
Бывают молекулы, в состав которых входит по три атома углерода.
Один атом углерода держит своей рукой (одной из четырёх) за руку (одну из четырёх) второй атом углерода,
а второй держит (одной из своих четырёх рук) третий атом углерода (за одну из его четырёх рук):
С**С**С или С–С–С.
Тут ** или одна чёрточка означают две взявшиеся «ручки».
У обоих концевых двух атомов углерода (то есть у первого и у третьего) остаётся ЕЩЁ ПО ТРИ свободных руки, то есть всего шесть свободных рук.
Эти шесть свободных рук оба эти концевые атомы углерода протягивают рукам одноруких атомов водорода – конечно же ШЕСТИ атомам водорода.
Один атом углерода протягивает три своих
свободных руки атомам водорода – и второй атом углерода точно так же протягивает три своих свободных руки атомам углерода.
Атом углерода вместе с присоединёнными к нему атомами водорода обозначается так: СН3– или так: –СН3, или так: Н3С–
При этом имеется в виду, что каждый из трёх атомов водорода (Н) присоединён только к атому углерода – между собой напрямую атомы водорода в этом случае не соединены.
А вот второй атом углерода, который протянул две своих руки другим атомам углерода, имеет только две свободных руки для соединения с атомами водорода, поэтому он соединяется только с двумя атомами водорода.
Это показывают так: –СН2–
Чёрточки означают, что «СН2» входит в состав молекулы, а не является свободной молекулой.
Можно считать эти чёрточки ручками атома углерода, протянутыми соседним атомам углерода (первому и третьему).
В целом эту молекулу из двух атомов углерода можно показывать так:
Н3С–СН2–СН3.
Или так:
СН3–СН2–СН3.
В обоих случаях имеется в виду, что три атома углерода (С) соединены между собой,
причём напрямую, а не через Н или три Н,
а к каждому из обоих концевых атомов углерода присоединены по три атома Н,
а к «промежуточному» второму атому углерода присоединены только два атома водорода (Н).
А можно написать формулу этой молекулы и так (если «сжать» до простой формулы, показывающей только число атомов разных элементов): С3Н8.
Вещество, молекулы которого имеют такой состав, называется ПРОПАНом (пропан).
Пропан тоже является газом в обычных условиях.
Название «пропан» можно часто заметить на цистернах на железной дороге.
Как и название «бутан» – название похожего на пропан газа, но его молекулы состоят не из трёх, а из четырёх атомов углерода.
Если в молекулу пропана добавить всего один атом кислорода (вставив его между атомом углерода и любым из атомов водорода), то в молекуле (теперь уже бывшего) пропана получится такая группа: –С–О–Н.
Такая группа (ОН) называется спиртовой (если рядом нет С=О) – об этом говориться в разделе про карбоксильную группу), а молекулы с такой группой называются спиртами или алкоголями.
Но не путайте эти спирты и алкоголи с магазинскими алкоголями – в химии это понятие шире, и подробнее об этом рассказано далее.
Атом кислорода вставлен между любым из атомов водорода и соединённым с ним атомом углерода.
Окончание «ол» означает наличие спиртовой (ОН) группы.
Формула пропанола выглядит так же, как формула пропана (СН3–СН2–СН3), но с дополнительной буквой О (означающей наличие атома кислорода):
СН3–СН2–СН2ОН.
Или так: С3Н7ОН.
(Это сжатый вариант, показывающий состав молекулы пропанола).
Здесь показан вариант, в котором атом кислорода (О) «вставлен» между концевым атомом углерода (С) и соединённым с ним атомом водорода (Н).
Но атом кислорода может быть вставлен и между вторым атомом углерода и соединённым с ним атомом водорода.
В таком случае получилась бы немного другая молекула пропанола – с тем же составом, что в обычном пропаноле, но с другим порядком соединения атомов в молекуле.
Свойства этого другого пропанола отличаются от свойств обычного пропанола.
А вообще такие молекулы, которые имеют одинаковый состав, но разный порядок соединения атомов (то есть разную СТРУКТУРУ), называются ИЗОМЕРАМИ, а явление существования изомеров называется изомерией.
С4
Бутан и бутанол.
Бывают молекулы, в состав которых входит по четыре атома углерода.
Один атом углерода держит своей рукой (одной из четырёх) за руку (одну из четырёх) второй атом углерода,
а второй атом углерода держит (одной из своих четырёх рук) третий атом углерода (за одну из его четырёх рук),
а третий атом углерода держит (одной из своих четырёх рук) четвёртый атом углерода (за одну из его четырёх рук).
Можно показать эьу цепочку из четырёх атомов углерода так:
С**С**С**С или С–С–С–С.
Тут ** или одна чёрточка означают две взявшиеся «ручки».
У обоих концевых двух атомов углерода (то есть у первого и у четвёртого) остаётся ЕЩЁ ПО ТРИ свободных руки, то есть всего шесть свободных рук.
Эти шесть свободных рук оба эти концевые атомы углерода протягивают рукам одноруких атомов водорода – конечно же ШЕСТИ атомам водорода.
Первый атом углерода протягивает три своих
свободных руки атомам водорода – и четвёртый атом углерода точно так же протягивает три своих свободных руки атомам водорода.
Атом углерода вместе с присоединёнными к нему атомами водорода обозначается так: СН3– или так: –СН3, или так: Н3С–
При этом имеется в виду, что каждый из трёх атомов водорода (Н) присоединён только к атому углерода – между собой напрямую атомы водорода в этом случае не соединены.
А вот второй и третий атомы углерода, которые протянули по две своих руки другим атомам углерода (второй атом – первому и третьему, а третий атом – второму и четвёртому), имеют только ПО ДВЕ свободных руки для соединения с атомами водорода, поэтому они (второй и третий) атомы углерода соединяются только с двумя атомами водорода.
Это показывают так: –СН2–
Чёрточки означают, что «СН2» входит в состав молекулы, а не является свободной молекулой.
Можно считать эти чёрточки ручками атома углерода, протянутыми соседним атомам углерода (первому и третьему у второго, а у третьего – второму т четвёртому).
В целом эту молекулу из четырёх атомов углерода можно показывать так:
Н3С–СН2–СН2–СН3.
Или так:
СН3–СН2–СН2–СН3.
В обоих случаях имеется в виду, что четыре атома углерода (С) соединены между собой,
причём напрямую, а не через Н или три Н,
а к каждому из обоих концевых атомов углерода присоединены по три атома Н,
а к «промежуточным» второму и третьему атомам углерода присоединены только по два атома водорода (Н).
А можно написать формулу этой молекулы и так (если «сжать» до простой формулы, показывающей только число атомов разных элементов): С4Н10.
Вещество, молекулы которого имеют такой состав, называется БУТАНом (бутан).
Бутан тоже является газом в обычных условиях.
Название «бутан» можно часто заметить на цистернах на железной дороге.
Как и название «пропан» – название похожего на бутан газа, но его молекулы состоят не из четырёх, а из трёх атомов углерода.
Если в молекулу бутана добавить всего один атом кислорода (вставив его между атомом углерода и любым из атомов водорода), то в молекуле (теперь уже бывшего) бутана получится такая группа атомов: –С–О–Н.
Такая группа (ОН) называется спиртовой (если рядом нет С=О – об этом говориться в разделе про карбоксильную группу), а молекулы с такой группой называются спиртами или алкоголями.
Но не путайте эти спирты и алкоголи с магазинскими алкоголями – в химии это понятие шире, и подробнее об этом рассказано далее.
Атом кислорода вставлен между любым из атомов водорода и соединённым с ним атомом углерода.
Окончание «ол» означает наличие спиртовой (ОН) группы.
Формула бутанола выглядит так же, как формула бутана (СН3–СН2–СН2–СН3), но с дополнительной буквой О (означающей наличие атома кислорода):
СН3–СН2–СН2–СН2ОН.
Или так: С4Н9ОН.
(Это сжатый вариант, показывающий состав молекулы бутанола).
Здесь показан вариант, в котором атом кислорода (О) «вставлен» между концевым атомом углерода (С) и соединённым с ним атомом водорода (Н).
Но атом кислорода может быть вставлен и между вторым атомом углерода и соединённым с ним атомом водорода.
В таком случае получилась бы немного другая молекула бутанола – с тем же составом, что в обычном бутаноле, но с другим порядком соединения атомов в молекуле.
Свойства этого другого бутанола отличаются от свойств обычного бутанола.
А вообще такие молекулы, которые имеют одинаковый состав, но разный порядок соединения атомов (то есть разную СТРУКТУРУ), называются ИЗОМЕРАМИ, а явление существования изомеров называется изомерией.
И молекула самого бутана тоже бывает бывает другой.
Здесь показана была молекула, где все атомы углерода соединены, как вагоны поезда:
С-С-С-С.
Такие молекулы называются линейными. Потому что атомы углерода расположены как бы в одну линию.
Но четвёртый атом углерода может присоединиться не к третьему атому углерода, а ко второму.
И тогда получится молекула с другим порядком соединения атомов, то есть изомер линейной молекулы бутана.
Такие углеродные цепочки называются разветвлёнными.
Признаком разветвлённости является наличие у одного и того же атома углерода связей с тремя атомами углерода.
Распределение атомов водорода в изомерах и разветвлённых молекулах происходит в сооответствии с валентностью, то есть у каждого углерода все свободные от связей с другими атомами углерода «ручки» соединяются с атомами водорода.
С5
Органические молекулы (углеводороды) с пятью атомами углерода:
Пентан и пентанол.
Бывают молекулы, в состав которых входит по пять атомов углерода.
Один атом углерода держит своей рукой (одной из четырёх) за руку (одну из четырёх) второй атом углерода,
а второй атом углерода держит (одной из своих четырёх рук) третий атом углерода (за одну из его четырёх рук),
третий атом углерода держит (одной из своих четырёх рук) четвёртый атом углерода (за одну из его четырёх рук),
а четвёртый атом углерода держит за ручку пятый аом углерода.
Можно показать эту цепочку из четырёх атомов углерода так:
С**С**С**С**С или С–С–С–С–С.
Тут ** или одна чёрточка означают две взявшиеся «ручки» атомов углерода.
Все свободные ручки, то есть не использованные для связи с другими атомам углерода, атомы углерода протягивают атомам водорода.
В целом эту молекулу из пяти атомов углерода можно показывать так:
Н3С–СН2–СН2–СН2–СН3.
Или так:
СН3–СН2–СН2–СН2–СН3.
В обоих случаях имеется в виду, что пять атомов углерода (С) соединены между собой,
причём напрямую, а не через Н или три Н,
а к каждому из обоих концевых атомов углерода присоединены по три атома Н,
а к «промежуточным» второму третьему и четвёртому атомам углерода присоединены только по два атома водорода (Н).
А можно написать формулу этой молекулы и так (если «сжать» до простой формулы, показывающей только число атомов разных элементов): С5Н12.
Вещество, молекулы которого имеют такой состав, называется ПЕНТАНом (пентан).
Если в молекулу пентана добавить всего один атом кислорода (вставив его между атомом углерода и любым из атомов водорода), то в молекуле (теперь уже бывшего) бутана получится такая группа атомов: –С–О–Н.
Атом кислорода вставлен между любым из атомов водорода и соединённым с ним атомом углерода.
Окончание «ол» означает наличие спиртовой (ОН) группы.
Формула пентанола выглядит так же, как формула пентана (СН3–СН2–СН2–СН3), но с дополнительной буквой О (означающей наличие атома кислорода):
СН3–СН2–СН2–СН2–СН2ОН.
Или так: С5Н11ОН.
(Это сжатый вариант, показывающий состав молекулы пентанола).
Здесь показан вариант, в котором атом кислорода (О) «вставлен» между концевым атомом углерода (С) и соединённым с ним атомом водорода (Н).
Но атом кислорода может быть вставлен и между вторым атомом углерода и соединённым с ним атомом водорода.
Или между третим атомом углерода и соединённым с ним атомом водорода.
В таком случае получилась бы немного другая молекула пентанола – с тем же составом, что в обычном пентаноле, но с другим порядком соединения атомов в молекуле.
Свойства этого другого пентанола отличаются от свойств обычного пентанола.
А вообще такие молекулы, которые имеют одинаковый состав, но разный порядок соединения атомов (то есть разную СТРУКТУРУ), называются ИЗОМЕРАМИ, а явление существования изомеров называется изомерией.
И молекула самого пентана тоже бывает бывает другой.
Здесь показана была молекула, где все атомы углерода соединены, как вагоны поезда:
С-С-С-С-С.
Такие молекулы называются линейными.
Потому что атомы углерода расположены как бы в одну линию.
Но пятый атом углерода может присоединиться не к четвёртому атому углерода, а ко второму или третьему.
И тогда получится молекула с другим порядком соединения атомов, то есть изомер линейной молекулы бутана.
Такие углеродные цепочки называются разветвлёнными.
Признаком разветвлённости является наличие у одного и того же атома углерода связей с тремя атомами углерода.
Распределение атомов водорода в изомерах и разветвлённых молекулах происходит в сооответствии с валентностью, то есть у каждого углерода все свободные от связей с другими атомами углерода «ручки» соединяются с атомами водорода.
С6 и так далее.
Наряду с выше показанными молекулами, содеращими от одного до пяти атомов углерода,
существуют молекулы из шести атомов углерода и соответствующего числа атомов водорода, из семи атомов углерода, восьми атомов углерода и так далее.
Они устроены точно так же, как показанные молекулы до пяти атомов углерода.
Поэтому нет смысла подробно описывать их по схемам выше.
Достаточно просто сообщить их названия и показать формулы.
6С
Шестиуглеродные молекулы имеют такую формулу:
СН3–СН2–СН2–СН2–СН2–СН3.
Или в сжатом виде:
С6Н14.
Вещество, молекулы которого имеют такой состав, называется ГЕКСаном (гексан).
«Гекс» означает шесть.
Показанная молекула гексана – линейная, но бывают и разветвлённые молекулы гексана – его изомеры с таким же составом, но с другим порядком соединения атомов.
Если в молекуле гексана появляется атом кислорода, то получается такая молекула:
СН3–СН2–СН2–СН2–СН2–СН2ОН.
Вещество, молекулы которого имеют такой состав, называются гексанОЛом.
ГексанОЛ – это спирт, как и любое вещество с группой ОН.
Гексан очень интересен тем, что его концевые атомы углерода могут соединиться, образовав цикл.
Такая молекула называется циклогексаном, то есть циклическим гексаном.
С7
Семиуглеродная органическая молекула называется ГЕПТаном (гептан), а семиуглеродный спирт (как гептан, но с атомом кислорода) – гептанОЛом (гептанол).
Состав гептана – С7Н16.
И так далее.
Восьмиуглеродная молекула – октан.
Состав октана – С8Н18.
Девятиуглеродная – нонан.
Состав нонана – С9Н20.
Десятиуглеродная – декан.
Состав декана – С10Н22.
11 атомов углерода – ундекан.
12 атомов углерода – додекан
13 – тридекан.
Чем больше атомов углерода – тем более тяжёлой получается молекула.
Поэтому октан и нонан – жидкие вещества.
Октан – это то самое вещество, которое влияет на октановое число бензина.
Формулы состава этих молекул не нужно зубрить.
Нужно просто понять закономерность: количество атомов водорода в два раза больше, чем атомов углерода, плюс ещё два атома водорода.
(Кроме метана – там так считать не нужно).
Если атомов углерода два, то атомов водорода 2*2+2=6 (этан).
Если атомов углерода три, то атомов водорода 3*2+2=8 (пропан).
Если атомов углерода четыре, то атомов водорода 4*2+2=10 (пропан).
Если атомов углерода пять, то атомов водорода 5*2+2=12 (пентан).
Если атомов углерода шесть, то атомов водорода 6*2+2=14 (гексан).
Если атомов углерода семь, то атомов водорода 7*2+2=16 (гептан).
Если атомов углерода восемь, то атомов водорода 8*2+2=18 (этан).
И т.д. для нонана, декана и т.д.
Ну а число атомов углерода подсказывается «приставками», которые придётся выучить, но их всё равно стоит знать, так как они часто встречаются в науке.
(Это конечно корни, а не приставки, но тут удобнее называть приставками.)
Приставка «пент» означает «пять».
Примеры слов – пент-аэдр.
Гекс – шесть.
Пример слова – гексаэдр.
Окт – восемь.
Примеры слов – октава, октаэдр.
Если в молекуле два атома углерода – приставка ЭТ.
Примеры – этан, этанол.
Если три атома углерода в молекуле – приставка ПРОП.
Примеры – пропан, пропанол.
Четыре углерода – БУТ.
Примеры веществ – бутан, бутанол.
Пять атомов углерода – ПЕНТ.
Примеры – пентан, пентанол.
Шесть атомов углерода – ГЕКС.
Примеры – гексан, циклогексан, гексанол.
Семь атомов углерода – ГЕПТ.
Примеры – гептан, гептанол.
Восемь атомов углерода – ОКТ.
Примеры веществ – октан.
Ещё раз кратко:
С1 – мет,
С2 – эт,
С3 – проп,
С4 – бут,
С5 – пент,
С6 – гекс,
С7 – гепт,
С8 – окт.
Вместе с окончаниями «ан» эти приставки дают такие названия:
метАН (С1),
этАН (С2),
пропАН (С3),
бутАН (С4),
пентАН (С5),
гексАН (С6),
гептАН (С7),
октАН (С8),
нонАН (9) и т.д.
Все эти вещества относятся к группе веществ, которая называется алканами.
Окончание «ан», которое одинаково у всех алканов, является подсказкой, что вещество относится к группе алканов (к классу алканов).
АЛКАНЫ –
это один из классов органических веществ, самый простой из всех.
Все алканы представляют собой цепочки атомов углерода,
в которых между атомами углерода только по одной одинарной связи (а бывают и другие связи),
а остальные связи атомы углерода «заняты» атомами водорода,
причём максмально возможным числом атомов водорода –
присоединить ещё больше атомов водорода, чем уже присоединено к атомам углерода, уже невозможно.
Поэтому второе название класса алканов – насыщенные.
Имеется в виду, что они насыщены атомами водорода.
При этом никаких других атомов, кроме С и Н, в молекулах алканов нет – ни кислорода (как у спиртов), ни серы, ни азота и т.д.
Наличие этих атомов превратило бы молекулу алкана в молекулу вещества другого класса (далее).
Определение алканам дают такое:
алканы – это класс органических веществ, в которых число атомов водорода рассчитывается по такой формуле:
число атомов углерода плюс единица и результат умножить на два.
Обозначим число атомов углерода как N, а число атомов водорода как M.
Тогда формула для вычисления числа атомов водорода записывается так:
(N+1)*2=M (числа атомов водорода).
По этой формуле у одно-углеродной молекулы
должно быть (1+1)*2=4 атома водорода,
что мы и видели в молекуле одно-углеродного метана – СН4.
С2
По этой формуле у двух-углеродной молекулы
должно быть (2+1)*2=6 атомов водорода,
что мы и видели в молекуле двух-углеродного этана – С2Н6.
С3
По этой формуле у трёх-углеродной молекулы
должно быть (3+1)*2=8 атомов водорода,
что мы и видели в молекуле трёх-углеродного пропана – С3Н8.
С4
По этой формуле у четырёх-углеродной молекулы
должно быть (4+1)*2=10 атомов водорода,
что мы и видели в молекуле четырёх-углеродного бутана – С4Н10.
С5
По этой формуле у пяти-углеродной молекулы
должно быть (5+1)*2=12 атомов водорода,
что мы и видели в молекуле пяти-углеродного пентана – С5Н12.
С6
По этой формуле у шести-углеродной молекулы
должно быть (6+1)*2=14 атомов водорода,
что мы и видели в шестиуглеродной молекуле гексана – С6Н14.
С7
По этой формуле у семи-углеродной молекулы
должно быть (7+1)*2=16 атомов водорода,
что мы и видели в семи-углеродной молекуле гептана – С7Н16.
С8
По этой формуле у восьми-углеродной молекулы
должно быть (8+1)*2=18 атомов водорода,
что мы и видели в восьми-углеродной молекуле октана – С8Н18.
С9
По этой формуле у девяти-углеродной молекулы
должно быть (9+1)*2=20 атомов водорода,
что мы и видели в девяти-углеродной молекуле нонана – С9Н20.
С10
По этой формуле у десяти-углеродной молекулы
должно быть (10+1)*2=22 атома водорода,
что мы и видели в десяти-углеродной молекуле декана – С10Н22.
И т.д. –
С11 (ундекан):
(11+1)*2=24, С11Н24.
С12 (додекан):
(12+1)*2=26, С12Н24.
С13 (тридекан):
(13+1)*2=28, С13Н28.
С14 (тетра-декан):
(14+1)*2=30, С14Н30.
С15 (пента-декан):
(15+1)*2=32, С15Н32.
С16 (гекса-декан):
(16+1)*2=34, С16Н34.
С17 (гепта-декан):
(17+1)*2=36, С17Н35.
С18 (окта-декан):
(18+1)*2=38, С18Н38.
Таковы алканы и их формулы.
У молекулы алкана можно «забрать» один атом водорода, отщепив его от любого из двух концевых атомов углерода. –
Например, у молекулы метана СН4 можно забрать один из четырёх атомов Н – и тогда останется группа атомов такого состава: СН3.
Или атом водорода можно забрать у молекулы этана: СН3–СН3.
И тогда от молекулы этана останется группа атомов такого состава:
СН3–СН2–.
Надеюсь, понятно, что при отнятии атома водорода получается то же самое, что и было, но на один атом водорода меньше.
Эти объекты, эти группы атомов, которые получаются при убирании одного атома водорода, называются углеводородными радикалами.
Этот термин используется часто – поэтому стоит понимать, что им обозначают.
Радикалы, формулы которых показаны выше, атом водорода убирается от концевого атома углерода – такие радикалы называются первичными.
Но у трёх-углеродных и более длинных алканов атом водорода можно убрать и у неконцевого атома углерода – и тогда получится радикал, который называется вторичным.
Но эти сведения вторичны, и и тут они разбираться пока не будут – только в учебниках.
В свободном виде в природе радикалы не существуют –
они обычно соединены с какой-то группой атомов взамен отнятого атома водорода.
Примеры групп атомов, которые могут быть соединены с радикалом вместо отнятого водорода:
О формулах радикалов.
Формулы радикалов такие же, как у алканов,
но в них на один атом водорода меньше.
(Значит, их не надо учить – надо просто из формулы алкана убрать один атом водорола).
Названия радикалов.
Названия радикалов такие же, как у алканов, из которых они получены, но окончание «ан» меняется на окончание «ил».
Например, меняем окончание у метАНа – получается метИЛ.
Отсюда слово метил-овый. Например, метиловый спирт – синоним метанола.
Так же:
(С2) этан – этИЛ (этиловый),
(С3) пропан – пропИЛ (пропиловый),
(С4) бутан – бутИЛ (бутиловый),
(С5) пентан – пентил,
(С6) гексан – гексил,
(С7) гептан – гептил,
(С8) октан – октил и т.д.
АЛЬДЕГИДЫ и кетоны
Выше в разговоре об отравлении спиртами упоминались ядовитые альдегиды – уксусный альдегид и метаналь, которые и были настоящими ядами, образующимися из спиртов уже внутри организма его собственными ферментами.
Разберём подробнее, что такое альдегиды.
А заодно и кетоны.
Происхождение альдегидов.
У спиртов (то есть веществ с ОН группами)
можно забирать по два атома водорода (Н) –
один от атома кислорода (О) спиртовой группы (ОН),
а второй – от атома углерода (С).
Например, у спирта метанола (формула СН3ОН)
заберём два атома водорода (2Н).
То есть: у исходного Н3С–ОН убираем 2 атома Н,
получается: Н2СО.
В результате убирания двух атомов водорода от молекулы спирта
получаются молекулы, которые такие же, как исходные спирты,
но содержат на два атома водорода
(не любых, а названных) меньше.
Такие молекулы называются альдегидами.
(То есть вещества, состоящие из таких молекул.)
Это если спиртовая группа была при первом атоме углерода;
такие спирты называются первичными.
Тогда получается альдегид.
А если спиртовая группа была не при первом атоме углерода, а при втором или другом –
тогда из спиртов получаются не альдегиды,
а КЕТОНЫ, но подробнее об этом далее.
Условно (для упрощения) можно сказать,
что альдегид – это бывший спирт (первичный),
лишённый двух атомов водорода
(отщеплённых от атома кислорода и соединённого с ним атома углерода,
то есть «по спиртовой группе»).
И точно так же можно сказать,
что кетон – это бывший вторичный спирт,
лишённый двух атомов водорода
(отщеплённых от атома кислорода и соединённого с ним атома углерода,
то есть «по спиртовой группе»).
Лишение двух атомов водорода – это один из способов окисления молекул.
(Подробнее об окислении в другой раз).
Поэтому фактически альдегид – это окисленный спирт (первичный).
Поэтому же часто говорят, что альдегиды являются продуктами окисления спиртов (первичных).
И наоборот – спирты (первичные) являются продуктами восстановления альдегидов
(восстановлением называется процесс, который противоположен окислению,
то есть не отщепление двух атомов водорода,
а присоединение двух атомов водорода).
В том смысле, что при восстановлении альдегидов в самом деле образуются спирты.
И точно так же можно сказать, что кетоны – это продукты окисления спиртов,
но не первичных, а вторичных,
то есть таких, у которых ОН группа была не при первом атоме углерода,
а при втором или третьем и т.д..
При возвращении атомов водорода «по кето-группе»
(то есть при восстановлении кетона)
снова образуется спиртовая (ОН) группа,
а вещество снова становится вторичным спиртом.
Формулы…
Между атомом углерода С и атомом кислорода О, от которых отняты атомы водорода,
образуется вторая связь,
то есть появляется одна двойная связь,
которая обозначается между С и О так:
С=О.
Итак, альдегиды (и кетоны) имеют группу атомов С=О.
Такая группа называется карбонильной группой.
Когда атом углерода карбонильной группы является первым по счёту в углеродной цепочке,
то карбонильная группа называется альдегидной.
У входящего в состав этой альдегидной группы атома углерода есть один атом водорода:
Н–С=О.
Вещества, молекулы которых имеют такую альдегидную группу, называются альдегидами.
Когда атом углерода карбонильной группы (С=О) является не первым по счёту, а вторым (и т.д.),
то он не связан с атомом водорода,
а связан (кроме атома кислорода карбонильной группы) с двумя соседними атомами углерода.
Карбонильная группа, в состав которой входит не первый атом углерода, а другой, называется кетогруппой,
а вещества, в составе которых есть кетогруппа, называются кетонами.
Но всё это только в том случае, если наряду с карбонильной группой нет так называемой более старшей
(то есть более окисленной группы) –
например, карбоксильной группы;
(её формула: НО–С=О или сжато так: –СООН).
Если она есть, то вещество будет не кетоном, а кетокислотой
(см. далее подробнее о карбоновых кислотах).
Не нужно путать С=О в составе карбонильной группы и в составе карбоксильной группы.
В составе карбоксильной группы тот же атом углерода связан ещё и с атомами ОН.
И не нужно путать спиртовую группу ОН с атомами ОН карбоксильной группы –
в составе карбоксильной группы ОН атомы связаны с атомом углерода,
который соединён ещё и с атомом кислородом двойной связью.
Итак, выше разобрались с определением альдегидов и кетонов и альдегидной и кетогруппами (разновидностями карбонильной группы).
Теперь о названиях и формулах альдегидов.
Названия альдегидов образуют, просто добавляя окончание «аль»
к названиям алканов,
имеющих такое же число атомов углерода, как и альдегид.
По тому же принципу получаем названия других альдегидов:
С5 – пентан-аль (пентиловый альдегид),
С6 – гексан-аль (гексиловый альдегид),
С7 – гептан-аль,
С8 – октан-аль и т.д.
Формулы альдегидов
пишутся так же, как формулы соответствующих спиртов, но два атома углерода убирают:
один атом водорода – от атома кислорода О,
а второй атов водорода – от атома углерода С,
который соединён с этим атомом кислорода.
Связь между атомом кислорода и атомом углерода рисуют двойной.
Стоит потренироваться – написать формулы спиртов и поубирать у них атомы водорода так, чтобы спиртовые группы стали альдегидными,
а формулы спиртов стали формулами альдегидов.
Органические (карбоновые кислоты).
Существует группаатомов, которая похожа на альдегидную группу,
но в ней между атомом водорода и атомом углерода «вставлен» атом кислорода –
вдобавок к уже имеющемуся атому кислорода.
То есть вместо группы Н–C=О
мы имеем группу НО–С=О.
Видно, что в этой группе на один атом кислорода больше, чем в альдегидной группе.
Такая группа называется карбоКСильной,
а молекулы с такой группой называются карбоновыми или органическими кислотами.
То есть так называются вещества, молекулы которых содержат в себе карбоксильную группу.
Бывают молекулы с одной карбоксильной группой – вещества, состоящие из таких молекул, называются моно-карбоновыми кислотами.
Молекулы с тремя карбоксильными группами называются трикарбоновыми кислотами.
Примеры трикарбоновой кислоты –
лимонная кислота (названиеи её аниона – цитрат)
и её изомер – изолимонная кислота
(название её аниона – изоцитрат).
Значение цитрата и изоцитрата см. в параграфе про цикл трикарбоновых кислот («цикл Кребса»).
Примеры дикарбоновых кислот –
Пяти-углеродная (С5) дикарбоновая кислота называется глутаровой.
Название её аниона или соли – глутарат.
Четырёх-углеродная дикарбоновая кислота (С4) называется «янтарной».
Название её аниона или – сукцинат.
Трёх-углеродная (С3) дикарбоновая кислота называется малоновой.
Название её аниона или соли – малонат.
Двух-углеродная дикарбоновая кислота (С2) называется щавелевой.
Название её аниона или соли – оксалат.
Одноуглеродных дикарбоновых кислот не бывает и быть не может по определению, так как дикарбоновый – это уже имеющий два атома углерода.
Немного о ролях и значении
дикарбоновых кислот.
Янтарная кислота очень важна в связи с участием в работе цикла Кребса.
Глутаровая кислота с кето-группой (кетоглутарат) тоже участвует в цикле Кребса.
Глутаровая кислота с аминогруппой (аминоглутарат = глутамат) – главный возбуждающий медиатор головного мозга.
А вот оксалаты бывают компонентами камней – это негативная роль.
Но к оксалоацетату оксалаты никакого отношения не имеют. Оксалоацетат хороший и очень нужный.
Теперь поговорим о самых простых названиях – о названиях монокарбоновых кислот.
Названия монокарбоновых кислот
(номенклатура монокарбоновых кислот).
У монокарбоновых кислот есть так называемые тривиальные названия, но их разрешается называть и теми названиями, которые не надо учить, если уже знаешь названия алканов с таким же числом атомов углерода.
Достаточно добавить окончание «овая» к названию алкана с таким же числом атомов углерода.
Перечислим названия всех монокарбоновых кислот, образуемых по такому же принципу.
И заодно в скобках дадим другие названия (синонимы) некоторых из кислот.
Одно-углеродная монокарбоновая кислота (С1):
метан-овая (муравьиная).
Двух-углеродная моно-карбоновая кислота (С2):
этан-овая (уксусная).
Трёх-углеродная моно-карбоновая кислота (С3):
пропан-овая.
Четырёх-углеродная моно-карбоновая кислота:
бутан-овая (масляная – потому что она есть в масле).
Пяти-углеродная (С5) монокарбоновая кислота:
пентан-овая.
Шести-углеродная (С6) моно-карбоновая кислота:
гексан-овая.
Семи-углеродная (С7) моно-карбоноваяк ислота:
гептан-овая.
И т.д. – октан-овая (октан),
нонан-овая (С9),
декан-овая (С10),
ундекановая (С11),
додекан-овая (С12),
три-декан-овая (С13),
тетра-декан-овая (С14),
пента-декан-овая (С15),
гекса-декан-овая (С16),
гепта-декан-овая (С17)
окта-декан-овая (С18) и т.д.
У гексадекановой (С16) есть синоним – пальмитиновая.
У окта-декан-овой тоже есть синоним – стеариновая.
Очень интересны эти пальмитиновая и стеариновая.
Их фрагменты (точнее, вся молекула без ОН атомов карбоксильной группы) входят в состав жиров.
Ещё интереснее 20-тиуглеродная кислота – эйкозановая, но об этом читайте в параграфах про омега-6-жиры и омега-3-жиры.
В итоге вместо формулы метана (С1)
будет такая формулы метановой (муравьиной) кислоты:
НСООН.
Вместо формулы этана (С2)
будет такая формула этановой кислоты (уксусной):
СН3–СООН.
Вместо формулы пропана (С3)
будет такая формула пропановой кислоты:
СН3–СН2–СООН.
Вместо формулы бутана (С4)
Будет такая формула бутан-овой (масляной) кислоты:
СН3–СН2–СН2–СООН.
Вместо формулы пентана (С5)
будет формула пентан-овой кислоты:
СН3–СН2–СН2–СН2–СООН.
Вместо формулы гексана
будет формула гексан-овой кислоты:
СН3–СН2–СН2–СН2–СООН.
Когда групп «СН2» становится много – разрешается сокращать для удобства их перечисление,
ставя просто скобки вокруг СН2 (вот так – (СН2))
и указывая после скобок число СН2 групп.
Например, (СН2)2 у масляной или (СН2)3 у пентановой.
Таким образом, формула пальмитиновой (С16) кислоты записывается так:
СН3–(СН2)14–СООН.
И это намного удобнее, чем писать «СН2» четырнадцать раз.
Но можно сжать ещё больше – всё, кроме СООН группы, сложить – и получится такой вид формулы:
С15Н31–СООН.
Напомню, что С15Н31 – это пример РАДИКАЛА, углеводородного радикала.
Формула стеариновой (С18) кислоты:
СН3–(СН2)16–СООН.
То же самое, но более сжато: С17Н35–СООН.
Немного о роли уксусной кислоты.
Она широко применяется в кулинарии, а в организме образуется из этанола (этилового спирта) после употребления водки или пива и т.д.
А вот так называемые тиоэфиры уксусной кислоты с так называемым коферментом А, которые называются ацетил-КоА, играют ЦЕНТРАЛЬНУЮ роль в обмене веществ клеток человека, да и всех других организмов, но об этом – в курсе биохимии – см. про цикл Кребса и т.д.
Между двумя атомами водорода могут образовываться не только обычные одинарные связи, но и двойные связи.
Двойные связи образуются, когда оба атома протягивают друг другу по две руки.
Двойная связь обозначается знаком «=».
Между атомами водорода она выглядить так: С=С.
Молекулы (соединения), состоящие из атомов водорода и углерода (то есть углеводородные = органические) и имеющие одну двойную связь или несколько, называются алкЕнами.
АлкЕны – это тоже класс органических соединений, как и алканы.
Двойные связи относятся к так называемым кратным связям, как и тройные связи.
Алкены относятся к ненасыщенным соединениям.
Названия алкенов почти точно такие же,
как у алканов с таким же числом атомов углерода,
но с одним отличием –
вместо окончания «ан» у алкЕНов окончание «ен».
То есть названия отличаются только одной буквой – «е» вместо «а» в окончании.
Поэтому зубрить названия алкенов не надо, если вы уже знаете названия алканов –
надо просто менять одну букву в название.
Примеры.
Этан – этен.
Пропан – пропен.
Бутан – бутен.
Пентан – пентен.
Гексан – гексен.
Гептан – гептен.
И т.д.
Окончание «ен» не просто означает принадлежность вещества к классу алкенов –
оно означает наличие в молекуле – двойной связи.
Оба атома углерода при наличии между ними двойной связи имеют ещё по две свободных связи, то есть по две валентности,
то есть могут образовывать ещё по две связи с другими атомами – углерода или водорода, кислорода и т.д.
Если в молекулах алкенов только одна двойная связь, то число атомов водорода в них ровно в два раза больше, чем число атомов углерода.
И на 2 атома водорода меньше, чем в молекулах алканов.
Примеры формул алкенов:
Если атомов углерода 2, то атомов водорода в 2 раза больше – 4.
Поэтому формула получается такой: С2Н4.
Это формула этена.
Его формулу можно показывать так:
СН2=СН2
Или так:
Н2С=СН2
Алкен С3 – проп-ен.
Если атомов углерода 3, то атомов водорода в 2 раза больше – 6.
Поэтому формула получается такой: С3Н6.
Это формула пропена.
Его формулу можно показывать так:
СН2=СН–СН3
Или так:
СН3–НС=СН2
Это одна и та же формула.
Одного и того же вещества (пропена).
Причём число атомов водорода учить тут не надо.
Нужно просто написать три атома углерода,
одну из двух связей нарисовать двойной (=),
а число атомов водорода вычислить, исходя из того, что каждый атом углерода должен образовать четыре связи с другими атомами.
Алкен С4 – бутен.
Если атомов углерода 4, то атомов водорода в 2 раза больше – 8.
Поэтому формула получается такой: С4Н8.
Это формула бутена.
Его формулу можно показывать так:
СН2=СН–СН2–СН3
Или так:
СН3–СН2–НС=СН2
Это одна и та же формула.
Одного и того же вещества (бутена).
Причём число атомов водорода учить тут тоже не надо.
Нужно просто написать 4 атома углерода,
одну из двух связей нарисовать двойной (=),
а число атомов водорода вычислить, исходя из того, что каждый атом углерода должен образовать четыре связи с другими атомами.
Но если двойная связь находится посередине молекулы, то есть между вторым атомом углерода и третьим атомом углерода, то это уже другое вещество – с другим порядком соединения атомов в молекуле, хоть и с таким же составом, как у бутена в первом примере, то есть это изомер первого бутена.
СН3–СН=СН–СН3
И тут снова число атомов водорода расставляется, исходя из того, что валентность углерода – четыре.
Ничего зубрить не надо.
Существуют правила называния изомеров, но тут мы их приводить не стане пока – это есть в учебниках химии за 10 класс.
Алкен С5 – пент-ен.
Если атомов углерода 5, то атомов водорода в молекуле алкена в 2 раза больше – 10.
Поэтому формула получается такой: С5Н10.
Это формула пентена.
Его формулу можно показывать так:
СН2=СН–СН2–СН2–СН3
Или так:
СН3–СН2–СН2–НС=СН2
Это одна и та же формула.
Одного и того же вещества (бутена).
Причём число атомов водорода учить тут тоже не надо.
Нужно просто написать 5 атомов углерода,
одну из двух связей нарисовать двойной (=),
а число атомов водорода вычислить, исходя из того, что каждый атом углерода должен образовать четыре связи с другими атомами.
Но если двойная связь находится в другом месте, то есть между вторым атомом углерода и третьим атомом углерода, то это уже другое вещество – с другим порядком соединения атомов в молекуле, хоть и с таким же составом, как у пентена в первом примере, то есть это изомер первого пентена.
Его формула такая:
СН3–СН=СН–СН2–СН3
Или такая (это тоже самое, но с другого конца):
СН3–СН2–СН=СН–СН3
И тут снова число атомов водорода расставляется, исходя из того, что валентность углерода – четыре.
Ничего зубрить не надо.
Алкен С6 (гекс-ен)
С6Н12
СН2=СН–СН2–СН2–СН2–СН3
И то же самое:
СН3–СН2–СН2–СН2–СН=СН2
Изомер гексена по положению двойной связи:
СН3–СН=СН–СН2–СН2–СН3
и то же самое:
СН3–СН2–СН2–СН=СН–СН3
И третий изомер:
СН3–СН2–СН=СН–СН2–СН3
Попробуйте сами написать формулы алкенов и их изомеров для С7, С8, С9 и т.д.