Как дать собаке энтеросгель
Как дать собаке энтеросгель
Энтеросгель для собак – первая помощь при отравлении
Содержание
О том, что данный препарат из группы энтеросорбентов эффективно помогает при отравлениях, знает практически каждый человек. Однако не менее результативно применяется Энтеросгель для собак и других домашних питомцев – он быстро устраняет токсичные вещества из желудка и кишечника, сорбируя их на своей поверхности.
Общее описание
Энтеросгель представляет собой желеобразную массу белого или полупрозрачного светлого цвета. Гель не имеет запаха, поэтому не вызывает негативной реакции при приеме у домашних животных. Энтеросорбент имеет пористую структуру, которая включает в себя молекулы кремния. Препарат применяется при диарее любого генеза, отравлениях, интоксикации организма.
Состав и действие
Энтеросгель – полимерное кремнийорганическое соединение, основным компонентом которого является полигидрат полиметилсилоксана. Эффективность Энтеросгеля обусловлена его физико-химическими свойствами.
Гелеобразующее вещество адсорбирует на себе продукты распада белковых соединений и среднемолекулярных веществ, поглощает высокомолекулярные токсины. Эластичные гелевидные частицы образуют защитную пленку на слизистых оболочках желудка и кишечника, не давая токсинам впитываться в стенки органов. Действовать лекарство начинает с того момента, как препарат попадает в ротовую полость собаки и проходит через пищевод, желудок, кишечник.
Адсорбирующий препарат обладает пористой структурой и способностью связывать в желудочно-кишечном тракте токсичные вещества, проникшие в кишечник:
Для домашних животных можно использовать Энтеросгель в качестве средства первой помощи при диарее любого характера (в том числе вирусной, бактериальной, протозойной либо грибковой природы), при отравлениях (пищевых, медикаментозных), аллергических реакциях, нарушениях детоксикационной функции печени.
Энтеросгель не всасывается в ЖКТ и сохраняет свое активное действие в течение 12 часов.
Энтеросгель можно использовать при отравлениях антигельминтиками, интоксикации организма, вызванными массовой гибелью глистов в организме.
Назначение
Клиническими исследованиями доказана эффективность Энтеросгеля при воспалительных заболеваниях, сопровождающихся развитием гнойной и гнилостной микрофлоры, в том числе в тканях эпидермиса.
Отравления у собак
Интоксикация происходит у животных при проникновении в организм ядовитых веществ, некачественного корма, токсических продуктов. Самые частые причины отравления:
Все отравления делятся на пищевые и непищевые. Первые характеризуются проникновением токсических веществ в организм питомца через пищеварительный тракт, вторые – через кожные покровы, слизистые оболочки, дыхательную или кровеносную системы. Пищевые отравления – самые часто диагностируемые, на втором – отравление крысиным ядом – зоокумаринами, затем по частоте случаем следует интоксикация организма медицинскими препаратами.
Опасно отравление крысиным ядом. При нем животное резко слабеет, слизистые оболочки бледнеют, у питомца возникает одышка, наблюдаются кровотечение из десен, прямой кишки, кашель с примесью крови. Главная опасность зоокумаринов состоит в том, что они нарушают процесс свертываемости крови. От воздействия ядов и внутренних кровотечений, ими вызываемых, животное погибает.
В большинстве случаев отравления характеризуются следующими симптомами:
Могут наблюдаться и другие симптомы, но бить тревогу и обращаться к ветеринару нужно уже тогда, когда животное отказывается от еды. При диарее следует как можно скорее дать питомцу сорбент – чем раньше начнет свое действие Энтеросгель, тем быстрее организм очистится от токсинов. Однако прием лекарства не избавляет от необходимости обращения к ветеринару.
Дозировка
Энтеросгель производится в виде геля и капсул. Давать собаке удобнее гель – его можно добавить в корм. Поскольку лекарство не имеет запаха, питомец даже не почувствует его во время еды. Можно давать лекарство и непосредственно в рот собаки – с ложки или с помощью шприца без иглы. В последнем случае нужно развести гель водой из расчета 1:1.
Точной дозировки лекарства в зависимости от веса питомца производитель не указывает, придерживаться достаточно следующих рекомендаций:
Если для лечения используются капсулы, то собакам крупных пород следует давать по 1 капсуле 3 раза в день. Для мелких собак содержимое капсулы придется делить на две части, что неудобно. Для лечения щенков рекомендуется использовать гель в разведенном виде, по 1/3 чайной ложки. После приема лекарства следует дополнительно попоить щенка водой.
При тяжелой интоксикации после консультации с ветеринаром дозу можно увеличить вдвое. Курс лечения составляет не более 3 дней, затем дозировка уменьшается до обычной.
Ограничения
Лекарство практически не имеет противопоказаний к применению, в том числе щенкам и беременным, а также кормящим самкам. Запрещено использовать при атонии либо полной кишечной непроходимости, перитоните, прободении кишечной стенки.
Случаев передозировки, аллергии на лекарственный препарат выявлено не было. После приема Энтеросгеля в крайне редких случаях могут наблюдаться позывы к рвоте либо запор. В этом случае следует отказаться от использования лекарства и обратиться к ветеринару за назначением другого лечения.
Аналоги и цена
В аптеке можно приобрести не только Энтеросгель, но и другие энтеросорбенты в различных формах: в виде геля (Сорбентогель), порошков для приготовления суспензии (Смекта, Атоксил), таблеток с адсорбирующим действием (активированный уголь). О возможности замены препарата аналогами рекомендуется проконсультироваться с ветеринаром.
Стоимость Энтеросгеля в среднем составляет 360-400 рублей за тюбик 225 г.
Отзывы
Марина, хозяйка питбультерьера
Мой пес достаточно воспитан, но иногда на улице, пока я не вижу, умудряется прихватить в рот что-нибудь несъедобное. Результат ясен – лежит, не ест, мается животом. На этот случай у меня в аптечке всегда есть Энтеросгель (он и мне, и детям тоже помогает). Даю насильно в рот чайную ложку пасты, следом с помощью шприца – воду, и так трижды в день в течение нескольких суток.
Антон, хозяин корги
У моего питомца наблюдалась аллергия на новый корм. Симптомы были схожи с отравлением, и я дал Энтеросгель. Лекарство помогло, но к ветеринару все же обращаться пришлось. С кормлением больше не экспериментирую, но пасту держу на всякий случай в аптечке – мало ли что!
Елизавета, владелец ветеринарной клиники
Многие лекарственные препараты, которые помогают и животным, можно купить в обычной аптеке. Об эффективности Энтеросгеля знают многие – наверняка приходилось лечить отравления с его помощью. А еще лекарство помогает и собакам – в тех же случаях – отравления, диарея. Так что на случай необходимости оказать первую помощь питомцу рекомендую держать его в ветеринарной аптечке.
Как давать собаке Энтеросгель: дозировка и некоторые особенности
Владелец любой собаки, хотя бы раз в жизни, сталкивается с необходимостью проведения детоксикации организма питомца. На помощь приходит препарат Энтеросгель, который изначально был разработан для очищения организма людей. Лишь спустя некоторое время, он стал активно применяться в ветеринарии.
Действие сорбента и на людей, и на собак аналогичное. А именно, препарат борется с последствиями и причинами интоксикации и восстанавливает поврежденные органы.
Форма выпуска
Энтеросгель выпускается в форме пасты (гидрогеля), расфасованного в тюбики по 225 и 22,5 г. Белого или почти белого цвета, в двух видах — сладкого и нейтрального вкуса. По структуре, представляет собой молекулярную губку гидрофобной природы на основе кремнийорганической матрицы, с повышенными сорбционными свойствами.
Энтеросгель не выпускается в формах порошка и таблеток, как свойственно другим энтеросорбентам. Однако, как показывает практика, именно благодаря сшитой матрице и ячеистой структуры геля достигается наибольшая эффективность препарата.
Инструкция по применению
При рвоте или поносе
Энтеросгель обладает низкой молекулярной массой и эффективен для вывода вредных веществ различной природы, включая токсины, аллергены, яды, соли тяжелых металлов, а так же билирубина, мочевины, холестерина. Поэтому список назначения препарата крайне широк.
Его рекомендуют применять взрослым собакам и щенкам с рождения, в следующих случаях и дозировках:
Сколько нужно взрослым?
Разовая дозировка для собак мелких пород, весом до 5 кг, идет в объеме 1 чайной ложка продукта (2 мл), для средних пород — 1,5-2 чайной ложки (2,5 — 3 мл), для крупных и гигантских пород от 1 до 2 столовых ложек (5-7 мл), по 3 раза в день.
При тяжелом отравлении
В случае тяжелого пищевого отравления, либо при передозировке лекарствами, требуется в первые сутки давать двойную дозировку сорбента. При хроническом течении заболевания продолжительность курса составляет 2-3 недели, в острых случаях в среднем 3-5 дней.
Щенкам
Энтеросгель разрешен в применении щенкам с рождения. В этом возрасте, симптомом для употребления сорбента служит жидкий стул, сопровождаемый вялостью и слабостью. В зависимости от веса, разовая дозировка составляет от половины до целой чайной ложки, 2 раза в день. Необходимо размешивать препарат с теплой, кипяченой водой в пропорции 1:1.
Важно! Прием Энтеросгеля уменьшает эффективность других лекарственных средств. Необходим раздельный прием препаратов, с интервалом не менее 2 часов.
Как принимать?
Энтеросгель обладает нейтральным запахом. Далеко не все собаки готовы его добровольно съедать, особенно в состоянии слабости и отсутствия аппетита. В случае применения пасты со сладким вкусом, повышается вероятность того, что ваш питомец сможет съесть ее самостоятельно.
Первоначально можно скатать гель в небольшие шарики (размер сферы в зависимости от породы собаки) и предложить питомцу попробовать его. Если собака категорически отказывается, владельцу придется идти на ухищрения.
Чтобы собака не выплюнула лекарство, необходимо зажать пасть, придержать закрытой несколько секунд, одновременно сделать поглаживающее движение по горлу. Это спровоцирует сглатывание Энтеросгеля. Пасту необходимо давать отдельно от кормления, не менее чем за 1 час до или 2 часа после еды.
Побочные эффекты и передозировка
Препарат не всасывается в пищеварительном тракте и выводится в неизмененном виде в среднем через 12 часов. Поэтому передозировка Энтеросгелем невозможна, что доказано клиническими исследованиями.
Однако, в отдельных случаях употребления повышенного объема геля, у собаки могут появиться симптомы запора, тошноты, отвращения к продукту. Симптомы проходят самостоятельно, при прекращении приема препарата.
При отравлении кислотными или щелочными жидкостями, органическими растворителями (этиленгликоль, метанол), или цианидами, Энтеросгель может спровоцировать возникновение рвоты и произойдет вторичный ожог пищевода. Не рекомендуется давать пасту в этом случае.
Также, под запретом применения находятся случаи с острой непроходимостью кишечника или атонии, перитонит, прободение стенки кишки.
Заключение
При попадании в организм собаки Энтеросгель в просвете желудочно-кишечного тракта связывает и выводит экзогенные и эндогенные токсические вещества. Микрофлора при этом не нарушается и налипания на стенки желудочно-кишечного тракта не происходит. Заметный эффект достигается быстро.
Однако, в случае если после применения сорбента прошло более 20 минут, а облегчение состояние не наступило, необходимо однократно ввести повторную порцию препарата в том же объеме. При отсутствии положительного результата спустя сутки с начала приема требуется срочная ветеринарная консультация.
Энтеросгель : инструкция по применению
Описание
Однородная пастообразная масса от белого до почти белого цвета без запаха.
Состав
Полиметилсилоксана полигидрат-0,7 г.
Вода очищенная-0,3 г.
Фармакотерапевтическая группа
Кишечные адсорбенты. Код ATX: А07В.
Энтеросгель имеет пористую структуру кремнийорганической матрицы (молекулярная губка) гидрофобной природы, которая характеризуется сорбционным действием по отношению только к среднемолекулярным токсическим метаболитам (м.м. от 70 до 1000).
Энтеросгель® обладает выраженными сорбционными и детоксикационными свойствами. В просвете желудочно-кишечного тракта препарат связывает и выводит из организма эндогенные и экзогенные токсические вещества различной природы, включая бактерии и бактериальные токсины, антигены, пищевые аллергены, лекарственные препараты и яды, соли тяжёлых металлов, радионуклиды, алкоголь. Препарат сорбирует также некоторые продукты обмена веществ организма, в том числе избыток билирубина, мочевины, холестерина и липидных комплексов, а также метаболиты, ответственные за развитие эндогенного токсикоза. Энтеросгель® не уменьшает всасывания витаминов и микроэлементов, способствует восстановлению нарушенной микрофлоры кишечника и не влияет на его двигательную функцию.
Препарат не всасывается в желудочно-кишечном тракте, выводится в неизменном виде в течение 12 часов.
Показания к применению
У взрослых и детей в качестве детоксикационного средства:
острые и хронические интоксикации различного происхождения;
острые отравления сильнодействующими и ядовитыми веществами, в том числе лекарственными препаратами и алкоголем, алкалоидами, солями тяжёлых металлов;
острые кишечные инфекции любого генеза в составе комплексной терапии (токсикоинфекции, сальмонеллёз, дизентерия, диарейный синдром неинфекционного происхождения, дисбактериоз);
гнойно-септические заболевания, сопровождающиеся выраженной интоксикацией, в составе комплексной терапии;
пищевая и лекарственная аллергия;
гипербилирубинемия (вирусный гепатит) и гиперазотемия (хроническая почечная недостаточность);
с целью профилактики хронических интоксикаций работникам вредных производств (профессиональные интоксикации химическими агентами политропного действия, ксенобиотиками, инкорпорированными радионуклидами, соединениями свинца, ртути, мышьяка, нефтепродуктами, органическими растворителями, окислами азота, углерода, фторидами, солями тяжёлых металлов).
Противопоказания
Индивидуальная непереносимость препарата, атония кишечника.
Беременность и лактация
Энтеросгель® не противопоказан при беременности и лактации.
Способ применения и дозы
Энтеросгель® пасту принимают внутрь за 1-2 часа до или после еды или приёма других лекарств, запивая водой.
Необходимое для приема количество препарата рекомендуется размешать в стакане в тройном объеме воды комнатной температуры или принимать внутрь, запивая водой.
Грудным детям рекомендуется 2,5 г (0,5 чайной ложки) препарата размешать в тройном объеме грудного молока или воды и давать перед каждым кормлением (6 раз в сутки).
При тяжёлых интоксикациях в течение первых трёх суток доза препарата может быть увеличена вдвое.
Продолжительность лечения при острых отравлениях 3-5 суток, а при хронических интоксикациях и аллергических состояниях 2-3 недели.
Повторный курс по рекомендации врача.
Побочное действие
Возможны тошнота, запор, При тяжёлой почечной и/или печёночной недостаточности возможно появление чувства отвращения к препарату.
Передозировка
Случаев передозировки не выявлено.
Взаимодействие с другими лекарственными средствами
Возможно уменьшение всасывания других препаратов при одновременном приёме с Энтеросгелем®.
Препарат может использоваться в комплексной терапии с другими лекарственными средствами при соблюдении правила раздельного во времени приёма 1-2 часа до или после приёма других лекарственных препаратов.
Туба из комбинированных материалов 225 г в упаковке № 1.
Условия хранения
При температуре от + 4 °C до + 30 °C в местах, недоступных для детей. Препарат годен после вскрытия упаковки в течение 3-х месяцев. Предохранять от высыхания после вскрытия упаковки. Беречь от замораживания.
Срок годности
3 года. Не использовать по окончании срока годности, указанного на упаковке.
Условия отпуска из аптек
ООО «ТНК СИЛМА». Россия, 399851, Липецкая обл., г. Данков, ул. Л. Толстого д. 32/2.
Энтеросгель ® (Enterosgel) инструкция по применению
Владелец регистрационного удостоверения:
Произведено:
Контакты для обращений:
Лекарственная форма
рег. №: ЛП-№(000036)-(РГ-RU) от 10.02.20 — Бессрочно Дата перерегистрации: 21.07.20 Предыдущий рег. №: Р N003719/02
Форма выпуска, упаковка и состав препарата Энтеросгель ®
Паста для приема внутрь в виде однородной массы от белого до почти белого цвета, без запаха.
| 100 г | |
| полиметилсилоксана полигидрат | 70 г |
Фармакологическое действие
Энтеросорбент, кишечный адсорбент.
Энтеросгель ® имеет пористую структуру кремнийорганической матрицы (молекулярная губка) гидрофобной природы, которая характеризуется сорбционным действием по отношению только к среднемолекулярным токсическим метаболитам (м.м. от 70 до 1000).
Энтеросгель ® обладает выраженными сорбционными и детоксикационными свойствами. В просвете ЖКТ препарат связывает и выводит из организма эндогенные и экзогенные токсические вещества различной природы, включая бактерии и бактериальные токсины, антигены, пищевые аллергены, лекарственные препараты, яды, соли тяжелых металлов, алкоголь. Препарат сорбирует также некоторые продукты обмена веществ организма, в т.ч. избыток билирубина, мочевины, холестерина, липидных комплексов, а также метаболиты, ответственные за развитие эндогенного токсикоза.
Энтеросгель ® не уменьшает всасывание витаминов и микроэлементов, способствует восстановлению нарушенной микрофлоры кишечника и не влияет на его двигательную функцию.
Фармакокинетика
Препарат не всасывается из ЖКТ.
Выделяется в неизмененном виде в течение 12 ч.
Показания препарата Энтеросгель ®
У взрослых и детей в качестве детоксикационного средства:
Открыть список кодов МКБ-10
| Код МКБ-10 | Показание |
| A02 | Другие сальмонеллезные инфекции |
| A03 | Шигеллез |
| A04 | Другие бактериальные кишечные инфекции |
| A05 | Другие бактериальные пищевые отравления, не классифицированные в других рубриках |
| A09 | Другой гастроэнтерит и колит инфекционного и неуточненного происхождения |
| A40 | Стрептококковый сепсис |
| A41 | Другой сепсис |
| B15 | Острый гепатит А |
| B16 | Острый гепатит В |
| B17.1 | Острый гепатит С |
| B18.1 | Хронический вирусный гепатит B без дельта-агента |
| B18.2 | Хронический вирусный гепатит С |
| K59.1 | Функциональная диарея |
| K63 | Другие болезни кишечника |
| L20.8 | Другие атопические дерматиты (нейродермит, экзема) |
| L50 | Крапивница |
| N18 | Хроническая болезнь почек |
| R54 | Острая интоксикация |
| T50.9 | Другими и неуточненными лекарственными средствами, медикаментами и биологическими веществами |
| T51 | Токсическое действие алкоголя |
| T56 | Токсическое действие металлов |
| T78.3 | Ангионевротический отек (отек Квинке) |
| T88.7 | Патологическая реакция на лекарственное средство или медикаменты неуточненная |
| Z29.8 | Другие уточненные профилактические меры |
Режим дозирования
Энтеросгель ® принимают внутрь за 1-2 ч до или после еды или приема других лекарственных средств, запивая водой.
Необходимое для приема количество препарата рекомендуется размешать в стакане в тройном объеме воды комнатной температуры или принимать внутрь, запивая водой.
При тяжелых интоксикациях в течение первых 3 сут доза препарата может быть увеличена вдвое.
Побочное действие
Прочие: при тяжелой почечной или печеночной недостаточности возможно появление чувства отвращения к препарату.
Как давать Энтеросгель собаке: показания и дозировка
Энтеросгель – это препарат из группы сорбентов. Изначально лекарство разрабатывалось для лечения человека, но позже нашло применение и в ветеринарной практике. Представляет собой полупрозрачную желеобразную массу белого цвета. Имеет нейтральный вкус и запах. Средство помещено в тюбики по 225 грамм или пакеты по 22,5 грамм. Вместе с инструкцией по применению упаковано в бумажные коробки.
Принцип действия
Препарат Энтеросгель дают собаке при отравлении токсичными веществами. Он обволакивает слизистые ткани ротовой полости и желудочно-кишечного тракта, образуя тончайшую неразрывную пленку. В отличие от активированного угля лекарство действует немедленно, без запивания большим объемом воды.
Уже через несколько минут после попадания в пищеварительный тракт собаки, гель начинает впитывать в себя все виды ядов. Пористая структура молекул основного вещества – кремния способна поглощать бактериальные токсины, пищевые аллергены, компоненты лекарства, соли тяжелых металлов. Кроме того, лекарство сорбирует избыток липидов, мочевины, билирубинов.
Далее препарат легко отстает от стенок ЖКТ и выводится из организма через кишечник. При этом лекарство не впитывается в слизистые, не мешает всасыванию питательных веществ, не нарушает баланс микрофлоры, не меняет цвет испражнений. Напротив, Энтеросгель создает защитный слой между калом и воспаленными тканями, чем ускоряет процессы заживления.
Показания к применению
Энтеросгель дают собаке при рвоте, поносе, тошноте и других симптомах интоксикации. Такое состояние может быть вызвано:
Диарея и рвотные позывы – частые симптомы болезней пищеварительного тракта: гастрита, энтерита, колита, застоя желчи. Прием Энтеросгеля является одним из методов комплексной терапии этих заболеваний у собаки.
Противопоказания
Запрещено давать Энтеросгель собаке, страдающей следующими заболеваниями:
Аллергия на компоненты Энтеросгеля встречается у собаки крайне редко.
Дозировка и длительность приема
Дозировка Энтеросгеля для взрослых собак рассчитывается по весу животного:
Благодаря отсутствию яркого вкуса и запаха питомцы сами слизывают гель с ложки. Если питомец упрямится, разведите препарат с водой в пропорции 3:1, наберите его в шприц, снимите иглу и залейте в пасть животному.
Энтеросгель дают собаке при поносе в течение 3-14 дней дважды в сутки, пока не исчезнут все симптомы отравления.
Для щенков и беременных сук
Перед тем как дать щенку или беременной собаке Энтеросгель, необходимо проконсультироваться с ветеринаром. В этом в возрасте и положении понос не всегда является симптомом отравления.
Тошнота и рвотные позывы у малышей могут указывать на переедание, а у будущей мамы – на гормональную перестройку.
Дозировку беременным собакам и щенкам врач назначает индивидуально. Основное условие – давать препарат отдельно от еды, через 1 час после приема и за 2 часа до следующего кормления. Воду при этом разрешается пить в неограниченном объеме.
Побочные действия
Энтеросгель – эффективный препарат щадящего действия. Он не всасывается в кровь, выводится из организма собаки через 10-12 часов после приема. При соблюдении инструкции по применению лекарство не вызывает побочных эффектов. При передозировке у животных появляется тошнота, урчание и бурление в животе, отвращение к средству.
Побочные эффекты в виде ожога пищевода могут появиться при отравлении щелочными и кислотными жидкостями. В этом случае перед приемом Энтеросгеля ветеринар останавливает рвотные позывы с помощью препаратов, воздействующих на соответствующие центры в головном мозге.
Аналоги
Полноценным аналогом препарата является Полисорб. Этот сорбент на основе диоксида кремния выпускается российским ЗАО с одноименным названием. Он производится в виде порошка, который необходимо разбавить водой до состояния суспензии и влить в пасть собаки с помощью шприца без иглы.
Еще один эффективный аналог – комплексная добавка Армалит. Основным компонентом препарата выступает цеолит, а вспомогательными веществами – гвоздика, полынь, пижма, органическая сера. Армалит часто назначают после проведения антигельминтной терапии, чтобы быстрее вывести погибших глистов и продукты их жизнедеятельности.
Цамакс – пищевая добавка на основе цеолита. Данный сорбент помогает естественным путем вывести из кишечника нитраты, ртуть, фенолы, соли тяжелых металлов. Кроме того, препарат обогащает организм собаки фосфором, магнием, кальцием, калием. Лекарство выпускается в виде порошка, который можно смешать с кормом или разбавить с водой.
Терапия острых аллергических состояний на догоспитальном этапе
К острым аллергическим заболеваниям относят анафилактический шок, обострение (приступ) бронхиальной астмы, острый стеноз гортани, отек Квинке, крапивницу, обострение аллергического конъюнктивита и/или аллергического ринита. Считается, что аллергическими
К острым аллергическим заболеваниям относят анафилактический шок, обострение (приступ) бронхиальной астмы, острый стеноз гортани, отек Квинке, крапивницу, обострение аллергического конъюнктивита и/или аллергического ринита. Считается, что аллергическими заболеваниями страдает в среднем около 10% населения земного шара. Особую тревогу вызывают данные ННПО скорой медицинской помощи, согласно которым за последние 3 года число вызовов по поводу острых аллергических заболеваний в целом по РФ возросло на 18%.
Основные причины возникновения и патогенез
Патогенез аллергических реакций на сегодняшний день достаточно полно изучен и подробно описан во многих отечественных и зарубежных монографиях по аллергологии и клинической иммунологии. Центральная роль в реализации иммунопатологических реакций принадлежит иммуноглобулинам класса Е (IgE), связывание которых с антигеном приводит к выбросу из тучных клеток медиаторов аллергии (гистамина, серотонина, цитокинов и др.).
Наиболее часто аллергические реакции развиваются при воздействии ингаляционных аллергенов жилищ, эпидермальных, пыльцевых, пищевых аллергенов, лекарственных средств, антигенов паразитов, а также при укусах насекомых. Лекарственная аллергия чаще всего развивается при применении анальгетиков, сульфаниламидов и антибиотиков из группы пенициллинов, реже цефалоспоринов (при этом следует учитывать риск перекрестной сенсибилизации к пенициллину и цефалоспоринам, составляющий от 2 до 25%). Кроме того, в настоящее время возросло число случаев развития латексной аллергии.
Клиническая картина, классификация и диагностические критерии
С точки зрения определения объема необходимой лекарственной терапии на догоспитальном этапе оказания помощи и оценки прогноза острые аллергические заболевания можно подразделить на легкие (аллергический ринит — круглогодичный или сезонный, аллергический конъюнктивит — круглогодичный или сезонный, крапивница), средней тяжести и тяжелые (генерализованная крапивница, отек Квинке, острый стеноз гортани, среднетяжелое обострение бронхиальной астмы, анафилактический шок). Классификация и клиническая картина острых аллергических заболеваний представлены в табл. 1.
При анализе клинической картины аллергической реакции врач СМП должен получить ответы на следующие вопросы (табл. 2).
При начальном осмотре на догоспитальном этапе следует оценить наличие стридора, диспноэ, свистящего дыхания, одышки или апноэ; гипотензии или синкопе; изменений на коже (высыпаний по типу крапивницы, отека Квинке, гиперемии, зуда); гастроинтестинальных проявлений (тошноты, болей в животе, диареи); изменений сознания. Если у больного отмечаются стридор, выраженная одышка, гипотензия, аритмия, судороги, потеря сознания или шок, то данное состояние рассматривается как угрожающее жизни.
Лечение острых аллергических заболеваний
При острых аллергических заболеваниях на догоспитальном этапе неотложная терапия строится по следующим направлениям:
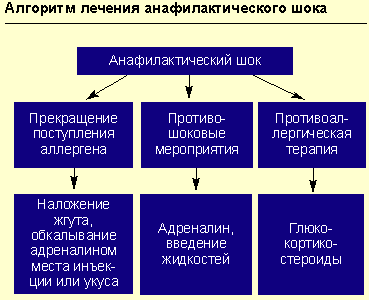
Прекращение дальнейшего поступления в организм предполагаемого аллергена.
Например, в случае реакции на лекарственный препарат, введенный парентерально, или при укусах насекомых — наложение жгута выше места инъекции (или укуса) на 25 мин (каждые 10 мин необходимо ослаблять жгут на 1-2 мин); к месту инъекции или укуса прикладывается лед или грелка с холодной водой на 15 мин; обкалывание в 5-6 точках и инфильтрация места инъекции или укуса 0,3-0,5 мл 0,1%-ного раствора адреналина с 4,5 мл изотонического раствора хлорида натрия.
Противоаллергическая терапия (антигистаминными препаратами или глюкокортикостероидами).
Введение антигистаминных препаратов (блокаторов Н1-гистаминовых рецепторов) показано при аллергическом рините, аллергическом конъюнктивите, крапивнице. Выделяют классические антигистаминные препараты (например, супрастин, димедрол) и препараты нового поколения (семпрекс, телфаст, кларотадин и др.). Необходимо отметить, что для классических антигистаминных препаратов в отличие от препаратов нового поколения характерно короткое время воздействия при относительно быстром наступлении клинического эффекта; многие из этих средств выпускаются в парентеральных формах. Антигистаминные препараты нового поколения лишены кардиотоксического действия, конкурентно влияют на гистамин, не метаболизируются печенью (например, фармакокинетика семпрекса не меняется даже у больных с нарушенными функциями печени и почек) и не вызывают тахифилаксии. Эти препараты обладают длительным воздействием и предназначаются для приема внутрь.
При анафилактическом шоке и при отеке Квинке (в последнем случае — препарат выбора) внутривенно вводится преднизолон (взрослым — 60-150 мг, детям — из расчета 2 мг на 1 кг массы тела). При генерализованной крапивнице или при сочетании крапивницы с отеком Квинке высокоэффективен бетаметазон (дипроспан в дозе 1-2 мл внутримышечно), состоящий из динатрия фосфата (обеспечивает быстрое достижение эффекта) и дипропионата бетаметазона (обусловливает пролонгированное действие). Для лечения бронхиальной астмы, аллергического ринита, аллергического конъюнктивита разработаны топические формы глюкокортикостероидов (флутиказон, будесонид). При отеке Квинке для предупреждения влияния на ткани гистамина необходимо комбинировать антигистаминные препараты нового поколения (семпрекс, кларитин, кларотадин) с глюкокортикостероидами (ГКС).
Побочные эффекты системных ГКС — артериальная гипертензия, повышенное возбуждение, аритмия, язвенные кровотечения. Побочные эффекты топических ГКС — осиплость голоса, нарушение микрофлоры с дальнейшим развитием кандидоза слизистых, при применении высоких доз — атрофия кожи, гинекомастия, прибавка массы тела и др. Противопоказания: язвенная болезнь желудка и 12-перстной кишки, тяжелая форма артериальной гипертензии, почечная недостаточность, повышенная чувствительность к глюкокортикоидам в анамнезе.
Симптоматическая терапия.
При развитии бронхоспазма показано ингаляционное введение b2-агонистов и других бронхолитических и противовоспалительных препаратов (беродуала, атровента, вентолина, пульмикорта) через небулайзер. Коррекцию артериальной гипотонии и восполнение объема циркулирующей крови проводят с помощью введения солевых и коллоидных растворов (изотонического раствора хлорида натрия — 500-1000 мл, стабизола — 500 мл, полиглюкина — 400 мл). Применение вазопрессорных аминов (допамина — 400 мг на 500 мл 5%-ной глюкозы, норадреналина — 0,2-2 мл на 500 мл 5%-ного раствора глюкозы, доза титруется до достижения уровня систолического давления 90 мм рт. ст.) возможно только после восполнения ОЦК. При брадикардии допускается введение атропина в дозе 0,3-0,5 мг подкожно (при необходимости инъекцию повторяют каждые 10 мин). При наличии цианоза, диспноэ, сухих хрипов показана также кислородотерапия.
Противошоковые мероприятия (см. рисунок).
При анафилактическом шоке больного следует уложить (голова ниже ног), повернуть голову в сторону (во избежание аспирации рвотных масс), выдвинуть нижнюю челюсть (при наличии съемных зубных протезов их нужно удалить).
Адреналин вводят подкожно в дозе 0,1-0,5 мл 0,1%-ного раствора (препарат выбора), при необходимости инъекции повторяют каждые 20 мин в течение часа под контролем уровня АД. При нестабильной гемодинамике с развитием непосредственной угрозы для жизни возможно внутривенное введение адреналина. При этом 1 мл 0,1%-ного раствора адреналина разводится в 100 мл изотонического раствора хлорида натрия и вводится с начальной скоростью 1 мкг/мин (1 мл в минуту). При необходимости скорость может быть увеличена до 2-10 мкг/мин. Внутривенное введение адреналина проводится под контролем частоты сердечных сокращений, дыхания, уровня артериального давления (систолическое артериальное давление необходимо поддерживать на уровне более 100 мм рт. ст. у взрослых и более 50 мм рт. ст. у детей).
Побочные эффекты адреналина — головокружение, тремор, слабость; сильное сердцебиение, тахикардия, различные аритмии (в том числе желудочковые), появление болей в области сердца; затруднение дыхания; увеличение потливости; чрезмерное повышение артериального давления; задержка мочи у мужчин, страдающих аденомой предстательной железы; повышение уровня сахара в крови у больных сахарным диабетом. Описаны также случаи развития некрозов тканей при повторном подкожном введении адреналина в одно и то же место вследствие местного сужения сосудов. Противопоказания — артериальная гипертензия; выраженный церебральный атеросклероз либо органическое поражение головного мозга; ишемическая болезнь сердца; гипертиреоз; закрытоугольная глаукома; сахарный диабет; гипертрофия предстательной железы; неанафилактический шок; беременность. Однако даже при этих заболеваниях возможно назначение адреналина при анафилактическом шоке по жизненным показаниям и под строгим врачебным контролем.
Типичные ошибки, допускаемые на догоспитальном этапе
Изолированное назначение Н1-гистаминовых блокаторов при тяжелых аллергических реакциях, равно как и при бронхообструктивном синдроме, не имеет самостоятельного значения, и на догоспитальном этапе это лишь приводит к неоправданной потере времени; использование дипразина (пипольфена) опасно усугублением гипотонии. Использование таких препаратов, как глюконат кальция, хлористый кальций, вообще не показано при острых аллергических заболеваниях. Ошибочным следует считать также позднее назначение ГКС, необоснованное применение малых доз ГКС, отказ от использования топических ГКС и b2-агонистов при аллергическом стенозе гортани и бронхоспазме.
Показания к госпитализации
Пациенты с тяжелыми аллергическими заболеваниями должны быть обязательно госпитализированы.
А. Л. Верткин, доктор медицинских наук, профессор
А. В. Тополянский, кандидат медицинских наук
Сорбиогель : инструкция по применению
Форма выпуска
В упаковке, шт.: коробка 30 шт.
Вес в упаковке, г: 365
Размер с упаковкой, мм: 110*80*100
Описание
Комплексное очищение организма
Удобное саше с продуктом в гелевой форме для быстрого связывания, нейтрализации и выведения из организма токсинов любого происхождения.
Для очищения организма при пищевых отравлениях, алкогольной интоксикации, кишечных инфекциях.
При вирусных и аллергических заболеваниях.
В составе комплексной терапии атеросклероза, сахарного диабета.
Поддержка организма при проживании в экологически неблагоприятных районах и работе на вредном производстве.
Полисорбовит и отруби пшеничные действуют как сорбент: связывают токсичные молекулы и препятствуют их обратному всасыванию.
Гуммиарабик и пектин способствуют восстановлению естественного состояния микрофлоры кишечника, которое нарушается при интоксикации.
Активные полисахариды и пектиновые вещества влияют на обмен холестерина, стимулируя выведение его избытка из организма.
Экстракт солянки осуществляет гепатопротекторное действие, шиповник и кукурузные рыльца способствуют нормализации желчеотделения.
Экстракт коры осины обладает противомикробным, противовоспалительным и антигельминтным действием; экстракт травы сенны улучшает моторику ЖКТ.
Состав
Фруктоза, вода, яблочный концентрат, полисорбовит, отруби пшеничные, пектин (загуститель, пищевые волокна), гуммиарабик, цитрусовая клетчатка (пищевые волокна), осины экстракт, шиповника эктракт, солянки экстракт, сенны экстракт, ароматизатор натуральный «Яблоко» жидкий (пропиленгликоль), лимонная кислота (регулятор кислотности), кукурузных рыльцев экстракт, сорбат калия (консервант), низин (консервант).
Применение
Рекомендации по применению:
Саше: взрослым по 2 ч.л. (10 грамм) на ночь во время еды.
Прием 10 грамм обеспечивает поступление:
Противопоказания
Индивидуальная непереносимость компонентов. Перед применением рекомендуется проконсультироваться с врачом. Не является лекарством.
Холера
Холера – это особо опасное инфекционное заболевание, которое вызывает сильную диарею и обезвоживание вплоть до гиповолемического шока и смерти. Чаще всего заражение происходит через загрязненную воду. При отсутствии лечения эта патология может привести к летальным осложнениям в течение нескольких часов даже у ранее здоровых людей. Современные методы очистки воды практически устранили холеру в промышленно развитых странах. Но эта болезнь все еще встречается в Африке и Юго-Восточной Азии. Риск эпидемии холеры наиболее высок, когда бедность, войны или стихийные бедствия вынуждают людей жить в тесноте без надлежащих санитарных условий.
Согласно статистическим данным, ежегодно в мире фиксируется около 5 млн случаев холеры, из которых около 130 тыс. заканчивается летально.
В каких странах можно заразиться холерой?
Повышенный риск инфицирования холерным вибрионом есть у людей, проживающих или пребывающих в длительной командировке в следующих странах:
Симптомы холеры
Большинство людей, инфицированных холерным вибрионом, не заболевают и даже не знают, что были заражены. Но при этом они выделяют бактерии со стулом в течение 7-14 дней, из-за чего все еще могут заразить других через загрязненную воду.
Как правило, клинические проявления холеры представлены умеренной или выраженной диареей, которая мало чем отличается от расстройства стула другого происхождения. Реже развиваются более серьезные симптомы. Как правило, это происходит внезапно, спустя 1-3 дня после заражения.
Симптомами холерной инфекции могут быть:








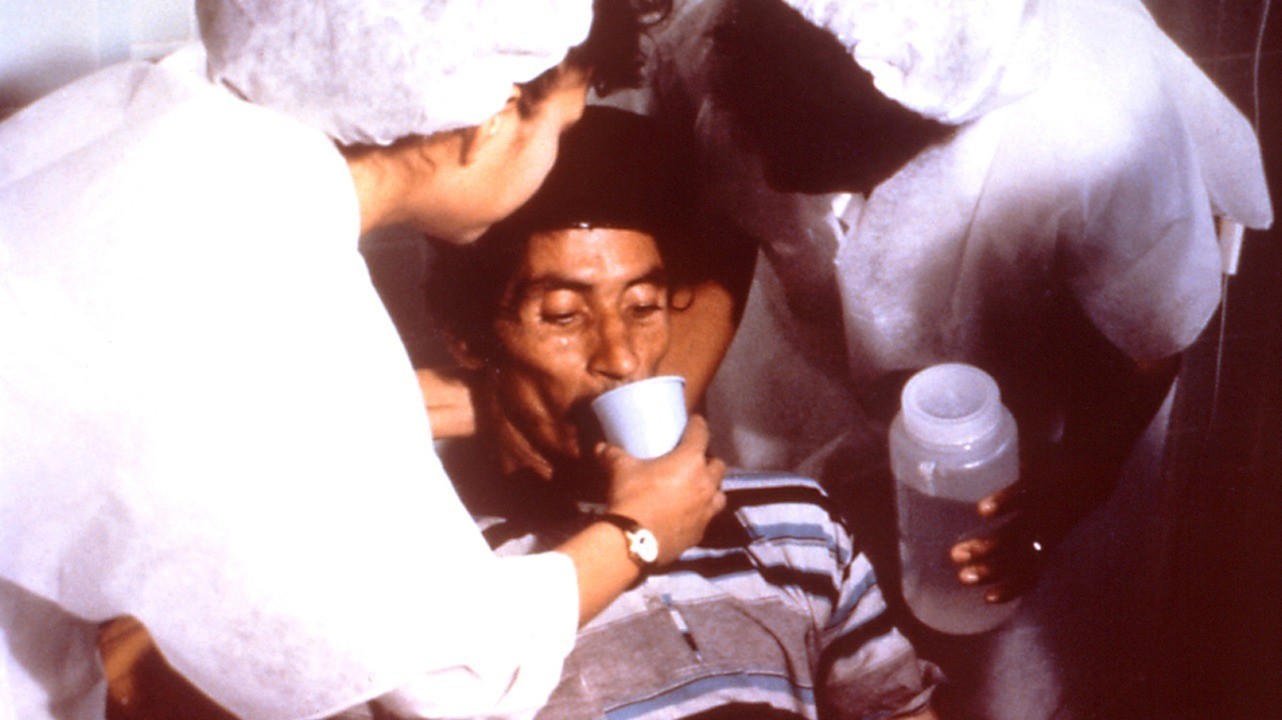
 Регидратацию и коррекцию водно-солевого баланса важно начать как можно раньше. Фото: belchonock / Depositphotos
Регидратацию и коррекцию водно-солевого баланса важно начать как можно раньше. Фото: belchonock / Depositphotos
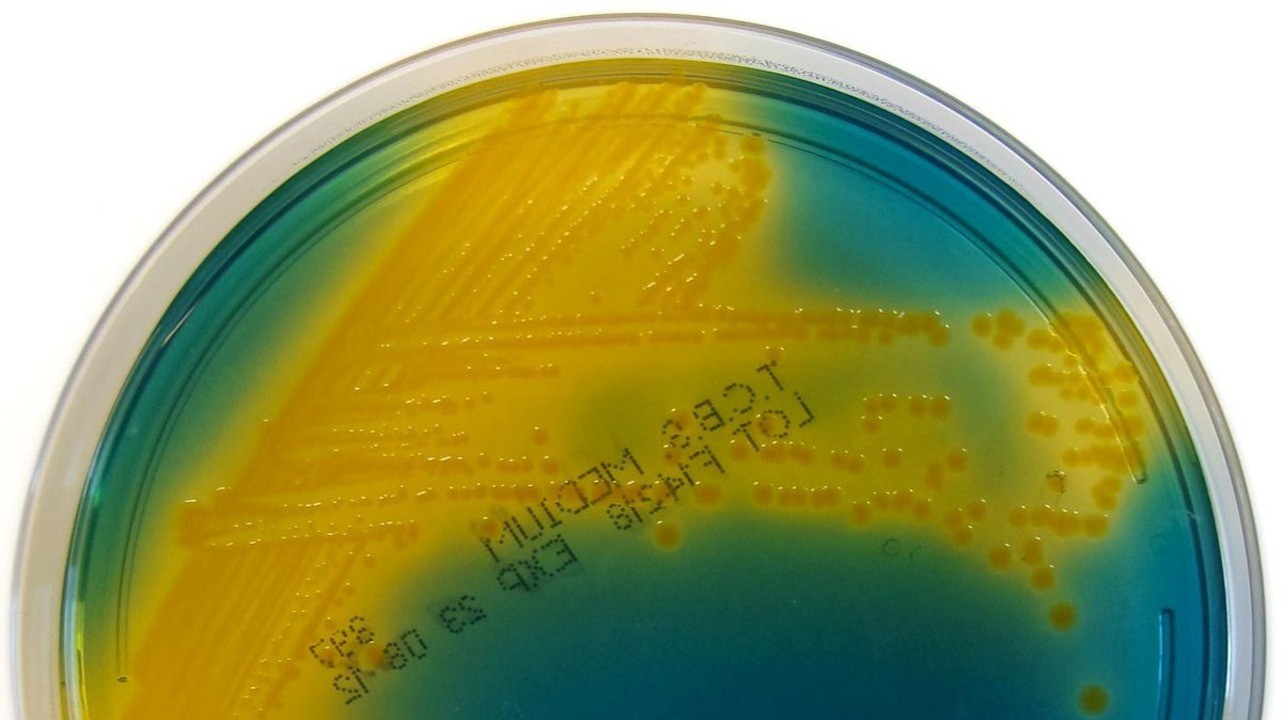 Бакпосев при холере – один из методов диагностики. Фото: Nathan Reading / Flickr (CC BY-NC-ND 2.0)
Бакпосев при холере – один из методов диагностики. Фото: Nathan Reading / Flickr (CC BY-NC-ND 2.0) Риск развития эпидемии холеры наиболее высок в антисанитарных условиях. Фото: Olgatribe / Depositphotos
Риск развития эпидемии холеры наиболее высок в антисанитарных условиях. Фото: Olgatribe / Depositphotos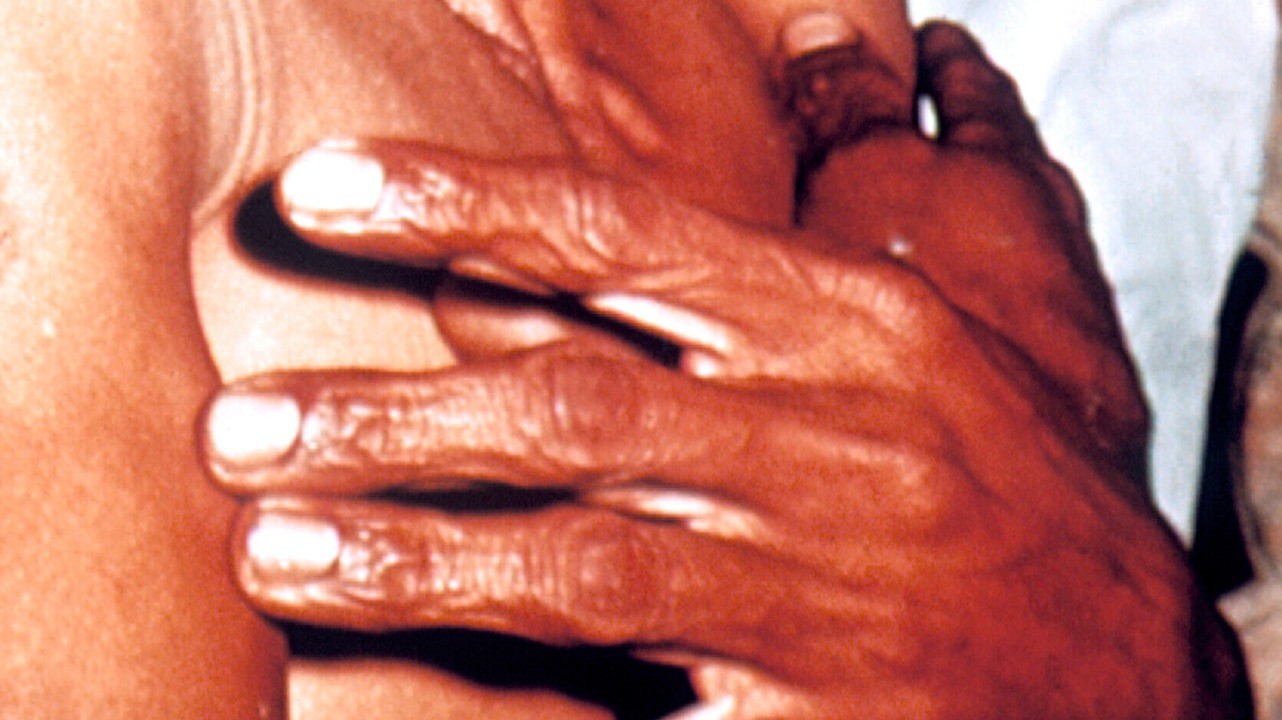 «Руки прачки» – характерный симптом холеры. Фото: PHIL CDC
«Руки прачки» – характерный симптом холеры. Фото: PHIL CDC



.gif)
.gif)
.gif)