Как вылечить впч
Как вылечить впч
«Эффективное лечение ВПЧ» — ложь или правда?
Ольга Золоткова СПИД.ЦЕНТР
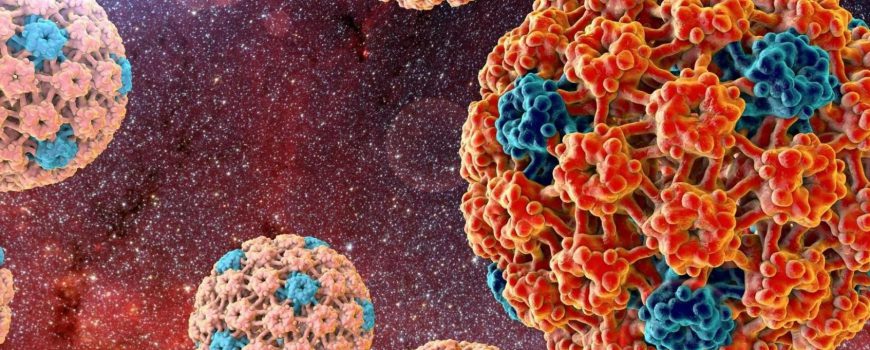
Вирус папилломы человека — самая распространенная вирусная инфекция, по данным ВОЗ. Она появляется у подавляющего большинства людей, ведущих сексуальную жизнь. Причем российские врачи, в частности гинекологи, регулярно рекомендуют пациентам проверяться на ВПЧ, аргументируя это так: если вирус найдут, то он «эффективно лечится». СПИД.ЦЕНТР объясняет, можно ли вылечить этот вирус на самом деле.
ВПЧ есть у всех?
Особенность этого вируса в том, что он высококонтагиозен, то есть передается как половым путем, так и при простом кожном контакте. Поэтому плохая новость: презервативы совершенно не гарантируют защиту от него. Им инфицируются большинство взрослых и многие дети, но это нестрашно и почти всегда проходит бесследно. В 90—98 % случаев через 1—2 года организм справиться с вирусом сам, в подобных случаях инфекция называется транзиторной.
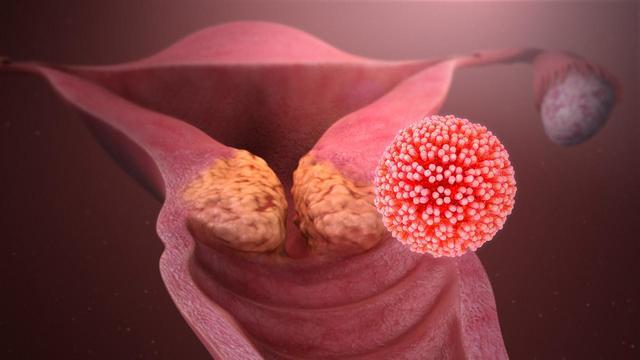
Но есть и опасности, например, если ВПЧ долгое время находится в женском организме, риск рака шейки матки повышается. По данным ВОЗ, два типа ВПЧ (16 и 18) вызывают до 70 % всех случаев рака шейки матки. Вирус папилломы человека выявляется при скрининге рака шейки матки.
Однако в то же время нет и не может быть термина «ВПЧ-положительный статус» — сегодня вирус обнаруживается, а через несколько месяцев его уже нет. До сих пор лекарства от ВПЧ еще не изобрели, при том что вакцины от некоторых типов давно существуют.
Обзор противовирусных и иммуномодулирующих «лекарств»
В России и странах СНГ гинекологи назначают противовирусную терапию ВПЧ. Схемы лечения громоздкие и дорогостоящие: пациентке вручают список из нескольких препаратов.
по теме
Лечение
«Химия» и жизнь: мифы о раке
Важно понимать, что ни по одному вышеперечисленному препарату нет серьезных и полных исследований — рандомизированных двойных слепых плацебо-контролируемых испытаний. Рекламно-хвалебные публикации и исследования с нерепрезентативными выборками размещены только на сайтах производителей и русскоязычных ресурсах. Кроме стран СНГ, эти средства нигде не зарегистрированы и не применяются.
Многие российские гинекологи утверждают, что препараты с недоказанной эффективностью успешно лечат ВПЧ: анализ на вирус после одного или нескольких курсов становится отрицательным. Но такой результат — не заслуга лечения, он означает, что инфекция была транзиторной и устранилась бы сама, даже без ненужной лекарственной и денежной нагрузки.
Мировая практика
Центр по контролю заболеваний США пишет, что специфическая терапия ВПЧ не рекомендуется. ВОЗ в информационном бюллетене говорит только о необходимости лечения последствий, которые может вызвать ВПЧ: рака шейки матки, анальных или генитальных бородавок. У мужчин онкогенные типы ВПЧ способны провоцировать рак прямой кишки и полового члена.
В современном мире медикаментозной терапии не существует, но большое внимание уделяется вакцинации.
Вакцинация от ВПЧ
Две вакцины прошли клинические испытания и зарегистрированы на рынке:
Препараты очень дорогие (цена одной инъекции составляет около 6 000 — 10 000 рублей), поэтому массовую вакцинацию могут себе позволить только развитые страны.
В идеале должны быть вакцинированы все подростки в возрасте 11—12 лет независимо от пола (два раза в течение полугода) и взрослые до 26 лет (три раза после 14 лет в течение полугода). В российской инструкции к вакцинам рекомендуется трехкратная вакцинация в любом возрасте.
Отдельно стоит упомянуть, что Американский альянс иммунологов рекомендует прививаться от ВПЧ при ВИЧ. Об эффективности вакцинации ВИЧ-положительных девушек говорят ВОЗ, клинические исследования Канадского института исследований здоровья и другие публикации.
Когда нужно сдавать тест на ВПЧ?
Анализ на ВПЧ назначается женщинам после 30 лет при аномальных результатах цитологии или гистологии. Просто так проводить его бессмысленно и затратно. Результаты ПАП-теста вместе с анализом на ВПЧ помогают выбрать правильный интервал до повторного цитологического исследования или кольпоскопии.
Положительный анализ на ВПЧ не означает рак, он лишь позволяет сделать приблизительный прогноз; к тому же вирус — не единственный фактор риска рака шейки матки.
Тест на ВПЧ не должен использоваться массово — это дополнительный (и дорогостоящий) метод скрининга.
Итог:
Доказанной противовирусной терапии ВПЧ не существует, как и лекарств, укрепляющих иммунитет.
Лечат не ВПЧ, а его последствия: предраковые состояния и рак шейки матки, новообразования на коже и слизистых. Лечение не медикаментозное, а хирургическое: лазер, криодеструкция, операция.
Сдавать анализ на ВПЧ всем подряд не нужно.
Как лечить вирус папилломы человека у женщин
Вирус папилломы человека (ВПЧ) провоцирует образование папиллом, бородавок, кондилом и является пусковым фактором в развитии рака шейки матки и гортаноглотки. Реже может поражать слизистую полости рта, пищевод, конъюнктиву глаз. Согласно данным всемирной организации здравоохранения, заболеваемость этой инфекцией за последние 10 лет увеличилась в 10 раз. В России распространенность ВПЧ-инфекции, по данным исследований в регионах, варьируется от 29% до 45%. Особая настороженность медицинского сообщества связана с тем, что около трети из всех выделенных генотипов вируса провоцирует развитие онкологической патологии.
Классификация течения папилломавирусной инфекции
Попадая в организм женщины, ВПЧ может проявлять разную активность, что зависит от состояния иммунитета. В зависимости от того, как ведет себя патоген, выделяют несколько вариантов папилломавирусной инфекции:
Классификация помогает врачу выбрать максимально эффективную лечебную тактику. Штаммы патогена также делят на группы в зависимости от способности вызывать онкологические заболевания: ВПЧ с высоким, средним и низким онкогенным риском. Среди 40 вариантов вируса, передающихся при половых контактах, 14 относят к высокому и среднему онкогенному риску: −16, −18, −31, −33, −35, −39, −45, −51, −52, −56, −58, −59, −66 и −68 типы.
Как передается вирус папилломы человека?
Среди населения женского пола зараженность ВПЧ достигает 70%. Однако наличие патогена в организме еще не означает болезнь. Если у человека здоровая иммунная система, то ВПЧ-инфекция, в большинстве, случаев носит транзиторный характер — он самостоятельно исчезает в течение 2 лет. Если этого не происходит, становится актуальным вопрос о том, как лечить вирус папилломы человека у женщин.
Основной путь передачи вируса — контактный:
Инфицированию вирусом наиболее подвержены молодые люди в возрасте 13-30 лет. При первом половом контакте риск заражения — около 60%. Вирус может проникать в организм также при отсутствии непосредственного соития. Именно девушки подвержены максимальному риску столкнуться с ВПЧ, а затем и с его последствиями. Это связано с особенностями строения их половых органов.
Вирус папилломы человека у женщин: причины возникновения
Среди населения женского пола зараженность ВПЧ достигает 70%. Однако наличие патогена в организме еще не означает болезнь. Если у человека здоровая иммунная система, то ВПЧ-инфекция, в большинстве, случаев носит транзиторный характер — он самостоятельно исчезает в течение 2 лет. Если этого не происходит, становится актуальным вопрос о том, как лечить вирус папилломы человека у женщин.
Частая смена половых партнеров также увеличивает риск как инфицирования новыми штаммами вируса, так и активизации уже имеющейся инфекции. Если снижается иммунитет, вирус встраивается в клеточный геном, что влечет за собой высокую вероятность возникновения рака — то, как вылечить ВПЧ у женщин на данной стадии медицинской науке только предстоит открыть. Поэтому так важно держать под контролем активность вируса и правильно стимулировать иммунную защиту.
Первые признаки ВПЧ у женщин и дополнительные симптомы
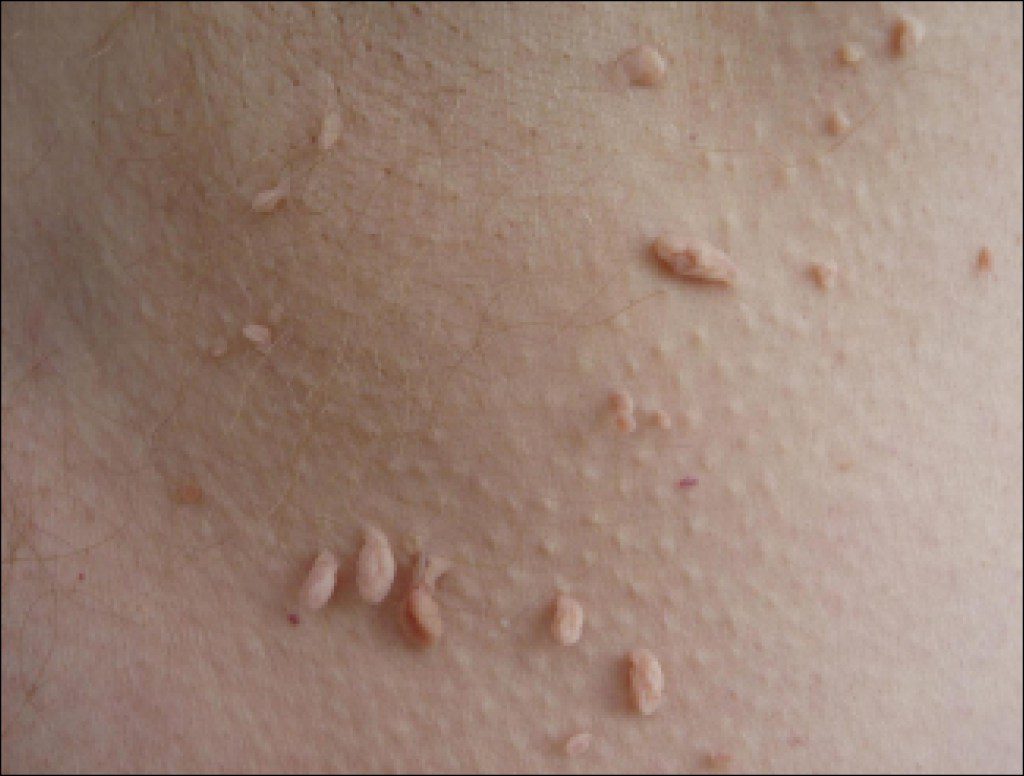
Самый явный признак наличия ВПЧ в организме женщины — появление папиллом на слизистых оболочках половых органов и коже аногенитальной области. Они не вызывают болезненных ощущений и, как правило, долго остаются незамеченными. Однако активность вируса может провоцировать появление других неприятных симптомов, из-за которых женщина незамедлительно обратится к гинекологу:
При осмотре врач видит доброкачественные образования на коже, изменения эпителия шейки матки, признаки воспаления. Рак может появиться лишь на поздних стадиях течения хронической папилломавирусной инфекции.
Лечится ли вирус папилломы человека?
Для того чтобы понять, чем сейчас лечат ВПЧ у женщин, следует разобраться какие подходы существуют в лечение папилломавирусной инфекции. На данный момент терапия ВПЧ-инфекции сводится к следующим мероприятиям:
Препаратов, которые приводят к полному исчезновению вируса из организма, нет. Однако исследования в данной области ведутся — фокус врачей сосредоточен на необходимости комбинированного лечения различных проявлений ВПЧ. Перспективными являются исследования в области генной инженерии. Ученые рассматривают возможность «переписывания» вирусного кода на самоуничтожение вместо распространения. Уменьшение вирусных копий восстанавливает местный иммунитет и устраняет хроническое воспаление.
Информация для врачей на тему «ВПЧ как лечить у женщин» на данный момент подробно изложена в актуальных клинических рекомендациях.
Когда необходимо обратиться к врачу?
Женщинам следует проходить профилактический осмотр у гинеколога не менее 1 раза в год. Также необходимость посетить врача возникает при появлении любых тревожащих симптомов:
В ситуации, когда произошел случайный половой акт, рекомендуется посетить гинеколога. Он проведет обследование, возьмет гинекологический мазок и соскоб на выявление ВПЧ.
Если папилломы возникают на других участках тела, необходима консультация дерматовенеролога. Когда папилломы или кондиломы разрастаются в области анального отверстия — может потребоваться вмешательство проктолога. Это поможет определиться с тактикой лечения и тем, какие средства от папилломы должны быть прописаны больной в конкретном случае для покупки в аптеке.
Общая схема терапии
Лечение при ВПЧ-инфекции должно быть комплексным и направлено на:
Использование средства также показано в период подготовки к удалению доброкачественных образований, вызванных ВПЧ, для снижения активности вируса и профилактики рецидивов. Препарат способствует регенерации кожных покровов и предотвращению присоединения вторичной инфекции.
Удаление папиллом и бородавок
Доброкачественные образования, вызванные ВПЧ, подлежат удалению, которое может проводиться следующими методами:
Среди новых разработок в лечении ВПЧ — система CRISPR/Cas9, которая практически полностью разрезает ДНК и встраивает свои участки, тем самым инактивируя дальнейшее распространение вируса.
Интимные противовирусные: консультируем покупателя
Обзор лекарств, применяющихся при лечении ВПЧ и герпесе, — механизм действия, преимущества и свойства, о которых стоит предупредить клиента
Первый стол регулярно отпускает местные противовирусные и иммуномодулирующие препараты, показанные для лечения герпетической и/или папилломавирусной инфекции (ВПЧ). Обе инфекции принадлежат к числу самых распространенных в мире патологий, передающихся половым путем. Как качественно и деликатно консультировать клиентов с этими болезнями, какие советовать противовирусные лекарственные средства при ВПЧ, какие от герпеса и на что обращать внимание — читайте в нашей статье.
ВПГ и ВПЧ: сходства и отличия
Прежде всего, важно понимать, что вирус простого герпеса (ВПГ) и вирус папилломы человека (ВПЧ), провоцирующие герпетическую и папилломавирусную инфекции соответственно, кардинально отличаются друг от друга.
«Галавит» при герпесвирусной инфекции способствует:
У взрослых и подростков старше 12 лет в комплексной терапии:
Суппозитории — 5 дней по 1 суппозиторию, затем по одному через день. Курс — 2 упаковки суппозиториев.
Таблетки подъязычные — 10 дней по 1 таблетке 4 раза в день. Затем продолжить прием через сутки в течение 10 дней по 4 таблетки в день.
ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ. НЕОБХОДИМО ПРОКОНСУЛЬТИРОВАТЬСЯ СО СПЕЦИАЛИСТОМ.
Генитальный герпес ассоциирован с заражением ВПГ 1‑го или 2‑го типа. По статистике, заболеванием страдают около 12 % популяции [1]. Однажды проникнув в организм, вирус «поселяется» в нем навсегда — на сегодняшний день не существует метода лечения от вируса герпеса, которое позволило бы окончательно избавиться от возбудителя. Симптомы генитального герпеса, которые возникают периодически, во время рецидивов, значительно снижают качество жизни. Интересно, что частота новых эпизодов заболевания зависит от типа вируса: при инфицировании ВПГ-1 фиксируют примерно 1 рецидив в год, в то время как при заражении ВПГ-2 их число может достигать 6 и более [2].
Несмотря на то, что специфического лечения ВПГ не существует, ряд препаратов может облегчить состояние при обострениях. Согласно отечественным и западным рекомендациям, с этой целью применяют пероральные противовирусные средства от герпеса на основе ацикловира и валацикловира. Однако в России также рекомендована местная терапия, не включенная в западные стандарты. За границей такие методы в рекомендациях отсутствуют ввиду их меньшей активности по сравнению с таблетками [3].
Несколько по‑другому обстоит ситуация с папилломавирусной инфекцией (ВПЧ). Она считается самым распространенным в мире заболеванием, передаваемым половым путем [4]. В какой‑то момент жизни ВПЧ заражается большинство взрослых людей, однако в 90 % случаев в течение двух лет после заражения происходит естественная элиминация вируса. В противном случае инфицированный становится пожизненным носителем.
К сожалению, лекарства от вируса папилломы человека не существует, так же как и в случае с вирусом простого герпеса. Однако первый, в отличие от второго, может быть смертельно опасен: ВПЧ 16‑го и 18‑го типов ассоциированы со злокачественными новообразованиями — в частности, с раком шейки матки и некоторыми другими опухолями. Единственное эффективное на сегодня медикаментозное лечение папилломавирусной инфекции заключается в эрадикации кондилом, которые являются проявлениями клинической и субклинической форм инфекции. С этой целью при лечении вируса папилломы человека применяют ряд местных противовирусных препаратов, доказавших активность в исследованиях. В то же время в отечественной практике врачи назначают и ЛС, имеющие сомнительную доказательную базу. Рассмотрим их преимущества и недостатки более детально.
Локальные иммуномодуляторы при ВПЧ и ВПГ
К числу «универсальных» средств, которые могут назначаться при различных вирусных инфекциях — от банальных респираторных до герпетической и папилломавирусной, — относятся интерфероны. В частности — препараты интерферона альфа-2b человеческого рекомбинантного.
Интерферон альфа-2b имеет противовирусные, иммуномодулирующие и антипролиферативные свойства. Он подавляет репликацию РНК- и ДНК-содержащих вирусов, усиливает активность макрофагов, увеличивает цитотоксичность лимфоцитов к клеткам-мишеням. Применение содержащих интерферон альфа-2b средств сопровождается повышением уровня иммуноглобулинов типа А, нормализацией IgE [5]. Однако эти терапевтические эффекты в полной мере проявляются при системном введении препарата, когда достигается его высокая концентрация в крови. При этом следует заметить, что могут развиваться достаточно мощные побочные эффекты, в том числе лихорадка, потеря аппетита, головные, мышечные, суставные боли и множество других неблагоприятных реакций.
Из-за специфического профиля безопасности инъекционные препараты интерферона назначаются только в очень серьезных случаях, когда риск побочных эффектов оправдан — например, при лечении гепатитов, ряда онкологических заболеваний и пр. ВПГ и ВПЧ-инфекции к таким ситуациям не относятся и не являются показаниями для системного назначения интерферона. В то же время в РФ зарегистрирован весьма внушительный перечень местных форм интерферона альфа-2b, в том числе и мазей/кремов для обработки слизистых оболочек при генитальном герпесе.
Теоретически локальные препараты интерферона должны обладать всеми преимуществами инъекционных и не иметь их побочных эффектов, поскольку местные формы или очень незначительно всасываются в системный кровоток, или вовсе не проникают в кровь. Однако, на сегодня нет достаточно надежных доказательств эффективности интерферонов при местном применении. Тем не менее, в отечественной практике их довольно часто назначают в составе комплексного лечения рецидивов генитальной герпетической инфекции.
Наряду с местными формами, содержащими только интерферон альфа-2b, в РФ зарегистрировано и несколько комбинированных препаратов:
+ Высокий профиль безопасности.
! Целесообразность применения местных форм ацикловира при генитальном герпесе подвергается серьезным сомнениям ввиду недостаточной активности, что подтверждено в западных рекомендациях [3].Препараты интерферона альфа-2b, как моно-, так и комбинированные, отпускаются как по рецепту, так и без — в зависимости от указания на правила отпуска в инструкции конкретного препарата. Важно обратить внимание посетителя на то, что препараты от ВПЧ первой линии лечения — пероральные формы ацикловира и валацикловира — должен выписать врач, поэтому нужно посоветовать незамедлительно обратиться за консультацией к доктору.
Синтетические противовирусные местные препараты
Эту группу ЛС можно условно разделить на средства, применяемые при генитальной герпетической инфекции, и противовирусные препараты, назначаемые для лечения папиллом и кондилом, связанных с папилломавирусной инфекцией.
Местные препараты при генитальном герпесе
Несколько ЛС, зарегистрированных в РФ, применяются для лечения и профилактики рецидивов генитального герпеса.
Тромантадин
Противовирусный препарат от герпеса, производное адамантана (подобно известным противовирусным римантадину и амантадину). Ингибирует прикрепление вируса к поверхности клеточной мембраны, препятствуя проникновению возбудителя внутрь клетки. Предотвращает слияние клеток и затрудняет распространение вируса за счет изменения синтеза гликопротеинов [5]. Выпускается в форме геля для наружного применения, который можно наносить на слизистые оболочки при обострении ВПГ-инфекции [5].
Отпуск: без рецепта.
! Есть данные о развитии контактной аллергической реакции при использовании препарата [7].
Иммуномодулятор, способный регулировать активность клеток врожденного и приобретенного иммунитета, в том числе макрофаги, нейтрофилы и натуральные киллеры. При этом этот противовирусный препарат против герпеса повышает устойчивость организма к бактериальным, вирусным и грибковым инфекциям, сокращая их частоту, выраженность и длительность (5). Кроме того, препарат нормализует образование антител и регулирует выработку интерферонов, а также блокирует избыточный синтез провоспалительных цитокинов и снижает уровень оксидантного стресса (5).
Отпуск: Без рецепта
+ Высокий профиль безопасности (5).
Азоксимера бромид
Российский препарат, предположительно, проявляющий иммуностимулирующий эффект. По данным инструкции [5], напрямую влияет на фагоциты и естественные киллеры, стимулирует образование антител и синтез интерферона, проявляет антиоксидантные и детоксикационные свойства. В отечественной практике применяется при широком спектре заболеваний — от гриппа до злокачественных новообразований.
Вагинальные суппозитории азоксимера бромида применяются для профилактики рецидивов генитального герпеса.
Отпуск: без рецепта.
+ Высокий профиль безопасности. По данным производителя [5], побочные эффекты не зарегистрированы.
! Суппозитории азоксимера бромида не показаны для лечения активной формы герпеса!
Местные противовирусные препараты для лечения ВПЧ (папилломавируса)
Некоторые топические противовирусные препараты, активные в отношении папилломавирусов, в отличие от ряда препаратов, помогающих от вируса герпеса, имеют прочную доказательную базу и применяются во всем мире для лечения проявлений ВПЧ — в частности, кондилом.
Имихимод
Модификатор иммунного ответа, не оказывающий противовирусного действия. Активность проявляет за счет способности индуцировать выработку интерферона-альфа и других цитокинов. Показан для лечения остроконечных кондилом в урогенитальной зоне [5].
Отпуск: по рецепту.
+ Прочная доказательная база. Препарат определенно снижает вирусную нагрузку. Доказано, что применение крема имихимода 5 %-ного 3 раза в неделю на ночь на протяжении 16 недель эффективно и безопасно для лечения кондилом. Частота рецидивов оценивается как низкая [8]. Имихимод рекомендован для лечения генитальных кондилом авторитетным американским регулятором FDA [8].
! При нанесении имихимода более чем в 10 % случаев наблюдаются зуд и боль [5], о чем следует предупредить покупателя.
Местные противовирусные средства растительного происхождения
Аммония глицирризинат
Активный компонент препарата — активированную глицирризиновую кислоту — получают из корня солодки. Оказывает комплексное иммуностимулирующее, противовирусное, противовоспалительное, противозудное действие. Глицирризиновая кислота прерывает репликацию ряда ДНК и РНК вирусов, в том числе вируса простого герпеса, папилломы человека, цитомегаловируса [5].
Показана в качестве препарата для лечения папилломавирусной инфекции и вируса простого герпеса, в том числе и при инфицировании вирусами онкогенного типа. Выпускается в форме спрея, который распыляют на слизистые оболочки и пораженные участки кожи.
Отпуск: без рецепта.
+ Имеет широкий спектр показаний, среди которых профилактика и лечение кандидозного вульвовагинита, дискомфорт в области половых органов. Может применяться при беременности и кормлении грудью; хорошо переносится.
Подофиллотоксин
Активный компонент подофиллина, производного растительных экстрактов, выделяемых из корневищ с корнями подофилла щитовидного — растения семейства барбарисовых. Обладает выраженными противоопухолевыми и противовирусными свойствами, оказывает цитотоксическое действие. При наружном применении прижигает и мумифицирует кондиломы. Применяется в качестве препарата для местного лечения от вируса папилломы человека. Выпускается в форме раствора для обработки остроконечных кондилом [8].
Отпуск: по рецепту.
+ Доказанный эффект. По данным исследований, 0,5 %-ный раствор подофиллотоксина уменьшает число аногенитальных бородавок с 6,3 до 1,1, разрушая около 70 % образований [8].
! Необходимо соблюдать осторожность при применении — попадание на здоровую кожу может приводить к изъязвлению. Местные реакции при применении, аллергические реакции. Первостольник, отпуская этот противовирусный препарат от папиллом и кондилом, должен обратить внимание клиента на эту особенность и напомнить, что ЛС следует хранить в недоступном для детей месте.
Тетрагидроксиглюкопиранозилксантен
Российский препарат. Активный компонент выделяют из растения копеечника альпийского или копеечника желтеющего.
Согласно инструкции, обладает противовирусной активностью в отношении ВПГ-1 и ВПГ-2, а также цитомегаловируса и некоторых других ДНК-содержащих вирусов. Кроме того, предположительно, препарат активирует клеточный и гуморальный иммунитет, ингибирует рост ряда бактерий и патогенных простейших, в том числе трихомонад, а также оказывает умеренное противовоспалительное действие. Применяют в форме мази в составе комбинированного лечения острых и рецидивирующих форм герпеса, в том числе генитального [5].
Отпуск: без рецепта.
+ Благоприятный профиль безопасности, возможность применять в составе комплексного лечения.
Полисахариды побегов Solanum tuberosum
Рецептурный российский препарат, активный компонент получают из побегов паслена клубненосного. По данным инструкции, проявляет противовирусный эффект в отношении ВПГ-1 и ВПГ-2, способствует индукции интерферонов и повышает иммунный ответ [5]. Следует заметить, что фармакокинетические свойства препарата не изучались. Вагинальные суппозитории применяются в комплексной терапии генитального герпеса.
Отпуск: без рецепта.
+ Высокий профиль безопасности. Побочные эффекты проявляются редко.
Десмодиума канадского травы экстракт
Противовирусный препарат от герпеса растительного происхождения, созданный из сухого экстракта травы десмодиума канадского. По данным инструкции, проявляет противовирусную активность в отношении вирусов герпеса, стимулирует выработку интерферона [5]. Мазь показана для применения при острых и рецидивирующих формах герпеса, в том числе урогенитального.
Отпуск: без рецепта.
+ Высокий профиль безопасности — побочные эффекты не выявлены.
Гипорамина экстракт
Российская разработка на основе экстракта листьев облепихи. По данным инструкции, активен в отношении вирусов простого герпеса, цитомегаловирусов и некоторых других [5]. Мазь, содержащая экстракт гипорамин, показана для лечения и профилактики эпизодов герпеса, в том числе и генитального.
Отпуск: без рецепта.
+ Высокий профиль безопасности; возможность использовать во время беременности и лактации (после консультации с врачом).
Мелиссы лекарственной листьев экстракт
По данным инструкции, проявляет противовирусную активность в отношении ВПГ, оказывает противовоспалительное действие [5]. Крем, содержащий экстракт листьев мелиссы, применяют при поражениях слизистых и кожи, в том числе и в урогенитальной зоне.
Отпуск: без рецепта.
+ Высокий профиль безопасности.
В заключение хочется еще раз подчеркнуть: широкий ассортимент позволяет первостольникам предлагать разные ЛС при запросах на местные средства для лечения проявлений ВПГ или лекарства от ВПЧ. Но при этом не следует забывать о необходимости рекомендовать посетителю обратиться к врачу, ведь именно доктор должен назначить препараты первой линии и подобрать при необходимости комплексную схему лечения папилломавирусной инфекции.
ВПЧ (вирус папилломы человека)
ВПЧ или вирус папилломы человека является самой распространенной инфекцией на земном шаре. По данным исследователей, более 90% людей всего мира заражены тем или иным типом ВПЧ. В настоящее время насчитывается более 70 разновидностей вируса папилломы человека, но лишь часть из них представляет для врачей интерес.
ВПЧ относится к роду папилломавирусов из семейства паповавирусов. Источником заражения является больной человек или вирусоноситель, то есть ВПЧ передается только от человека к человеку.
Известны три пути передачи данной инфекции:
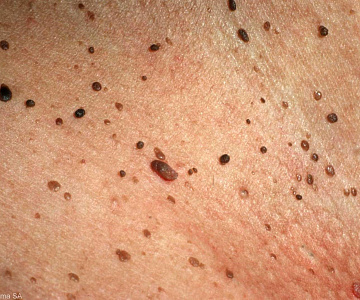
ВПЧ поражает кожные покровы и слизистые оболочки: на них образуются различные бородавки, папилломы и кондиломы.
Вирус обитает в крови человека и до определенного времени себя никак не проявляет. Но стоит только ослабнуть иммунитету, как на коже и/или слизистых появляются разрастания. Этим и объясняется довольно длительный инкубационный период: от нескольких недель до десятков лет.
Условно все типы ВПЧ можно разделить на 2 группы:
ВПЧ, «виновные» в образовании бородавок;
ВПЧ, «виновные» в развитии папиллом и кондилом;
В чем опасность ВПЧ?
ВПЧ способен вызвать злокачественную опухоль (рак кожи или слизистых). Выделяют 3 типа его онкогенности:
Таблица: Соответствие типа ВПЧ заболеванию
| Заболевания | Типы ВПЧ |
| Поражения кожи: | |
| Бородавки на подошве стопы (мозоли) | 1, 2, 4 |
| Обычные бородавки | 2, 4, 26, 27, 29, 57 |
| Плоские бородавки | 3, 10, 28, 49 |
| Бородавки Butcher | 7 |
| Веруциформная эпидермодисплазия | 2, 3, 5, 8, 9, 10, 12, 14, 15, 17, 19, 20-25, 36, 37, 46, 47, 50 |
| Поражения слизистых половых органов: | |
| Остроконечные кондиломы | 6, 11, 42-44, 54 |
| Поражения эпителия без прорастания в другие слои (интраэпителиальные поражения), могут быть предраковым состоянием | 6, 11, 16, 18, 30, 31, 33?, 39, 40, 42, 43, 51, 52, 55, 57-59, 61, 62, 64, 67-70 |
| Рак шейки матки, вульвы, влагалища, области анального отверстия и полового члена | 16, 18, 31, 33, 35, 39, 45, 51, 52, 54, 56, 66, 68 |
| Поражения не генитальных слизистых: | |
| Поражения слизистой рта (фокальная эпителиальная гиперплазия) | 13, 32 |
| Рецидивный папилломатоз дыхательных путей | 6, 11, 30 |
| Злокачественные образования головы, шеи, легких | 2, 6, 11, 16, 18, 30 |
Все фото на странице: сайт кафедры дерматовенерологии Томского военно-медицинского института
Самая распространенная клиническая форма ВПЧ. Сначала они выглядят как куполообразные папулы, размеры которых не превышают булавочную головку. Затем они начинают расти и одновременно темнеть, поверхность их становится шершавой. Вокруг материнской бородавки образуются дочерние, в этот период возможны боль и жжение.
Располагаются бородавки с тыльной стороны кистей и стоп, в области подбородка, на веках, на волосистой части головы, между пальцами, на подошве.
Подошвенные бородавки болезненны, из-за них человек не может ходить. Низкий онкогенный риск.
Данный вид бородавок выглядит как кожный рог (длинные нитевидные папулы). Как правило, они локализуются на руках и пальцах кистей, часто возникают в месте порезов. Вызывается ВПЧ 2 и 7, это доброкачественное образование, не склонное к перерождению.
Такие бородавки немного возвышаются над уровнем кожи, имеют склонность к группировке. Цвет у плоских бородавок телесный или бледно-коричневый, располагаются на лбу и плечах. Могут локализоваться на половом члене, шейке матки, в области наружных половых органов и в анусе.
Наследственное заболевание. Встречается очень редко в виде дерматоза. Выглядит как множество плоских бородавчатых высыпаний или пигментированных пятен. Высыпания чешуйчатые, сливаются между собой, локализуются на лице, шее, верхних конечностях. По внешнему виду заболевание схоже с отрубевидным лишаем. Возможно перерождение в рак. Вызывается ВПЧ 2, 3, 5, 8-10, 12, 14, 15, 17, 19, 20-25, 37, 47, 50 типов.
Локализуются по бокам ногтя, врастают в кожу и приводят к дистрофии ногтевой пластинки. Не склонны озлокачествляться.
Выглядит как единичное образование исключительно в верхнем слое эпидермиса (чаще на голове). Очаг от 5 до 50мм выглядит как разрастающийся роговой слой кожи, иногда покрывается корками. Вызывается ВПЧ 16-го типа. Образования склонны к перерождению в плоскоклеточный рак.
Внешний вид образований напоминает цветную капусту или петушиный гребень. Чаще всего кондиломы располагаются на крайней плоти, головке пениса, около мочеиспускательного канала, вокруг ануса, на малых половых губах, на слизистой влагалища, шейке матки, в уголках рта, в устье мочеиспускательного канала.
Образования в ротоглотке.
Эффективных препаратов, которые могут вылечить от ВПЧ на сегодняшний день не разработано. В некоторых случаях он может самостоятельно элиминироваться из организма в течении нескольких лет. Иногда могут применяться методы лечения, которые сводятся к устранению внешних проявлений, то есть к разрушению образований. Вирусы, которые становятся их причиной, обычно неопасны и не вызывают рак, поэтому удаление папиллом, кондилом и других новообразований может понадобится скорее в косметических целях. Решение о необходимости такого лечения принимает врач совместно с пациентом на основе распространенности процесса и дискомфорта, который он может доставлять.
Деструктивные методы лечения обладают различной эффективностью и не дают гарантии, что папилломы/кондиломы не возникнут вновь. К ним относятся:
Химические методы лечения:
Использование цитостатических препаратов:
Вызвать рак могут штаммы высокого онкогенного риска. А те типы, которые вызывают появление кондилом, или папилом, обычно неопасны.
ВПЧ высокого онкогенного риска действительно может вызывать изменения в тканях и приводить к онкологическому процессу. Но между первичными изменениями и развитием рака обычно проходят годы а иногда десятки лет. Поэтому, если выявить изменения на начальных стадиях и вовремя провести лечение, прогноз обычно благоприятный. Преимуществом является то, что органы, которые подвержены риску, хорошо доступны для осмотра. Поэтому рутинный регулярный осмотр врачом является эффективным и надежным способом профилактики рака наружных половых и других органов из группы риска в случае инфицирования ВПЧ.
ВПЧ: как лечить и предотвратить
Вирус папилломы человека (ВПЧ) — что это? Вирус может не проявляться годами, но однажды даст о себе знать. Как он ведет себя в организме и как можно вылечить? Отвечаем на главные вопросы.
1. Что такое вирус папилломы человека
Это вирус, который проникает в слизистые клетки эпителия — обычно во время полового контакта (включая петтинг). У женщин и мужчин он распространяется с одинаковой скоростью, но вот проявления и последствия заражения могут быть различными.
2. ВПЧ: типы и виды
Сегодня медики выявили более полутора сотен разных типов ВПЧ. Большая часть проявляется в виде папиллом на коже — они могут возникать на любых частях тела. Около 40 видов вируса выбирают селиться на тканях половых органов. Все типы ВПЧ высокозаразны — считается, что каждый взрослый человек хотя бы раз в жизни будет контактировать с носителем вируса.
Сам по себе факт заражения не означает, что вирус разовьется в болезнь. В большинстве случаев он будет находиться в «спящем режиме» в клетках плоского эпителия. Спровоцировать его активацию могут аутоиммунные заболевания или сезонные недуги, когда иммунная система оказывается ослабленной.
Одно из проявлений ВПЧ — появление остроконечных кондилом (их еще называют аногенитальными бородавками). Это образования на коже и слизистых половых органов и смежных областей. Кроме чисто эстетической проблемы ВПЧ создает угрозу рака, хотя в целом этот вирус считается низкоонкогенным. В группе риска — все женщины и мужчины половозрелого возраста, которые занимаются сексом.
3. ВПЧ: лечение и профилактика
Остроконечные кондиломы выглядят непривлекательно, они могут селиться в таких местах:
Эти образования не вызывают болевых или дискомфортных ощущений, их достаточно просто удалить. Врачи используют препараты в виде мазей, примочек или выбирают хирургические методы:
Важна своевременная диагностика, поскольку около 15 типов ВПЧ являются онкогенными — они проникают в нижние слои эпителия и вызывают развитие рака шейки матки, ануса или прямой кишки, влагалища. Опухоль может вырасти в полости рта и горла.
Стоит помнить о ежегодном скрининге в рамках традиционного чекапа организма или при посещении профильных специалистов (гинеколога и уролога). Очень действенным способом профилактики считают вакцинацию* — так можно обезопасить себя (а значит, и партнера) от заражения.
Заказать лекарства с доставкой можно в приложении Здравсити
ВПЧ у женщин
ВПЧ (вирус папилломы человека) — это достаточно часто диагностируемая инфекция, которая поражает как мужчин, так и женщин. Сегодня ученым известно около 100 разнообразных типов этого вируса, из которых каждый вызывает разные заболевания. Почти 30 из них провоцируют поражение женских половых органов. Среди них есть несколько типов вируса, которые характеризуются повышенным риском развития онкологии. По официальным данным, почти у 70 % взрослых женщин обнаруживается ВПЧ в организме. Это самая распространенная инфекция половых путей после генитального герпеса.
Симптомы ВПЧ у женщин (признаки)
Проявиться вирус может далеко не сразу после заражения. У женщин инфекция может вызвать появление различных недугов. Чаще всего у представительниц слабого пола папилломавирус провоцирует появление остроконечных кондилом. Это бородавки на широкой ножке, которые образуются:
Обнаружить их, как правило, удается только во время гинекологического осмотра. Поэтому женщина может длительное время не догадываться о своей проблеме. Тип вируса, который вызывает появление остроконечных кондилом, не провоцирует рак.
В подавляющем большинстве случаев, симптомов ВПЧ у женщин практически не наблюдаются. Вирус может спровоцировать появление плоских бородавок, которые не вызывают никакого беспокойства, кроме косметического дефекта. Некоторые типы папилломавируса способны вызвать появление образований также:
Опасным симптомом ВПЧ является цервикальная неоплазия. Это предраковое состояние слизистой матки, которое должно стать основанием для срочного начала лечения. Вызвать появление такой серьезной проблемы могут вирусы 16 и 18 типов. От момента заражения этими вирусами до появления первых признаков развития рака может пройти от 10 до 20 лет и более.
Причины заражения
По данным медицинской статистики, почти 50 % взрослого населения планеты заражены ВПЧ. Главным путем передачи вируса является физический контакт с инфицированным. В большинстве случаев заражение происходит во время незащищенного полового контакта. Вирус очень легко передается от человека к человеку. Поэтому, если у один из партнеров инфицированный, то почти с вероятностью в 100 % второй заразиться. Папилломавирус у женщин передается:
В более редких случаях инфицирование может произойти при поцелуе. Такая передача вируса происходит, если у одного из партнеров есть бородавки на слизистых рта или горла. Специалисты отмечают, что к косвенным причинам заражения относят:
Практически никогда не передается возбудитель бытовым путем. Поэтому пользование вещами больного, например, предметами личной гигиены, такими как полотенца или расчески, не могут спровоцировать инфицирование здорового человека. Иногда дети рождаются уже зараженными папилломавирусом человека. Это случается, если мать забеременела, имея симптомы ВПЧ у женщин, и не прошла лечение. Передача вируса малышу происходит при прохождении им родовых путей.
К какому врачу обратиться?
Как правило, диагностировать проблему удается только во время прохождения планового осмотра. Распознать первые признаки ВПЧ у женщин может:
Доктор внимательно осматривает пациентку, выслушивает ее жалобы. Для того чтобы понимать, как бороться с заболеванием, врачу необходимо знать, с каким типом вируса он имеет дело. Поэтому пациентку сразу направляют на обследование. Но перед этим врач также поинтересуется у нее:
Иногда в ходе опроса специалист может определить истинные причины и пути заражения. Эта информация будет полезна при составлении программы лечения. Врач также может посоветовать пациентке получить консультацию дерматовенеролога или онколога. Помощь этих специалистов, как правило, необходима при обнаружении в ходе диагностических исследований различных осложнений или сопутствующих заболеваний.
Лечение у женщин
Методы терапии определяет врач. Только доктор знает, какое лечение ВПЧ у женщин приносит лучший эффект. Справиться с папилломами помогают как медикаментозные, так и хирургические методики. В первую очередь, усилия специалистов будут направлены на удаление бородавок. Для этого может применяться:
Альтернативным методом будет медикаментозная терапия. Доктор может назначить пациентке прием специальных препаратов, которые приводят к гибели папиллом. Такой метод лечения получил название цитотоксической терапии. Однако прием препаратов разрешен далеко не всем. К недостаткам метода относят большое число рецидивов, наличие множественных побочных эффектов.
Комплексное лечение ВПЧ у женщин не может не включать приема иммуномодулирующих средств. Препараты помогают укрепить защитные силы организма, что позволяет ему более эффективно противостоять инфекции. При этом, усиливается как местный, так и общий иммунитет пациентки.
Диагностика папилломавируса у женщин
Самостоятельно распознать наличие инфекции в организме невозможно. Подтвердить диагноз может только комплексное обследование пациентки. В первую очередь, женщине назначают кольпоскопию. Это исследование проводится с помощью специального прибора, который позволяет детально и прицельно осмотреть слизистую гениталий. Помимо этого, больной предстоит пройти:
Получив данные обследования, врач начинает разрабатывать для пациентки программу лечения. При этом, он учитывает общее состояние здоровья женщины, ее возраст и характер течения заболевания.
Можно ли вылечить навсегда?
Удаление бородавок не означает излечение от папилломавируса. Многие женщины интересуются, можно ли навсегда избавиться от инфекции? Однако ответы врачей неутешительные. Если вирус попал в организм, то изгнать полностью его из своего тела практически невозможно.
Исключением является только молодой возраст заболевшей. В медицинской практике есть случаи, когда сильный иммунитет девушек полностью убивал вирус. Однако это чаще исключение из правил. Поэтому вопрос, можно ли вылечить навсегда ВПЧ у женщин, остается до сих пор открытым.
Специалисты со всех уголков мира пытаются разработать средство, которое бы помогло организму справиться с вирусом. Но пока попытки отыскать лекарство безуспешны. Однако существует большое количество лекарств, которые помогают его подавлять. Лекарства позволяют не допускать появления новых бородавок, а также не дают клеткам трансформироваться в злокачественные.
Принимать такие средства можно только по назначению врача. Женщинам, которые страдают от ВПЧ, важно постоянно наблюдаться у врача, так как в любой момент недуг может вновь обостриться. Поэтому всем носителям вируса приходится ежегодно проходить обследование, чтобы не допустить появления рака.
Вирус папилломы человека — какое лечение ВПЧ эффективно?
Что такое вирус папилломы человека?
Группа вирусов ВПЧ входит в семейство папилломавирусов, которое включает 5 родов, порядка 43 разновидностей и почти 170 типов, именно ВПЧ является причиной образования бородавок. Существует его прямая взаимосвязь связь с раком шейки матки: в 92% случаев заболевания раком обнаруживается этот вирус.
Какие анализы сдают на вирус папилломы человека?
Основные направления в исследовании — это определение вирусной нагрузки, то есть количественный показатель и определение типа вируса методом ПЦР.
Папилломы это опасно?
По сути, папиллома — это доброкачественная опухоль, но она таит в себе и опасности. Во-первых, возможно повреждение ее целостности, приводящее к формированию рубцов, редко к заражению крови. Не рекомендуется удалять механически папилломы самостоятельно, это может привести к генерализации процесса и распространению папиллом по всему телу. Самая главная опасность папиллом заключается в том, что они вирусные. Большинство видов ВПЧ не представляют угрозу для здоровья и жизни человека, но ВПЧ 16 и 18 типа могут спровоцировать развитие злокачественных образований. Доброкачественные папилломы, как правило, доставляют много неприятностей человеку. Они могут увеличиваться до больших размеров, могут образовываться в области половых органов. Некоторые виды ВПЧ вызывают предраковые заболевания.
Вирус папилломы человека заразен?
ВПЧ может передаваться различными путями. При контактно-бытовом способе передачи вирус через кожу при рукопожатиях и использовании средств личной гигиены, после примерки чужой одежды и нижнего белья, при посещении общественных бассейнов и саун. Особо опасным считается половой путь передачи вируса, так как при этом существует высокий риск заражения ВПЧ онкогенного типа. Вероятность передачи вируса половым путем намного выше, если у партнера есть остроконечные кондиломы. ВПЧ может передаваться от матери к ребенку во время родов, крайне редко это происходит во время беременности. При этом чаще всего у детей развивается папилломатоз гортани, опасный серьезными нарушениями дыхательной функции. Возможно заражение ребенка от матери при кормлении грудью.
Как лечат вирус папилломы человека?
Медикаментозное лечение вируса проводится с помощью лекарственных препаратов, которые воздействуют на причину заболевания, а также восстанавливают функцию иммунной системы. Существуют различные схемы внутривенного введения лекарств, врачи, как правило, назначают лечение индивидуально, стандартных схем нет. Какие препараты обычно назначают? Циклоферон, Интерферон альфа, Панавир, Ингарон. Таблетированные формы противовирусных препаратов: Изопринозин, Ликопид, Лавомакс, Алпизарин. Свечи: Генферон, Бетадин, Виферон. Мази: Оксолиновая мазь, San Fen Zhong мазь, Стефалин, Салициловая мазь. Витамины: Аевит, Алфавит.
Вакцинация против ВПЧ (Гардасил)
Полностью избавиться от ВПЧ при современном уровне фармацевтической промышленности еще невозможно, но можно предупредить заражение инфекцией и для этого проводится вакцинация таким препаратом, как Гардасил. В некоторых странах эти прививки уже являются обязательными, в России сделать вакцинацию можно добровольно. При выборе такого способа профилактики ВПЧ необходимо пройти предварительное обследование на определение наличия вируса в организме. В состав вакцин входят синтетически модифицированные белки, сходные со структурой вируса. Введение в организм этих белков активизирует работу иммунной системы и приводит к выработке антител, защищающих от развития ВПЧ после проникновения возбудителя в организм. Разработчики вакцины советуют ставить препарат девочкам и мальчикам от 10 до 12 лет. Связано это с тем, что в этом возрасте половых контактов в подавляющем большинстве случаев нет, а иммунная система работает в полную силу, что способствует хорошей ответной реакции на препарат.
Вирус папилломы человека может вызывать рак?
Самым опасным типом ВПЧ, вызывающий злокачественные образования считаются следующие: ВПЧ-16; ВПЧ-18; ВПЧ-31, 33, 45, 56, 58; ВПЧ-51, 59, 68; ВПЧ-35, 39, 52.
Какие разновидности рака вызывает ВПЧ
Наиболее часто рак шейки матки вызывается вирусом папилломы человека 16 и 18 типов, они же вызывают рак половых органов. ВПЧ 16 в 50% случае является причиной рака гортани.
ВПЧ передается половым путем?
ВПЧ передается половым путем, и при этом сами половые контакты становятся основной причиной заражения папиллома вирусом. Расскажем об этом подробнее.
Папилломы, расположенные на половом члене являются признаком папилломавирусной инфекции, следственно заражение половым путем вполне логично. Инкубационный период при ВПЧ длится от 1 до 12 месяцев. При этом сами папилломы могут совсем не вырастать, и только при снижении функции иммунной системы может произойти начало их образования. Поэтому обнаружение ВПЧ в организме на ранних стадиях развития заболевания возможно исключительно с помощью специальных анализов. В настоящее время, ВПЧ является одним из самых распространенных заболеваний и риск заражения партнера при незащищенном половом акте является практически 100%.
Папилломы — это онкологическое заболевание?
Все разновидности ВПЧ по степени риска возникновения злокачественного перерождения можно разделить на следующие: низкой степени риска, средней степени риска и высокой степени онкогенного (канцерогенного) риска.
Остроконечные кондиломы в области гениталий, как правило, не вызываются вирусом с высокой степень онкогенности. Плоскоклеточные папилломы являются злокачественными новообразованиями. Пациенты, у которых диагностируются плоскоклеточные папилломы находятся в группе повышенного риска и требуют незамедлительного лечения.
Если у пациента обнаружен ВПЧ онкогенной группы, для профилактики появления онкологических процессов в организме необходимо уделять внимание иммунной системе, регулярно сдавать анализы и наблюдаться у врача.
Можно ли рожать, если есть вирус папилломы человека?
Если в организме женщины обнаружен ВПЧ, но при этом нет внешних проявлений в виде образования папиллом, то рожать можно спокойно и не волноваться. Если есть остроконечные кондиломы в области гениталий, то существует очень высокий риск заражения ребенка ВПЧ во время прохождения по родовым путям. Первый самостоятельный вдох ребенка может произойти прямо в родовых путях, вирус попав в горло малыша приводит к разрастанию папиллом на его голосовых складках. Поэтому при наличии генитальных папиллом и активной формы ВПЧ показано кесарево сечение.
Может ли вирус папилломы человека пройти без лечения?
По статистическим данным, в 85 % случаев ВПЧ после заражения устраняется организмом самостоятельно, благодаря хорошей работе иммунной системы. Этот процесс может длиться от нескольких месяцев до нескольких лет. Иногда пребывание вируса в организме человека можно не обнаружить даже при медицинском обследовании. Полностью подтвердить наличие ВПЧ можно при наличии образований на коже — папиллом.
Что делать, если обнаружили вирус папилломы человека?
Как удаляют папилломы?
Удалить папиллому можно медикаментозно. Но наиболее эффективным методом принято считать хирургическую методику, лазерную хирургию и электрохирургическое удаление. Обычный хирургический метод удаления применяется не часто, после него часто возникают рецидивы возникновения образований. Удаление с помощью лазера считается самым лучшим в мире, при этом удаление безболезненно и безопасно, не оставляет после себя шрамов и рубцов. Радиохирургическое удаление производят под местной анестезией, результат достаточно хороший и стойкий.
Где чаще всего образуются папилломы?
Чаще всего папилломы локализуются в области подмышек и в паху, рядом с половыми органами. Нередко образования встречаются под молочными железами, на шее, веках.
Что делать, если папилломы обнаружили в гортани?
Папилломатоз гортани — весьма тяжёлое заболевание, при котором нарушается голосообразование и дыхательная функция. В детском возрасте распознают симптомы заболевания в возрасте от одного до пяти лет. Если вы отмечаете хриплый голос у ребенка, кашель, затруднение дыхания или ощущение кома в горле, необходимо сразу показать его врачу.
Папилломавирусная инфекция сегодня: клиническое разнообразие, лечение и профилактика
Папилломавирусы относятся к семейству Papovaviridae и в течение многих тысяч лет паразитируют на людях. Это мелкие безоболочечные 20-гранные ДНК-содержащие вирусы, которые поражают эпителиальные клетки разных анатомических зон.
Папилломавирусы относятся к семейству Papovaviridae и в течение многих тысяч лет паразитируют на людях. Это мелкие безоболочечные 20-гранные ДНК-содержащие вирусы, которые поражают эпителиальные клетки разных анатомических зон. Вирусы папилломы человека (ВПЧ) классифицируются на пять эволюционных групп: альфа, бета, гамма, мю и ню. Представители группы альфа поражают генитальный тракт, а остальные только кожу. Диаметр вируса 55 нм, геном ВПЧ представлен длинной двуспиральной циркулярной ДНК с размером 8 тысяч пар основ. В зависимости от времени экспрессии гены ВПЧ делятся на ранние и поздние, соответственно они кодируют ранние Е1-Е7 и поздние L1- и L2-протеины.
Оценить распространенность папилломавирусной инфекции (ПВИ) среди населения очень трудно. Предполагается, что генитальные бородавки встречаются приблизительно у 1% сексуально-активного населения, у 5–40% инфекция протекает субклинически или бессимптомно. У беременных женщин частота выявления всех типов ВПЧ составляет 30–65%, а типов высокого онкогенного риска — 20–30% [1].
Наиболее распространенный путь передачи — это прямой контакт с кожным покровом или слизистой оболочкой больного человека или вирусоносителя. Вирус сохраняет жизнеспособность в воде (бассейне, бане), а также передается при половых контактах. Папилломавирусы, инфицирующие кожу и слизистые оболочки аногенитального тракта, являются одной из самых распространенных сексуально-трансмиссивных инфекций, с которой женщины и мужчины встречаются в первые годы сексуальной активности. Пик инфицирования ВПЧ во всем мире составляет от 17 до 25 лет, затем распространенность инфекции снижается и вновь повышается в возрасте 35–44 или 45–54 лет. Вероятно, это отражает возрастающую социальную тенденцию разводов и новых партнерских отношений, формирующихся в старшем возрасте. Факторами риска инфицирования ПВИ являются другие инфекции, передающиеся половым путем (ИППП), применение оральных контрацептивов, курение и недостаточность клеточного иммунитета у инфицированных лиц. В 1989 г. доказана вертикальная передача вируса, что подтверждают сообщения об обнаружении ВПЧ в амниотической жидкости беременных и у детей, рожденных от матерей-носителей ВПЧ [2]. Возможный риск колеблется по данным разных авторов от 3% до 80% [3]. Данный разброс объясняется различиями в методике проведения полимеразной цепной реакции (ПЦР) на выявление ДНК ВПЧ. При этом ПВИ может передаваться трансплацентарно и интранатально (в частности, ВПЧ 6 и 11)). Риск инфицирования прямо пропорционален тяжести инфекции (количеству вирусных частиц) и времени безводного промежутка в родах, однако проведенные исследования свидетельствуют о том, что родоразрешение путем кесарева сечения не снижает риск инфицирования плода, что свидетельствует о преимущественно внутриутробном его заражении [2]. Интранатальное инфицирование может приводить к ювенильному рецидивирующему респираторному папилломатозу (частота составляет 1,7–2,6 на 100 000 детей и 1 на 1500 родов среди женщин с генитальной ПВИ) [4]. Все проведенные статистические исследования однозначно указывают на то, что единственным путем приобретения онкогенных типов ВПЧ, поражающих гениталии, является половой путь [5].
С учетом тропизма ВПЧ подразделяют на мукотропные и дермотропные. В зависимости от канцерогенности известные папилломавирусы можно условно разбить на три основные группы: неонкогенные (ВПЧ 1, 2, 3, 5, 10, 63), низкого онкогенного риска (в основном ВПЧ 6, 11, 42, 43, 44), высокого онкогенного риска (ВПЧ 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59 и 68). Различия в онкогенных свойствах ВПЧ связаны со способностью определенных типов вирусов определять число митозов в пораженных клетках.
Для вируса папилломы человека характерен широкий спектр эпителиальных пролиферативных повреждений. Гиперплазия и гиперкератоз как основные патоморфологические и клинические проявления кожной инфекции, вызванной ВПЧ, а также обширность и глубина поражений зависят от типа вируса. ВПЧ 1-го, 2-го, 4-го и 63-го типа может быть причиной вульгарных и подошвенных бородавок. Плоские бородавки могут быть вызваны 3-м, 10-м, 28-м, 41-м, 49-м и 75-м типами ВПЧ. Среди дерматотропных вирусов выделена подгруппа вирусов, ассоциированных с верруциформной эпидермодисплазией и актиническими кератомами: типы 5, 8, 9, 12, 14, 15, 17, 19–25, 36, 46 и 47. ВПЧ 5-го и 8-го типов индентифицированы как причина развития плоскоклеточной карциномы у больных верруциформной эпидермодисплазией [6, 7]. У пациентов, страдающих рецидивирующим респираторным папилломатозом, чаще обнаруживают ВПЧ 6-го и/или 11-го типа.
На сегодняшний день выделяют около 40 генитальных типов ВПЧ. Причиной генитальных бородавок (остроконечных кондилом) в 90% случаев являются 6-й и 11-й типы папилломавируса. Показано, что диспластические процессы шейки матки наиболее часто развиваются на фоне персистирующих генитальных инфекций, наибольшую роль из которых отводят ВПЧ [8, 9]. Типы 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58 и 59 могут быть причиной развития цервикальных интраэпителиальных неоплазий (CIN), вульварных интраэпителиальных неоплазий (VIN), рака гортани. Рак шейки матки — один из немногих видов злокачественных новообразований с установленной этиологией заболевания. За открытие роли ВПЧ в развитии рака шейки матки немецкий ученый Harald zur Hausen был удостоен в 2008 г. Нобелевской премии в области медицины и физиологии. Ежегодно в мире регистрируется около 0,5 млн новых случаев цервикального рака, и согласно прогнозу экспертов в отсутствие активного вмешательства к 2020 г. это число увеличится более чем на 700 000 случаев [10].
Длительный латентный период инфекции, развитие рака лишь у некоторых инфицированных ПВИ дают основание полагать, что помимо персистенции генома ВПЧ необходимым для развития рака условием являются нарушение структуры и функции клеточных генов. В качестве инициирующего фактора выступают мутации в различных участках гена Е1-Е2, который в норме отвечает за эписомальный статус ДНК ВПЧ. В результате повреждения Е1 происходит интеграция генома ВПЧ в хромосомы клетки хозяина. Поскольку Е1-Е2 регулируют и контролируют вирусную транскрипцию, их разрушение заканчивается неконтролируемой экспрессией генов Е6-Е7, которые непосредственно запускают процессы опухолевой трансформации. Онкогенные свойства продуктов Е6-Е7 обусловлены их способностью образовывать комплексы с белками р53 (для Е6) и рRb (для Е7). При изменении нормальных функций р53 клетка, которая должна была погибнуть, начинает бесконтрольно делиться, образуя опухолевидный рост. В патогенезе канцерогенеза имеет место супрессия местного иммунитета, обусловленная синтезом вирусного онкобелка Е7. Белок Е7 нейтрализует противовирусную и противоопухолевую активность интерферона альфа-2 за счет его способности избирательно блокировать большинство генов, индуцируемых интерфероном, сводя на нет все усилия интерферонотерапии. Также белок Е7 ингибирует экспрессию генов основного комплекса гистосовместимости, затрудняя распознавание опухолевых клеток иммунной системой хозяина. Биологические свойства и молекулярная структура ВПЧ-белков изучены достаточно полно, тем не менее, конкретные пути реализации канцерогенного эффекта вируса требуют дальнейшего уточнения. У пациентов, инфицированных наиболее агрессивными вариантами ВПЧ, а также имеющих генетические, гормональные, иммунные и другие кофакторы, ПВИ будет развиваться до предраковых состояний и может прогрессировать в рак.
Инкубационный период ПВИ колеблется от 1 до 12 месяцев (в среднем 3 месяца). Клинические проявления ПВИ гениталий могут быть различными: остроконечные кондиломы, папилломы с экзофитным ростом, плоские папилломы. Кондиломы представляют собой бородавчатые возвышения, которые могут быть единичными, но чаще множественными, слившимися в группы и напоминающими цветную капусту или петушиные гребни. Их поверхность покрыта многослойным плоским эпителием, нередко с ороговением. Особенно быстрый рост остроконечных кондилом наблюдается при беременности, у подростков и у ВИЧ-инфицированных индивидов (развитие гигантской опухоли Бушке–Левенштейна). Вполне естественно, что эпидемия ВПЧ-инфекции у взрослых не могла не отразиться на увеличении показателей заболеваемости аногенитальными бородавками среди детей. Данные современных методов показали, что папилломавирусные поражения у детей связаны с теми же типами ВПЧ, что и у взрослых, но в силу физиологических особенностей и незрелости защитных механизмов дети и подростки более уязвимы, чем взрослые.
Субклинические формы представлены интраэпителиальными папилломами с эндофитным ростом. Папилломы шейки матки обычно бывают плоскими или интраэпителиальными («атипичными»). Выявляются с помощью кольпоскопии, цитологического и гистологического исследований. Тяжесть течения и скорость регрессии определяется типом ВПЧ.
Однако аногенитальные бородавки образуют только вершину айсберга под названием «ВПЧ-инфекция». Большинство клинических случаев представлено пациентками с латентной формой ВПЧ-инфекции, у которых ВПЧ часто случайно диагностируется при проведении ПЦР-диагностики или онкоцитологическом исследовании соскоба из цервикального канала (признаки койлоцитической атипии).
Клиническая диагностика остроконечных кондилом и папиллом обычно не вызывает затруднений, если это не ранняя стадия заболевания, когда образования малых размеров, или не «атипичная» форма ПВИ. Но даже при не вызывающей сомнения клинике ВПЧ-инфекцию необходимо подтверждать лабораторно. Основным методом диагностики является цитологический. Обнаружение койлоцитов, трансэпителиальной лимфоцитарной инфильтрации и базально-клеточной гиперплазии в биоптате считается подтверждением ПВИ гениталий. Широко используется определение ДНК 12 типов ВПЧ высокого онкогенного риска методом полимеразной цепной реакции (ПЦР) в реальном времени (типы ВПЧ 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59) в соскобе цервикального канала, уретры или в моче. Внедряется в практику метод амплификации нуклеиновых кислот (МАНК). Серологическим методом диагностики является выявление антител против вирусоспецифичных протеинов Е2, Е6 и Е7, наличие которых является маркером текущей инфекции. Для этого используется ЕLISA — тест с высокоочищенными рекомбинантными протеинами Е6 и Е7. Снижение концентрации этих антител является показателем успешно проводимой терапии ПВИ и цервикальных неоплазий.
Установлено, что регрессия ВПЧ-обусловленных повреждений напрямую зависит от состояния Т-клеточного иммунитета и нейтрализующие антитела блокируют распространение вирусной инфекции. И хотя часто ВПЧ-обусловленные образования самостоятельно поддаются регрессии, у многих, особенно у лиц с иммунодефицитами, ПВИ приобретает персистирующий характер и способна к реинфекции. Резистентность ВПЧ к лечению связана с особенностью строения вируса, позволяющей длительно персистировать в организме, усугубляя уже имеющийся вторичный иммунодефицит. Сложный цикл внутриядерной репликации, возможность существования инфекции в эписомальной и интегрированной формах, трудности изучения патогенеза вируса на биологических моделях обуславливают отсутствие патогенетической терапии ПВИ на сегодняшний день [11].
В соответствии с руководством «Клинические рекомендации. Дерматовенерология» под ред. А. А. Кубановой (2010) и Европейским руководством по лечению ИППП терапия проявлений ВПЧ-инфекции должна удовлетворять следующим требованиям: деструкция, предупреждение развития осложнений, уменьшение числа рецидивов, улучшение качества жизни пациентов. Поскольку отсутствует метод элиминации ВПЧ, лечение направлено на устранение клинических признаков ВПЧ: любых разновидностей бородавок или патологии шейки матки при наличии атипичных клеток в мазках и биоптатах. Традиционные методы лечения бородавок общеизвестны и включают крио-, электро-, радиоволновую и лазерную хирургию, а также обработку цитотоксическими (подофиллин, подофиллотоксин, 5-фторурацил), химическими веществами (Солкодерм, Веррукацид, Дуофил и пр.), вызывающими цитолиз и некроз ткани [13]. В настоящее время наиболее эффективным, особенно при обширных высыпаниях и рецидивирующем течении заболевания, в том числе и в детской практике, является использование комбинированных методов терапии — сочетанное применение физических, химических или медикаментозных методов, которое включает местное лечение и применение различных системных неспецифических противовирусных (Лавомакс) и иммуномодулирующих препаратов (интерфероны и индукторы интерферонов) [12, 13]. Так, для лечения респираторного папилломатоза у детей используются криодеструкция, эндоларингеальный фонофорез цитостатиков, фотодинамическая терапия, интерферонотерапия (интерферон альфа-2) иммунокорригирующая терапия (мурамилпептид). Перспективным методом в лечении клинических манифестаций ВПЧ могло быть применение лечебных вакцин. Недостатком вакцинотерапии является ее узкое терапевтическое действие, тогда как около 40 штаммов ВПЧ паразитируют гениталии. Следовательно, с повестки дня не снимается необходимость лечебного метода, обладающего свойством элиминации вируса. Поэтому проводится поиск новых средств, включая индукторы интерферона для лечения генитальных кондилом и других клинических манифестаций ВПЧ.
Адекватная иммунотерапия способствует подавлению активности ВПЧ, снижая частоту рецидивов, и его элиминации. Среди других хорошо изученных препаратов, применяемых в комплексном лечении ПВИ, в клинической практике используются интерферон альфа-2, 5% Имиквимод, инозин пранобекс, индол-3-карбинол (Индинол, Промисан). Рекомендуется внутриочаговое введение интерферонов, особенно в случае иммунодефицита, или системное назначение в течение 4 недель. Клинические данные свидетельствуют об высокой эффективности сочетания лазерной терапии с локальным применением интерферонов или индукторов интерферона. Так, применение СО2-лазерного иссечения аногенитальных остроконечных кондилом у детей является безопасным, относительно атравматичным и эффективным методом лечения [15]. Для лечения беременных рекомендуют физические деструктивные методы: СО2-лазер, радионож, криотерапия.
ВПЧ — генетически стабильный ДНК-вирус, поэтому вероятность его генетической трансформации ничтожно мала. Генетическая стабильность означает, что инфекцию этим вирусом можно предупредить на длительный срок путем вакцинации. В 2006 г. Управление по контролю за продуктами питания и лекарственными средствами США (FDA) зарегистрировало первую в мире квадривалентную вакцину Гардасил, продемонстрировавшую эффективность в предупреждении инфекции ведущими типами ВПЧ (6/11/16/18). В дополнение к защите против четырех вакцинных типов Гардасил обеспечивает частичную перекрестную защиту против персистирующей инфекции и цервикальных поражений, вызванных десятью невакцинными типами ВПЧ высокого риска, включая ВПЧ 31, 33, 35, 45, 52 и 58, которые филогенетически родственны ВПЧ 16 и 18. В настоящее время квадривалентная вакцина зарегистрирована и применяется более чем в 130 странах мира. В 2008 г. зарегистрирована также двухвалентная вакцина Церварикс, содержащая два типа капсидных белков L1 ВПЧ — 16 и 18. В контексте профилактики наилучших результатов можно достичь сочетанием скрининговых программ обследования с повсеместной разумной организацией плановой добровольной вакцинации населения, особенно определенных медико-социальных контингентов (подростки из группы рискового поведения, сексуально-активные женщины, принимающие комбинированные оральные контрацептивы, лица с иммунодефицитом различного генеза).
Литература
Е. И. Касихина, кандидат медицинских наук, доцент
ГОУ ДПО РМАПО, Москва
Папилломавирусная инфекция: современная точка зрения на проблему
Опубликовано в журнале:
Практическая медицина ‘5 (37) октябрь 2009 г.
Е.В. Файзуллина
Казанский государственный медицинский университет
Генитальная папилломавирусная инфекция является распространенным заболеванием, передающимся половым путем. Вирус папилломы человека (ВПЧ) — высокоспецифичная в отношении человека инфекция, обладающая способностью инфицировать эпителиальные клетки, вызываемая вирусом из семейства Papovaviridea. Инфицирование ВПЧ половых органов, так же как и кожных покровов, происходит при наличии микротравм, при этом резервуаром ВПЧ-инфекции служат уретра, бартолиниевы железы, семенная жидкость. Идентифицировано более ста видов ВПЧ, из которых 35 инфицируют урогенитальный тракт человека, вызывая поражение покровного эпителия кожи и слизистых оболочек половых органов. ВПЧ-инфекция является наиболее распространенной инфекцией, передаваемой половым путем (ИППП), которой инфицирована большая часть сексуально активного населения. Кроме этого, папилломавирусы — единственная группа вирусов, для которых доказана индукция опухолей у человека. Число инфицированных в мире за последнее десятилетие увеличилось в 12 раз (Молочков В.А., 2004).
МКБ X пересмотра, раздел А 63. Аногенитальные бородавки.
Этиология
Вирус, относящийся к роду А семейства Papovaviridea, сохраняется при температуре 50?С в течение 30 минут. В процессе репликационного цикла геном вируса экспрессирует от 8 до 10 белковых продуктов; за онкогенные свойства вируса ответственны онкопротеины Е6 и Е7. По онкогенной активности различают ВПЧ низкой степени риска — HPV6, 11,42,43,44; средней – HPV31,33,35, 51,52, 58 и высокой — HPV16, 18,45,56 степени риска. Одним или более типами ВПЧ инфицировано не менее 50% взрослого населения, живущего активной половой жизнью, в большинстве случаев генитальная ВПЧ-инфекция у них является нераспознанной, протекающей субклинически или асимптомно. Генитальная ВПЧ-инфекция имеет высокую контагиозность; заражение при однократном половом контакте происходит примерно в 60% случаев.
Патогенез
Инвазия вируса происходит через микроповреждения тканей. ВПЧ инфицирует стволовые клетки базального слоя, которые затем являются постоянным источником инфицирования эпителиальных клеток. Вирусы инфицируют делящиеся незрелые клетки базально-клеточного слоя, находящиеся близко к поверхности, что во многом объясняет частоту инфицирования шейки матки и нижней трети влагалища и вульвы.
Однако по мнению В.А. Молочкова и соавт. (2004), инфицирование эпителиальных клеток ВПЧ является необходимым, но не достаточным событием для развития рака. Для формирования необратимой неоплазии необходимы следующие факторы: во-первых, активная экспрессия генов Е6 и Е7, причем высокоонкогенных типов ВПЧ-16 и 18; во-вторых, индукция метаболических механизмов конверсии эстрадиола в 16-ОН; в третьих, индукция множественных повреждений хромосомной ДНК в инфицированной клетке, которая завершает процесс перерождения.
Первая стадия неоплазии CIN I характеризуется активной репликацией вируса и его бессимптомным выделением. Опухолевая трансформация возникает с большей вероятностью при взаимодействии ВПЧ с другими инфекционными агентами (цитомегаловирусы, вирус простого герпеса 2 типа, С. trachomatis, микоплазма и уреаплазма).
Факторы риска
ВПЧ является необходимым, но не достаточным фактором цервикальной неоплазии. Предрасполагающими факторами риска для развития заболевания могут быть: неблагополучный социально-экономический статус и сексуальное поведение, нарушения клеточного и гуморального иммунитета, сопутствующие сексуально-трансмиссивные заболевания (гонорея, сифилис герпес, трихомониаз хламидиоз и т.д.), молодой возраст, курение, беременность, дисбиоз вагинального биотопа, гипо- и авитаминозы (Марченко Л.А., 2001).
Риск ВПЧ-инфекции наиболее высок у гомосексуалистов. Не исключены случаи перинатальной передачи инфекции младенцам, рожденным от инфицированных матерей во время родоразрешения через естественные родовые пути, за счет аспирации околоплодных вод, цервикального или вагинального секрета; случаи папилломатоза гортани, трахеи, бронхов у детей, рожденных с применением операции кесарева сечения, что, по мнению ряда авторов, свидетельствует о возможности трансплацентарной передачи инфекции и нецелесообразности применения кесарева сечения с единственной целью — предупреждения заражения новорожденного ВПЧ (Koutsky L.A., Kiviar N.B.,1999).
Течение заболевания и клинические разновидности
Инкубационный период при аногенитальных бородавках составляет от 1 до 3 месяцев. В большинстве случаев ВПЧ-инфекция не манифестирует сразу, оставаясь некоторое время асимптомной. Прогрессия ВПЧ-инфекции высокого онкогенного риска в цервикальную интраэпителиальную неоплазию и рак in situ обычно происходит в сроки от 5 до 30 лет.
1. Клинические формы (видимые невооруженным взглядом):
1.1. Экзофитные кондиломы (остроконечные типичные, паппилярные, папуловидные);
1.2. Вестибулярный паппиломатоз ( мелкие паппиломовидные образования преддверья влагалища).
2. Субклинические формы (не видимые невооруженным глазом и бессимптомные, выявляемые только при кольпоскопии и/ или цитологическом или гистологическом исследовании):
Плоские кондиломы (типичная структура с множеством койлоцитов);
Малые формы (различные поражения метапластического эпителия с единичными койлоцитами);
Кондиломатозный цервицит/вагинит.
3. Латентные формы (отсутствие клинических, морфологических или гистологических изменений при обнаружении ДНК ВПЧ);
Клинические проявления ВПЧ-инфекции могут быть следующими: остроконечные кондиломы, фиброэпителиальные образования на поверхности кожи и слизистых на тонкой ножке, на широком основании в виде одиночных узелков, либо в форме множественных выростов по типу «цветной капусты».
Манифестация генитальной ВПЧ-инфекции сопровождается появлением генитальных бородавок. Экзофитные формы остроконечных кондилом представляют из себя типичное проявление инфекции, обусловленной доброкачественными типами вируса ВПЧ6 и ВПЧ11. Эндофитные кондиломы могут быть плоскими и инвертированными, располагаются на шейке матки и имеют вид плоских или слегка возвышающихся бляшек, определяются при расширенной кольпоскопии.
Субклиническая форма болезни обнаруживается только при кольпоскопии в виде мелких плоских бородавок или устанавливается на основании характерной гистологической картины в виде койлоцитоза. Отсутствие клинических и гистологических признаков инфекции при выявлении ДНК ВПЧ свидетельствует о латентной или асимптомной инфекции.
Наружное отверстие уретры у женщин поражается в 4-8% случаев, более глубокое поражение мочеиспускательного канала вызывает явления вялотекущего уретрита.
Генитальные бородавки, как правило, бессимптомны, и часто случайно выявляются при осмотре или на основании Pap-мазка. В связи с этим вначале больные не предъявляют жалоб на связанный с ними дискомфорт. Однако, крупные, травмированные, изъязвленные или подвергшиеся вторичной инфекции бородавки сопровождаются зудом, болью, неприятным запахом. Уретральные бородавки у мужчин могут вызывать раздвоение струи мочи, обструкцию уретрального отверстия.
У больных с нарушением клеточного иммунитета (ВИЧ-инфекция, иммуносупрессивная терапия, беременность), — развиваются очень крупные генитальные бородавки — гигантская кондилома Бушке-Левенштейна, инвазивная и деструирующая опухоль, ассоциирующаяся с ВПЧ 6 и 1 1 типа.
Диагностика папилломавирусной инфекции
Лабораторная диагностика ВПЧ-инфекции проводится на основании цитологического, гистологического исследования биоптатов, определения антител к ВПЧ, обнаружения ДНК ВПЧ и онкобелка Е7.
Клинический осмотр наружных половых органов, вульвы, влагалища следует проводить при хорошем освещении. Для выявления субклинической генитальной ВПЧ-инфекции проводится расширенная кольпоскопия. Ложноположительные результаты при этом методе обычно являются следствием воспалительных и дискератических процессов вульвы и влагалища.
Кольпоскопия и биопсия показаны всем женщинам с цервикальной интраэпителиальной неоплазией класса II (CIN II) или класса III (CINIII), независимо от подтверждения у них наличия ВПЧ-инфекции.
Наиболее простые методы для идентификации ВПЧ — иммунологические методы: РСК, ИФА, ПИФ.
Диагностика ВПЧ-инфекции шейки матки включает тестирование по Папониколау (РАР-тест). Молекулярно-биологические методы реакция гибридизации in situ, ПЦР, ДНК-зонд. Гистологическое исследование биоптатов тканей эпителия и эпидермиса используются и при малосимптомных или асимптомных формах вирусных заболеваний гениталий. Использование молекулярно-биологических методов исследования целесообразно для доказательства наличия ВПЧ с его типированием, так как и ДНК-гибридизация, и полимеразная цепная реакция позволяют выявить онкогенные типы вируса 16 и 18.
Основным методом диагностики ВПЧ является цитологический — обнаружение койлоцитарных клеток в биоптате эпителия шейки матки (клетки МПЭ промежуточного и поверхностного типа с многоядерным строением), патогномоничные для ВПЧ.
При гистологическом исследовании генитальных бородавок обнаруживается умеренное утолщение рогового слоя с папилломатозом, паракератозом и акантозом; могут присутствовать фигуры митоза. Диагностически важным считается наличие в глубоких участках мальпигиева слоя койлоцитов — больших эпителиальных клеток с круглыми гиперхромными ядрами и выраженной перинуклеарной вакуолизацией.
Лечение
При выборе метода лечения ВПЧ-инфекции учитывается анамнез, соматический статус, предшествующая противовирусная терапия, локализация, количество, размеры остроконечных и плоских кондилом. Тактика лечения должна быть индивидуальной с учетом переносимости тех или иных методов лечения. Местное лечение АБ направлено на удаление кондилом и атипически измененного эпителия, с применением различных видов химических коагулянтов, цитостатиков и физиохирургических методов лечения. После удаления папилломатозных разрастаний для профилактики рецидива АБ необходима местная и общая терапия противовирусными препаратами, индукторами интерферона, неспецифическими иммуномодуляторами. Больных с папилломавирусной инфекцией следует предупредить, что данное заболевание является сексуально трансмиссивным, поэтому обследование и лечение необходимо проводить обоим партнерам, а на период терапии и ближайшие 6-9 месяцев рекомендовать барьерные методы контрацепции.
Местное лечение ВПЧ (данные приведены по Подзолковой Н.М. с соавт, 2007).
В течение трех лет (2006-2008 гг.) нами были обследованы и пролечены 650 женщин с аногенитальными бородавками (АБ). Данные представлены в таблице 1.
Таблица 1.
Группы пациенток по локализации и распространенности АБ
| Группа | Локализация ОК | Количество пациенток | % |
|---|---|---|---|
| 1. | Влагалище | 17 | 2,6 |
| 2. | Вульва | 173 | 23,6 |
| 3. | Влагалище + вульва | 258 | 39,7 |
| 4. | Влагалище + большие половые губы | 126 | 19,4 |
| 5. | Влагалище + вульва + большие половые губы | 76 | 11,7 |
| Всего | 650 | 100 | |
Таблица 2.
Число сеансов радиоволновой деструкции АБ, требующихся для достижения стойкой ремиссии заболевания у женщин
| Группа | 1 сеанс | 2 сеанс (10-12 дней) | 3 сеанс (14-21 день) | Более 3 сеансов | Всего | |||||
|---|---|---|---|---|---|---|---|---|---|---|
| Чел. | % | Чел. | % | Чел. | % | Чел. | % | Чел. | % | |
| 1 | 7 | 41,2 | 10 | 58,82352941 | 0 | 0 | 0 | 0 | 17 | 100 |
| 2 | 121 | 69,9 | 41 | 23,69942197 | 11 | 6,4 | 0 | 0 | 173 | 100 |
| 3 | 118 | 45,7 | 112 | 43,41085271 | 25 | 9,7 | 3 | 1,2 | 258 | 100 |
| 4 | 13 | 10,3 | 77 | 61,11111111 | 29 | 23,0 | 7 | 5,6 | 126 | 100 |
| 5 | 0 | 0,0 | 23 | 30,26315789 | 41 | 53,9 | 12 | 15,8 | 76 | 100 |
| Итого: | 650 | |||||||||
Пациенткам применялся деструктивный метод удаления с помощью радиоволнового излучателя фирмы «Сургитрон» (США), с последующим противовирусным лечением препаратом «Панавир» в виде пяти внутривенных инъекций 0,04 мг/мл раствора по схеме введения на первый, третий, пятый, восьмой и одиннадцатый дни лечения. Препарат вводился медленно струйно. Места удаления обрабатывались гелем «Панавир» ежедневно 3 раза в день до полного заживления мест деструкции.
Наибольшему число женщин первой (58,8%) и четвертой (61,1%) клинических групп, для достижения стойкого клинического эффекта потребовалось два сеанса деструкции. Чем более распространенным был патологический процесс (чем больше порядок и номер групп), тем большее число сеансов радиоволновой деструкции требовалось для достижения стойкого клинического результата. При этом лечение препаратом «Панавир» было эффективным в 86,5% случаев у пациентов всех пяти клинических групп.
Полученный клинический эффект во многом объясним высоким противовирусным эффектом препарата. Активной субстанцией «Панавира» является растительный полисахарид, полученный из растения Solanum tuberosum и относящийся к классу высокомолекулярных гексозных гликозидов сложного строения: глюкоза (38,5%), галактоза (14,5%), рамноза (9%), манноза (2,5%), ксилоза (1,5%), уроновые кислоты (3,5%)
«Панавир» обладает цитопротективным действием, защищая клетки от воздействия вирусов, поскольку способен тормозить их репликацию в инфицированных культурах клеток, что приводит к существенному снижению инфекционной активности вирусов.
«Панавир» индуцирует синтез интерферона в организме, повышает жизнеспособность инфицированных клеток. Механизм действия препарата основан на препятствии адгезии вируса в клетку посредством ингибирования пенетрации и препятствию раскрытия вирусного капсида. На следующем этапе препарат действует на транскрипцию ДНК вируса с последующим нарушением репликации вирусной ДНК и нарушением синтеза капсидных белков, что приводит к нарушению сборки вирусных частиц и окончательной гибели вирусной клетки.
Считаем целесообразным применение препарата «Панавир» в комплексном лечении АБ различных локализаций.
Вирус папилломы человека
Вирус папилломы человека — это самая распространенная причина рака шейки матки у женщин. При этом ВПЧ нельзя вылечить. Единственным эффективным способом защиты от инфекции остается вакцинация.
Что такое ВПЧ?
Вирус папилломы человека (ВПЧ) известен тем, что из-за него на коже и слизистых оболочках могут появиться плоские и остроконечные бородавки. В медицине такие новообразования называют соответственно папилломами и кондиломами. Но самое опасное в ВПЧ это то, что он является частой причиной рака шейки матки.
Как передается ВПЧ?
«Заражение ВПЧ происходит через контакт слизистых и кожи. Основной путь заражения – половой, но он осуществляется через контакт поверхностей кожи и слизистой с носителем ВПЧ, а не через сперму и другие биологические жидкости. Именно поэтому презервативы не предотвращают заражение ВПЧ. Заразиться ВПЧ в общественных туалетах, раздевалках фитнес-клубов, саунах практически невозможно».
ВПЧ очень распространен, около 14 миллионов человек заражаются им ежегодно. В течение жизни им заболевает практически каждый (80% людей к 50 годам жизни) сексуально активный непривитый человек, но узнают о болезни очень немногие. Даже если вы сдавали тесты на ВПЧ и все они были отрицательными, остается вероятность, что вы заразились и избавились от вируса между тестами самостоятельно (обычно это происходит в возрасте до 30 лет.
Можно ли заразиться ВПЧ повторно?
К сожалению, да. После встречи с вирусом не развивается стойкого иммунитета, и заражение от новых половых партнеров вполне вероятно. Кроме того, если былозаражение одним типом вируса, у не вырабатывается иммунитет против других типов.
Виды ВПЧ
Видов ВПЧ очень много, больше 200. Обычно их разделяют в зависимости от их способности вызывать рак. Все разновидности вируса условно делятся на три группы:
Если произошло заражение одним из «опасных» вирусов, это вовсе не значит, что обязательно будет рак. Чаще всего наша иммунная система побеждает ВПЧ в среднем за 1-2 года. Даже если ВПЧ сохраняется в организме, предраковое состояние или рак могут так никогда и не возникнуть.
Следует понимать, что разные виды ВПЧ поражают разные участки тела. Далеко не все из них связаны с гинекологией. Например, «кожные» вирусы (типы 1, 2, 3, 4 и 10) вызывают обычные или плоские бородавки. Кроме того, не все вирусы, затрагивающие кожу и слизистые гениталий (полового члена, мошонки, области промежности или анального отверстия, влагалища, вульвы или слизистой оболочки шейки матки), способны провоцировать рак. Так, ВПЧ 6-го и 11-го типов в 90% наблюдений ответственны за возникновение генитальных кондилом, но рак шейки матки они не вызывают.
Как защититься от ВПЧ?
«От ВПЧ защитит только вакцинация. Вакцина, особенно девятивалентная, защищает от наиболее опасных типов ВПЧ, но не от всех известных. Девочек и мальчиков нужно прививать с 9 лет».
Стадии развития болезни
Если обнаружен ВПЧ, не стоит паниковать! Он может исчезнуть к следующему обследованию. Наличие вируса не означает болезнь. Если же ВПЧ сохраняется в организме, приходите на обследования регулярно, хотя бы раз в год. Вирус может представлять угрозу, только если не контролировать его последствия. Дисплазию нужно вовремя лечить, тогда рак не разовьется.
Такое развитие болезни встречается редко (инфекция приводит к трансформации клеток менее, чем у 1% зараженных), но представляет реальную опасность.
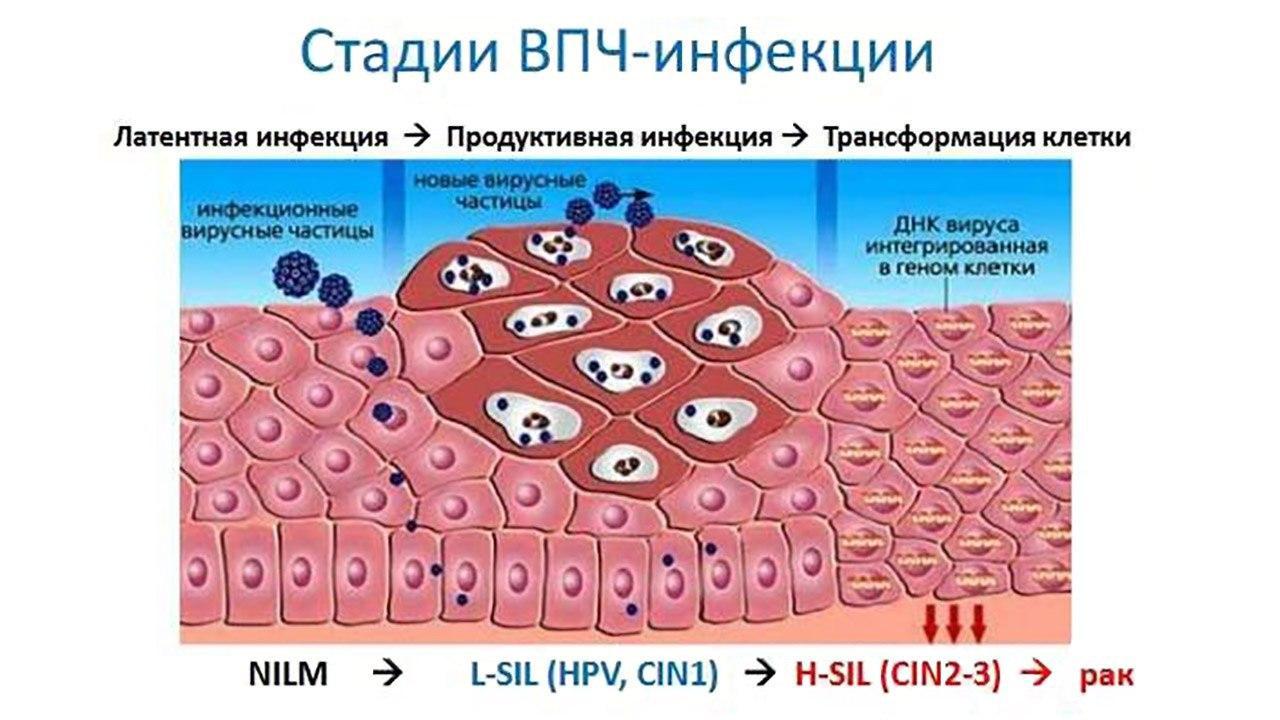
Продолжительность развития болезни в этом случае индивидуальна. У некоторых пациентов начальный этап может длиться годами, так и не приводя к онкологии. Вероятность развития онкологического процесса повышается с возрастом. От заражения до появления дисплазии (предракового состояния) и рака шейки матки в среднем проходит 10–20 лет (рис. 2).
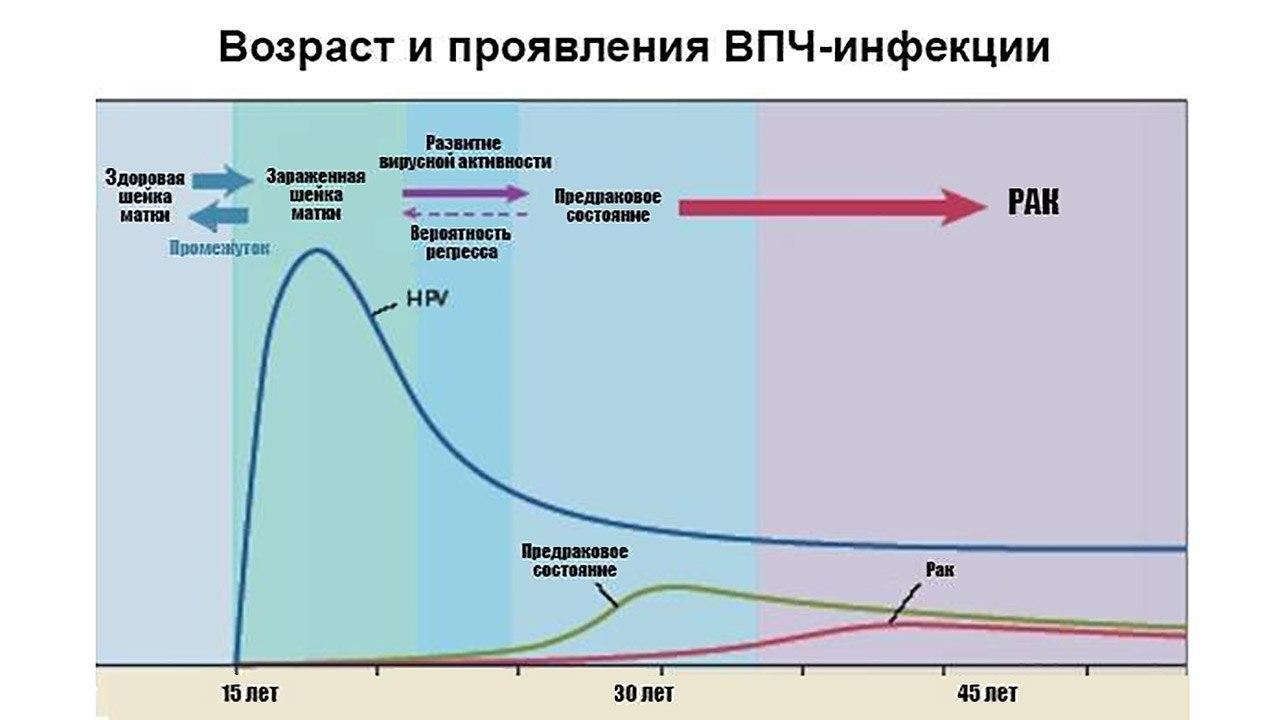
Симптомы
Кондиломы: лечить или удалять?
«Если кондиломы беспокоят косметически, кровят или задеваются одеждой, их нужно лечить. В остальных случаях можно не трогать».
Диагностика
От своевременного выявления ВПЧ высокого онкогенного риска во многом зависит эффективность лечения и предотвращения развития рака. Считается, что диагностику ВПЧ следует регулярно проходить всем женщинам после 30 лет.
К какому врачу обратиться
Если вы женщина, и у вас нет никаких симптомов или жалоб, вам все равно нужно ходить к гинекологу 1 раз в год. Врач может назначить вам анализ на ВПЧ в рамках общей проверки здоровья.
Обратиться к врачу следует также в случае обнаружения на теле подозрительных новообразований. Выбор специалиста будет зависеть от расположения бородавок или новых родинок. Если вас беспокоит область половых органов и заднего прохода, целесообразно записаться на прием к венерологу, урологу или гинекологу. В противном случае вам поможет дерматолог.
Нужно ли мужчинам проверяться на ВПЧ?
«Мужчинам проверяться не нужно – положительный тест ничего не меняет. ВПЧ все равно не лечится, а презервативы не предотвращают передачу вируса партнеру. Мужчинам до 45 лет рекомендовано вакцинироваться – чем раньше, тем лучше».
Какие анализы сдать
В рамках скрининга женского здоровья в России обычно делают ПАП-тест и одновременно с ним после достижения 30-летнего возраста сдают анализ на наличие/отсутствие ВПЧ высокого онкогенного риска (котестинг).
ПАП-тест (мазок Папаниколау) хорошо знаком большинству женщин. Он берется из канала шейки матки, а также ее внешней поверхности и со сводов влагалища. Это цитологическое исследование позволяет увидеть малейшие изменения в клетках. Чтобы сделать его еще более информативным, прибегают к анализу на ВПЧ.
Когда есть выбор между «обычной» и «жидкостной» цитологией, следует выбрать «жидкостную». Этот метод позволяет очистить образец и сохранить большее число клеток для исследования.
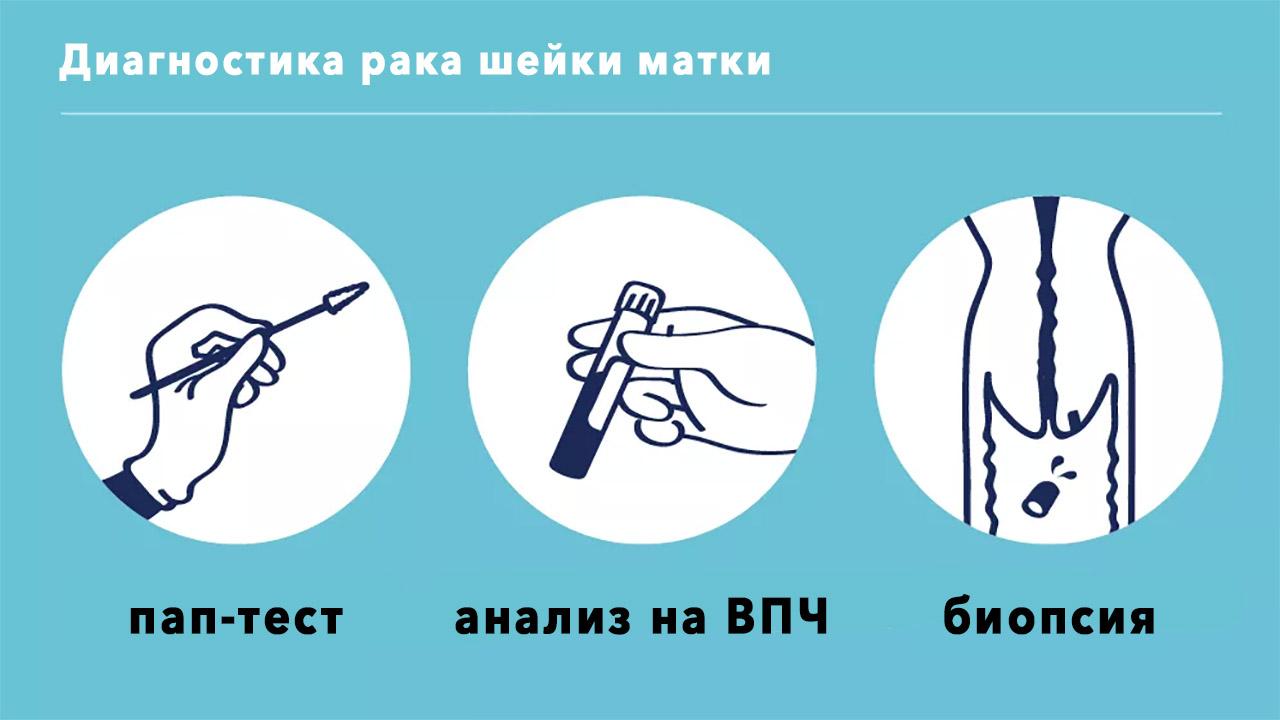
Лечение начинают только в случае диагностирования дисплазии шейки матки по результатам ПАП-теста и биопсии.
Нужно ли искать ВПЧ, если у меня появились генитальные кондиломы
Если вы обнаружили у себя кондиломы, обследование вам не нужно. Появление бородавок само по себе говорит о заражении вирусом. Анализ из шейки матки или влагалища будет лишним, но в случае необходимости, можно взять анализ из самих кондилом.
ВПЧ и беременность
Женщинам, планирующим беременность, специалисты рекомендуют провести комплексное обследование в целях обнаружения ВПЧ-инфекции. При беременности у больной ВПЧ женщины могут появиться генитальные бородавки или аномальные клеточные изменения шейки матки. Их можно обнаружить с помощью обычного скрининга.
Вакцина не рекомендуется беременным женщинам. Исследования показывают, что она не вызывает проблем у детей, рожденных женщинами, которые были вакцинированы во время беременности, но все же необходимы дополнительные исследования. Будущая мама не должна получать какие-либо дозы вакцины против ВПЧ до завершения беременности.
Риск передачи ВПЧ ребенку во время родов очень низок. Даже если младенцы заражаются вирусом папилломы человека, их организм обычно избавляется от вируса самостоятельно.
Лечение
Эффективного лечения ВПЧ не существует, лечить можно только проявления болезни. Женщины, у которых обнаружен вирус папилломы человека, должны просто наблюдать за инфекцией. В этом случае следует раз в год сдавать ПАП-тест (цитологический мазок). Он поможет исключить развитие рака шейки матки.
Кондиломы: удалять или нет?
Хирургическое вмешательство обычно рекомендуют, если кондиломы значительно разрослись, причиняют дискомфорт, находятся во влагалище, уретре или вокруг заднего прохода и не поддаются другим видам лечения. Кондиломы следует удалить, если у врача есть повод считать, что они могут спровоцировать рак (например, они сочетаются с предраковым состоянием кожи).
Кондиломы бесполезно удалять с целью защиты от вируса своего полового партнера, так как вирус при этом может сохраняться в организме. Избавление от бородавок также не снижает риск развития рака в будущем. После удаления кондилом всегда есть вероятность, что они возникнут снова.
Чем НЕ лечат ВПЧ: иммуномодуляторы и противовирусные препараты
Положительный анализ на ВПЧ часто становится поводом принимать различные лекарства, несмотря на то, что эта инфекция не лечится. Против ВПЧ вам не помогут:
Вылечить ВПЧ нельзя, можно лишь защититься от него путем вакцинации.
Прогноз
Осложнения
Осложнения из-за вируса папилломы человека могут представлять угрозу, однако их можно избежать, если регулярно обследовать организм на предмет новообразований.
Кондиломы
Малое количество кондилом может не причинять человеку дискомфорта, однако их разрастание в некоторых случаях значительно влияет на качество жизни: сексуальную активность, психологическое состояние. Кроме того, кондиломы могут:
Рак шейки матки
Часто с ВПЧ связывают проблемы, причиной которых он не является:
Профилактика заболевания
Учитывая, что ВПЧ не лечится, нельзя недооценивать важность профилактики заражения.
Как не заразиться
В первую очередь необходимо повышать уровень защитных сил организма. Если есть вредные привычки, лучше от них отказаться или хотя бы существенно уменьшить употребление алкоголя и табака. Продукты распада табачных смол попадают во влагалищную слизь, ослабляя местные защитные свойства влагалища, делая шейку более уязвимой для ВПЧ.
Важным моментом профилактики вируса папилломы человека является разборчивость в выборе сексуальных партнеров. В моногамных отношениях риск инфицирования ВПЧ гораздо ниже, чем в полигамных. Определенную роль в профилактике играет и половое воспитание детей, но более важную – осведомленность родителей о возможностях вакцинопрофилактики.
Вакцинация
Мальчикам вакцинация тоже нужна. Она не только способствует снижению распространения инфекции, но и защищает от генитальных бородавок.
Вакцины против ВПЧ защищают сразу от нескольких типов вируса:
Вакцины против ВПЧ отличаются высокой степенью безопасности, они не содержат живых вирусов. Среди нежелательных эффектов после вакцинации: покраснение в месте инъекции, головная боль, головокружение, тошнота. Вакцины ВПЧ никак не влияют на возможность иметь детей и не вызывают бесплодия.
Заключение
Инфекция, вызываемая вирусом папилломы человека, очень часто никак не проявляет себя и до конца жизни может остаться незамеченной. Многие пациенты узнают о заражении только в случае появления на коже или слизистых характерных бородавок. Главная опасность ВПЧ – риск развития рака, которому женщины подвержены больше, чем мужчины. Регулярное обследование на наличие вируса в организме рекомендовано всем женщинам старше 25 лет наряду с ПАП-тестом.
Иммунотерапия генитальной папилломавирусной инфекции
Генитальная папилломавирусная инфекция (ПВИ) является одной из самых частых инфекций, передаваемых половым путем (ИППП). Только в США ею поражено около 20 млн и ежегодно заражается 5,5 млн человек. Чрезвычайная опасность и важная социальная значимость это
Генитальная папилломавирусная инфекция (ПВИ) является одной из самых частых инфекций, передаваемых половым путем (ИППП). Только в США ею поражено около 20 млн и ежегодно заражается 5,5 млн человек [16]. Чрезвычайная опасность и важная социальная значимость этой инфекции обусловлена ее этиологической ролью в развитии практически всех случаев рака шейки матки, около 50% других раков аногенитальной области, а также целого ряда разновидностей злокачественных новообразований верхних дыхательных путей и кожи [18, 23].
В России, где официально регистрируются лишь случаи аногенитальных (венерических) бородавок, интенсивный показатель заболеваемости ими, составивший в 2004–2005 гг. 32,9–32,1 случая на 100 тысяч населения, свидетельствует об эпидемическом характере распространенности этой категории ПВИ [5]. В то же время, даже с учетом 10-кратного роста регистрируемой за последние 10 лет заболеваемости ПВИ [7], эти цифры не отражают масштабов ее истинной распространенности. Во многом это связано со сложностью диагностики субклинических и латентных форм инфекции.
При половом заражении вирус папилломы человека (ВПЧ) чаще всего приводит к развитию аногенитальных бородавок, классической формой которых являются остроконечные кондиломы — доброкачественные мягкие папилломатозные разрастания, расположенные, как правило, в аногенитальной области и обычно обусловленные ВПЧ 6 и 11 и реже другими, в том числе высокоонкогенными, типами ВПЧ. В целом же не менее 35 типов ВПЧ (16, 18 и др.) вызывают дисплазию и рак половых органов (шейки матки, вульвы, влагалища, полового члена), гортани и заднего прохода [3].
Пик частоты ВПЧ-инфекции гениталий приходится на 18–25 лет — возраст наивысшей половой активности. После 30 лет ее распространенность снижается, но существенно возрастает частота дисплазий и рака шейки матки, причем пик частоты последнего приходится на 45 лет.
К числу важных в эпидемиологическом и клиническом отношении особенностей ПВИ-инфекции, наряду с ее нередким субклиническим течением, относится длительность инкубационного периода (от нескольких месяцев до нескольких лет), что также существенно затрудняет ее диагностику и лечение [11].
ВПЧ относятся к подгруппе А семейства паповавирусов (Papovaviridae). Вирионы не имеют оболочки, диаметр их равен 50–55 нм. Геном представлен двуспиральной кольцевидно скрученной ДНК, включает около 8000 основных пар и кодирует всего 8 открытых рамок считывания. В процессе репликационного цикла геном вируса экспрессирует от 8 до 10 белковых продуктов. Ранние белки (early), контролирующие репликацию вируса, транскрипцию и клеточную трансформацию, кодируются онкопротеинами Е6 и Е7. Поздние белки (late) L1 и L2 кодируют структурные белки вириона. Белок L1 формирует капсомеры. Белки Е1 и Е2 регулируют репликацию вирусной ДНК и экспрессию генов. Онкогены Е6 и Е7 всегда выявляются в опухолевых клетках, зараженных ВПЧ, в то время как другие фрагменты вирусного генома могут быть утеряны в процессе его длительной персистенции.
В инфицированных эпителиальных клетках на начальных стадиях вирусный генетический материал персистирует в эписомальной форме, при этом клетка способна продуцировать вирусные частицы. На более поздних стадиях геном вируса интегрирует в клеточный геном, и способность к репродукции вируса утрачивается. Интеграция вирусной ДНК в клеточную может индуцировать несколько важных событий. Во-первых, она часто сопровождается потерей вирусного материала, при этом обязательно обеспечивается сохранение генов Е6 и Е7; во-вторых, независимо от делеций вирусный геном в интегрированной форме не способен к полной репликации; в-третьих, индуцируется нестабильность клеточного генома. Так, показано, что в канцерогенез шейки матки вовлечены определенные участки хромосом, что указывает на множественность генетических нарушений в опухолевой клетке. При интеграции вирусного генома в клеточный не только сохраняется транскрипция вирусных генов, прежде всего Е6 и Е7, но и активируется транскрипция некоторых клеточных генов.
Обнаружениe существенных различий в спектре синтезируемых этой опухолью РНК указывает на разнообразие генетических механизмов, вовлеченных в процесс канцерогенеза, обусловленного ВПЧ. В частности, белки Е6 и Е7 могут инактивировать белки-супрессоры опухолевого роста р53 и рRb105 соответственно. Кроме того, указанные онкобелки влияют на некоторые белки-циклины и циклин-зависимые киназы, являющиеся регуляторами цикла деления клетки [15, 22].
В настоящее время доказано, что ВПЧ является онкогенным вирусом, связанным не только с цервикальными и аногенитальными раками, но и с плоскоклеточным раком гортани, предстательной железы, кожи [1] и др. (особенно на фоне иммуносупрессии).
Чаще всего в ткани генитальных опухолей обнаруживаются ВПЧ 6, 11, 16, 18, 31, 33, 35, 41, 42, причем у одного больного может быть несколько типов ВПЧ одновременно. ВПЧ инфицирует пролиферирующие эпителиальные клетки базального слоя эпителия через механические, бактериальные и другие микроповреждения.
Репликация ДНК ВПЧ происходит только в клетках базального слоя, поэтому методы лечения, направленные на удаление поверхностного слоя эпидермиса, неэффективны и сопровождаются рецидивом заболевания. Инфицированные клетки базального слоя служат постоянным источником инфицирования эпителиальных клеток, проходящих затем последовательные стадии дифференцировки с персистирующим, репликативно неактивным вирусом.
После инфицирования ВПЧ в клетках эпидермиса нарушается нормальный процесс дифференцировки, особенно это касается клеток шиповатого слоя, в котором наблюдается клональная экспансия инфицированных ВПЧ клеток базального слоя, прошедших только первичную стадию дифференцировки. Эта клональная экспансия связана с их трансформацией и последующей иммортализацией. Трансформация и иммортализация клеток эпидермиса контролируется генами ВПЧ, кодирующими ранние (early) белки Е6 и Е7. При этом наблюдается деформация внутренних слоев эпидермиса и утолщение кожи, а клетки шиповатого слоя при переходе в зернистый оказываются наиболее активными в синтезе ДНК. Эта фаза жизненного цикла ПВИ включает второй этап репликативной дессиминации вируса внутри эпидермиса, в результате чего значительно поражается зернистый слой эпидермиса, при отсутствии экспрессии поздних (late) генов L1 и L2. Последняя, как показано, наступает на конечной стадии дифференцировки в ороговевающем слое, где и наблюдается активная сборка зрелых вирусных частиц, их выделение из клетки и почкование прямо на поверхности кожи. Именно эти участки кожи инфекционно опасны в отношении контактного заражения.
Иммунный ответ хозяина играет важную роль в предотвращении клинической манифестации ВПЧ-инфекции. ВПЧ вызывает как гуморальный, так и клеточный типы иммунного ответа. Клеточный иммунитет, особенно Т-клеточная иммунная система, играет основную роль как в персистенции очагов ПВИ, так и в их спонтанном регрессе, который имеет место в 90% случаев и может наступить через 6–8 месяцев после начала заболевания.
Роль иммунных нарушений в патогенезе ВПЧ-инфекции подтверждается данными о более высокой частоте ВПЧ-ассоциированных заболеваний у реципиентов трансплантата внутренних органов [12] и ВИЧ-инфицированных [20], обнаружении нарушения Т-клеточного иммунитета у больных с генитальными бородавками, снижении количества клеток Лангерганса в очагах цервикальной интраэпителиальной неоплазии, а также большим количеством CD4 + и CD8 + Т-лимфоцитов в инфильтрате регрессирующих генитальных бородавок [21], предотвращении ВПЧ-инфицирования экспериментальных животных и развития у них опухолевого процесса после иммунизации неструктурными белками ВПЧ (Е6 и Е7) [14].
Важная роль клеточного звена иммунитета в патогенезе ВПЧ-инфекции также подтверждается данными о полной ремиссии ВПЧ-ассоциированных заболеваний после специфической стимуляции Т-клеточного иммунного ответа на гиперэкспрессию онкобелков Е6 и Е7 (гиперэкспрессия онкобелков Е6 и Е7 на клеточной поверхности возникает при интеграции ВПЧ в геном клетки) [8, 19].
В этой связи важно отметить, что онкобелки Е6 и Е7 довольно иммуногенны, хорошо распознаются Т-лимфоцитами и проявляют свой эффект через формирование комплексов со специфическими белками — р53 и Rb, которые обычно выполняют в клетке противоопухолевую функцию. У вирусов с высоким онкогенным потенциалом комплексы Е6-р53 и Е7-Rb более стабильны, а инфицированные вирусом клетки неотвратимо становятся раковыми.
Клинически выделяют 4 типа генитальных бородавок.
Без лечения генитальные бородавки могут спонтанно инволюцировать (в 90% случаев), длительно персистировать или увеличиваться в размере и количестве, трансформируясь в рак (10%). Рак in situ без лечения переходит в инвазивный рак в 36% случаях за 3,8–5,7 года [18]. С меньшей частотой спонтанной инволюции подвергаются более длительно существующие очаги поражений. Отсутствие спонтанной инволюции генитальных бородавок также может быть связано с повторным инфицированием новыми типами ВПЧ. Реинфекция же одним и тем же типом ВПЧ встречается не часто, возможно благодаря приобретенному иммунитету.
Прогноз генитальных бородавок зависит от типа обусловливающих их ВПЧ, сопутствующих заболеваний (включая ИППП). Если ВПЧ 16 обычно приводит к развитию плоскоклеточного рака, то ВПЧ 18 — к развитию аденокарценомы шейки матки — формы рака с очень плохим прогнозом. Плохим прогностическим фактором является и молодой возраст пациентки [10].
Для выявления ВПЧ-инфекции чаще всего применяются молекулярно-генетические методы: неамплификационные (дот-блот, саузерн-блот гибридизация, гибридизация in situ на фильтре и ткани) и амплификационные (ПЦР и HC-анализ (Hybrid Capture)). При сравнении эффективности методов цервикальной цитологии и ПЦР в обнаружении ВПЧ-инфекции установлено, что ПЦР-метод является более чувствительным, чем цитологический.
В то же время ценность ВПЧ-типирования в клинической практике все еще не совсем ясна. Во всяком случае, положительные результаты не являются определяющими в предсказании исхода этой инфекции. Это связано как с возможностью технических ошибок при выявлении ВПЧ высокого риска, так и с необходимостью тщательного наблюдения за лицами с обнаруженными у них ВПЧ среднего и высокого риска, поскольку клинические и гистологические признаки ВПЧ-инфекции развиваются через 1–8 месяцев после первоначальной экспозиции вируса и даже нелеченные элементы могут регрессировать спонтанно, длительно существовать как доброкачественные или прогрессировать в предраковые поражения и рак.
Для использования в скрининге и мониторинге терапии тестирования на ДНК ВПЧ и для уверенности в надежности результатов используемый тест должен отвечать ряду требований. Это выявление широкого спектра генотипов ВПЧ высокого онкогенного риска (не менее 10 высокораспространенных) и невыявление низкоонкогенных типов ВПЧ, снижающих специфичность исследования. Кроме того, важной задачей ВПЧ-теста является возможность определения вирусной нагрузки. При этом выявление вируса в количестве, не превышающем порогового, имеет малое клиническое значение, так как говорит о высокой вероятности спонтанного излечения. При этом как положительные должны учитываться только случаи вирусной нагрузки, превышающей порог. В то же время при послеоперационном мониторинге введение порога неоправданно, поскольку выявление вируса даже с низкой нагрузкой может быть маркером рецидива [9].
Несмотря на то, что генитальные бородавки редко персистируют, а тем более увеличиваются в размере и количестве и обычно регрессируют спонтанно, выраженный онкогенный потенциал целого ряда типов ВПЧ, особенно в условиях иммуносупрессии, ставит проблему лечения генитальных бородавок в разряд весьма актуальных проблем современной медицины.
Исходя из биологических особенностей ПВИ, помимо удаления генитальных бородавок большое внимание должно быть уделено лечению субклинической и латентно протекающих ВПЧ-инфекций. Кроме того, решающее значение для предотвращения рецидива и приостановления процесса канцерогенеза имеет элиминация ВПЧ.
В настоящее время эффективность различных методов лечения генитальных бородавок, даже с учетом проведения повторных курсов, составляет 60–80% [13]. Рецидивы в 25–50% случаев наступают в течение первых трех месяцев после лечения и чаще всего обусловлены реактивацией вируса.
Поскольку в большинстве случаев больные с генитальными бородавками страдают и другими ИППП, их половые партнеры должны быть также соответствующим образом обследованы, в том числе на ВПЧ и ВИЧ-инфекции. Лечение генитальных бородавок, как и других ИППП, следует проводить обоим половым партнерам, причем в период его проведения им следует воздерживаться от половой жизни. После окончания лечения необходима барьерная контрацепция в сроки до 6 месяцев.
При разработке стратегии лечения важно учитывать возраст больного, локализацию, количество элементов, площадь очагов поражения, частоту рецидивов, наличие сопутствующей соматической патологии (в том числе урогенитальных инфекций), переносимость метода лечения, а также клинический опыт врача.
Наиболее часто применяются следующие методы лечения остроконечных кондилом.
1. Физические методы:
2. Химическая цитодеструкция:
3. Антивирусная и иммуномодулирующая химиотерапия:
4. Фотодинамическая терапия:
В большинстве случаев бывает достаточно криодеструкции, электрокоагуляции, лечения лучами лазера или фотодинамической терапии (ФДТ).
При распространенном, рецидивном процессе более эффективна комбинация местного и общего лечения. При этом обычно вначале проводится деструктивное лечение. Затем, в связи с тем, что латентная стадия жизненного цикла ВПЧ протекает в клетках базального слоя эпидермиса и физическими методами очаг поражения трудно удалить полностью (ДНК ВПЧ могут быть на расстоянии до 1 см от видимых границ опухоли), сразу после регенерации эпидермиса, во избежание рецидива, осуществляется противовирусная терапия препаратами ИНФ или кремом имиквимод. В случае рецидива применяют антивирусные и иммунотропные препараты.
Все ИНФ эффективны в отношении ВПЧ. При остроконечных кондиломах их применяют (инъекции внутрь очага или системно) в качестве терапии резерва, особенно при отсутствии эффекта от общепринятой терапии. ИНФ — это цитокины первой фазы иммунного ответа, обладающие антивирусными, антипролиферативными и иммуностимулирующими свойствами благодаря способности усиливать цитотоксическую активность Т-лимфоцитов и стимулировать их способность уничтожать клетки с измененной антигенной структурой.
Как известно, большинство вирусов индуцирует синтез ИНФ (альфа и бета), обладающих выраженной противовирусной и иммуномодулирующей активностью. В клинической практике при лечении ВПЧ-ассоциированных заболеваний широко используется ИНФ альфа-2.
Внутриочаговые инъекции под основание генитальных бородавок проводят препаратами ИНФ альфа-2 в дозе 5 млн МЕ 3 раза в неделю в течение 3 недель. ИФН применяют также с целью предварительной терапии крупных очагов поражения для уменьшения их площади перед деструктивным методом, а также с целью профилактики рецидивов [17].
Необходимо отметить техническую трудность проведения местного обкалывания генитальных бородавок, выраженный гриппоподобный синдром при парентеральном введении ИНФ, а также выраженную болезненность при проведении таких манипуляций.
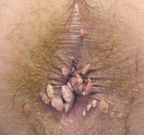
При лечении эндоуретральных кондилом используют ежедневные инстилляции ИФН альфа-2 в дозе 25 млн МЕ в течение 6 недель и с цитологическим контролем через 2 и 6 недель после окончания курса лечения, а затем — каждые 3 месяца в течение года. Рецидив служит показанием к проведению повторного курса лечения [17].
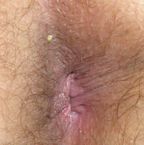
Под нашим наблюдением находилось 18 пациентов (12 мужчин и 6 женщин) с диагнозом «остроконечные кондиломы аногенитальной области». Возраст пациентов варьировал от 19 до 38 лет и в среднем составлял 24,7 года. Для идентификации типа ВПЧ в каждом случае проводилась ПЦР, необходимо отметить, что наиболее часто выявлялись ВПЧ 6, 11, 31 и 33 типов, при этом в группе женщин из 6 пациенток у 5 был выявлен ВПЧ 6 типа. Все пациенты ранее неоднократно проходили лечение по поводу остроконечных кондилом с применением различных методов деструкции: электрокоагуляция, криодеструкция, лазерная вапоризация и др. В среднем количество рецидивов составляло 2,8, при этом средний межрецидивный период составлял 2,1 месяца и ни в одном случае его продолжительность не превышала 4 месяцев.
Всем пациентам проводился 14-дневный курс терапии ректальными суппозиториями Виферон по 3 млн МЕ в сутки, местно применялся гель Виферон. На 15 день проводилась деструкция новообразований методом электрокоагуляции, после чего рекомендовалось продолжить применение ректальных суппозиториев Виферон по 1 млн МЕ в сутки в течение еще 15 дней. Ближайшие результаты лечения в каждом случае были хорошими (рис. 1, 2). В период наблюдения в течение не менее 8 месяцев рецидивов заболевания не было ни в одном случае. Особо необходимо отметить хорошую переносимость применявшихся препаратов, поскольку побочных эффектов или осложнений также не наблюдалось.
Полученные результаты позволяют рассматривать Виферон как эффективный препарат для иммунотерапии ВПЧ-ассоциированных генитальных неоплазий и рекомендовать его широкое внедрение в практику специалистов.
Литература
А. В. Молочков, доктор медицинских наук, профессор
МОНИКИ им. М. Ф. Владимирского, Москва