Как выработать гормон роста
Как выработать гормон роста
Как “догнать” рост?
Известно, что одной из характеристик физического развития детей и подростков является рост. “Можно ли как-то повлиять на рост?” — часто спрашивают заботливые родители. На этот и другие вопросы отвечает Елена ЛОБЫКИНА, доктор медицинских наук, профессор, врач-диетолог ГБУЗ КО “Новокузнецкий центр медицинской профилактики”:
— Для ответа на этот вопрос немного напомню, как рост происходит. В течение жизни ребенка, до момента достижения окончательного роста, идет смена периодов ускоренного и замедленного роста. Формирование костей заканчивается в среднем к 25 годам. К этому возрасту происходит формирование так называемого “пика костной массы”, когда происходят ускорение линейного роста, интенсивное нарастание костной массы и увеличение размеров кости. Выделяют три периода наибольшего скачка роста: первый год жизни (рост увеличивается на 50% от длины тела при рождении); 5-6 лет и 13-15 лет (пубертатный скачок роста). Участвуют в процессах роста практически все гормоны, особенно это относится к гипофизу, щитовидной железе и половым железам (особенно в период пубертата). В связи с этим при задержке роста необходимо исключить заболевания этих эндокринных органов.
— Какие факторы способствуют замедлению роста ребенка?
— На рост влияют наследственность, конституциональные особенности и наличие заболеваний. Дефицит гормона роста встречается редко, чаще встречаются конституциональные особенности роста (особенно у мальчиков). Плохо растут дети невысоких родителей с так называемым “семейным замедленным созреванием”. Задержка роста и пубертата могут наблюдаться как при резком дефиците массы тела в результате недостаточной калорийности или несбалансированного питания (нервная анорексия, попытка похудеть на низкокалорийных диетах), так и при ожирении у подростков. Главный ориентир, на который надо обратить внимание при исключении гормональной проблемы задержки роста (дефицита гормона роста), — это отсутствие динамики роста ребенка в течение года.
— Может ли питание влиять на рост ребенка?
— Да, может. Для поддержания концентрации и ритма секреции гормона роста полноценное и сбалансированное питание (достаточное количество и правильный баланс не только белков, жиров и углеводов, но и витаминов и минеральных веществ) крайне необходимо. Это достаточно частая причина отставания в росте у детей.
В первые годы жизни задержка роста может возникнуть из-за недостаточности питания, нарушения кишечного всасывания. Если ребенок с раннего детства отстает в росте от сверстников, а причина отставания неясна, необходимо обязательно исключить скрытое течение у ребенка целиакии — заболевания, сопровождающегося непереносимостью глютена (клейковины) — белка, который содержится в пшенице и некоторых других злаках. Нарушения функции кишечника приводят к развитию всасывания необходимых пищевых веществ.
— Как естественным путем, с помощью питания, повысить секрецию гормона роста?
— Доказано, что белково-энергетическое недоедание, дефицит в питании витаминов (А, Д) и минеральных веществ (кальция, железа, йода, цинка и др.) приводят к нарушению роста. Белок необходим для правильного формирования костной и хрящевой ткани, а также для образования гормонов, регулирующих рост, в том числе и самого гормона роста. Соответственно, недостаток белка в пище напрямую может влиять на задержку роста. Кроме того, дефицит полноценного белка нарушает процессы всасывания витаминов и минеральных веществ из пищи. Дефицит белка может проявляться у детей снижением мышечной массы (в том числе и массы тела) и болью в мышцах, линейной деформацией костей, изменениями со стороны кожи (изменение цвета, сухая шелушащаяся кожа, длительно не заживающие язвы и раны).
— Как на рост влияет витамин D?
— Витамин D за счет регуляции фосфора и кальция и повышения всасывания кальция в кишечнике регулирует костный обмен, предупреждая развитие рахита и остеопороза. Пищевые источники — это печень животных, желток яиц, молоко, масло, сметана, икра. Профилактика дефицита витамина D может быть достигнута путем увеличения солнечного облучения, употребления продуктов, богатых витамином D, и ежедневного приема витамина D. У нас принято активное назначение витамина D детям до 1-2 лет с целью профилактики рахита, затем про витамин D “забывают”, особенно в подростковом возрасте. Между тем в нашей стране среди всех групп населения наблюдается дефицит витамина D различной степени, что требует при ликвидации дефицита подключения лечебных доз, и не в режиме курсового, а более длительного его применения.
— Можно ли передозировать витамин D?
— Получить передозировку можно, если без исследования крови, например, назначить высокие взрослые лечебные дозы витамина D маленькому ребенку. В реальной практике у детей и подростков получить передозировку трудно, если только не принимать месяц по бутыльку капель витамина в неделю. Это крайности. Уж слишком дефицитен витамин D в питании россиян любого, в том числе детского и подросткового возраста. Поэтому вышеуказанные дозировки являются минимальными профилактическими дозами. Наоборот, чаще должен возникать вопрос: “А достаточна ли для моего ребенка эта доза?”
— Что еще поможет “догнать” рост?
— Для образования гормона роста необходим цинк, который стимулирует образование и минерализацию костной ткани, участвует в образовании ферментов, регулирующих рост и обмен белка. Около 30% всего содержащегося в организме цинка находится в костях. Основной источник цинка — мясные продукты. Помимо этого, к продуктам, богатым цинком, относятся тыква, семена кабачков, мясо краба, арахис.
К сожалению, Западная Сибирь относится к регионам не только дефицитным по йоду, но и железу. Отмечают, что латентный (скрытый) железодефицит может встречаться у 50 — 60% подростков. Логично полагать, что питание и дыхание любой клетки, тем более растущей, как кость, будет нуждаться в хороших дотациях железа. Кроме этого, гипоксия, развивающаяся при дефиците железа, будет влиять и на синтез гормона роста.
Контролируют линейный рост (особенно в первые годы жизни ребенка) и гормоны щитовидной железы, для образования которых необходим йод и животный белок. Напомню, что идеальной комбинацией этого являются морская рыба и морская капуста. Гораздо меньше йода содержится в нашем традиционном (“безрыбном”) рационе питания. Не забывайте про любую возможность включать в рацион обогащенные йодом продукты питания (например, соль и хлеб). В организме все очень взаимосвязано.
Таким образом, только разнообразное, не однотипное изо дня в день, питание, с включением всех групп продуктов, может улучшить ростовые показатели ребенка и подростка.
— Какие еще факторы, кроме питания, могут влиять на рост?
— Для нормального роста ребенка также важны: качество и продолжительность сна. Увеличение продолжительности сна способствует увеличению выделения гормона роста. Подросткам в этот период спать желательно 8-10 часов. Помимо сна регулярная физическая аэробная нагрузка: занятия плаванием, гимнастикой (турник), легкой атлетикой. Анаэробные физические упражнения (марафоны, тяжелая атлетика) могут привести к задержке темпов и в конечном счете к достижению небольшого конечного роста.
Гормон роста (соматотропный гормон)
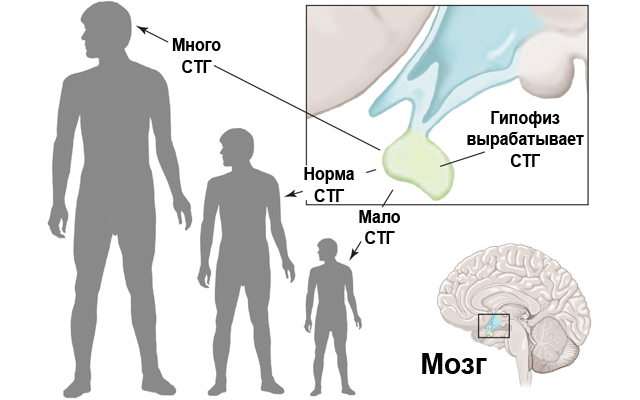
Гормон роста (соматотропный гормон) выделяется передней долей гипофиза. В статье описаны: особенности секреции гормона роста и факторы на нее влияющие; функции гормона роста; положительные и отрицательные эффекты введения соматотропного гормона в организм человека; влияние силовой и аэробной тренировок на концентрацию гормона роста в крови молодых и пожилых людей.
Гормон роста (соматотропный гормон, СТГ)
Соматотропный гормон (СТГ), известный как гормон роста (ГР, GH), является полипептидом (белком), секретируемым передней долей гипофиза. Органами-мишенями, то есть органами, на которые действует гормон, являются все клетки организма человека.
Функции гормона роста
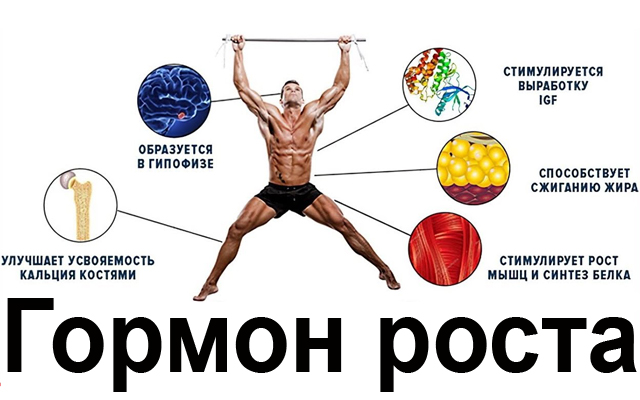
Функциями гормона роста являются: активация синтеза ИФР-1 в печени; увеличение линейного роста костей; повышение синтеза белков; уменьшение катаболизма белков; снижение отложения подкожного жира; стимуляция продукции глюкозы печенью; ускорение восстановления тканей после травм.
Секреция гормона роста
Секрецию гормона роста контролируют два гормона, вырабатываемые в гипоталамусе: соматолиберин и соматостатин. Соматолиберин стимулирует синтез и секрецию гормона роста, в то время как соматостатин подавляет секрецию гормона роста, однако не влияет на его синтез. Гормон роста выделяется в течение дня волнообразно, приблизительно каждые два часа и имеет максимальный всплеск секреции во время фазы медленного сна.
Положительные эффекты введения гормона роста в организм человека
Положительными эффектами введения гормона роста в организм человека являются: увеличение синтеза и уменьшение катаболизма белков; снижение отложения подкожного жира; стимуляция продукции глюкозы печенью; ускорение восстановления тканей после травм. Однако прием гормона роста обеспечивает скромный прирост силы как у молодых, так и у пожилых людей.
Негативные эффекты введения гормона роста в организм человека
Негативными эффектами введения гормона роста являются: гипертензия, акромегалия, остеоартрит и деформация позвонков, апноэ во сне, сахарный диабет, повышенный риск рака толстой кишки, усиленное потоотделение и образование папиллом, увеличение органов.
Влияние силовой тренировки на концентрацию гормона роста в крови
Силовая тренировка вызывает повышение концентрации гормона роста в крови у мужчин и женщин через 30 минут после начала тренировки. На концентрацию гормона роста в крови существенно влияют: большой объем силовой работы и выполнение большого количества подходов; интервал отдыха (оптимально 1 мин.); величина отягощения (оптимально 8-10 ПМ).
У пожилых людей в ответ на силовую тренировку концентрация гормона роста в крови меняется незначительно (до 4 мкг/л).
Влияние аэробной тренировки на концентрацию гормона роста в крови
Аэробная тренировка вызывает повышение концентрации гормона роста в крови через 15 минут после начала тренировки. Под влиянием аэробных упражнений женщины достигают значительно больших значений концентрации гормона роста в крови по сравнению с мужчинами. Чем выше интенсивность аэробных упражнений, тем выше секреция гормона роста. На уровень секреции гормона роста существенно влияет степень ожирения. Чем она выше, тем ниже секреция гормона роста. Уровень секреции гормона роста при выполнении аэробной тренировки у пожилых людей в 5-7 раз ниже, чем у молодых, однако различия минимизируются, если пожилые люди занимаются фитнесом.
Гормон роста или соматотропный гормон: эффект у взрослых и детей
Соматотропный гормон (СТГ) – это белок, который поддерживает в организме обмен веществ и рост клеток, поэтому его чаще называют гормоном роста. Но это не единственные достоинства соматотропина.
Мы расскажем, почему человек не сможет жить полноценной жизнью без соматотропного гормона.
Где вырабатывается соматотропный гормон?
Гормон роста выделяет главная эндокринная железа организма – гипофиз. В его передней доле есть особая группа клеток – соматофоры, где и образуется гормон роста. Соматофоры составляют 50% клеток передней доли гипофиза. Они получают регулирующие импульсы напрямую из мозга.
Регулятором секреции гормона роста является гипоталамус. Он связан с гипофизом через особый «мостик», который называют «ножкой».
Гипоталамус выделяет 2 гормона, которые контролируют уровень СТГ:
Интересный факт!
В названии соматотропина зашифрован весь спектр его действия на организм. «Сома» – это греческое название тела, а «соматотропин» означает «направленный на тело». Такое имя гормону дали неслучайно, ведь, в отличие от других гормонов, у СТГ нет какого-то одного подконтрольного органа – его действие распространяется практически на все тело.
Как действует соматотропный гормон?
К СТГ чувствительны все клетки тела. Он обеспечивает не только их рост, но и дифференцировку – развитие по наследственной программе, которая позволяет клетке выполнять конкретную функцию.
Основные ткани-мишени СТГ – это:
На кости и мышцы гормон действует прямо, а на остальные ткани – через печень.
Гормон роста активен в крови в течение нескольких минут. За это время печень использует его, чтобы выделить особые вещества – инсулиноподобные факторы роста (ИФР). Ранее их называли соматомединами, что в переводе с латыни звучит как «посредник соматотропина». Соматомедины переименовали в инсулиноподобный фактор роста, поскольку они на 41 – 43% схожи с инсулином и действуют, как он.
Однако через 30 – 40 минут инсулиновый эффект прекращается и начинается противоположный – антиинсулиновый. Сам СТГ действует против инсулина, поскольку стимулирует выделение глюкагона, который увеличивает уровень глюкозы.
Подпишитесь на Здоровьесберегающий видеоканал

Соматотропный гормон у детей и подростков
Именно благодаря соматотропину детские кости растут в длину, мышцы накапливают белок, и растет хрящевая ткань трубчатых костей (кости конечностей). Уровень СТГ увеличивается по мере взросления ребенка. Пик его концентрации отмечают в период полового созревания.
ИФР стимулируют рост не только костей и мышц, но и внутренних органов. Благодаря инсулиноподобному фактору в период активного роста масса сердца, легких, почек и других органов также увеличивается.
Интересный факт!
В крови гормон роста циркулирует в свободной форме и в соединении с белками. Есть несколько форм гормона, но самым активным считается СТГ с молекулярной массой 20 000 дальтон, хотя основная масса гормона весит чуть больше – 22 000 дальтон.
Дефицит СТГ у детей
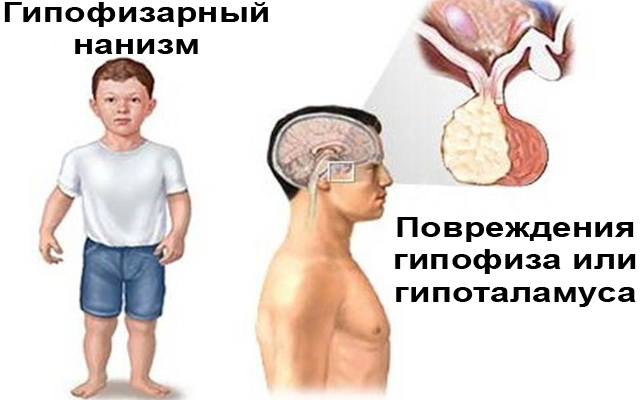
Из-за соматотропной недостаточности у детей развивается карликовость. По-научному эта болезнь называется гипофизарным нанизмом (по-гречески nanos – карлик). При нанизме ребенок резко отстает в росте и физическом развитии от сверстников.
Выделяют абсолютный и относительный дефицит соматотропного гормона. При абсолютном гипофиз выделяет недостаточно СТГ.
Причиной абсолютного дефицита гормона роста могут быть:
Почти в 75% случаев никакой патологии найти не удается, и тогда дефицит соматотропина считается относительным, то есть количество гормона в норме, но его эффекты неощутимы.
Относительная недостаточность соматотропина возникает, если:
При некоторых формах относительной недостаточности СТГ его концентрация в крови повышена. Это связано с тем, что в крови после выброса соматотропного гормона не повышается уровень его посредника – ИФР. Именно инсулиноподобный фактор роста обеспечивает обратную связь с гипофизом и тормозит выработку СТГ. Но при отсутствии посредника обратная связь нарушается, а гипофиз выделяет еще больше гормона роста.
Интересный факт!
При патологии печени образование ИФР может снижаться. В ответ на это гипофиз усиливает выработку СТГ. Но без посредника соматотропный гормон недостаточно стимулирует кости, мышцы и внутренние органы. Поэтому рост ребенка или подростка замедляется.
Нанизм и малый рост – два разных состояния, связанные с низким уровнем СТГ
Дети с недостатком соматотропного гормона рождаются с нормальной массой тела и длиной конечностей. Педиатр подозревает нанизм, если рост ребенка увеличивается менее чем на 4 см в год.
Нанизм проявляется к 3 – 4 годам жизни, а до этого ребенок растет нормально. Дело в том, что с материнским молоком малыш получает пролактин. Это еще один гормон гипофиза, который структурно схож с СТГ. В раннем детском возрасте пролактин действует подобно гормону роста. Но как только грудное вскармливание прекращают, дефицит СТГ дает о себе знать. Именно поэтому конечности у людей с карликовостью непропорциональны телу и остаются такими же, какие были в 4 года.
Интересный факт!
Пигмеи (племена, живущие в центральной Африке) значительно меньше ростом, чем люди на других континентах. Исследования показали, что у них изначально выделяется меньше гормона роста, чем, например, у европейцев. Однако это не значит, что у пигмеев есть соматотропная недостаточность. Вынужденные передвигаться по непроходимым лесам в джунглях, пигмеи стали приспосабливаться к новым условиям. Высокий рост стал неудобной особенностью, и организм постепенно начал менять генетическую программу. Уровень СТГ у пигмеев снижается почти сразу после рождения, но продукция его продолжается, и его уровень в разные возрастные периоды отличается от уровня остальных людей. По этой причине их голова, туловище и конечности растут пропорционально, а маленький рост считается эволюционным признаком, а не патологией.
Зачем нужен гормон роста взрослым?
Раньше считалось, что низкий уровень соматотропного гормона опасен только для детей, а у взрослых он не так важен. Но оказалось, что гормон роста у взрослых регулирует обмен веществ, влияет на психическое здоровье и сохраняет молодость. СТГ активирует синтез нуклеиновых кислот – РНК и ДНК, ускоряя заживление ран и противодействуя старению организма. А дефицит гормона роста у взрослых проявляется различными нарушениями.
Помимо гипофизарного нанизма, дефицит СТГ может возникать при недостаточности гипофиза – гипопитуитаризме. Это тяжелое заболевание, при котором гипофиз повреждается и теряет способность выделять один или сразу несколько гормонов. Но иногда дефицит гормона роста возникает и при здоровом гипофизе.
Интересный факт!
Недостаток соматотропина может возникать из-за любого фактора, который повышает уровень глюкозы в крови, в том числе и при приеме некоторых препаратов.
Соматотропный гормон против ожирения
Вы могли заметить, что чем выше человек, тем он, как правило, реже страдает ожирением и наоборот. Конечно, длинные мышцы и кости требуют больше питательных веществ, и «лишних» калорий высокие люди съедают меньше. Но дело не только в росте, но и в гормоне, благодаря которому человек растет ввысь.
В 1991 году стало известно, что дефицит гормона роста у взрослых приводит к ожирению, причем жир, в основном, накапливается в области талии. Без преувеличения можно сказать, что соматотропный гормон – защитник от ожирения.
У здорового человека при понижении уровня глюкозы в крови или голодании увеличивается уровень грелина – гормона голода. Он выделяется как в пищеварительном тракте, так и в центральной нервной системе. Грелин стимулирует выделение гормона роста, который, в свою очередь, мобилизует жир – вызывает его расщепление и утилизацию. Результат – Вы теряете лишние килограммы жира.
Интересный факт!
Соматотропный гормон выделяется волнообразно. Каждые 20 – 30 минут отмечается «взрыв» – внезапная секреция большой порции гормона. После этого его продукция временно прекращается.
«Груда» мышц и крепкие кости: анаболический эффект гормона роста
Без достаточной поддержки гормона роста теряется мышечная масса, медленно заживают раны, кости становятся хрупкими, и может легко возникнуть перелом. Все дело в анаболическом эффекте соматотропина – его способности стимулировать образование белков.
В клетках, которые ответственны за образования костной ткани, есть рецепторы к СТГ. Они не исчезают после периода полового созревания, поэтому некоторые эффекты соматотропина сохраняются. У взрослых гормон роста стимулирует минерализацию костей – усиливает накопление кальция и фосфора, поддерживая плотность костной ткани и предупреждая развитие переломов.
Интересный факт!
СТГ активирует витамин D в почках, что влияет на усвоение кальция и фосфора, предупреждает их потерю с мочой и способствует укреплению костей.
Эмоциональная стабильность
Гормон роста увеличивает уровень эндорфинов – гормонов удовольствия, которые стимулируют центральную нервную систему. При дефиците соматотропного гормона появляется слабость, утомляемость, тревога, склонность к депрессии, человек плохо контролирует свои эмоции.
Интересный факт!
Для людей с низким уровнем СТГ типична склонность к изоляции от общества.
Почему увеличивается уровень СТГ?
После травм и операций выделяется много гормона роста, ведь организму нужно стимулировать рост клеток. То же самое происходит при голодании и алкоголизме, а также при значительной физической активности. Это нормально. Но есть и тяжелые болезни, которые вызваны избытком гормона роста – гигантизм у детей и акромегалия у взрослых.
Гигантизм
Если уровень гормона роста повышается в детстве или подростковом возрасте, кости и мышцы растут очень быстро и чрезмерно. Иногда ребенок не просто обгоняет своих сверстников в росте, а становится намного выше всех остальных. При этом пропорции конечностей, туловища и головы не нарушаются.
Интересный факт!
Патологическим считается рост выше 2 метров у мужчин и выше 190 см у женщин.
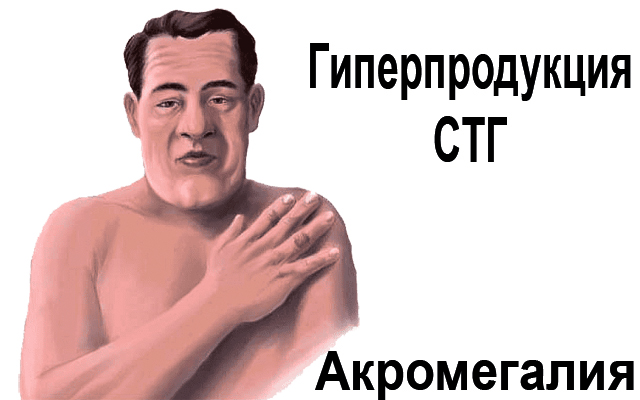
Акромегалия
Это вариант «гигантизма» у взрослых. Но проявляется избыточная продукция соматотропина у них иначе. Поскольку после 18 – 19 лет окостенение заканчивается и зоны роста костей «закрываются», СТГ не может подействовать на кости, а значит, рост человека останется таким же, каким был к совершеннолетию. Но остальные ткани-мишени не теряют чувствительность к гормону, ведь он выступает в качестве регулятора обмена веществ.
При гиперпродукции СТГ увеличивается масса внутренних органов и наблюдается так называемый периостальный рост тканей – растут надкостница, хрящ и мягкие ткани. Причем этот рост не может считаться нормальным, поскольку увеличиваются только некоторые ткани. В результате пропорции тела нарушаются, изменяется строение внутренних органов, страдают их функции, и ухудшается обмен веществ.
Акромегалия развивается постепенно и вызывает следующие изменения:
Интересный факт!
Если Вы принимаете препараты, понижающие давление, противозачаточные таблетки, либо регулярно делаете уколы инсулина, уровень СТГ может повышаться.
Что делать при дефиците или избытке соматотропного гормона?
После 20 лет уровень гормона роста постепенно снижается – каждые 10 лет на 14%. Причем снижается не только его суточная выработка, но и выделение в ответ на стимулы. Частично причиной тому является снижение чувствительности гипофиза, которая обостряется, если у человека есть другие болезни, например, гипотиреоз, нарушение липидного обмена (увеличение свободных жирных кислот), сахарный диабет и ожирение.
В отличие от детей, взрослым труднее догадаться, что некоторые ткани продолжают расти из-за акромегалии. Вы можете заметить изменения во внешности через несколько лет после начала заболевания. Но обратите внимание на свое самочувствие. Если Вас беспокоят постоянная потливость, головная боль, боль в суставах или нарушение менструального цикла, необходимо выяснить, нет ли у Вас опухоли гипофиза, желудка, поджелудочной железы и других органов, которые могут выделять большое количество соматотропного гормона.
Если Вы заметили признаки дефицита или избытка СТГ, следует сдать биохимический анализ крови.
Как сдавать анализ крови на СТГ?
Если Вы просто сделаете анализ крови на СТГ, то зря потратите время, ведь, чтобы выявить отклонения в уровне СТГ нужно стимулировать и подавить выделение гормона с помощью специальных функциональных тестов.
Ребенку пробы назначают, если он отстает в физическом развитии либо, наоборот, растет быстрее сверстников.
Взрослым анализ показан, если:
Интересный факт!
В крови исследуют уровень соматотропного гормона и инсулиноподобного фактора. Именно ИФР может указать врачу на избыток или недостаток гормона роста. В отличие от соматотропного гормона, уровень его посредника в течение дня остается стабильным и позволяет судить о средней концентрации СТГ в крови.
Тест на стимуляцию
За 10 – 12 часов до пробы нужно воздержаться от любой пищи. В день исследования врач берет анализ крови на СТГ, а потом вводит раствор инсулина или аргинин, которые стимулируют выделение СТГ. В течение дня исследование делают повторно, чтобы оценить реакцию гипофиза на стимулы.
Важно!
Прежде чем делать пробы, проконсультируйтесь с врачом. Есть ряд препаратов, которые могут повлиять на результат анализа. Даже если Вы принимаете биологически активные добавки, врач должен об этом знать. Дело в том, что в БАДы могут добавить аргинин (важная для организма аминокислота) и витамин PP, которые повышают уровень СТГ.
Тест на подавление
Эта проба нужна, чтобы выявить опухоли гипофиза, которые выделяют гормон самостоятельно и не реагируют на подавляющие импульсы.
К тесту готовятся точно так же, как и при пробе на стимуляцию. Но вместо инсулина и аргинина, пациент просто выпивает раствор глюкозы. Если в гипофизе есть автономная опухоль, уровень СТГ в течение дня остается высоким.
Важно!
У взрослых без стимуляции норма соматотропного гормона в крови натощак составляет 0 – 5 нг/мл (нанограмм на миллилитр), но обычно его уровень не превышает 2 нг/мл.
Как лечат избыток и недостаток гормона роста?
Если в организме выделяется слишком много соматотропного гормона, врачи, как правило, выполняют операцию и удаляют опухоль, ставшую причиной гигантизма или акромегалии. Если тест на подавление показал, что гипофиз реагирует на стимулы, врачи могут назначить медикаменты, чтобы нормализовать уровень СТГ в крови.
Соматотропиновая терапия
Соматотропный гормон используют для лечения его значительного дефицита, то есть, когда гипофиз перестает выделять СТГ.
До 80 годов прошлого века врачи использовали природный соматотропин, который получали из гипофиза людей. Однако исследования показания, что человеческий соматотропин может вызвать тяжелую патологию мозга – болезнь Крейтцфельдта-Якоба. Поэтому в настоящее время используют синтетические аналоги гормона роста.
Введение соматотропина улучшает самочувствие больных, но при неправильном использовании возможны следующие побочные эффекты:
Интересный факт!
Некоторые спортсмены используют соматотропин не по назначению, а чтобы нарастить мышечную массу и повысить выносливость. Но соматотропин – это допинг, и он запрещен Всемирным антидопинговым агентством.
3 совета, которые помогут повысить уровень СТГ в крови без лекарств
Если врач не считает нужным назначать соматотропин, но Вы хотите поддерживать его нормальный уровень, несмотря на возраст, используйте физиологические стимуляторы секреции гормона роста.
1. Бегом за гормоном роста
Чтобы сохранить нормальный уровень соматотропного гормона и его нужные для здоровья эффекты, можно просто активно заниматься физической нагрузкой. 8 недель активных тренировок повышают количество инсулиноподобного фактора роста на 15% даже у людей старше 60 лет.
В 2017 году группа ученых из разных стран провела исследование, в котором принимали участие военные молодого и среднего возраста. 13 недель они активно тренировались. Тренировки включали как бег, так и силовые упражнения. У всех участников после нагрузки повысился уровень ИФР. Фактически активные тренировки помогают противодействовать старческим изменениям, повышая уровень соматотропного гормона. Подробнее об исследовании читайте, перейдя по ссылке в списке литературы.
СТГ по праву считается «фитнес-гормоном». Он одновременно действует на белковый, углеводный и жировой обмен, перераспределяя использования энергии так, что организм начинает сжигать жиры, но «не трогает» углеводы или белки. Более того, СТГ способен одновременно увеличивать мышечную массу за счет накопления белков.
Интересный факт!
Гормон роста выделяется, когда Вы мерзнете или испытываете стресс, например, боль или тревожность.
2. Практиковать интервальное голодание
Интервальное голодание – модный способ «сидеть на диете», несильно ограничивая себя во вкусной еде, а точнее, делать это ненадолго. Суть интервального голодания – употреблять пищу только в определенные часы, которые называют «пищевым окном». В остальное время есть, что бы то ни было, нельзя. Разрешены только вода и травяной чай без сахара. При интервальном голодании резко падает уровень глюкозы, а это стимулирует выброс СТГ.
Интересный факт!
При голодании уровень СТГ повышается в 15 раз, но стоит Вам что-то съесть, его концентрация в крови резко снижается. Исследования показали, что при длительном голодании уровень гормона роста может увеличиться аж на 1250%, хотя и 5-дневного голодания достаточно, чтобы концентрация СТГ возросла на 300 процентов. Гормон роста помогает организму перейти в состояние кетоза – расщеплять жир, создавая кетоновые тела и используя их в качестве источника энергии.
3. Высыпайтесь
Любое нарушение сна может снизить синтез гормона роста. СТГ в 3 раза активнее вырабатывается в ночное время, У детей он начинает выделяться уже в фазу медленного сна – вскоре после засыпания, но основная его часть поступает в кровь позже. Так что, дети действительно растут во сне.
Чтобы «взрослый» гипофиз получил сигнал от «вышестоящих инстанций», нужно погрузиться в глубокий сон, дойдя до 3 – 4 фазы. Для поддержания нормального уровня соматотропного гормона нужно спать как минимум 6,5 часов.
Интересный факт!
Роль гормона роста при бесплодии
Репродуктивная система неразрывно связана с соматотропным гормоном и клетками, которые его выделяют. Небольшое количество СТГ вырабатывают яичники.
Гормон роста влияет на половые органы как прямо, так и через регуляторные механизмы. Он стимулирует выработку прогестерона и эстрадиола в яичниках в зависимости от фазы менструального цикла.
Для мужчин соматотропный гормон оказался не менее важным. У многих представителей сильного пола с бесплодием и неподвижными сперматозоидами обнаруживают относительный дефицит гормона роста. При этом лечение соматотропином улучшает образование спермы и подвижность сперматозоидов. Подробнее об исследовании читайте, перейдя по ссылке в списке литературы.
Интересный факт!
Соматотропный гормон улучшает качество ооцитов, помогает созреванию яйцеклетки и повышает шансы на успешное ЭКО. А поскольку гормон еще и структурно похож на пролактин, он оказывает позитивное влияние на течение беременности.
Гормон роста
Дата публикации: 6 апреля 2022 г.
Время прочтения: 5 минут
Ни один человек не может нормально жить без нормального уровня соматотропного гормона. Чаще всего его называют гормоном роста. Это активный белок, который занимает в организме важное место по части обмена вещества и выработки новых клеток. Синтез его происходит в гипофизе, благодаря чему воздействуют на процессы непосредственно из мозга.
О гормоне
В организме человек формируется огромное количество химических соединений, которые управляют процессами развития организма, регулируют работу важных для жизнедеятельности желёз, контролируют обмен веществ. Соматотропный гормон роста формируется в гипофизе под непосредственным контролем гипоталамуса. Он отвечает за рост организма, регулирование обменных процессов, в том числе расщеплении белков, жиров и углеводов, а также работу желез внутренней секреции.
Самые большие концентрации соматотропина наблюдаются в детском возрасте, когда малыш активно растёт. Дефицит гормона роста влечёт за собой отставание ребёнка в процессе роста от сверстников. В запущенных случаях это может повлечь задержки общего развития, что чревато опасными последствиями.
Важно отметить, что переизбыток соматотропина также приводит к нежелательным последствиям. В данном случае ребёнок обгоняет сверстников по всем параметрам и рост не прекращается даже после завершения периода полового созревания. Это может перерасти в гигантизм или акромегалию.
Максимальные дозы синтеза гормона роста происходят в период с рождения малыша до окончания пубертатного возраста. Однако за его концентрацией важно следить и во взрослом периоде. Он отвечает за многие важные процессы в организме, в том числе выработку клеток, формирование тканей и правильный обмен веществ.
Функции
Соматотропин выполняет ряд важных функций для поддержания здоровья человека. Это процессы, без которых невозможна нормальная жизнедеятельность человека, а также восстановление после стрессов, физических нагрузок и других неприятных последствий.
Расщепление жиров
Гормон роста вырабатывается в ночное время, когда организм отдыхает. Происходит так потому, что в дневные часы человеку хватает потребляемых с пищей углеводов. Они дают энергию. В ночные часы активно вырабатывается соматотропин, расщепляя отложения жиров. Именно поэтому после пробуждения мы выглядим несколько худее, чем в течение дня.
Но данные процессы не работают, если человек предпочитает плотно поесть перед сном или лечь спать позже обычного. Чтобы соматотропин вырабатывался в соответствии с природной функцией, важно соблюдать ряд правил:
Расщепляя жиры, гормон вырабатывает нужную нам энергию. При этом в переработку идут даже отложившиеся давно жиры, застоявшиеся в организме. Человек «худеет» не прилагая к этому особых усилий.
Поддержание упругости кожи
Участие в регенерации тканей, а также усиленная выработка белка помогает поддерживать кожу в тонусе и активно поддерживать кожу в тонусе. Она подтягивается, становится более упругой и ровной, замедляется процесс появления морщин.
Увеличение силы мышц и прочности костей
Под воздействием гормона роста и при достаточном количестве его выработки гипофизом происходит укрепление мышц и костей, они становятся более упругими и эластичными, дольше сохраняют «молодость». Существенно уменьшается риск развития остеопороза, в результате которого минеральные вещества вымываются из костей. Также сокращается риск переломов.
Благодаря спортивным тренировкам можно усилить процесс укрепления, так как при физических нагрузках соматотропин вырабатывается сильнее и быстрее.
Чтобы походить с помощью выработки гормона роста и занятий в фитнес-центре, обязательно отказаться от употребления перед тренировкой шоколада, а также сладких напитков, кофе и чая. Они являются источниками поступления в организм углеводов, которых будет достаточно на взятие нагрузок. Выработка соматотропина будет приостановлена.
Регулировка жирового обмена
Гормон роста регулирует и снижает выработку вредного холестерина, который способен оседать на стенках сосудов и провоцировать развитие атеросклероза, инфарктов, инсультов, нарушений сосудистой системы.
Функции гормона роста достаточно обширны. Он расщепляет поступающие в организм вещества и энергетически подпитывает органы и ткани. В результате нормальной работы синтеза гормонов происходит укрепление организма в целом, появляется упругость костей, тканей, нормализация метаболизма.
Нормативные показатели
Пациенты любого возраста могут быть исследованы на количественное содержание гормона в сыворотке крови. Для этого достаточно посетить ближайшую лабораторию для забора биоматериала. Анализ назначается в следующих случаях:
Чтобы показатели секреции гормона роста были качественными, важно правильно подготовиться к посещению лаборатории. Для этого соблюдают режим голодания от 8 до 12 часов, без употребления кофе, чая, сладких соков и газировки. Можно пить только чистую питьевую воду без газа.
Обязательно воздержаться от физических и эмоциональных перегрузов хотя бы за сутки до исследования, а также от курения не менее чем за три часа до сдачи крови. Перед забором венозной крови рекомендуется посидеть в состоянии покоя не менее получаса перед кабинетом лаборантов.
Существуют таблицы, которые определяют референсные значения гормона роста. Стоит ориентироваться на них при оценке результата, но заниматься самолечением категорически запрещено. Диагностику и назначение соответствующей терапии проводит только врач.
Уровень инсулиносвязанного гормона изменяется в зависимости от пола и возраста пациента. Здесь даются подробные таблицы с усреднёнными значениями:
| Возраст и пол пациента | Концентрация (нг/мл) |
| женщины от 16 до 19 лет | 176–249 |
| мужчины от 16 до 19 лет | 57–425 |
| пациенты в возрасте от 19 до 22 лет | 105–345 |
| граждане в возрасте от 23 до 25 лет | 107–367 |
| люди от 26 до 30 лет | 88–537 |
| пациенты от 31 до 35 лет | 41–246 |
| пациенты 36 – 40 лет | 57–241 |
| пациенты 41 – 45 лет | 43–210 |
| граждане от 46 до 50 лет | 75–196 |
| от 51 до 55 лет | 55–250 |
| пациенты от 56 до 60 лет | 35–200 |
| пациенты от 61 до 65 лет | 50–187 |
| пациенты от 66 до 70 лет | 37–220 |
| пожилые люди от 71 до 80 лет | 25–200 |
| люди старше 80 лет | 17–325 |
В целом у взрослого населения показатель выработки соматотропина у женщин должен быть ниже 8 мкг/л, у мужчин – до 3 мкг/л.
Повышенные и пониженные значения: как с ними бороться
Если гормон роста вырабатывается некорректно, в этом случае идёт речь о понижении или повышении количественных значений. Увеличение показателей соматотропина наблюдается в случае алкоголизма или соблюдения диеты пациентом. Показатели меняются также при активных физических нагрузках.
Речь может идти о гигантизме и акромегалии, если количественные значения сильно превышают норму выработки гормона. Чрезмерный синтез соматотропного гормона приводит к усиленному росту в детском и подростковом возрасте. При этом пропорции тела сохраняются.
Акромегалия представляет собой рост, но только уже не костей и тканей, как у подростков, а внутренних органов, так как наблюдается у взрослых пациентов. Увеличивается их размеры и вес, что создаёт существенные проблемы для нормальной жизнедеятельности. Всё это указывает на то, что гормон роста в крови повышен.
Также повышение уровня вырабатываемого железой гормона роста происходит после перенесённых травм и операций. В этот момент организму нужна активная стимуляция клеток и рост новых для поддержания здоровья организма и его восстановления. Самототропин вырабатывается в усиленном режиме, наблюдается избыток гормона роста.
Недостаток вещества характеризуется задержкой в росте и общем развитии. Нужна срочная помощь, чтобы не спровоцировать отклонения у ребёнка. У взрослых сниженные показатели также опасны, так как могут спровоцировать развитие различных заболеваний, к примеру, остеопороз.
Чтобы восполнить недостаток гормона роста, следует наладить режим сна и отдыха. Действительность такова, что наибольшая концентрация соматотропина наблюдается в ночной период. Поэтому ложиться спать нужно не позднее 22 часов, предварительно подготовившись и отложив гаджеты.
Важно правильно и сбалансированно питаться. Нельзя отказывать себе в потреблении белка, содержащегося в мясе и рыбе. Повысить уровень гормона можно также за счёт умеренных физических перегрузов.
После консультации с доктором можно перейти на приём лекарственных препаратов и аминокислот. Важно не заниматься самостоятельным, бесконтрольным приёмом, чтобы не навредить организму.
Советы от врачей
Железа, вырабатывающая гормон роста, должна работать как часы, в противном случае качество жизни будет существенно снижено. Чтобы этого не произошло, обязательно наладить режим дня. Следует вовремя ложиться спать и высыпаться положенное время, качественно отдыхать и заниматься спортом. Умеренные физические нагрузки способствуют питанию мышц и формированию правильного мышечного каркаса.
Режим питания и сбалансированность продуктов – один из ключевых моментов. В организм пациента должно поступать достаточное количество белков, жиров и углеводов. Не стоит есть перед сном или переедать в течение дня, рекомендуется придерживаться «правильного» питания с полезными продуктами.
При подозрении на отклонения в нормативах содержания соматотропного гормона рекомендуется незамедлительно обратиться к доктору и получить назначение на анализ крови. Лабораторное исследование покажет, необходима ли человеку восстановительная терапия.
Справиться с патологическим недостатком или переизбытком соматотропина можно только с помощью отслеживания лечащего доктора. Самостоятельное лечение или бесконтрольный приём аминокислот способен привести к обратному результату. Не стоит заниматься самолечением, даже если уже сданы все анализы и по протоколу исследования видны нарушения нормативного содержания гормона роста.
Возможности медикаментозной коррекции недостатка гормона роста у взрослых
Каковы основные причины соматотропной недостаточности у взрослых? Каковы ее клинические проявления? Какие методы лабораторно подтверждают диагноз? Как известно, гормон роста (ГР) был последним из классических гормонов, который начали применять с
Каковы основные причины соматотропной недостаточности у взрослых?
Каковы ее клинические проявления?
Какие методы лабораторно подтверждают диагноз?
Как известно, гормон роста (ГР) был последним из классических гормонов, который начали применять с целью заместительной гормональной терапии у взрослых. У детей история медикаментозной коррекции низкорослости насчитывает около тридцати лет, ко взрослым же лечение с использованием биосинтетических препаратов ГР впервые было применено около десяти лет назад. В течение многих лет с целью терапии использовался ГР, получаемый из гипофизарных экстрактов, однако в 1985 году, когда были описаны четыре случая болезни Крейтцфельдта — Якоба у реципиентов гипофизарного ГР, использование последнего было запрещено. Это послужило отправной точкой для начала работ по производству биосинтетического ГР [2].
Использование ГР у детей и произошедший параллельно научный прорыв в отношении диагностирования дефицита гормона роста у взрослых привели к появлению в клинической эндокринологии новой нозологии и, соответственно, новых методов обследования и лечения. Ни один конгресс или симпозиум, проходящий в настоящее время, не обходится без докладов, посвященных проблемам диагностики дефицита ГР (ДГР) у взрослых, выявлению нарушений, сопровождающих заболевание, и принципам подбора терапии.
Для того чтобы создать более точное представление о спектре нарушений, развивающихся на фоне соматотропной недостаточности, необходимо кратко напомнить о структуре ГР, механизмах его секреции и влиянии на органы и системы. ГР, синтезируемый соматотрофами передней доли гипофиза, относится к особому семейству пептидных гормонов, в состав которого кроме ГР входят пролактин (ПРЛ) и плацентарный соматомаммотропин человека (СМЧ). Секреция ГР находится под контролем двух гипоталамических гормонов: соматостатина или соматотропин-ингибирующего фактора (СИФ), который оказывает блокирующее действие на синтез и секрецию соматотрофами ГР. Соматотропин — рилизинг гормон (СРГ) — оказывает стимулирующее действие на соматотрофы, что проявляется увеличением продукции ГР.
Как многие гормоны, ГР синтезируется в определенном импульсном режиме, пики секреции приходятся на 22.00 и 4.00 часа.
Несмотря на существование специфических рецепторов ГР, его действие осуществляется посредством специфических факторов, аналогичных по своей структуре инсулину: инсулиноподобного ростового фактора I (ИФР-I) и инсулиноподобного ростового фактора II (ИФР-II). ИФР-I, действуя через собственные рецепторы, оказывает ростовые эффекты преимущественно в постэмбриональном онтогенезе организма. Действие ИФР-II проявляется преимущественно в процессе эмбриогенеза.
Многочисленные исследования, результаты которых публикуются в современных медицинских изданиях, красноречиво свидетельствуют о наличии серьезных нарушений в соматическом и психологическом статусе пациентов с декомпенсированной недостаточностью гормона роста. Эти нарушения характеризуются изменением соотношения жировая/мышечная ткань в сторону снижения удельного веса последней, увеличения удельного веса жировой ткани и сопровождаются висцеральным отложением последней. При проведении денситометрии обнаруживается снижение плотности костной ткани (МПК). Scacchi at al отметили обратно пропорциональную зависимость между индексом массы тела (ИМТ) и периодом полужизни ГР, а также амплитудой секреции ГР. Процент содержания жировой ткани находился в обратной зависимости от интегрального показателя концентрации ГР, определяемого в течение 24 часов.
Со стороны метаболических нарушений необходимо выделить снижение толерантности к углеводам при проведении инсулинтолерантного теста, увеличение продукции инсулина, проинсулина, повышение содержания триглицеридов плазмы крови, липопротеидов низкой и очень низкой плотности [3].
Не до конца изучено влияние недостаточности ГР на увеличение риска развития сердечно-сосудистых заболеваний, однако при ретроспективном исследовании 333 пациентов с гипопитуитаризмом выявлено, что в течение 22 лет случаи кардиоваскулярной смерти встречались в два раза чаще по сравнению с группой контроля. При проведении эхокардиографии исследователи обнаруживали снижение массы левого желудочка, уменьшение толщины перегородки и задней стенки желудочков, а также снижение фракции выброса левого желудочка.
Еще сравнительно недавно проблема дефицита ГР у взрослых не находила отражения в исследованиях эндокринологов, хотя вопросы, связанные с недостаточностью секреторной функции гипофиза, возникали с того времени, когда были впервые описаны пациентки с синдромом Шиена (Шихана). Данная патология обусловлена развитием инфарктов и кровоизлияний в раннем послеродовом периоде и характеризуется развитием пангипопитуитаризма. Долгие годы пациентки получали заместительную гормональную терапию глюкокортикоидами, тиреоидными гормонами, половыми стероидами, однако при этом продолжали предъявлять неспецифические жалобы на повышенную утомляемость, слабость, немотивированное увеличение массы тела. При попытке исследовать уровень гормонов сыворотки крови с целью выяснения степени компенсации имеющихся нарушений патологических отклонений обнаружено не было, а сниженному уровню ГР не придавали значения. В дальнейшем многочисленные клинические и лабораторные исследования продемонстрировали, что снижение секреции ГР в организме взрослого человека приводит к целому ряду нарушений, которые остаются незамеченными и не имеют такой яркой клинической окраски, как, например, гиперсекреция ГР и развивающаяся вследствие этого акромегалия.
Перечислим причины развития соматотропной недостаточности у взрослых
Количество пациентов, подвергшихся тем или иным вмешательствам на селлярной области, растет год от года, и связано это с повышением разрешающей способности диагностических методов, используемых при обследовании больных, и расширением лечебных возможностей современной медицины. Исходя из этого можно прогнозировать, что количество пациентов, нуждающихся в проведении скринингового обследования ДГР, будет увеличиваться год от года. Современная фармакология, в свою очередь, располагает целым спектром препаратов, призванных компенсировать соматотропную недостаточность; ниже приводится перечень средств, имеющихся на сегодняшний день в отечественной аптечной сети.
«Золотым стандартом» в диагностике ДГР у взрослых справедливо считается инсулинотолерантный тест. Необходимо оговориться, что его проведение возможно только после компенсации вторичного гипотиреоза и вторичного гипокортицизма, в противном случае результаты теста могут быть недостоверными.
В рамках исследования, проведенного в клинике эндокринологии ММА им. И. М. Сеченова и посвященного изучению целесообразности назначения препарата генноинженерного гормона роста взрослым, была обследована группа больных с подозрением на наличие соматотропной недостаточности.
В группу вошли 15 человек в возрасте от 15 до 45 лет: 12 женщин (80%) и трое мужчин (20%). Девять женщин (60%) были прооперированы по поводу макропролактином гипофиза, трое мужчин (20%) и трое женщин (20%) подверглись оперативному вмешательству по поводу краниофарингиомы гипофиза, у одного мужчины (6,7%) при проведении МРТ выявлена агенезия гипофиза. Среди всех обследованных пациентов задержка роста зафиксирована у троих мужчин (20%) в возрасте 16, 21 и 27 лет, оценка роста у них проводилась с использованием таблицы «Перцентильный график роста для мальчиков». У первого пациента рост был равен 148 см, при оценке перцентильных значений величина стандартного отклонения (SDS) составила –3,5. Рост второго и третьего пациентов был равен 145 и 152 см соответственно, но в связи с невозможностью оценить величину SDS исходя из паспортного возраста последняя была рассчитана исходя из костного. В первом случае паспортный возраст ровнялся 13-14 годам и SDS –2, во втором случае костный возраст соответствовал 16 годам и SDS –3. Структура эндокринных заболеваний, выявленных у пациентов с подозрением на соматотропную недостаточность, отражена в табл. 2.
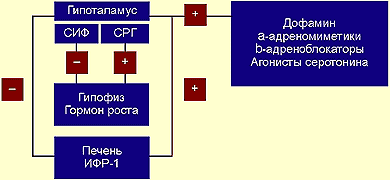 |
| Регуляция секреции гормона роста |
Перед проведением провокационных тестов, направленных на диагностику соматотропной недостаточности, всем пациентам был проведен комплекс лабораторно-диагностических мероприятий для уточнения соматического и гормонального статуса пациентов.
Большинство пациентов получали заместительную гормональную терапию по поводу вторичного гипотиреоза, вторичной надпочечниковой недостаточности, несахарного диабета; у всех было проведено скрининговое исследование концентрации свободного Т4, пролактина, ЛГ, ФСГ, эстрадиола с целью коррекции доз получаемых препаратов.
Исследование соматического статуса предусматривало определение следующих показателей: расчет индекса массы тела (ИМТ), вычисление отношения объем талии/объем бедер (ОТ/ОБ), определение уровня глюкозы, холестерина, триглицеридов, ЛПНП, ЛНВП, АЛТ, АСТ. Проводилось ЭКГ и измерение артериального давления с целью исключения патологии со стороны сердечно-сосудистой системы.
Для оценки качества жизни пациентов с рассматриваемой патологией использовался опросник, разработанный специально для пациентов с дефицитом ГР — QoL-AGHDA (Quality of Life — Assessment of Growth Hormone — Deficiency in Adults) и содержащий 25 вопросов, на которые необходимо было ответить «да» или «нет». Каждый положительный ответ оценивался в один балл; чем больше оказывалась полученная в результате сумма, тем ниже показатель качества жизни.
В ходе обследования были получены следующие результаты.
Нормальные показатели ИМТ (18 30) диагностировано у четырех человек (26,7%). У одного пациента наряду с задержкой роста был выявлен дефицит массы тела, ИМТ составил 15,9 (6,7%). У одной пациентки (6,7%) обнаружен сахарный диабет II типа. Признаки висцерального ожирения выявлены у четырех пациенток (26,7%).
При обследовании у шести пациенток обнаружено повышение гликемии натощак, которое составило 7,025 ± 0,12 ммоль/л; показатели гликемии у 11 пациентов были в пределах нормы и варьировали от 3,6 до 5,5 ммоль/л. Для исключения возможных нарушений углеводного обмена: тощаковой гипергликемии, нарушения толерантности к углеводам, сахарного диабета, гиперинсулинемии всем пациентам был проведен оральный глюкозотолерантный тест с 75 г глюкозы. При определении гликемии через 2 часа после приема 75 г глюкозы последняя составила 6,6 ± 0,14 ммоль/л. Сахарный диабет был выявлен у одной пациентки (гликемия 11,9 ммоль/л), еще у двоих пациентов определено нарушение толерантности к углеводам (гликемия 8,3 и 9,0 ммоль/л). При исследовании уровня С-пептида сыворотки крови были получены следующие результаты: базальная гиперинсулинемия (>2,5 нг/мл) обнаружена у пяти пациентов (3,33%) и составила 3,89 ± 0,1 нг/мл. Более чем двукратное увеличение концентрации С-пептида через 120 минут после стимуляции отмечено у девяти пациентов (60%) и составило 10,5 ± 0,4 нг/мл. При оценке липидного обмена гиперхолестеринемия выявлена у десяти пациентов (66,6%), гипертриглицеридемия обнаружена у семи пациентов (46,6%).
Всем пациентам был проведен инсулинотолерантный тест с целью подтверждения дефицита гормона роста. В условиях стационара пациентам внутривенно вводился инсулин короткого действия: Humulin R или Actrapid HM, из расчета 0,1 ЕД/кг [1]. Исходно через каждые 15 минут в дальнейшем пациентам проводилось определение гликемии в капиллярной крови и забор крови для последующего выявления уровня гормона роста в сыворотке крови.
В ответ на инсулин-индуцированную гипогликемию у 12 обследованных (80%) концентрация ГР не превысила 5 нг/мл, а составила в среднем 0,76 ± 0,013 нг/мл. У троих на фоне гипогликемии было зарегистрировано повышение уровня ГР до 30,78 ± 0,45 нг/мл.
По результатам проведенного теста девяти пациентам была назначена терапия генотропином (Pharmacia&Upjohn). Двое пациентов с задержкой роста получают препарат в настоящее время, у семи человек завершился шестимесячный курс терапии. При расчете дозы препарата использовались рекомендации Janssen и соавт., дозировка генотропина определялась из расчета 0,018 МЕ/кг для шести пациентов, а для трех пациентов с задержкой роста доза была вычислена из расчета 0,1 МЕ/кг [2].
Спустя 6 месяцев после начала терапии все пациенты прошли повторное обследование. Сколько-нибудь значимых изменений ИМТ отмечено не было, показатель ОТ/ОБ снизился у пяти человек, у двоих он остался на прежнем уровне. У троих пациентов выявлено некоторое снижение концентрации холестерина, составившее 8,4, 9,7 и 26,6% от первоначального уровня. У троих пациентов не определено каких-либо изменений, у одного пациента выявлено повышение концентрации холестерина на 17% от исходного. По показателям содержания триглицеридов выявлены следующие данные: у четверых пациентов снижение ТГ составило 56,4, 47,2, 3,7 и 6,3% от исходного. В одном случае динамики отмечено не было, а у двоих человек зафиксировано повышение концентрации ТГ, составившее 68 и 92% от исходного уровня. Снижение уровня ТГ и холестерина на фоне терапии генотропином подтверждается данными зарубежных исследователей, демонстрирующих нормализацию показателей липидного обмена на фоне заместительной терапии.
Перед началом терапии средний показатель качества жизни составил 12,5 балла, а на последней неделе терапии он снизился до 8,9 балла (необходимо отметить, что, по данным Holmes и соавт., у здоровых пациентов, обследованных в Швеции, он составляет 3,7).
Пациент с задержкой роста за 6 месяцев лечения вырос на 5 см, и его рост на момент окончания терапии составил 157 см.
Среди зафиксированных пациентами побочных эффектов чаще всего встречались: отеки, артралгии и миалгии, которые развивались на 3-6-й неделе терапии; о них сообщили четверо пациентов. Аналогичные данные демонстрируют и зарубежные исследователи, проводившие наблюдения за более многочисленными группами пациентов, получавших ГР.
По результатам проведенного исследования можно сделать следующие выводы.
Литература
1. Алгоритмы диагностики и лечения болезней эндокринной системы/ Под ред. И. И. Дедова, 1997.
2. Дедов И. И., Тюльпаков А. Н., Петеркова В. А. Соматотропная недостаточность, 1998.
3. Monson J. P. Growth Hormone Therapy. Oxf, 1999. Р. 93-103.
Гормон роста: проба, нормы, избыток, недостаток
В статье мы расcкажем:
Тест на гормон роста человека – один из наиболее специфических, потому что одной пробы крови недостаточно, чтобы получить полную картину уровня соматропина в организме.
GH секретируется гипофизом импульсов, и его концентрация зависит от времени суток. Во время сна тело вырабатывает его больше всего. Эндокринные нарушения приводят к низкому росту, гигантизму или акромегалии. В свою очередь, инъекции гормона роста рекомендуются на интернет-форумах людьми, занимающимися спортом или упражнениями на выносливость, потому что GH способствует сжиганию жира и увеличивает мышечную массу.

Гормон роста ( соматропин ) – это гормон, вырабатываемый клетками гипофиза. Секреция соматропина зависит от возраста и пола, и его основная функция – анаболическая стимуляция набора веса, роста и обмена веществ. Слишком низкий или слишком высокий уровень соматропина может привести к задержке роста. У детей с дефицитом гормона роста можно использовать лечение рекомбинантным человеческим соматропином.
Как работает соматропин?
Гормон роста (GH) или соматропин – это полипептидный гормон, состоящий примерно из 191 аминокислоты, вырабатываемый передней долей гипофиза в ответ на регулирование соматостатином (ингибирование GH) и соматолиберином (увеличение его секреции).
Соматотропин посредством инсулиноподобного фактора роста (IGF-1) стимулирует рост тканей, эпифизарных хрящей длинных костей и органов тела, кроме того, он стимулирует синтез нуклеиновых кислот, усиливает процессы деления клеток и белка и влияет на липолиз и гипергликемию.
Секреция соматропина зависит от пола, возраста и состояния питания пациента и является пульсирующей и также зависит от времени суток. Ночью и во время сна организм производит больше всего гормона роста.
Нарушения выработки гормона роста в основном связаны с повреждением и дисфункцией гипофиза и могут привести к недоразвитию пациента. Тесты на уровень соматропина выполняются для: диагностики причин низкого роста или гигантизма у детей или слишком высокого роста – акромегалии у взрослых, в случае подозрения на опухоль гипофиза, продуцирующую гормоны (включая GH), и в ходе лечение пациентов рекомбинантным гормоном роста.
Симптомы и последствия дефицита гормона роста
Симптомы и последствия дефицита соматропина различаются в зависимости от возраста пациента, у детей и у взрослых.
Дефицит гормона роста у детей
Дети с дефицитом соматропина в первую очередь характеризуются слишком маленьким для своего возраста ростом и задержкой в физическом развитии. Кроме того, слишком низкий уровень гормона роста у детей может сопровождаться гипогликемией, длительной желтухой, отложением жира в брюшной полости.
Дефицит гормона роста у взрослых
Дефицит соматропина у взрослых проявляется в виде плохого настроения, чувства постоянной усталости и нехватки энергии для жизни. У пациентов наблюдается снижение мышечной массы, силы и выносливости с одновременным увеличением количества абдоминального жира, бледностью и истончением слоев кожи и увеличением количества морщин, истончением волос на голове и всем теле, снижением активности потовых желез. Лабораторные и визуальные исследования показывают нарушения липидного обмена (повышение уровня холестерина и триглицеридов, снижение уровня «хорошего» холестерина ЛПВП), снижение плотности костей, приводящее к остеопорозу, нарушение функции почек и атрофические изменения мышц левого желудочка.
Избыток гормона роста у детей
Повышенный уровень гормона роста у детей приводит к гигантизму, который характеризуется разрастанием длинных костей (например, бедра, голени, плечевой кости) и тканей. В результате невылеченного гипофизарного гигантизма ребенок может вырасти более чем до 210 сантиметров за короткое время. Гипертония или задержка полового созревания также могут быть симптомами, связанными с гигантизмом.
Избыток гормона роста у взрослых
Избыток гормона роста у мужчин и женщин, у которых уже завершился рост длинных костей, может привести к акромегалии, то есть разрастанию мягких тканей, включая стопы, руки, челюсть, нос, уши, а также увеличение сердца или языка. Слишком высокий уровень соматропина у взрослых также может вызывать деформации, гипертрофию и боль в суставах и костях, увеличение внутренних органов, повышенное потоотделение, гирсутизм и утолщение кожи, а также диабет с инсулинорезистентностью.

Соматропин – как выглядит тест на гормон роста? Как к нему подготовиться?
Один тест на GH имеет небольшую диагностическую ценность. Поэтому соответствующий тест на уровень гормона роста обычно заключается в заборе крови из локтевого сгиба пациента несколько раз. Тест следует проводить в одно и то же время, предпочтительно утром, после голодания, то есть без еды и питья в течение примерно 8-10 часов.
Для проведения теста пациенту сдают первый образец крови и, в зависимости от цели теста, вводят либо внутривенно/перорально, либо инсулин, глюкагон, клонидин, GHRH с аргинином или L-допа (предшественник дофамина) для стимуляции или глюкозу для определения ингибирования. Затем у него берут еще одну (от 2 до 4) пробу крови для дальнейшего определения уровня соматотропина.
С помощью тестов стимуляции вы можете определить, связана ли причина дефицита или избытка GH с проблемами с гипофизом. Испытания на торможение полезны при проверке, есть ли в опухолях повышенная секреция гормона роста. Стоимость разового определения уровня гормона роста составляет от 15 до 20 долларов, а результат теста – из-за сложной методики – занимает до 4 рабочих дней.
Нормы и расшифровка результатов анализов у новорожденных, детей и взрослых
Из-за высокой вариабельности циркадного ритма и пульсирующего характера секреции гормона роста и зависимости уровня ЛГ, интерпретация одного теста на ЛГ трудна и неуместна из-за сна или бодрствования, физических упражнений, стресса, уровня глюкозы, других гормонов и лекарств.
Добавки. Безопасно ли использование гормона роста?
Благодаря тому, что GH способствует сжиганию жира и увеличивает мышечную массу, добавки с гормоном роста обычно представляют интерес для людей, занимающихся силовыми видами спорта, физическими упражнениями и видами спорта на выносливость.
Использование инъекций или таблеток, содержащих гормон роста, также рекомендуется бодибилдерами на интернет-форумах, но это не безопасно для организма. Длительный прием гормона роста может привести к гипогликемии и увеличению концентрации свободных жирных кислот в плазме, а в крайних случаях даже к развитию акромегалии. Безопаснее принимать добавки, содержащие так называемые предшественники гормона роста и соответствующую диету, повышающую синтез соматропина в организме. Чтобы нарастить мышечную массу, желательно употреблять много белка, содержащегося в яйцах, птице, рыбе и бобовых. Правильная диета в сочетании со сбалансированной физической активностью должна стать ключом к успеху.

Лечение гормоном роста: эффекты и побочные эффекты терапии
Введение рекомбинантного гормона роста человека GH (rhGH) разрешается детям с диагнозом идиопатический гипопитуитаризм, хроническая почечная недостаточность, Синдромы Тернера и Прадера-Вилли, а также в случае недоношенных детей, рожденных с внутриутробной гипотрофией.
Взрослые, которым показана терапия GH, также принимают соматотропин в виде подкожных инъекций, что снижает массу жировой ткани и увеличивает массу мышечной ткани. Лечебную дозу гормона роста врач определяет индивидуально для каждого пациента.
Эффекты терапии гормоном роста, описанные в литературе, показывают, что при раннем начале лечения гормоном роста возможно что в первый год терапии скорость роста ребенка составляет примерно от 8,9 до 9,8 см. Условием безопасной терапии является то, что пациент находится под постоянным наблюдением эндокринолога и проводится полная гормональная диагностика. Уколы гормона роста детям вводят до тех пор, пока эпифизы костей не атрофируются, а лечение взрослых зависит от рекомендаций лечащего врача.
Прием рекомбинантного гормона роста небезразличен для организма и может иметь побочные эффекты, такие как диабет, гипертония или инсулинорезистентность, а также головные боли, тошнота и рвота, нарушения зрения.
Гормон роста в современной клинической практике
Рекомбинантные препараты гормона роста человека используются в клинической эндокринологической практике с 1985 г. Согласно материалам международного научного общества по изучению гормона роста, в настоящее время около 100 тыс. детей во всем мире лечатся рекомбинантным гормоном роста. До этого, начиная с 1958 г., во всех странах использовались исключительно препараты соматотропного гормона (СТГ), полученные экстрактным путем из гипофизов трупов человека. В связи с особенностями приготовления иметь в наличии достаточное количество такого препарата не представлялось возможным. Кроме того, в ходе лечения было показано, что подобная терапия сопряжена с риском развития смертельно опасного недуга, поражающего центральную нервную систему – летальной формы подострого губчатого энцефалита, болезни Крейтцфельдта–Якоба. В связи с этим с 1985 г. использование экстрактных препаратов гормона роста было запрещено.
Современные генно-инженерные технологии производства рекомбинантных препаратов СТГ позволяют получать препарат в значительно большем количестве. Количество производимого препарата достаточно не только для удовлетворения потребности пациентов с дефицитом СТГ, но и позволяет значительно расширить диапазон применения гормона роста для ростостимулирующей терапии при различных вариантах низкорослости, при этом полностью исключается развитие болезни Крейтцфельдта–Якоба.
Физиология гормона роста
Секреция СТГ гипофизом имеет пульсирующий характер с выраженным суточным ритмом. Основное количество СТГ секретируется в ночное время, в начале глубокого сна, что особенно выражено в детстве. Регуляция секреции СТГ осуществляется посредством СТГ-рилизинг гормона (СТГ-РГ) и СТГ-ингибирующего фактора (соматостатин). Их эффекты опосредуются гипоталамическими нейротрансмиттерами, которые оказывают либо стимулирующее (a-адренергические, серотонинергические, дофаминергические рецепторные системы), либо ингибирующее (a-адренергические и серотонинергические антагонисты, b-адренергические агонисты) влияние на секрецию СТГ (1).
Стимулирующие секрецию СТГ эффекты оказывают тиреоидные и половые гормоны, вазопрессин, АКТГ, меланоцитостимулирующий гормон. Глюкокортикостероиды оказывают как стимулирующее (при острой нагрузке высокими дозами), так и тормозящее (при длительном хроническом избытке гормона) влияние на секрецию СТГ.
СТГ является основным гормоном, стимулирующим линейный рост тела. Он способствует удлинению костей, росту и дифференцировке внутренних органов, развитию мышечной ткани. Основные эффекты СТГ на уровне костной ткани состоят в стимуляции роста хряща и синтеза белка, индуцировании митоза клеток. Ростостимулирующие воздействия СТГ опосредуются через инсулиноподобные факторы роста (ИФР-1, ИФР-2), которые синтезируются под влиянием СТГ главным образом в печени.
Влияние СТГ на углеводный и жировой обмен может осуществляться в два этапа: «острого» и «запаздывающего» эффектов. «Острые» эффекты состоят в инсулиноподобном действии (стимуляция гликогенеза в печени, синтез белка в печени и мышцах, утилизация глюкозы в жировой и мышечной ткани), «запаздывающие» эффекты проявляются противоположным действием (стимуляция гликогенолиза, липолиза и торможение утилизации глюкозы тканями).
Гипофизарная карликовость – заболевание, обусловленное врожденной или приобретенной недостаточностью секреции гормона роста (1). Другие названия этого состояния – соматотропная недостаточность, гипофизарный нанизм. Достижения современной медицины позволяют полностью вылечить карликовость путем заместительной терапии при своевременно начатом лечении, при сохранении первичной причины низкорослости – соматотропной недостаточности. В условиях адекватной заместительной терапии и достижении нормального роста пациента более правильным будет постановка диагноза «соматотропная недостаточность».
В последние годы на фоне развития фундаментальных наук (молекулярная генетика, генная инженерия, иммунология и др.) достигнуты значительные успехи в понимании этиологии и патогенеза соматотропной недостаточности.
С внедрением новых технологий рекомбинантного синтеза гормона роста человека коренным образом изменилась судьба людей, страдающих гипофизарной карликовостью: современная диагностика и лечение позволяют им достичь нормального роста. В НИИ детской эндокринологии ЭНЦ накоплен двадцатилетний опыт диагностики и лечения более трех тысяч пациентов с соматотропной недостаточностью.
Различают следующие варианты дефицита СТГ:
Врожденный дефицит гормона роста развивается вследствие первичного нарушения секреции СТГ на уровне гипофиза или гипоталамуса, не способного адекватно стимулировать соматотрофы аденогипофиза. Приобретенная соматотропная недостаточность является чаще всего следствием операций в гипоталамо-гипофизарной области, реже – воспалительных заболеваний этой области.
Нанизм (низкорослость) классифицируют также и на основании уровня нарушений регуляции секреции и действия СТГ: гипоталамический (дефицит биосинтеза и секреции СТГ-рилизинг гормона (СТГ-РГ, соматолиберин)); гипофизарный (первичная патология гипофиза);
тканевой, обусловленный повышением резистентности тканей к действию СТГ (патология рецепторов к СТГ на уровне тканей-мишеней).
Может наблюдаться изолированная соматотропная недостаточность (25%) и множественный дефицит гормонов гипофиза (75%) (при выпадении функции и других гормонов гипофиза). В случаях множественного дефицита гормонов гипофиза наиболее часто встречается сочетание соматотропной недостаточности с вторичными гипотиреозом и гипогонадизмом; реже – СТГ-дефицита с вторичным гипотиреозом и с недостаточной секрецией пролактина, что обусловлено врожденной патологией, вызванной аномалией генов Рit-1 или Prop-1. Реже (10%) снижается или отсутствует секреция адренокортикотропного гормона (АКТГ). Доля больных с пангипопитуитаризмом – полное «выпадение» всех гормонов гипофиза – не превышает 10% всех случаев соматотропной недостаточности.
Частота нанизма в популяции, обусловленного дефицитом СТГ, составляет 1 : 15 000. Наиболее распространенная форма – идиопатическая (65-75%). Вместе с тем по мере совершенствования диагностических методов и использования их в клинической практике (генетические исследования, компьютерная и магнитно-резонансная томография головного мозга) доля детей с идиопатическим дефицитом СТГ уменьшается, в то время как частота выявления патологии, связанной с органическими изменениями в гипоталамо-гипофизарной области, возрастает.
Дети с соматотропной недостаточностью отличаются существенным отставанием в росте, задержкой скорости роста и костного созревания при сохранении нормальных пропорций тела. Вследствие недоразвития костей лицевого черепа, для пациентов характерно «кукольное» лицо: мелкие черты лица, широкий выступающий лоб и запавшая переносица. Также обращают на себя внимание тонкие волосы и высокий голос. Нередко наблюдается избыток веса, сочетающийся с нарушением «состава тела»: избыточное развитие жировой и недостаточное развитие мышечной ткани. Для детей с ранним проявлением дефицита роста (до 1 года жизни) ожирение не характерно. У мальчиков, как правило, отмечается микропенис (1). При изолированной соматотропной недостаточности наблюдается задержка полового развития.
При пангипопитуитаризме к клинической симптоматике, представленной выше, присоединяются симптомы выпадения других гормонов гипофиза (тиреотропного гормона – ТТГ, АКТГ, лютеинизирующего гормона – ЛГ, фолликулостимулирующего гормона – ФСГ, вазопрессина).
Однократное определение СТГ в крови для диагностики соматотропной недостаточности не имеет существенного диагностического значения вследствие эпизодического характера секреции СТГ и из-за возможности получения крайне низких (нулевых) базальных значений СТГ даже у здоровых детей. В связи с этим используется определение пика выброса СТГ на фоне стимуляции, исследование ИФР-1 и его связывающего белка в крови. Провокационные тесты основаны на способности различных фармакологических препаратов стимулировать секрецию и выброс СТГ соматотрофами.
Помимо стимулированных уровней СТГ, диагностическое значение в выявлении соматотропной недостаточности у детей имеет уровень ИФР-1 (соматомедина С). Концентрация ИФР-1 в сыворотке крови не подвержена таким резким пиковым колебаниям, как СТГ, в связи с чем возможно его однократное определение. Снижение уровня ИФР-1 в сыворотке крови косвенно свидетельствует о наличии СТГ-дефицита и необходимости проведения СТГ-стимуляционных тестов.
В современной клинической практике наиболее широко используются пробы с инсулином, клонидином, СТГ-РГ, аргинином, леводопой. Любой из перечисленных выше стимуляторов способствует значительному выбросу (свыше 10 нг/мл) гормона роста у 75-90% здоровых детей. Тотальная соматотропная недостаточность диагностируется в случае пика выброса СТГ на фоне стимуляции менее 7 нг/мл, частичный дефицит – при пике выброса СТГ от 7 до 10 нг/мл (2, 3, 6).
При лечении гипофизарного нанизма у детей отмечается четкий дозозависимый эффект, особенно выраженный в первый год лечения. Рекомендуемой стандартной расчетной дозой гормона роста при терапии дефицита СТГ является 0,033 мг/кг/сутки. Препарат вводится подкожно в плечи и бедра однократно ежедневно в вечернее время (20.00-22.00) (4). Доза титруется по весу и уровню ИФР-1 в сыворотке 1 раз в 6 месяцев.
Критерием эффективности терапии является увеличение скорости роста (от имевшейся до начала лечения) в несколько раз. Максимальная скорость роста отмечается в первый год лечения (по данным разных авторов, средняя скорость роста составляет от 8 до 13 см/год – так называемые «догоняющие» темпы роста), затем она постепенно замедляется (5).
Опыт НИИ детской эндокринологии ЭНЦ по лечению детей с гипофизарным нанизмом генно-инженерными препаратами гормона роста и зарубежный опыт различных эндокринологических клиник свидетельствуют о высокой эффективности заместительной терапии рекомбинантными препаратами гормона роста человека (рГР). При рано начатом и регулярном лечении возможно достижение нормальных, генетически запрограммированных величин роста.
Помимо увеличения линейного роста, в процессе терапии СТГ возникают определенные изменения в гормональном, метаболическом, психическом статусе пациентов. Гормон роста оказывает влияние на все виды метаболизма: белковый, жировой, углеводный, минеральный. Метаболические эффекты проявляются в первую очередь увеличением мышечной массы и мышечной силы, активизацией липолиза и уменьшением объема жировой ткани. В крови снижаются уровни липопротеидов низкой плотности (ЛПНП), увеличиваются в пределах нормы уровни щелочной фосфатазы, фосфора, мочевины, свободных жирных кислот. Под влиянием СТГ происходит улучшение почечного кровотока, повышение сердечного выброса, увеличение всасываемости кальция в кишечнике и минерализация костей. Повышается жизненный тонус пациентов, значительно улучшается качество жизни.
Лечение рГР не вызывает быстрого прогрессирования костного созревания. Терапию рГР проводят до момента закрытия зон роста или достижения его социально-приемлемой величины. Клиническим ориентиром служит скорость роста не менее 2 см в год (6).
В соответствии с распоряжением Правительства РФ от 31.12.2008 г. №2053-Р, дети с доказанным гипофизарным нанизмом подлежат бесплатному обеспечению рГР, входящим в перечень централизованно закупаемых за счет средств федерального бюджета лекарственных средств.
Гормон роста синтезируется в течение всей жизни. Для взрослого человека он необходим как анаболический гормон, препятствующий процессам старения, улучшающий сократительную функцию сердца, функцию печени, почек, повышающий минеральную плотность костной ткани и мышечный тонус. Поэтому в настоящее время заместительная терапия гормоном роста при доказанной соматотропной недостаточности показана на протяжении всей жизни. После закрытия зон роста гормон роста применяется в метаболической дозе, которая в 7-10 раз меньше ростостимулирующей и составляет 0,0033 мг/кг/сут. (5).
Первый отечественный опыт использования заместительной терапии при закрытых зонах роста у взрослых с соматотропной недостаточностью, полученный в ЭНЦ, показал безопасность и высокую метаболическую эффективность такого лечения.
Термин идиопатическая низкорослость применим к детям, чей рост значительно отстает от возрастной нормы (ниже двух стандартных отклонений, 2SD) по неизвестной или наследственной причине. Это гетерогенная группа детей, низкий рост которых не может быть объяснен наличием какой-либо патологии и отвечает следующим минимальным критериям:
Идиопатическая низкорослость может быть подразделена на три категории:
Конституциональная задержка роста и пубертата, так же как семейная низкорослость, укладываются в понятие вариантов нормального роста. Дети от родителей с низким ростом, как правило, за счет генетически запрограммированных потенций роста низкорослы в той же степени, что и их родители. Ребенок от родителей, в анамнезе которых имеется задержка роста и пубертата, с большой степенью вероятности унаследуют этот характер развития.
Дети с конституциональной задержкой роста и пубертата имеют нормальный рост и вес при рождении, нормальные темпы роста до 1-2 лет. В старшем возрасте скорость роста снижается, кривая ее динамики находится ниже 3 перцентили или параллельна ей. Костный возраст, как правило, соответствует возрасту роста, скорость роста составляет не менее 5 см/год. Стимулированная секреция СТГ нормальная – более 10 нг/мл, интегрированная суточная секреция СТГ, как правило, снижена. Пубертат нормальный, но задержан во времени на сроки отставания костного возраста и наступает при достижении костного созревания у мальчиков 11,5-12 лет, у девочек – 10,5-11 лет. Сроки достижения конечного роста сдвинуты во времени, конечный рост обычно нормальный без гормональной терапии.
Соматопауза — дефицит гормона роста у взрослых
Гормон роста (соматотропин, GH, STH), выделяемый гипофизом, имеет хорошо документированное значение для стимулирования роста в детском возрасте, но это не единственная его роль.
Дефицит гормона роста в зрелом возрасте проявляется такими неблагоприятными последствиями, как:
Старение организма и соматопауза
К сожалению, одним из первых последствий старения, связанных с эндокринной системой, является соматопауза — постепенное снижение секреции гормона роста гипофизом. Появляется соматопауза довольно рано — в возрасте 30-40 лет.
Последствия дефицита соматотропина: рост живота, снижение физической подготовки, ухудшение либидо, особенно заметны для сильного пола из-за явной чувствительности каждого мужчины к признакам «мужественности», а также к склонности к абдоминальному ожирению и атеросклерозу, вызванным другими факторами.
» data-medium-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/01/Ухудшение-либидо.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/01/Ухудшение-либидо.jpg?fit=825%2C550&ssl=1″ loading=»lazy» src=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/01/%D0%A3%D1%85%D1%83%D0%B4%D1%88%D0%B5%D0%BD%D0%B8%D0%B5-%D0%BB%D0%B8%D0%B1%D0%B8%D0%B4%D0%BE.jpg?resize=900%2C600&ssl=1″ alt=»Ухудшение либидо» width=»900″ height=»600″ srcset=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/01/Ухудшение-либидо.jpg?w=900&ssl=1 900w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/01/Ухудшение-либидо.jpg?resize=450%2C300&ssl=1 450w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/01/Ухудшение-либидо.jpg?resize=825%2C550&ssl=1 825w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/01/Ухудшение-либидо.jpg?resize=768%2C512&ssl=1 768w» sizes=»(max-width: 900px) 100vw, 900px» data-recalc-dims=»1″/> Ухудшение либидо
Таким образом, по аналогии с менопаузальной заместительной гормональной терапией,у многих возникает мысль о предотвращении последствий соматопаузы путем введения гормона роста. Значит ли это, что эндокринологи нашли рецепт продления молодости и жизненной силы? Увы, при назначении гормона роста обычно возникает много трудностей, например, очень высокая цена лечения.
Гормон роста выделяется пульсирующим (прерывистым) образом, и процесс соматопаузы развивается постепенно. Чтобы определить, есть ли дефицит гормона роста, лучше всего проводить тесты стимуляции (измерение уровня гормона роста после стимуляторов). Эти тесты утомительны, трудоемки и дороги.
Излишне говорить, что в настоящее время гормон роста используется спортивной псевдомедициной как «почти идеальный» допинг-агент, который увеличивает мышечную массу и физическую работоспособность.
» data-medium-file=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/01/Гормон-роста.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/01/Гормон-роста.jpg?fit=825%2C550&ssl=1″ loading=»lazy» src=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/01/%D0%93%D0%BE%D1%80%D0%BC%D0%BE%D0%BD-%D1%80%D0%BE%D1%81%D1%82%D0%B0.jpg?resize=900%2C600&ssl=1″ alt=»Гормон роста» width=»900″ height=»600″ srcset=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/01/Гормон-роста.jpg?w=900&ssl=1 900w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/01/Гормон-роста.jpg?resize=450%2C300&ssl=1 450w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/01/Гормон-роста.jpg?resize=825%2C550&ssl=1 825w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/01/Гормон-роста.jpg?resize=768%2C512&ssl=1 768w» sizes=»(max-width: 900px) 100vw, 900px» data-recalc-dims=»1″/> Гормон роста
Известно также, что используются препараты не очень высокого качества, полученные путем модификации плацентарного гормона HCS, а не с помощью современного метода генной инженерии. Эти препараты содержат примесь другого плацентарного гормона ХГЧ (который стимулирует выработку тестостерона яичками) — при их использовании происходит повышение уровня тестостерона и многие другие побочные эффекты. Такое произошло с известным спортсменом Бен Джонсоном.
Поэтому эндокринологи, прежде чем назначать какие-либо лекарства, досконально обследуют пациента. Диагноз должен быть подтвержден на 100%. Это не должно быть временное снижение гормона или ухудшение состояния по какой-либо причине, кроме возрастной. Дальше должен осуществляться строгий подбор препарата и его дозы. Самостоятельно принимать любые лекарства этого ряда строго запрещено.
Добавить комментарий Отменить ответ
Вы должны быть авторизованы, чтобы оставить комментарий.
Гормон роста в современной клинической практике
В последние годы на фоне развития фундаментальных наук (молекулярная генетика, генная инженерия, иммунология и др.) достигнуты значительные успехи в понимании этиологии и патогенеза врожденной соматотропной недостаточности. С внедрением новых технологий
В последние годы на фоне развития фундаментальных наук (молекулярная генетика, генная инженерия, иммунология и др.) достигнуты значительные успехи в понимании этиологии и патогенеза врожденной соматотропной недостаточности.
С внедрением новых технологий рекомбинантного синтеза гормона роста человека коренным образом изменилась судьба людей, страдающих гипофизарной карликовостью.
С 1985 г. в клинической практике используются рекомбинантные препараты гормона роста человека. Согласно материалам международного научного общества по изучению гормона роста (2001), около 100 000 детей во всем мире получают лечение рекомбинантным гормоном роста человека. До этого, начиная с 1958 г., во всех странах использовались исключительно препараты соматотропного гормона (СТГ), полученные экстрактным путем из гипофизов трупов человека. Понятно, что иметь в наличии достаточное количество препарата не представлялось возможным. Кроме того, было показано, что подобное лечение сопряжено с риском развития смертельно опасного недуга, поражающего центральную нервную систему — болезни Крейтцфельдта–Якоба. С 1985 г. использование экстрактных препаратов гормона роста было официально запрещено.
Практически неограниченные возможности получения генно-инженерных препаратов СТГ выводят на новый, современный уровень лечение и мониторинг пациентов с соматотропной недостаточностью, что обеспечивает достижение нормального роста и полноценного качества жизни этих людей.
Различают врожденный и приобретенный дефицит СТГ; органический (как результат внутричерепного повреждения различной этиологии) и идиопатический (при отсутствии какой-либо специфической органической патологии гипоталамо-гипофизарной области). Врожденный дефицит гормона роста развивается вследствие первичного нарушения секреции СТГ на уровне гипофиза или гипоталамуса, не способного адекватно стимулировать соматотрофы аденогипофиза. Приобретенная соматотропная недостаточность является чаще всего последствием операции на гипоталамо-гипофизарной области, реже — воспалительных заболеваний этой области.
Различают также формы нанизма — в зависимости от нарушения уровня регуляции секреции и действия СТГ: гипофизарный (первичная патология гипофиза); гипоталамический (дефицит биосинтеза и секреции СТГ-рилизинг-фактора (СТГ-РФ)); тканевая резистентность к действию СТГ (патология рецепторов к СТГ на уровне тканей-мишеней). Соматотропная недостаточность может быть изолированной (25%) и множественной (75%), когда выпадает функция и других гормонов гипофиза. В случае множественного дефицита гормонов гипофиза наиболее часто встречается сочетание соматотропной недостаточности со вторичным гипотиреозом и вторичным гипогонадизмом, реже — СТГ-дефицит и вторичный гипотиреоз с недостаточной секрецией пролактина, что обусловлено врожденной поломкой гена РIT-1 или гена PROP-1. Реже снижается или совсем не осуществляется секреция адренокортикотропного гормона (АКТГ) (10%). Пангипопитуитаризм — «выпадение» функции всех гормонов гипофиза — не превышает 10%.
Частота нанизма, обусловленного дефицитом СТГ гипофиза, составляет 1:15 000 (Vimpani et al., 1977). Наиболее распространенная форма — идиопатическая (65–75%). Вместе с тем по мере совершенствования диагностических методов и использования их в клинической практике (генетические исследования, компьютерная и магнитно-резонансная томография головного мозга) доля детей с идиопатическим дефицитом СТГ уменьшается, в то время как частота диагностируемых органических причин дефицита СТГ возрастает. Классификация этиологии соматотропной недостаточности представлена ниже.
I. ВРОЖДЕННЫЙ ДЕФИЦИТ СТГ.
Изолированный дефицит СТГ.
А. Мутации гена гормона роста (GH-1).
1) Тип IA: Делеция гена СТГ, аутосомно-рецессивный тип наследования.
2) Тип IБ: Аутосомно-рецессивный тип наследования.
3) Тип II: Аутосомно-доминантный тип наследования.
4) Тип III: Х-связанная рецессивная форма наследования.
Б. Мутации гена рецептора к СТГ-РФ (GHRH-R).
Множественный дефицит гормонов аденогипофиза.
1) Мутации гена P1T-1.
2) Мутации гена PROP-1.
1) Патология срединной трубки:
2) Дисгенезия гипофиза:
— врожденная аплазия гипофиза;
— врожденная гипоплазия гипофиза;
II. ПРИОБРЕТЕННЫЙ ДЕФИЦИТ СТГ.
— глиома зрительного перекреста.
— хирургическое повреждение гипофизарной ножки.
— вирусный, бактериальный энцефалит и менингит;
— неспецифический (аутоиммунный) гипофизит.
— аневризмы сосудов гипофиза;
— лейкемия, медуллобластома, ретинобластома;
— другие опухоли головы и шеи;
— общее облучение всего тела (например, при пересадке костного мозга).
— конституциональная задержка роста и пубертата;
— психосоциальный (депривационный) нанизм.
III. ПЕРИФЕРИЧЕСКАЯ РЕЗИСТЕНТНОСТЬ К ДЕЙСТВИЮ СТГ
Секреция СТГ гипофизом имеет пульсирующий характер с выраженным суточным ритмом. Основное количество СТГ секретируется в ночное время в начале глубокого сна, что особенно выражено в детстве.
Регуляция секреции СТГ осуществляется посредством СТГ-РФ (соматолиберина) и СТГ-ингибирующего фактора (соматостатина). Их эффекты опосредуются гипоталамическими нейротрансмиттерами, которые оказывают либо стимулирующее (α-адренергические, серотонинергические, дофаминергические рецепторные системы), либо ингибирующее (α-адренергические и серотонинергические антагонисты, β-адренергические агонисты) влияние на секрецию СТГ.
Стимулирующие эффекты на секрецию СТГ оказывают тиреоидные и половые гормоны, вазопрессин, АКТГ, меланоцитостимулирующий гормон. Глюкокортикостероиды оказывают как стимулирующее (при острой нагрузке высокими дозами), так и тормозящее (при длительном хроническом избытке гормона) влияние на секрецию СТГ.
СТГ является основным гормоном, стимулирующим линейный рост. Он способствует росту костей в длину, росту и дифференцированию внутренних органов, развитию мышечной ткани. Основные эффекты СТГ на уровне костной ткани состоят в стимуляции роста хряща и синтеза белка, индуцировании митоза клеток. Ростстимулирующие воздействия СТГ опосредуются через инсулинподобные факторы роста (ИФР-I, ИФР-II), которые синтезируются главным образом в печени под влиянием СТГ.
Влияние СТГ на углеводный и жировой обмен может осуществляться в два этапа — «острых» и «запаздывающих» эффектов. «Острые» эффекты состоят в инсулинподобном действии — стимуляции гликогенеза в печени, синтезе белка в печени и мышцах, утилизации глюкозы в жировой и мышечной ткани. «Запаздывающие» эффекты проявляются противоположным действием — стимуляцией гликогенолиза, липолиза, торможением утилизации глюкозы тканями.
Диагностика СТГ-дефицита
Тщательно собранный анамнез крайне важен на начальном этапе обследования. При сборе анамнеза следует уточнить следующие моменты.
Сроки появления задержки роста. Пренатальная задержка роста характерна для детей с внутриутробной задержкой роста, с генетическими синдромами, хромосомной патологией, наследственным СТГ-дефицитом вследствие делеции гена СТГ. Для детей с классической соматотропной недостаточностью характерна постнатальная задержка роста. В случае врожденного СТГ-дефицита патология в росте отмечается с первых месяцев жизни. У 70–80% детей с гипофизарным нанизмом отставание в росте проявляется до 5-летнего возраста.
Для детей с органическим генезом дефицита СТГ (краниофарингиома, посттравматический и др.) характерны более поздние сроки проявления дефицита роста — после 5–6-летнего возраста.
Перинатальная патология. При идиопатическом СТГ-дефиците выявляется высокая частота перинатальной патологии с асфиксией и фетальным дистрессом вследствие травмы в родах при ягодичном и ножном предлежании, наложении акушерских щипцов, вакуум-экстракции, стремительных или, наоборот, длительных родов.
Гипогликемии. Наличие в анамнезе гипогликемий натощак характерно для детей раннего возраста с врожденным СТГ-дефицитом. В 10% случаев гипогликемии выявляются клинически, вплоть до судорожных синдромов. В большинстве случаев необходимо выявить эквиваленты гипогликемии — потливость, беспокойство, повышенный аппетит.
Семейный анамнез. У детей с транзиторным СТГ-дефицитом (конституциональная задержка роста и пубертата) семейный анамнез позволяет в большинстве случаев выявить аналогичные случаи низкорослости и задержки полового развития в детском и подростковом возрасте у одного из родителей либо ближайших родственников. Наличие у одного из родителей или сибсов гипофизарной карликовости позволяет заподозрить эту же патологию у ребенка.
Хронические заболевания, а также лекарственные препараты, которые могут повлиять на процессы роста. К заболеваниям, которые могут сопровождаться нарушением роста у детей, относятся следующие.
Клиника
На фоне резкого отставания в росте, задержки скорости роста и костного созревания у детей сохраняются нормальные пропорции тела. Вследствие недоразвития костей лицевого черепа черты лица мелкие, переносица западает. Характерно «кукольное» лицо. Волосы тонкие. Голос высокий. Часто встречается избыток веса, однако для детей с ранним проявлением дефицита роста (до 1 года жизни) ожирение не характерно.
У мальчиков, как правило, имеется микропенис. Половое развитие задержано и наступает в сроки, когда костный возраст ребенка достигает пубертатного уровня.
Если имеет место пангипопитуитаризм, то к клинической симптоматике, представленной выше, присоединяются симптомы выпадения других функций гипофиза (тиреотропного гормона (ТТГ), АКТГ, лютеинизирующего гормона (ЛГ), фолликулостимулирующего гормона (ФСГ), вазопрессина). Симптомы снижения функции щитовидной железы при вторичном гипотиреозе выражены, как правило, в меньшей степени, чем при первичном гипотиреозе. В ряде случаев диагноз может быть поставлен только после получения гормональных данных (свободный Т4, ТТГ).
Значительная доля детей с СТГ-дефицитом имеет сопутствующий дефицит гонадотропинов. Клиническая симптоматика подтверждается данными пробы с люлиберином и сниженными уровнями половых гормонов в крови.
Сопутствующий дефицит АКТГ встречается довольно редко и в основном диагностируется лабораторно — по сниженному уровню базального кортизола и АКТГ и значительному выбросу кортизола на фоне пробы с синактеном.
Наличие помимо дефицита роста таких жалоб, как головные боли, нарушение зрения, рвота, позволяет заподозрить внутричерепную патологию (краниофарингиома).
Клинический осмотр позволяет различить: детей с генетическими синдромами (Шерешевского–Тернера, Секкеля, Блума, Рассела–Сильвера и др.); явными формами скелетных дисплазий (ахондроплазии и др.); детей с эндокринной патологией (врожденный гипотиреоз, болезнь Иценко–Кушинга, синдром Мориака); пациентов с нарушенным питанием.
Диагностика многих редких смешанных синдромов первичного нарушения роста и хромосомной патологии основана главным образом на типичном фенотипе (рис. 1).
 |
| Рисунок 1. Синдром Ларона, семейная форма у сестер 6 и 4 лет. Задержка роста, недоразвитие лицевого скелета, выступающий лоб, запавшая переносица, голубые склеры |
Прогерия (синдром Гетчинсона–Гилфорда). Клиническая картина представлена чертами прогрессирующего преждевременного старения. Рост и вес, нормальные при рождении, значительно отстают уже к первому году жизни. Основная симптоматика развивается с 2–3-летнего возраста: тотальная алопеция, атрофия потовых и сальных желез, отсутствие подкожно-жирового слоя, склеродермо-подобные изменения кожи, выраженная венозная сеть на голове, дистрофия ногтей, экзофтальм, тонкий клювовидный нос, малый лицевой и большой мозговой череп. Голос тонкий. Пубертат обычно не наступает. Интеллект средний или выше среднего. Часто диагностируются асептические некрозы головки бедренной кости, вывих тазобедренного сустава. Характерен ранний распространенный атеросклероз коронарных, мезентериальных сосудов, аорты, головного мозга. Продолжительность жизни — в среднем 12–13 лет, основная причина летальности — острый инфаркт миокарда, застойная сердечная недостаточность, инсульты.
Синдром Рассела–Сильвера. Характеризуется внутриутробной задержкой роста, асимметрией туловища (укорочение конечностей с одной стороны), укорочением и искривлением 5-го пальца, «треугольным» лицом, задержкой умственного развития. У трети больных развивается преждевременное половое развитие. Характерны почечные аномалии и гипоспадии.
Синдром Секкеля (птицеголовые карлики). Характеризуется внутриутробной задержкой роста, микроцефалией, гипоплазией лицевого черепа с крупным носом, низким расположением ушей (часто аномально развитых), задержкой умственного развития, клинодактилией 5-го пальца.
Синдром Прадера–Вилли. Дети с этим синдромом, наряду с задержкой роста с рождения, имеют выраженное ожирение, крипторхизм, микропенис, гипоспадию, нарушение толерантности к углеводам, задержку умственного развития.
Синдром Лоуренса–Муна–Барде–Бидля. Включает в себя низкий рост, ожирение, пигментную дегенерацию сетчатки, атрофию дисков зрительных нервов, гипогонадизм, задержку умственного развития. Часто встречаются неполные формы синдрома, с наличием лишь некоторых описанных признаков.
Синдром Шерешевского–Тернера (дисгенезия гонад). Типичная клиническая симптоматика для кариотипа 45ХО представлена сниженной массой тела при рождении, лимфатическим отеком стоп, голеней и кистей у новорожденных, низким уровнем роста волос на шее сзади, короткой шеей с крыловидными складками, бочкообразной грудной клеткой, широко расставленными сосками. Характерны птоз, эпикантус, низкое расположение ушей. Вторичные половые признаки отсутствуют. Костный возраст соответствует паспортному или несколько отстает. В связи с наличием стертых форм данного синдрома, с различными вариантами мозаицизма, у всех девочек с задержкой роста целесообразно проводить исследование кариотипа.
Показатели роста
Рост оценивается по данным перцентильных таблиц стандартов роста и веса, отдельно для мальчиков и девочек.
Помимо абсолютных показателей роста, крайне важным показателем процесса роста является скорость роста. Перцентильные таблицы скорости роста разработаны J. M. Tanner, P. S. W. Davies (1985). У детей с дефицитом СТГ скорость роста не превышает 4 см в год, чаще всего она составляет 1–2 см в год.
Оценка пропорциональности скелета важна в первую очередь для исключения различных форм скелетных дисплазий как генеза нанизма. В частности, целесообразно вычислять коэффициент «верхний сегмент: нижний сегмент», объем размаха рук.
В настоящее время известны различные формы скелетных дисплазий (остеохондродисплазии, диссоциированное развитие хряща и фиброзного компонента скелета, дизостозы и др.). Ахондроплазия является наиболее частой формой хондродистрофий. Клиническая симптоматика типична и включает в себя выраженную задержку роста за счет диспропорционального укорочения конечностей, особенно проксимальных сегментов.
Для определения костного возраста используются два метода: Гролиха и Пайла или Таннера и Уайтхауса. При врожденном дефиците гормона роста костный возраст отстает от паспортного более чем на 2 года.
Рентгенологическое исследование черепа проводится с целью визуализации формы и размеров турецкого седла и состояния костей черепа. При гипофизарном нанизме турецкое седло нередко малых размеров. Характерные изменения турецкого седла имеют место при краниофарингиоме — истончение и порозность стенок, расширение входа, супраселлярные или интраселлярные очаги обызвествления; признаки повышения внутричерепного давления — усиление пальцевых вдавлений, расхождение черепных швов.
Показана компьютерная и магнитно-резонансная томография головного мозга. Морфологические и структурные изменения при идиопатическом гипопитуитаризме включают в себя гипоплазию гипофиза, разрыв или истончение гипофизарной ножки, эктопию нейрогипофиза, синдром «пустого турецкого седла».
Проведение компьютерной и магнитно-резонансной томографии головного мозга необходимо при любом подозрении на внутричерепную патологию (объемный процесс) и всем детям с доказанным дефицитом гормона роста.
Гормональная диагностика дефицита СТГ
Однократное определение СТГ в крови для диагностики соматотропной недостаточности не имеет диагностического значения вследствие эпизодического характера секреции СТГ и из-за возможности получения крайне низких (нулевых) базальных значений СТГ даже у здоровых детей.
В связи с этим используется определение пика выброса СТГ на фоне стимуляции, исследование ИФР и их связывающих белков в крови.
Провокационные тесты основаны на способности различных фармакологических препаратов стимулировать секрецию и выброс СТГ соматотрофами.
В клинической практике наиболее широко используются пробы с инсулином, клонидином, СТГ-РФ, аргинином, леводопой, пиридостигмином (табл.). Любой из перечисленных выше стимуляторов способствует значительному выбросу (свыше 10 нг/мл) гормона роста у 75–90% здоровых детей.
Тотальная соматотропная недостаточность диагностируется в случае пика выброса СТГ на фоне стимуляции менее 7 нг/мл, частичный дефицит — при пике выброса СТГ от 7 до 10 нг/мл.
Необходимое условие проведения СТГ-стимулирующих проб — эутиреоидное состояние щитовидной железы. В случае гипотиреоза необходим предварительный курс лечения тиреоидными препаратами в течение 3–4 нед.
Наиболее диагностически значимой константой в выявлении дефицита СТГ у детей являются ИФР, в частности ИФР-I (соматомедин С) и ИФР-II (соматомедин В). СТГ-дефицит напрямую связан со сниженным уровнем ИФР-I и ИФР-II в плазме крови.
В диагностике соматотропного дефицита у детей высокоинформативным показателем является уровень высокомолекулярного соматомединсвязывающего белка 3. Уровень его в плазме крови зависит от секреции гормона роста и снижен у детей с СТГ-дефицитом.
Важное место в выявлении дефицита СТГ занимает диагностика рецепторной резистентности к СТГ (синдром Ларона). Молекулярная основа данного состояния — патология гена рецептора СТГ. Секреция гормона роста гипофизом не нарушена, но существует рецепторная резистентность к СТГ.
Клиническая симптоматика синдрома Ларона такая же, как при гипофизарном нанизме, но уровень гормона роста при проведении стимуляционных тестов значительно повышен, а уровень ИФР крови сильно снижен.
Для диагностики синдрома Ларона используется ИФР-I- стимулирующий тест. Этот тест заключается в введении генно-инженерного СТГ (0,033 мг/кг/сут, подкожно, в течение 4 дней) и определении уровней ИФР-I и ИФР-связывающего белка 3 до первой инъекции СТГ и через день после окончания пробы. У детей с синдромом Ларона отсутствует повышение уровней ИФР-I и ИФР-связывающего белка-3 на фоне стимуляции, в отличие от пациентов с гипофизарным нанизмом.
Лечение больных с синдромом Ларона гормоном роста неэффективно. Значительный практический интерес представляет терапия детей с этим синдромом рекомбинантным ИФР-I.
Лечение соматотропной недостаточности
С 1985 г. для лечения детей с соматотропной недостаточностью используются исключительно генно-инженерные препараты гормона роста человека.
В настоящее время в России прошли клиническую апробацию и разрешены к использованию следующие рекомбинантные препараты гормона роста человека: В настоящее время в России прошли клиническую апробацию и разрешены к использованию следующие рекомбинантные препараты гормона роста человека: Нордитропин® (НордиЛет®) (Ново Нордиск, Дания); хуматроп (Лилли Франс, Франция); генотропин (Пфайзер Хелс АБ, Швеция); сайзен (Индустрия Фармасьютика Серано С. п. А., Италия); растан (Фармстандарт, Россия).
При лечении гипофизарного нанизма у детей имеется четкая связь «доза–ростовой эффект», особенно выраженная в первый год лечения.
Рекомендуемая стандартная доза СТГ при терапии классического дефицита СТГ — 0,033 мг/кг/на инъекцию, ежедневно, подкожно, в вечернее время 20.00–22.00.
Критерием эффективности терапии является увеличение скорости роста от исходной в несколько раз. Она достигает в первый год лечения, по данным разных авторов, от 8 до 13 см в год. Максимальная скорость роста отмечается в первый год лечения, особенно в первые 3–6 мес, затем имеет место замедление скорости роста от первого ко второму году лечения (при сохранении скорости роста более 5–6 см в год).
 |
| Рисунок 2. Эффективность лечения гормонами роста пациентов с СТГ-дефицитом: а) не леченный гормоном роста, 48 лет, 124 см; б) леченный гормоном роста, 22 года, рост 180 см |
Опыт детской клиники ЭНЦ РАМН по лечению детей с гипофизарным нанизмом различными генно-инженерными препаратами гормона роста и зарубежный опыт различных эндокринологических клиник свидетельствует о высокой эффективности заместительной терапии рекомбинантными препаратами гормона роста человека. При рано начатом и регулярном лечении возможно достижение нормальных, генетически запрограммированных границ роста. На рисунке 2 представлен ребенок с пангипопитуитаризмом, достигший роста 180 см, с сравнении с ростом нелеченного взрослого с той же патологией и конечным ростом 124 см.
Помимо увеличения линейного роста, в процессе терапии гормоном роста отмечаются определенные изменения в гормональном, метаболическом, психическом статусе пациентов. Анаболический, липолитический и антиинсулиновый эффекты проявляются увеличением мышечной силы, улучшением почечного кровотока, повышением сердечного выброса, увеличением всасываемости кальция в кишечнике и минерализации костей. В крови снижаются уровни β-липопротеинов, увеличиваются в пределах нормы уровни щелочной фосфатазы, фосфора, мочевины, свободных жирных кислот. Повышается жизненный тонус пациентов, значительно улучшается качество жизни.
Лечение гормоном роста не вызывает быстрого прогрессирования костного созревания.
Пациенты с изолированным выпадением соматотропной функции имеют спонтанный пубертат по достижении костным возрастом пубертатных значений.
 |
| Рисунок 3. Эффективность лечения рекомбинантным гормоном детей с внутриутробной задержкой роста из тройни: а) до лечения (слева направо: рост первой сестры 104,1 см; брата — 108,5 см; второй сестры — 103,8 см); б) через 12 мес лечения (рост первой сестры 113,9 см; брата — 118,7 см; второй сестры — 114,3 см) |
У детей с пангипопитуитаризмом, помимо лечения гормоном роста, необходима сопутствующая заместительная терапия другими препаратами по показаниям — L-тироксином, глюкокортикостероидами, адиуретином-SD. При дефиците гонадотропинов назначается терапия половыми гормонами: у девочек по достижении костного возраста 11 лет (этинил-эстрадиол, 0,1 мкг/кг, per os, ежедневно), у мальчиков — при костном возрасте 12 лет (препараты тестостерона, 50 мг/м 2 поверхности тела в месяц, в/м — в первый год лечения, 100 мг/м 2 /мес — во второй год лечения, 155 мг/м 2 в месяц — в третий год лечения).
Лечение гормоном роста проводят до закрытия зон роста или достижения социально-приемлемого роста. Клиническим ориентиром служит скорость роста менее 2 см в год.
Гормон роста синтезируется в течение всей жизни. Для взрослого человека он необходим как анаболический гормон, препятствующий процессам старения, улучшающий сократительную функцию сердца, функцию печени, почек, повышающий минеральную плотность костной ткани, мышечный тонус. Поэтому в настоящее время заместительная терапия гормоном роста при доказанной соматотропной недостаточности проводится всю жизнь. После закрытия зон роста гормон роста применяется в метаболической дозе, которая в 7–10 раз меньше ростстимулирующей и составляет 0,0033 мг/кг/сут.
Первый отечественный опыт использования заместительной терапии при закрытых зонах роста у взрослых с соматотропной недостаточностью (И. И. Дедов и соавт., 2004) показал безопасность и высокую метаболическую эффективность такого лечения.
Побочные эффекты
С 1989 г. в ЭНЦ РАМН ведется Национальный регистр детей с соматотропной недостаточностью. Анализ лечения более 3000 пациентов, наблюдающихся в детской клинике ЭНЦ РАМН, показал высокую ростстимулирующую эффективность и безопасность применения гормона роста при данной патологии.
 |
| Рисунок 4. Эффективность лечения рекомбинантным гормоном у ребенка с синдромом Сильвера–Рассела: а) до лечения (рост — 78,2 см); б) через 12 мес. лечения (рост — 89,1 см); в) через 24 мес лечения (рост — 96,2 см). Прибавка в росте + 18 см за 24 мес |
В первые дни лечения возможны отечность век, пастозность голеней, которые проходят в течение 1–2 нед. Это связано с задержкой жидкости. Редко может наблюдаться повышение внутричерепного давления. В этих случаях отменяют гормон роста на несколько дней, после чего продолжают лечение гормоном роста в половинной дозе, постепенно повышая до терапевтической.
Крайне редко наблюдается, значит, теоретически возможно в клинической практике нарушение толерантности к углеводам, в связи с чем необходимо мониторировать уровень глюкозы крови каждые 3 мес терапии.
При приобретенной гипофизарной недостаточности вследствие оперативного лечения краниофарингиомы, гамартомы, аденомы гипофиза, облучения головного мозга и др. лечение гормоном роста назначают через 6–12 мес после оперативного вмешательства при отсутствии продолженного роста или рецидива объемного образования. Двадцатилетний опыт лечения таких пациентов, продемонстрировал эффективность и безопасность использования гормона роста при данной форме соматотропной недостаточности.
Практически неограниченные возможности создания рекомбинантных СТГ человека расширили потенциальные показания к его применению как у детей, так и у взрослых, не ограничиваясь рамками только классического гипофизарного нанизма.
К настоящему времени имеются данные (как зарубежных исследователей, так и наши собственные) об эффективном лечении гормоном роста детей с внутриутробной задержкой роста (рис. 3), семейной низкорослостью, синдромами Шерешевского–Тернера, Прадера–Вилли, Рассела–Сильвера
(рис. 4), анемией Фанкони, болезнью Иценко–Кушинга, гликогенозом, с хронической почечной недостаточностью, скелетными дисплазиями, муковисцидозом.
И. И. Дедов, доктор медицинских наук, профессор, академик РАН и РАМН
В. А. Петеркова, доктор медицинских наук, профессор
Е. В. Нагаева, кандидат медицинских наук
ЭНЦ РАМН, Москва