Рнк что это
Рнк что это
Что такое РНК?
Рибонуклеиновая кислота (РНК) — одна из трёх основных макромолекул (две другие — ДНК и белки), которые содержатся в клетках всех живых организмов.
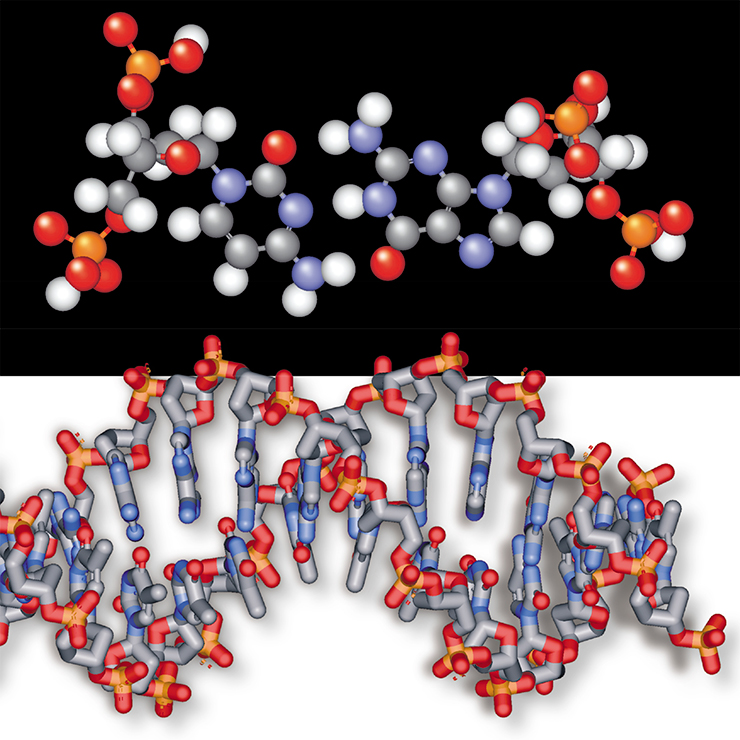
РНК состоит из длинной цепи, в которой каждое звено называется нуклеотидом. Каждый нуклеотид состоит из азотистого основания, сахара рибозы и фосфатной группы. Последовательность нуклеотидов позволяет РНК кодировать генетическую информацию. Все клеточные организмы используют РНК (мРНК) для программирования синтеза белков.
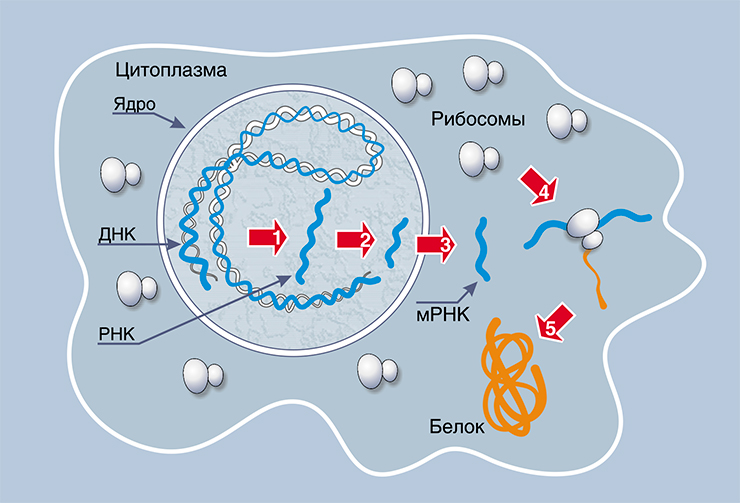
Клеточные РНК образуются в ходе процесса, называемого транскрипцией, то есть синтеза РНК на матрице ДНК, осуществляемого специальными ферментами — РНК-полимеразами. Затем матричные РНК (мРНК) принимают участие в процессе, называемом трансляцией. Трансляция — это синтез белка на матрице мРНК при участии рибосом. Другие РНК после транскрипции подвергаются химическим модификациям, и после образования вторичной и третичной структур выполняют функции, зависящие от типа РНК.
Геномы ряда вирусов состоят из РНК, то есть у них она играет роль, которую у высших организмов выполняет ДНК. На основании разнообразия функций РНК в клетке была выдвинута гипотеза, согласно которой РНК — первая молекула, которая была способна к самовоспроизведению в добиологических системах.
Рнк что это
ГяРНК свойственна исключительно эукариотам, её нет у прокариот («доядерные» организмы, например бактерии и вирусы). Некоторые вирусы для хранения и передачи генетической информации следующим поколениям используют РНК вместо ДНК.
ГяРНК и её производное — информационная (или матричная) РНК переносят генетическую информацию от ядерной ДНК к цитоплазме.
Количество видов гяРНК равно количеству генов, так как она служит прямой копией кодирующих последовательностей генома. В процессе транскрипции РНК с ДНК ключевую роль играет фермент РНК-полимераза II. Информационная РНК образуется в результате процессинга гяРНК, при котором происходят вырезание некодирующих участков (интронов) и склеивание кодирующих экзонов. Таким образом, в состав иРНК входят кодирующая информация соответствующих видов гяРНК, а также фланкирующий лидерный и трейлерный участки, по этой причине она значительно короче.
Транспортная РНК
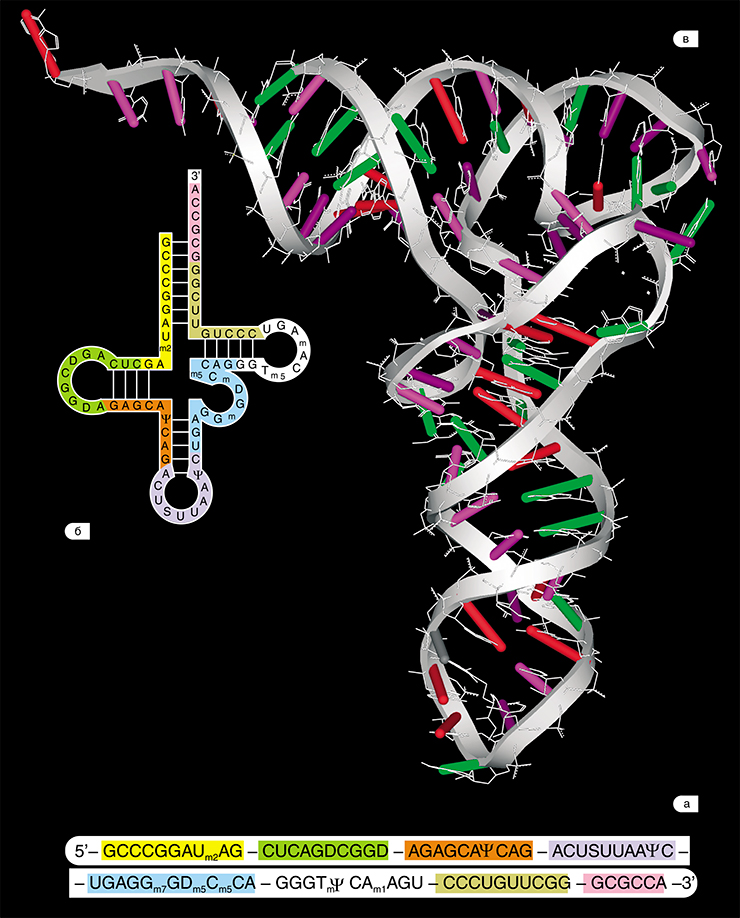
Каждая молекула тРНК состоит примерно из 75 связанных между собой нуклеотидов, образующих длинную цепь. В результате взаимодействия входящих в её состав оснований тРНК имеет конформационную структуру «клеверный лист», который затем скручивается в L-форму. Очень часто в состав тРНК помимо Ц, Г, А и У входит ряд редких оснований, некоторые из которых модифицированы путём метилирования. Важная особенность тРНК: «заряженная» молекула несёт на своём 3′-конце аминокислоту, а посередине конформационной структуры «клеверный лист» находятся три специфических основания, именуемые антикодоном. Последовательность оснований в антикодоне напрямую зависит от вида аминокислоты, прикреплённой к 3′-концу.
Так, например, тРНК, антикодон которой имеет последовательность 5′-ЦЦА-3′, может нести только аминокислоту триптофан. Следует отметить, что данная зависимость лежит в основе передачи генетической информации, носителем которой выступает тРНК.
Транскрипция молекул тРНК происходит с кодирующих её последовательностей в ДНК при участии фермента РНК-полимеразы III. Различают более 40 семейств тРНК, которые, в свою очередь, подразделяют на несколько видов.
Рибосомальная РНК
Существует несколько субъединиц рРНК, которые различаются по коэффициенту седиментации (осаждения), измеряемому в единицах Сведберга (S). Данный коэффициент зависит от скорости осаждения субъединиц при центрифугировании в насыщенной водной среде.
Каждая рибосома состоит из большой и малой субъединиц. Они содержат большое количество белков, синтезированных посредством трансляции иРНК, а также РНК, которая не подвергается трансляции. Термин «рибосомальная РНК» относят именно к нетранслируемому материалу. В малой субъединице находится 18S рРНК, а в большой — 4S, 5,8S и 28S рРНК.
Траскрипция рРНК с ДНК происходит при помощи двух дополнительных РНК-полимераз. РНК-полимераза I транскрибирует 5S, 5,8S и 28S в виде одного длинного 45S-тpaнскрипта, который затем разделяется на необходимые части. Таким образом обеспечивается равное количество молекул. В организме человека в каждом гаплоидном геноме присутствует примерно 250 копий последовательности ДНК, кодирующей 45S-транскрипт. Они расположены в пяти кластерных тандемных повторах в коротких плечах хромосом 13, 14, 15, 21 и 22.
Данные участки известны как ядрышковые организаторы, так как их транскрипция и последующий процессинг 45S-транскрипта происходят внутри ядрышка.
Не менее чем в трёх кластерах хромосомы 1 существует 2000 копий 5S-pPHK гена. Их транскрипция протекает в присутствии РНК-полимеразы III снаружи ядрышка. Затем они доставляются к местам сборки рибосом при помощи рибосомальных белков.
В рРНК насчитывают около 95 псевдоуридиновых участков, образованных посредством изомеризации уридина малой ядрышковой РНК.
Малая ядрышковая РНК. Малая (низкомолекулярная) ядрышковая РНК в основном участвует в направлении или проведении модификаций оснований в рРНК и малой ядерной РНК, таких, как, например, метилирование и псевдоуридинизация. Большинство малых ядрышковых РНК находятся в интронах других генов.
Сигналраспознающая РНК. Сигналраспознающая РНК распознаёт сигнальную последовательность белков, предназначенных для экспрессии, и участвует в их переносе через цитоплазматическую мембрану.
Микро-РНК. Существует примерно 200 микро-РНК человека длиной в 22 основания, производных расщепления рибонуклеазой Н их предшественников (двухцепочечных «зашпиленных» РНК) в соответствии с инвертированными повторами. Они контролируют трансляцию структурных генов путём комплементарного связывания с З’-концами нетранслируемых участков иРНК.
Митохондриальная РНК
Митохондриальная ДНК представляет собой непрерывную петлю и кодирует 13 полипептидов, 22 тРНК и 2 рРНК (16S и 23S). Большинство генов находятся на одной (тяжёлой) цепи, однако некоторое их количество расположено и на комплементарной ей лёгкой. При этом обе цепи транскрибируются в виде непрерывных транскриптов при помощи митохондриоспецифической РНК-полимеразы. Данный фермент кодируется ядерным геном. Длинные молекулы РНК затем расщепляются на 37 отдельных видов, а мРНК, рРНК и тРНК совместно транслируют 13 мРНК. Большое количество дополнительных белков, которые поступают в митохондрию из цитоплазмы, транслируются с ядерных генов.
У пациентов с системной красной волчанкой обнаруживают антитела к снурп-белкам собственного организма. Кроме того, считают, что определённый набор генов малой ядерной РНК хромосомы 15q играет важную роль в патогенезе синдрома Прадера—Вилли (наследственное сочетание олигофрении, низкого роста, ожирения, гипотонии мышц).
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Мир РНК, или Что есть жизнь
Оксана Максименко,
кандидат биологических наук, Институт биологии гена РАН
«Коммерсантъ Наука» №6, сентябрь 2017
Центральную догму биологии, сформулированную Фрэнсисом Криком в конце 1950-х, изучают в классическом виде: ДНК → РНК → белок. Но данных достаточно, чтобы усомниться в буквальном понимании этого главного принципа жизни.
Последний пример: в июньской публикации Scientific Reports российские ученые из Института биоорганической химии и Федерального научно-клинического центра физико-химической медицины показали, что разнообразие изоформ белков в клетках значительно меньше теоретически возможного. Журналисты поспешили сообщить, что меняется представление о центральной догме молекулярной биологии. Однако догма меняется уже 70 лет, потому что исходно была всего лишь гипотезой. Словом «догма» ее создатель Крик назвал потому, что нравилось это слово! Важно другое: как и почему меняется главная гипотеза молекулярной биологии.
Слишком много РНК
Генетическая информация считывается с кодирующих последовательностей генома, представленных генами. Только малая часть генома эукариот (растения, животные, грибы) содержит гены, а основная часть представлена протяженными нуклеотидными последовательностями с малоизученными функциями. В геноме человека только четверть покрыта генами и только 1% последовательностей ДНК кодирует информацию, записываемую в функциональных молекулах РНК (часть догмы «ДНК → РНК»). То есть 1% геномной ДНК содержит информацию обо всех молекулах РНК. Зачем нужны оставшиеся 99%?
В последние годы стало понятно, что межгенные участки ДНК несут в себе регуляторную функцию: в них заложены системы и элементы, обеспечивающие тонкую настройку работы генов, их включение или выключение в определенных тканях организма или на конкретных стадиях развития. С такими элементами связываются различные комплексы, которые содержат молекулы регуляторных белков и РНК. Уже на этом уровне очевидно, что модель «ДНК → РНК → белок» полноценно не работает, так как основная масса ДНК не дает начала РНК, а несет другие функции.
Часть генов кодирует РНК с регуляторными функциями. Эти РНК не содержат информации о последовательности белка, а преимущественно организуют синтез белка в клетке. Основная часть таких РНК — компоненты рибосом (рибосомальные РНК), комплексы, осуществляющие трансляцию, а также молекулы-переносчики аминокислот (транспортные РНК), необходимые участникам процесса синтеза белка на матрице РНК (трансляции). 90% всей РНК клетки относится к перечисленным типам.
Среди оставшихся 10% молекул РНК представлены все белок-кодирующие РНК, но даже среди этих РНК найдены некодирующие молекулы, в частности, малые ядерные РНК. Эти РНК — необходимые компоненты комплекса сплайсинга. Сплайсинг — процесс удаления из первичной молекулы РНК некодирующих участков (интронов) и последовательного соединения кодирующих (экзонов); в итоге получается матричная РНК (мРНК), содержащая готовую к считыванию информацию о последовательности белка.
Именно этот комплекс готовит предшественников мРНК к синтезу правильных белков — путем вырезания из середины РНК последовательностей, не несущих в себе информации о составе белка, но содержащих регуляторные элементы. Так что и часть догмы «РНК → белок» имеет свои ограничения.
Молекулярный «контроль качества»
А что мы знаем про так называемые «белок-кодирующие» гены? В клетках прокариот (бактерии) для такого типа генов все просто: на матрице ДНК транскрибируются молекулы РНК, на их базе идет синтез белковых молекул. Чаще всего молекулы РНК готовы для синтеза уже во время транскрипции.
В клетках эукариот все гораздо сложней: синтезирующиеся в процессе транскрипции молекулы РНК не готовы к трансляции (синтезу белка), прежде они должны претерпеть ряд изменений. Определенный набор модификаций вносится на концы молекул РНК (и РНК становится стабильной, а также попадает в определенные зоны клетки — «фабрики белка»), из середины молекул вырезаются интроны. Без сплайсинга и объединения экзонов правильную белковую молекулу не синтезировать.
С усложнением геномов вклад сплайсинга в процесс созревания мРНК увеличивается: у дрожжей только 4% белок-кодирующих генов подвергается сплайсингу, у дрозофилы — 83%, а у человека — 94%. Основная часть генов человека содержит более одного интрона в своем составе, и более половины генов человека могут сплайсироваться несколькими способами. Так что сплайсинг — это дополнительный регуляторный механизм, контролирующий количество «правильных» РНК, на матрице которых может запускаться синтез белковых молекул.
Кроме этого, сплайсинг часто является своего рода «контролем качества» молекул РНК, регулирует их стабильность. А так как альтернативный сплайсинг приводит к образованию на основе одной и той же молекулы РНК разных вариантов зрелых мРНК, это способ обеспечить дополнительное разнообразие белков в клетке. Такое разнообразие нужно для лучшей приспосабливаемости организма: разные изоформы белка могут работать в разных типах клеток, транспортироваться в разные компартменты или формировать разные поверхности узнавания для лигандов и т. д.
О чем «шумят» гены
Далеко не для всех изоформ белков известны функции, а во многих случаях для альтернативно сплайсированных молекул РНК не удается обнаружить белковый продукт. Авторы указанной статьи в Scientific Reports, изучавшие продукты альтернативного сплайсинга на модели мха, не обнаружили белков для большей части альтернативно сплайсированных молекул мРНК. В работах, выполненных на других модельных организмах, для многих альтернативно сплайсированных вариантов мРНК белковые молекулы также не были найдены.
Возможно, такие молекулы — побочный продукт регуляции «количества» генной экспрессии, «генный шум»; либо некоторые изоформы белка нужны в крайне ограниченных количествах.
Кроме этого, во многих интронах генов находятся регуляторные элементы, управляющие процессами сплайсинга, и там же могут находиться некодирующие РНК, участвующие в клеточном метаболизме. Так что и многообразие изоформ, и даже экспрессии белка могут контролироваться непосредственно молекулами РНК, без участия ДНК.
С развитием полногеномных технологий появляется все больше работ о некодирующих молекулах РНК. В геноме человека описан огромный пул таких РНК — «длинных» и «коротких»: они осуществляют важные регуляторные функции в клетке. Эти РНК следят за стабильностью белок-кодирующих РНК, активируют или репрессируют гены, являются сенсорами при разных стрессах. Функции основной части некодирующих РНК еще не описаны, это целый мир, без которого клетка и организм не могут существовать.
Накопленные на сегодня данные наталкивают на мысль, что на молекулярном уровне жизнь — это форма реализации функций РНК. ДНК хранит информацию, белок отвечает за клеточный метаболизм, а жизнь клетки (и организма) организуется и контролируется на этапе функционирования молекул РНК.
Существуют даже предположения, что именно РНК на заре эволюции была первым биополимером, способным к самовоспроизводству. РНК, с одной стороны, подобно ДНК, способна быть хранилищем генетической информации (геномы огромной группы вирусов представлены РНК). С другой — известны и РНК с каталитической функцией, способные выполнять часть функций белков. Сторонники РНК-мира считают, что свойства РНК, позволившие им воспроизводить за счет собственной ферментной активности записанную в последовательностях нуклеотидов информацию, сыграли решающую роль в становлении генетического аппарата живых организмов.
Время для подобных обобщений еще не пришло. Ученые только начинают понимать, что система, которую они изучают уже 100 лет, гораздо сложней, чем казалось даже 20 лет назад.
РНК (рибонуклеиновая кислота)
РНК (рибонуклеиновая кислота), так же как и ДНК, относится к нуклеиновым кислотам. Молекулы-полимеры РНК намного меньше, чем у ДНК. Однако в зависимости от типа РНК количество входящих в них нуклеотидов-мономеров различается.
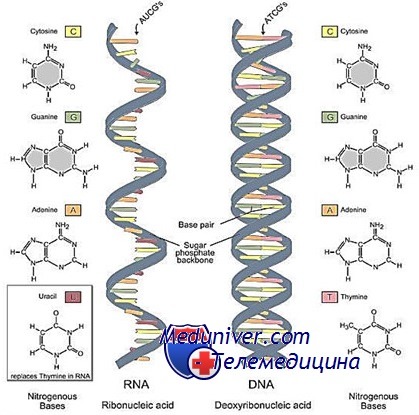
В состав нуклеотида РНК в качестве сахара входит рибоза, в качестве азотистого основания — аденит, гуанин, урацил, цитозин. Урацил по строению и химическим свойствам близок к тимину, который обычен для ДНК. В зрелых молекулах РНК многие азотистые основания модифицированы, поэтому в реальности разновидностей азотистых оснований в составе РНК намного больше.
Главной функцией РНК в клетках живых организмов можно назвать реализацию генетической информации. Именно благодаря разным типам рибонуклеиновой кислоты генетический код считывается (транскрибируется) с ДНК, после чего на его основе синтезируются полипептиды (происходит трансляция). Итак, если ДНК в основном отвечает за хранение и передачу из поколения в поколение генетической информации (основной процесс – репликация), то РНК реализует эту информацию (процессы транскрипции и трансляции). При этом транскрипция происходит на ДНК, так что этот процесс относится к обоим типам нуклеиновых кислот и тогда с этой точки зрения можно сказать, что и ДНК отвечает за реализацию генетической информации.
При более подробном рассмотрении функции РНК намного разнообразнее. Ряд молекул РНК выполняют структурную, каталитическую и другие функции.
Существует так называемая гипотеза РНК-мира, согласно которой вначале в живой природе в качестве носителя генетической информации выступали только молекулы РНК, при этом другие молекулы РНК катализировали различные реакции. Данная гипотеза подтверждена рядом опытов, показывающих возможную эволюцию РНК. На это указывает и то, что ряд вирусов в качестве нуклеиновой кислоты, хранящей генетическую информацию, имеют молекулу РНК.
Согласно гипотезе РНК-мира ДНК появилась позже в процессе естественного отбора как более устойчивая молекула, что важно для хранения генетической информации.
Выделяют три основных типа РНК (кроме них есть и другие): матричная (она же информационная), рибосомальная и транспортная. Обозначаются они соответственно иРНК (или мРНК), рРНК, тРНК.
Информационная РНК (иРНК)
Почти все РНК синтезируются на ДНК в процессе транскрипции. Однако часто транскрипция упоминается как синтез именно информационной РНК (иРНК). Связано это с тем, что последовательность нуклеотидов иРНК в последствии определит последовательность аминокислот синтезируемого в процессе трансляции белка.
Перед транскрипцией нити ДНК расплетаются, и на одной из них с помощью комплекса белков-ферментов синтезируется РНК по принципу комплементарности, так же как это происходит при репликации ДНК. Только напротив аденина ДНК к молекуле РНК присоединяется нуклеотид, содержащий урацил, а не тимин.
На самом деле на ДНК синтезируется не готовая информационная РНК, а ее предшественник — пре-иРНК. Предшественник содержит участки последовательности нуклеотидов, которые не кодируют белок и которые после синтеза пре-иРНК вырезаются при участии малых ядерных и ядрышковых РНК («дополнительные» типы РНК). Эти удаляющиеся участки называются интронами. Остающиеся части иРНК называются экзонами. После удаления интронов экзоны сшиваются между собой. Процесс удаления интронов и сшивания экзонов называется сплайсингом. Усложняющей жизнь особенностью является то, что можно вырезать интроны по-разному, в результате получатся разные готовые иРНК, которые будут служить матрицами для разных белков. Таким образом, вроде бы один ген ДНК может играть роль нескольких генов.
Следует отметить, что у прокариотических организмов сплайсинга не происходит. Обычно их иРНК сразу после синтеза на ДНК готова к трансляции. Бывает, что пока конец молекулы иРНК еще транскрибируется, на ее начале уже сидят рибосомы, синтезирующие белок.
После того как пре-иРНК созревает в информационную РНК и оказывается вне ядра, она становится матрицей для синтеза полипептида. При этом на нее «насаживаются» рибосомы (не сразу, какая-то оказывается первой, другая — второй и т. д.). Каждая синтезирует свою копию белка, т. е. на одной молекуле РНК могут синтезироваться сразу несколько одинаковых белковых молекул (понятно, что каждая будет находиться на своей стадии синтеза).
Рибосома, передвигаясь от начала иРНК к ее концу, считывает по три нуклеотида (хотя вмещает шесть, т. е. два кодона) и присоединяет соответствующую транспортную РНК (имеющую соответствующий кодону антикодон), к которой присоединена соответствующая аминокислота. После этого с помощью активного центра рибосомы ранее синтезированная часть полипептида, соединенная с предшествующей тРНК, как-бы «пересаживается» (образуется пептидная связь) на аминокислоту, прикрепленную к только что пришедшей тРНК. Таким образом, молекула белка постепенно увеличивается.
Когда молекула информационной РНК становится не нужна, клетка ее разрушает.
Транспортная РНК (тРНК)
Транспортная РНК — это достаточно маленькая (по меркам полимеров) молекула (количество нуклеотидов бывает разным, в среднем около 80-ти), во вторичной структуре имеет форму клеверного листа, в третичной сворачивается в нечто подобное букве Г.
Живая природа на Земле использует всего около 20-ти аминокислот для синтеза различных белковых молекул (на самом деле аминокислот куда больше). Но поскольку, согласно генетическому коду, кодонов больше 60-ти, то каждой аминокислоте может соответствовать несколько кодонов (на самом деле какой-то больше, какой-то меньше). Таким образом, разновидностей тРНК больше 20, при этом разные транспортные РНК переносят одинаковые аминокислоты. (Но и тут не так все просто.)
Рибосомная РНК (рРНК)
Рибосомную РНК часто также называют рибосомальной РНК. Это одно и то же.
Рибосомная РНК составляет около 80% всей РНК клетки, так как входит в состав рибосом, коих в клетке бывает достаточно много.
В рибосомах рРНК образует комплексы с белками, выполняет структурную и каталитическую функции.
В состав рибосомы входят несколько разных молекул рРНК, отличающиеся между собой как по длине цепи, вторичной и третичной структуре, выполняемым функциям. Однако их суммарная функция — это реализация процесса трансляции. При этом молекулы рРНК считывают информацию с иРНК и катализируют образование пептидной связи между аминокислотами.
Рнк что это
Рибонуклеи́новые кисло́ты (РНК) — нуклеиновые кислоты, полимеры нуклеотидов, в состав которых входят остаток ортофосфорной кислоты, рибоза (в отличие от ДНК, содержащей дезоксирибозу) и азотистые основания — аденин, цитозин, гуанин и урацил (в отличие от ДНК, содержащей вместо урацила тимин). Эти молекулы содержатся в клетках всех живых организмов, а также в некоторых вирусах.
Клеточные РНК образуются в ходе процесса, называемого транскрипцией, то есть синтеза РНК на матрице ДНК, осуществляемого специальными ферментами — РНК-полимеразами. Затем матричные РНК (мРНК), принимают участие в процессе, называемом трансляцией. Трансляция — это синтез белка на матрице мРНК при участии рибосом. Другие РНК после транскрипции подвергаются химическим модификациям, и после образования вторичной и третичной структур выполняют функции, зависящие от типа РНК.
Для одноцепочечных РНК характерны разнообразные пространственные структуры, в которых часть нуклеотидов одной и той же цепи спарены между собой. Некоторые высокоструктурированные РНК принимают участие в синтезе белка клетки, например, транспортные РНК служат для узнавания кодонов и доставки соответствующих аминокислот к месту синтеза белка, а рибосомные РНК служат структурной и каталитической основой рибосом.
Однако функции РНК в современных клетках не ограничиваются их ролью в трансляции. Так малые ядерные РНК принимают участие в сплайсинге эукариотических матричных РНК и т. д.
Помимо того, что молекулы РНК входят в состав некоторых ферментов (напр., теломеразы) у некоторых РНК обнаружена собственная энзиматическая активность, например способность вносить разрывы в другие молекулы РНК или, наоборот, «склеивать» два РНК-фрагмента. Такие РНК называются рибозимами.
Геномы некоторых вирусов состоят из РНК, то есть у них она выполняет роль, которую у высших организмов выполняет ДНК. На основании разнообразия функций РНК в клетке была выдвинута гипотеза, согласно которой РНК — первая молекула, которая была способна к самовоспроизведению в добиологических системах.
Содержание
История изучения
Химический состав и модификации мономеров
Структура
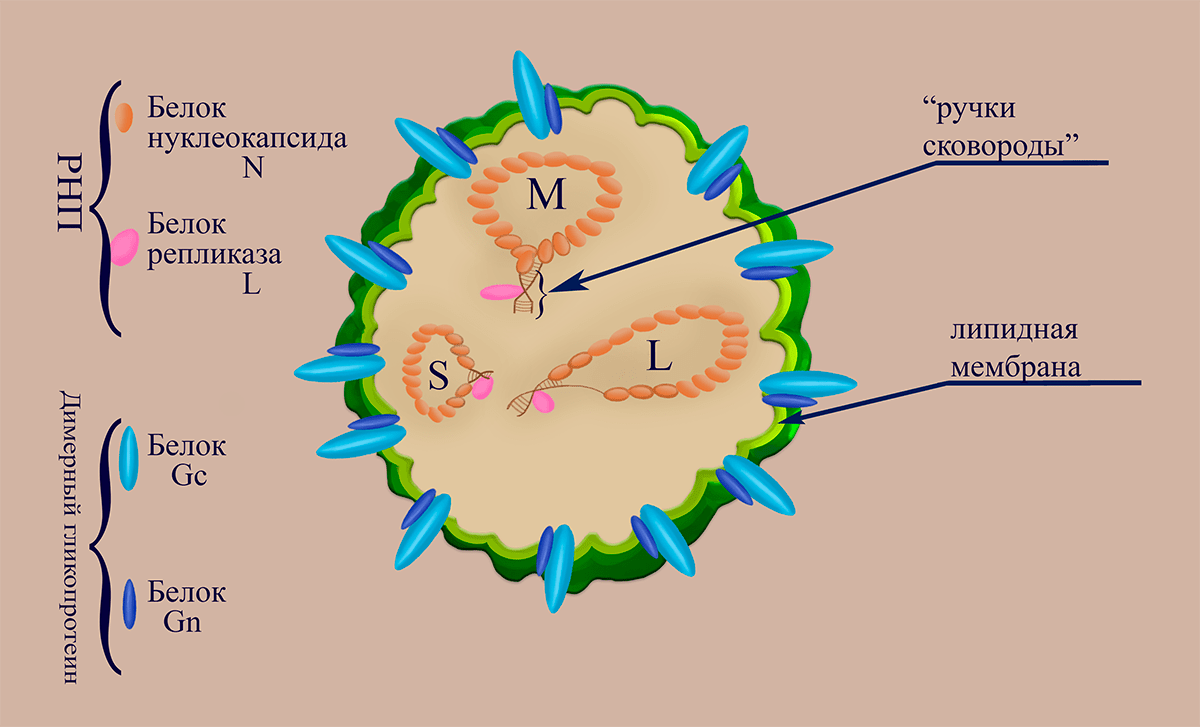
Многие типы РНК, например, рРНК и мяРНК в клетке функционируют в виде комплексов с белками, которые ассоцииируют с молекулами РНК после их синтеза или (у эукариот) экспорта из ядра в цитоплазму. Такие РНК-белковые комплексы называются рибонуклеопротеиновыми комплексами или рибонуклеопротеидами.
Сравнение с ДНК
Между ДНК и РНК есть три основных отличия:
Синтез
Типы РНК
Участвующие в трансляции
Информация о последовательности аминокислот белка содержится в мРНК. Три последовательных нуклеотида (кодон) соответствуют одной аминокислоте. В эукариотических клетках транскирибированный предшественник мРНК или пре-мРНК процессируется с образованием зрелой мРНК. Процессинг включает удаление некодирующих белок последовательностей (интронов). После этого мРНК экспортируется из ядра в цитоплазму, где к ней присоединяются рибосомы, транслирующие мРНК с помощью соединённых с аминокислотами тРНК.
Участвующие в регуляции генов
В процессинге РНК
Геномы, состоящие из РНК
Как и ДНК, РНК может хранить информацию о биологических процессах. РНК может использоваться в качестве генома вирусов и вирусоподобных частиц. РНК-геномы можно разделить на те, которые не имеют промежуточной стадии ДНК и которые для размножения копируются в ДНК-копию и обратно (ретровирусы).
РНК-содержащие вирусы
Многие вирусы, например, вирус гриппа, на всех стадиях содержат геном, состоящий исключительно из РНК. РНК содержится внутри обычно белковой оболочки и реплицируется с помощью закодированных в ней РНК-зависимых РНК-полимераз. Вирусные геномы, состоящие из РНК разделяются на
Ретровирусы и ретротранспозоны
У других вирусов РНК-геном есть в течение только одной из фаз жизненного цикла. Вирионы так называемых ретровирусов содержат молекулы РНК, которые при попадании в клетки хозяина служат матрицей для синтеза ДНК-копии. В свою очередь, с матрицы ДНК считывается РНК-геном. Кроме вирусов обратную транскрипции применяют и класс мобильных элементов генома — ретротранспозоны [51]
Гипотеза РНК-мира
Жизнь начиналась с РНК
Исследования нуклеиновых кислот являются одной из самых «горячих точек» в биологии. Благодаря уникальным свойствам РНК находят все более широкое применение в медицине и технике. Но знает об этом пока лишь узкий круг специалистов.
Рибонуклеиновой кислоте, иначе – РНК – не повезло. Она не пользуется такой широкой известностью, как ее близкий «родственник» – ДНК, несмотря на большое химическое сходство. Однако открытия последних двадцати лет радикально поменяли наши взгляды на роль и функции этих, как выяснилось, очень «умелых» молекул. Плодом этих открытий стала принципиально новая идея о том, что современной жизни предшествовал совершенно самодостаточный древний «мир РНК».
Как это обычно бывает, новое знание, расширяя горизонт, породило и массу новых вопросов. Каковы были механизмы «эволюции» в мире РНК? Зачем, откуда и как появились ДНК и белки? Как произошел переход от «мира РНК» к современному миру? О поисках, которые ведутся в этом направлении, читателям рассказывают академик Валентин Викторович Власов и его сын, кандидат химических наук, Александр Власов
Почему в цикле статей, посвященных проблеме возникновения жизни, появляется статья об РНК, а не о других, более известных органических молекулах – ДНК или белках? Возможно, наши читатели слышали и об РНК, но вот что? Уверены, ничего примечательного – по одной простой причине: пока лишь специалисты-биологи знают, что именно РНК являются «волшебными» молекулами, давшими начало жизни. Что когда-то в древности, на только что остывшей Земле, возник и существовал загадочный «мир РНК»…
Прежде чем отправиться к «началу начал», давайте запасемся необходимыми знаниями о строении нуклеиновых кислот – ДНК (дезоксирибонуклеиновой) и РНК (рибонуклеиновой). По своему химическому составу РНК является двойняшкой, хотя и не полным близнецом, ДНК, основного хранителя генетической информации в живой клетке. Нуклеиновые кислоты представляют собой полимерные макромолекулы, состоящие из отдельных звеньев – нуклеотидов. Скелетом макромолекулы являются молекулы пятиуглеродного сахара, соединенные остатками фосфорной кислоты. К каждой молекуле сахара присоединяется одно азотистое основание. Нуклеотиды, которые различаются между собою только разными азотистыми основаниями, обозначаются буквами A, U, G, C (в РНК) и A, T, G, C (в ДНК).
Честно говоря, насчет РНК никто не задумывался долгие годы. Существовала догма, что вот есть клетка, есть хромосомы, в которых есть ДНК – хранитель генетической информации.
В конце концов, на рибосомах синтезируются белки. А РНК – она где-то в промежутке, переносчик информации от ДНК – и только. А потом посыпались открытия, которые заставили совершенно по-другому взглянуть на РНК
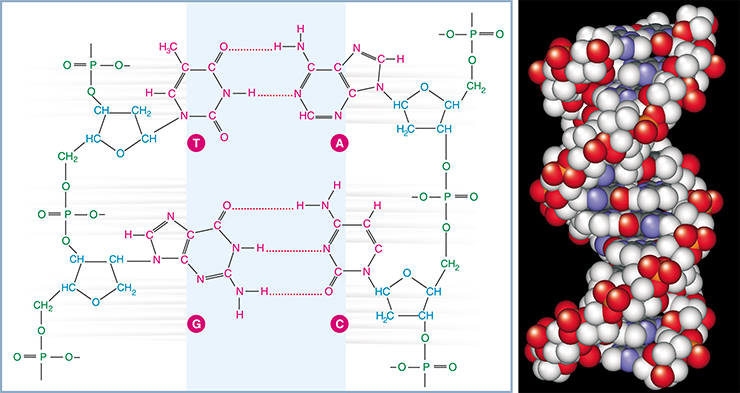
Главное отличие нуклеиновых кислот заключается в их углеводной компоненте. В РНК сахар – рибоза, а в ДНК – дезоксирибоза: там, где у ДНК имеется атом водорода (Н), у РНК стоит оксигруппа (ОН). Результаты таких незначительных, на неискушенный взгляд, различий поражают. Так, ДНК существуют в основном в форме всем известных жестких спиралей, в которых две цепи ДНК удерживаются вместе за счет образования водородных связей между комплементарными нуклеотидами.
РНК также могут формировать спирали из двух цепочек, похожие на спирали ДНК, однако в большинстве случаев РНК существуют в виде сложных структур-клубков. Структуры эти формируются не только за счет образования упомянутых водородных связей между разными участками РНК, но и благодаря оксигруппе рибозы, которая может образовывать дополнительные водородные связи и взаимодействовать с фосфорной кислотой и ионами металлов. Глобулярные структуры РНК не только внешне напоминают белковые структуры, но и приближаются к ним по свойствам: они могут взаимодействовать с самыми разными молекулами, как маленькими, так и полимерными.
Кого Считать «Живым»?
Почему же именно РНК мы называем праматерью ныне существующей жизни? Чтобы ответить на этот вопрос, давайте разберемся, где проходит граница между живым и неживым.
Поскольку над проблемой происхождения жизни работают ученые из разных областей, каждый оперирует терминами близкой ему науки. Химики обязательно вспомнят слово «катализатор», математики – «информация». Биологи будут считать живой систему, содержащую вещество (генетическую программу), которое может копироваться (или, по-простому, размножаться). При этом необходимо, чтобы в ходе такого копирования могли происходить некоторые изменения наследственной информации и возникать новые варианты систем, т. е. должна существовать возможность эволюции. Еще биологи обязательно заметят, что такие системы должны быть пространственно обособлены. Иначе возникшие более прогрессивные системы не смогут воспользоваться своими преимуществами, поскольку их более эффективные катализаторы и другие продукты будут беспрепятственно «уплывать» в окружающую среду.
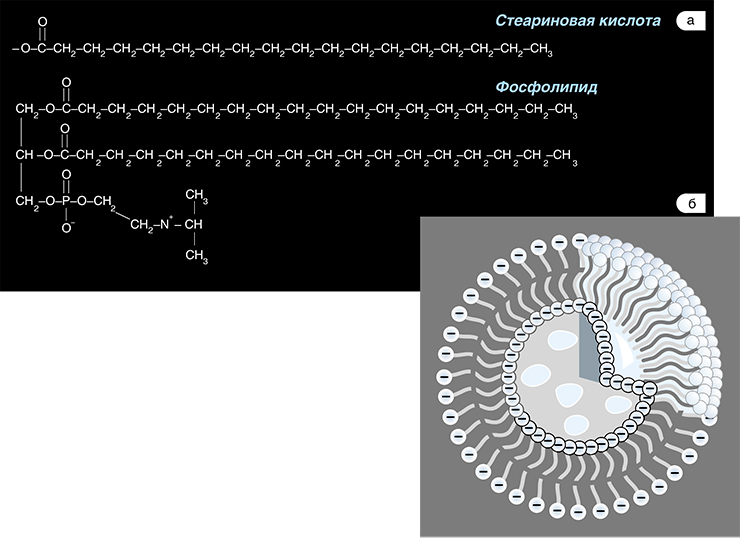
Каким же образом первые молекулярные системы были обособлены от окружающей среды? Колонии молекул могли, например, удерживаться вместе за счет адсорбции на какой-нибудь минеральной поверхности или пылевых частицах. Однако возможно, что уже самые примитивные системы располагали, подобно современным живым клеткам, настоящей мембранной оболочкой. Дело в том, что такая «протоклетка» с липидной мембраной может образоваться очень просто. Многие молекулы с заряженными группами (например, жирные кислоты) в водной среде образуют микроскопические пузырьки – липосомы. Это слово должно быть хорошо известно прекрасной половине наших читателей: липосомы широко используются в косметических кремах – крохотные жировые капсулы начиняются витаминами и другими биологически активными веществами. А вот чем были наполнены древние «протоклетки»? Оказалось, что на роль «начинки» претендуют именно РНК.
РНК умеет все?
Жизнь, без сомнения, должна была начаться с образования «умелых» молекул, которые могли бы сами себя размножать и выполнять все другие «хозяйственные работы», необходимые для существования клетки. Однако на роль таких умельцев не подходит ни ДНК, ни белок. ДНК – отличный хранитель генетической информации, но сама себя размножать не умеет. Белки – непревзойденные катализаторы, но не могут работать в качестве «генетических программ». Возникает парадокс курицы и яйца: ДНК не может образоваться без белка, а белок – без ДНК. И только РНК, как выяснилось, может ВСЕ. Но не будем забегать вперед.
Рассмотрим давно известные функции РНК, связанные с работой (экспрессией) гена в клетке. При включении гена сначала происходит локальное расплетение ДНК и синтезируется РНК-копия генетической программы. В результате сложных обработок ее специальными белками получается матричная РНК (мРНК), которая и явля-ется программой для синтеза белка. Эта РНК переносится из ядра в цитоплазму клетки, где она связывается со специальными клеточными структурами – рибосомами, настоящими молекулярными «машинами» для синтеза белка. Белок синтезируется из активированных аминокислот, присоединенных к особым транспортным РНК (тРНК), причем каждая из аминокислот присоединена к своей специфической тРНК. Благодаря тРНК аминокислота фиксируется в каталитическом центре рибосомы, где она «пришивается» к синтезируемой белковой цепи. Из рассмотренной последовательности событий видно, что молекулы РНК играют ключевую роль в декодировании генетической информации и биосинтезе белка.
Чем больше углублялись в изучение различных биосинтетических процессов, тем чаще обнаруживали ранее неизвестные функции РНК. Оказалось, что кроме процесса транскрипции (синтеза РНК путем копирования участка ДНК) в ряде случаев, наоборот, может происходить синтез ДНК на РНК-матрицах. Этот процесс, названный обратной транскрипцией, используют в ходе своего развития многие вирусы, в том числе печально известные онкогенные вирусы и ВИЧ-1, вызывающий СПИД.
Таким образом, выяснилось, что поток генетической информации не является, как первоначально считалось, однонаправленным – от ДНК к РНК. Роль ДНК как изначально главного носителя генетической информации стала подвергаться сомнению. Тем более что многие вирусы (гриппа, клещевого энцефалита и другие) вообще не используют ДНК в качестве генетического материала, их геном построен исключительно из РНК. А далее посыпались одно за другим открытия, которые заставили совершенно по-другому взглянуть на РНК.
На Все «Молекулы» Мастер
Наиболее удивительным было открытие каталитической способности РНК. Прежде считалось, что катализировать реакции умеют только белки, ферменты. Ученые, например, никак не могли выделить ферменты, осуществляющие разрезание и сшивание некоторых РНК. После длительных исследований выяснилось, что РНК прекрасно справляются с этим сами. Структуры РНК, действующие подобно ферментам, назвали рибозимами (по аналогии с энзимами, белками-катализаторами). Вскоре было обнаружено множество разнообразных рибозимов. Особенно широко их используют для манипулирования своими РНК вирусы и другие простые инфекционные агенты. Таким образом, РНК оказались мастерами на все руки: они могут выступать в роли носителей наследственной информации, могут служить катализаторами, транспортными средствами для аминокислот, образовывать высокоспецифичные комплексы с белками.
Конечно, полную картину еще предстоит реконструировать – осталось много нерешенных вопросов. Например, в современной клетке активацию аминокислот и их присоединение к соответствующим тРНК осуществляют специфичные белки-ферменты. Возникают вопросы: могла ли эта реакция осуществляться без участия белков, только с помощью РНК? Могли ли сами РНК катализировать синтез РНК из нуклеотидов или присоединение азотистых оснований к сахару? В общем-то, после открытия рибозимов такие потенциальные способности РНК уже не вызывали особых сомнений. Но наука требует, чтобы гипотезы экспериментально подтверждались.
Дарвиновская Эволюция в Пробирке
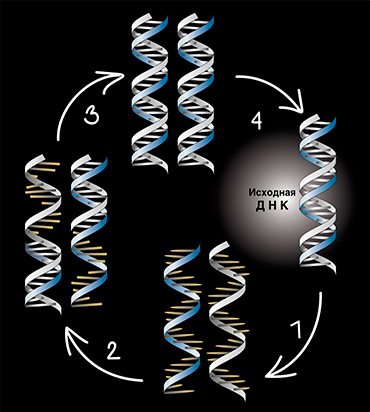
Хороший метод зачастую позволяет осуществить революцию в науке. Именно так можно сказать о методе полимеразной цепной реакции (ПЦР), который позволяет размножать нуклеиновые кислоты в неограниченных количествах. Кратко опишем суть метода. Для размножения ДНК в методе ПЦР используются ферменты ДНК- полимеразы, т. е. те самые ферменты, которые при размножении клеток синтезируют из активированных мономеров-нуклеотидов комплементарные цепочки ДНК.
При методе ПЦР в пробирку с ДНК вносят смесь активированных нуклеотидов, фермент ДНК-полимеразу и так называемые праймеры – олигонуклеотиды, комплементарные концам размножаемой ДНК. При нагревании раствора цепи ДНК расходятся. Затем, при охлаждении, с ними связываются праймеры, образуя короткие фрагменты спиральных структур. Фермент присоединяет к праймерам нуклеотиды и собирает цепочку, комплементарную цепочке исходной ДНК. В результате реакции из одной двуцепочечной ДНК получается две. Если повторить процесс, получится четыре цепочки, а после n повторений – 2 n молекул ДНК. Все очень просто.
Изобретение ПЦР и разработка методов химического синтеза ДНК позволили создать потрясающую технологию молекулярной селекции. Принцип молекулярной селекции тоже прост: сначала синтезируется множество молекул, обладающих разными свойствами (так называемая молекулярная библиотека), а затем из этой смеси отбираются молекулы с желаемым свойством.
Библиотеки нуклеиновых кислот – это смеси молекул, имеющих одинаковую длину, но отличающихся последовательностью нуклеотидов. Получить их можно в том случае, если при химическом синтезе на автоматическом синтезаторе добавлять на каждой стадии удлинения нуклеотидной последовательности одно-временно все четыре нуклеотида. Каждый из них будет включаться в растущую нуклеиновую кислоту с равной вероятностью, в результате чего на каждом этапе присоединения будет получаться 4 варианта последовательностей. Если таким образом синтезировать нуклеиновую кислоту длиной в n звеньев, то разнообразие полученных молекул составит 4 в степени n. Поскольку обычно используются участки длиной 30–60 мономеров, то в результате синтеза получается от 4 30 до 4 60 разных молекул! Цифры, привычные разве что для астрономов.
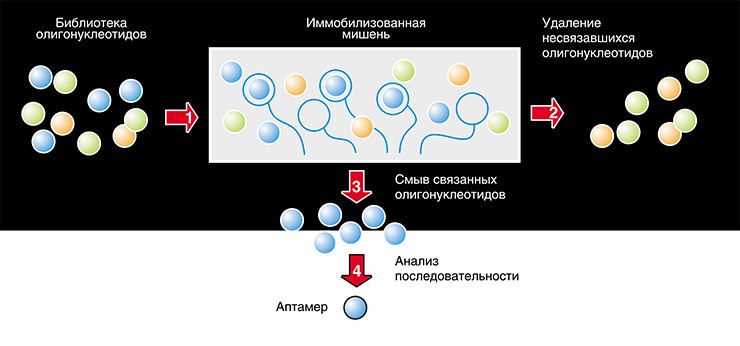
Так как в зависимости от состава нуклеиновые кислоты сворачиваются в разные пространственные структуры, синтез статистических последовательностей дает огромное множество молекул, различающихся по свойствам. С образовавшихся ДНК – с помощью фермента РНК-полимеразы – считывается РНК. В результате получается библиотека уже одноцепочечных РНК. Далее производится процедура отбора: раствор РНК пропускается через колонку, в которой находится нерастворимый носитель с химически присоединенными молекулами-мишенями, чтобы «выловить» так называемый будущий аптамер, т. е. РНК, способную связывать определенные молекулы. Затем колонку промывают для удаления несвязавшихся РНК, а затем смывают РНК, задержавшиеся на колонке за счет связывания с целевыми молекулами (это можно сделать, например, нагревая колонку).
С выделенных РНК с помощью обратной транскрипции делают ДНК-копии и получают из них обычные двуцепочечные молекулы ДНК. С последних же можно считывать искомые РНК-аптамеры, а затем – размножать их методом ПЦР в неограниченных количествах. Конечно, так происходит в идеальном случае, на практике все получается сложнее. Обычно исходный препарат РНК содержит огромный избыток «по-сторонних» молекул, избавиться от которого трудно. Поэтому полученную РНК вновь и вновь пропускают через колонку, чтобы выделить РНК, образующие самые прочные комплексы с целевыми молекулами.
С помощью такого метода были получены тысячи разных РНК-аптамеров, которые образуют специфические комплексы с различными органическими соединениями и молекулами.
Рассмотренная схема молекулярной селекции может быть применена для получения молекул с любыми свойствами. Например, были получены РНК, способные катализировать реакции синтеза РНК и белков: присоединение азотистых оснований к рибозе, полимеризацию активированных нуклеотидов на цепочках РНК, присоединение аминокислот к РНК. Эти исследования еще раз подтвердили, что в условиях предбиологической эволюции из случайных полимеров могли возникать молекулы РНК со специфическими структурами и функциями.
Делайте Ваш Заказ!
Метод молекулярной селекции обладает очень большими возможностями. С его помощью можно решать задачи поиска нужных молекул даже в том случае, если исходно нет идеи, как такие молекулы должны быть устроены. Однако, если придумать процедуру отбора, их можно выделить по принципу требуемых свойств, а затем уже заняться и вопросом, как эти свойства достигаются. Продемонстрируем это на примере выделения РНК, способных связываться с клеточными мембранами и модулировать их проницаемость.
Древние рибоциты должны были поглощать «питательные» вещества из окружающей среды, удалять продукты метаболизма и делиться в ходе размножения.
И все эти процессы требуют управления проницаемостью мембран. Поскольку мы полагаем, что никаких других функциональных молекул, кроме РНК, в рибоцитах не было, какие-то РНК обязательно должны были взаимодействовать с мембранами. Однако с химической точки зрения они совершенно не подходят для роли регуляторов проницаемости мембран.
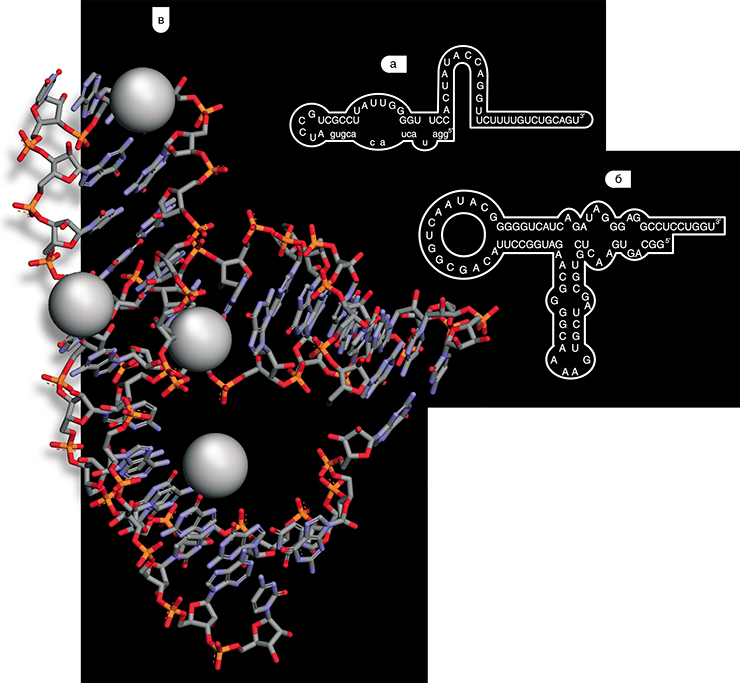
Мембраны современных клеток и липосом, построенные из жирных кислот, несут отрицательный заряд. Поскольку РНК также заряжены отрицательно, то по закону Кулона они должны отталкиваться от липидной поверхности и тем более не могут проникать в глубь липидного слоя. Единственный известный способ взаимодействия нуклеиновых кислот с поверхностью мембран – через двухзарядные ионы металлов. Эти положительно заряженные ионы могут играть роль мостиков, располагаясь между отрицательно заряженными группами на поверхности мембраны и фосфатными группами нуклеиновой кислоты. Поскольку такие мостиковые взаимодействия достаточно слабые, с мембраной может связаться только очень большая нуклеиновая кислота благодаря множеству слабых связей с поверхностью мембраны. Так маленькие враги привязали Гулливера к земле множеством тоненьких веревок.
Тут и помог исследователям метод молекулярной селекции. Из библиотеки РНК удалось выделить не-сколько молекул, которые очень успешно связывались с мембранами, а при достаточно высокой концентрации – даже разрывали их! Эти РНК обладали необычными свойствами. Они как бы помогали друг другу: смесь молекул разных сортов связывалась с мембранами гораздо лучше, чем молекулы одного сорта. Все стало ясным после изучения вторичных структур этих РНК. Оказалось, что в них имеются петли с комплементарными участками. За счет этих участков «мембранные» РНК могут формировать комплексы-сообщества, которые способны образовывать множественные контакты с мембраной и делать то, что одной молекуле РНК не под силу.
Этот селекционный эксперимент подсказал, что у РНК есть дополнительный способ приобретения новых свойств путем образования сложных надмолекулярных комплексов. Этот механизм мог использоваться и для удерживания эволюционирующих систем РНК в виде колоний на поверхностях еще до того, как эти системы обзавелись изолирующей мембраной.
«Мир РНК»: Был, Есть и Будет!
Множество данных свидетельствует о том, что «мир РНК» действительно существовал. Правда, не совсем ясно – где. Некоторые специалисты полагают, что начальные этапы эволюции происходили не на Земле, что на Землю были занесены уже функционально активные системы, которые приспособились к местным условиям. Однако с химической и биологической точки зрения это не меняет сути дела. В любом случае остается загадкой – в результате каких процессов в окружающей среде рибоциты образовались и за счет каких компонентов существовали. Ведь требуемые для жизни рибоцитов нуклеотиды – сложные молекулы. Трудно представить, что эти вещества могли образовываться в условиях пребиотического синтеза.
Вполне возможно, что древние РНК значительно отличались от современных. К сожалению, следов этих древних РНК экспериментально обнаружить нельзя, речь идет о временах, удаленных от нас на миллиарды лет. Даже скалы тех времен давно «рассыпались в песок». Поэтому речь может идти только об экспериментальном моделировании процессов, которые могли протекать на самых ранних стадиях молекулярной эволюции.
Почему произошел переход от «мира РНК» к современному миру? Белки, располагающие гораздо большим набором химических групп, чем РНК, являются лучшими катализаторами и структурными элементами. По-видимому, некоторые древние РНК стали использовать белковые молекулы в качестве «орудий труда». Такие РНК, способные к тому же синтезировать для своих целей полезные молекулы из окружающей среды, получали преимущества в размножении. Естественным путем отбирались соответствующие аптамеры и рибозимы.
А затем эволюция сделала свое дело: возник аппарат трансляции, и постепенно ответственность за катализ перешла к белкам. Орудия оказались столь удобными, что вытеснили своих «хозяев» из многих сфер деятельности.
Читатель вправе спросить: а зачем вообще нужно исследовать эволюцию РНК, ведь древний «мир РНК» исчез? Неужели только ради «чистого искусства», удовлетворения интересов фанатичных исследователей? Однако, не зная прошлого, нельзя понять настоящее. Изучение эволюции и возможностей РНК может подсказать новые направления поиска процессов, протекающих в современных живых клетках. Например, совсем недавно были обнаружены мощные системы регуляции активности генов с участием двуцепочечных РНК, с помощью которых клетка защищает себя от вирусных инфекций. Эта древняя система клеточной защиты, вероятно, скоро найдет применение в терапии.
Поэтому неудивительно, что в наше время исследования нуклеиновых кислот продолжают оставаться одной из самых «горячих точек» в молекулярной биологии. Благодаря уникальным свойствам РНК находят все более широкое применение в медицине и технике. Возникший в незапамятные времена «мир РНК» будет не только продолжать незримо существовать в наших клетках, но и возрождаться в виде новых биотехнологий.
Редакция благодарит сотрудников Института химической биологии и фундаментальной медицины СО РАН к.х.н. В. В. Коваля, к.х.н. С. Д. Мызину и к.х.н. А. А. Бондаря за помощь в подготовке статьи
Кодирующие некодирующие РНК
Несмотря на многолетние усилия, мир некодирующих РНК еще таит в себе немало загадок
Автор
Редактор
Среди всех областей и без того бурно развивающейся молекулярной биологии одной из наиболее процветающих является биология некодирующих РНК — РНК, которые никогда не «переводятся» в белки. Каждый год становятся известны всё новые и новые виды некодирующих РНК, участвующих в самых замысловатых молекулярных процессах. Кроме того, накапливается всё больше свидетельств того, что некоторые некодирующие РНК все-таки транслируются, правда, не в большие белки, а в короткие пептиды. Как же так получается? Каковы функции кодируемых этими РНК пептидов? Пока на эти вопросы нет исчерпывающего ответа. Тем не менее, что-то все-таки начинает проясняться, и об этом мы сегодня и поговорим.
«Биомолекула» не раз писала о разных аспектах биологии некодирующих РНК: об РНК-интерференции — важнейшем механизме регуляции экспрессии генов, ключевую роль в котором играют некодирующие РНК [2]; об РНК-регуляторах [3]; о двухцепочечных РНК [4] и о применении антисмысловых РНК в медицине [5].
Хотя ученые постоянно открывают всё новые и новые типы некодирующих РНК, наши старые знакомые, давно известные нкРНК, совсем недавно начали открываться с новой стороны. Оказывается, некоторые из них не такие уж и некодирующие, а могут подвергаться трансляции с образованием вполне функциональных пептидов. Пока возможность трансляции удалось доказать только для длинных некодирующих РНК, предшественников микроРНК и кольцевых РНК. Наш обзор посвящен именно этой таинственной и малоизученной стороне биологии (не)кодирующих РНК.
Длинные некодирующие РНК
К числу длинных некодирующих РНК относят нкРНК, длина которых превышает 200 нуклеотидов. В клетках днкРНК вовсе не являются диковинкой: по оценкам, в человеческом геноме имеется около 16 тысяч генов, которые в общей сложности кодируют 28 тысяч длинных некодирующих РНК. Таких РНК больше, чем генов, которые их кодируют, потому что транскрипт, считанный с одного гена, разрезается на несколько самостоятельных молекул, каждая из которых функционирует как днкРНК. Группа длинных некодирующих РНК очень разнородна: некоторые ее представители являются антисмысловыми РНК (то есть транскриптами, считанными с белок-кодирующих генов, но в обратном направлении); другие соответствуют вырезанным из мРНК интронам; наконец, третьи считываются с длинных межгенных промежутков.
Функции, которые могут выполнять длинные некодирующие РНК, также в высшей степени разнообразны. Они могут регулировать транскрипцию белок-кодирующих генов, связываться с различными белками, влияя на их функционирование, а также контролировать процессы созревания других РНК, их экспорт из ядра и синтез белка. Кажется логичным, что в некоторых длинных некодирующих РНК могут найтись хотя бы совсем короткие открытые рамки считывания: длинная последовательность будет содержать рамку считывания с бóльшей вероятностью, чем короткая. Кроме того, длинные некодирующие РНК локализуются преимущественно в цитоплазме, где и происходит трансляция, и созревают так же, как мРНК: они транскрибируются РНК-полимеразой II, подвергаются сплайсингу, имеют кэп и поли(А)-хвост. Действительно, недавно подсчитали, что более 40% днкРНК потенциально могут транслироваться в пептиды, состоящие более чем из десяти аминокислотных остатков. Каким же образом удалось это установить? Как правило, применяли метод, известный как рибосомное профилирование (хотя, заметим, часто используют не совсем правильный перевод термина — «рибосомальный профилинг» — прим. ред.) [1].
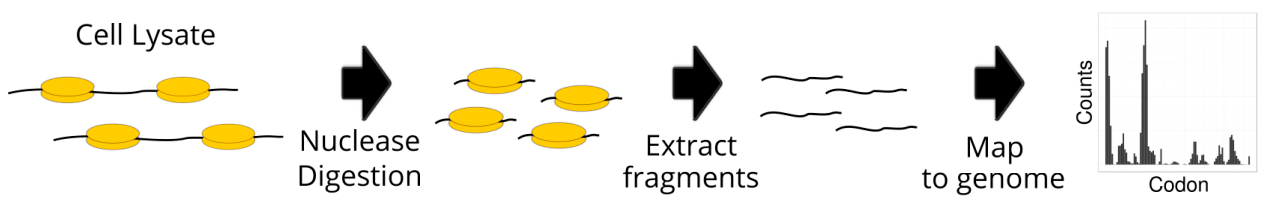
Рибосомное профилирование
О том, что такое полимеразная цепная реакция и секвенирование, можно прочитать в статьях нашего спецпроекта «12 методов в картинках»: «Полимеразная цепная реакция» [6] и «Секвенирование нуклеиновых кислот» [7].
Рисунок 1. Основные этапы рибосомного профилирования
Функциональные пептиды пока известны только для четырех длинных некодирующих РНК. У дрозофилы есть днкРНК pncr003:2L, которая содержит две открытые рамки считывания, соответствующие пептидам длиной менее 30 аминокислотных остатков. Оба этих пептида обнаруживаются в диадах — местах соединения Т-трубочек и цистерн саркоплазматического ретикулума в мышечных клетках. При нокауте или нокдауне соответствующего гена у мух наблюдается повышенная аритмия сердечных сокращений. Вероятнее всего, оба пептида участвуют в обмене кальция в мышечных клетках и взаимодействуют с кальциевой АТФазой саркоплазматического ретикулума, которая откачивает ионы кальция из цитозоля в саркоплазматический ретикулум в ходе расслабления мышцы [1].
О нокауте и нокдауне читайте в статье нашего спецпроекта «12 методов в картинках» «Генная инженерия. Часть II: инструменты и техники» [8].
У мышей есть пептид миорегулин (MLN), состоящий из 46 аминокислотных остатков и считывающийся с длинной некодирующей РНК. Он синтезируется в скелетных мышцах, но не в сердечной и гладких мышцах. Миорегулин связывается с изоформой кальциевой АТФазы саркоплазматического ретикулума, специфичной для скелетных мышц, и подавляет её работу, препятствуя откачке кальция из цитоплазмы в саркоплазматический ретикулум. Мыши, нокаутные по миорегулину, оказываются выносливее мышей дикого типа и имеют бóльшее содержание кальция в саркоплазматическом ретикулуме [1].
Мышиная длинная некодирующая РНК, известная как DWORF, тоже специфична для мышечной ткани и содержит открытую рамку считывания из 34 кодонов. Соответствующий пептид также взаимодействует с кальциевой АТФазой саркоплазматического ретикулума, препятствуя ее связыванию с миорегулином и другими пептидами, подавляющими ее активность, и таким образом способствует ее активной работе [1].
Человеческая длинная некодирующая РНК LINC00961 кодирует пептид из 90 аминокислотных остатков, получивший название SPAR. У мышей тоже есть этот пептид, однако он состоит из 75 аминокислот. SPAR локализуется в поздних эндосомах и лизосомах и взаимодействует с лизосомной АТФазой. У мышей, нокаутных по SPAR’у, наблюдается повышенная способность к регенерации мышц за счет усиленной работы сигнального пути mTORC1, который у мышей дикого типа подавляется SPAR’ом [1].
Предшественники микроРНК
МикроРНК представляют собой короткие одноцепочечные РНК длиной от 18 до 22 нуклеотидов. Процессинг микроРНК включает два основных этапа. На первом этапе длинный транскрипт, считанный с гена микроРНК и обозначаемый «при-микроРНК», разрезается на более короткие предшественники — пре-микроРНК. Далее пре-микроРНК выходят из ядра в цитоплазму и разрезаются на собственно микроРНК. Понятно, что микроРНК слишком коротки, чтобы что-то кодировать. А вот предшественники, например, при-микроРНК, вполне могут содержать открытые рамки считывания. Кроме того, при-микроРНК имеют кэп на 5′-конце и поли(А)-хвост на 3′-конце, как мРНК.
Пока что только у растений удалось выявить белковые продукты при-микроРНК. Первичный транскрипт miR171b люцерны усеченной содержит две рамки считывания, соответствующие пептидам длиной 20 и 5 аминокислотных остатков. Наиболее длинный пептид (miPEP171b) удалось выявить в зачатках боковых корней растения. Выяснилось, что miPEP171b способствует накоплению микроРНК, соответствующей тому же гену. Хотя бы одна открытая рамка считывания имеется у примерно 50 при-микроРНК резуховидки Таля — популярного модельного объекта. Удалось показать, что один из кодируемых ими пептидов, miPEP165a, консервативен среди всех капустноцветных и тоже повышает накопление микроРНК, считываемой с того же гена. Обработка проростков искусственным miPEP165a приводила к увеличению длины корней. Аналогичный эффект на соответствующие микроРНК показан для ряда других пептидов, считываемых с при-микроРНК, однако конкретный механизм, лежащий в основе этого эффекта, остается загадкой [1].
Кольцевые РНК
Благодаря отсутствию концов трансляция кольцевых РНК, число нуклеотидов в которых кратно трем, может приводить к образованию длинных полипептидов (теоретически бесконечной длины), состоящих из повторяющихся блоков одних и тех же аминокислот. В этом случае ограничение длины пептида будет связано лишь с процессивностью (то есть способностью функционировать, не отсоединяясь от матрицы) рибосомы. Если же число нуклеотидов в кольцевой РНК не кратно трем, то каждый оборот трансляции будет сопровождаться сдвигом рамки считывания, и продуктом будет цепочка из повторов трех различных полипептидов. Нечто похожее происходит у некоторых вироидов — субвирусных агентов, геном которых представлен кольцевой молекулой РНК. У них три разных полипептида образуются с одной и той же кольцевой РНК за счет сдвигов рамки считывания. Однако свидетельств в пользу существования такой «бесконечной» трансляции в клетках пока нет [10].
Пока совсем немного экспериментальных свидетельств и в целом трансляции клеточных кольцевых РНК. У дрозофилы удалось «поймать» рибосому с помощью профилирования на 37 кольцевых РНК, однако для большинства РНК соответствующие им пептиды не идентифицированы. Удалось, однако, выделить пептид, считываемый с кольцевой РНК circMbl. Другая кольцевая РНК, circ-ZNF609, содержит открытую рамку считывания длиной 753 нуклеотида, и многие молекулы этой РНК выделены в составе полисомных комплексов (то есть связанными с несколькими рибосомами). Кроме того, в ней содержится последовательность, соответствующая IRES. С помощью искусственных конструктов удалось показать возможность трансляции открытой рамки считывания из circ-ZNF609, однако сам пептид не выделили. У человека обнаружили 250 кольцевых РНК, связанных с полисомами, и идентифицировали 33 пептида, закодированных кольцевыми РНК [1].
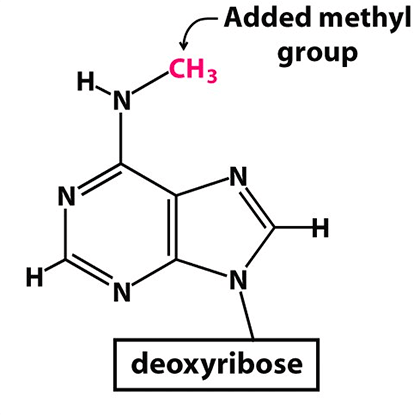
Рисунок 2. Метилированный аденозин (m 6 A)
Многие мРНК (как клеточные, так и вирусные) подвергаются особой модификации — метилированию аденозина (сокращенное обозначение m 6 A). Метилирование аденозина заключается в присоединении метильной группы к атому азота у шестого атома углерода аденина (рис. 2).
Зеленый флуоресцентный белок стал верным помощником ученых в изучении самых разнообразных клеточных процессов. Об открытии и применении GFP можно прочитать в нашей статье «Флуоресцирующая Нобелевская премия по химии» [11]
На что может влиять трансляция некодирующих РНК
Различным аспектам аутоиммунитета посвящен спецпроект «Биомолекулы» «Аутоиммунные заболевания».
Подводя итог, можно сказать, что мы только-только начали приоткрывать завесу тайны над трансляцией некодирующих РНК и знаем совсем немного, поэтому будем с нетерпением ждать новых открытий в этой интереснейшей области молекулярной биологии.
РНК у истоков жизни?
16 августа 2013
РНК у истоков жизни?
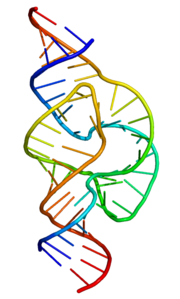
Сторонники теории мира РНК утверждают, что жизнь на нашей планете началась с рибозимов — молекул РНК, способных к катализу без участия белковых ферментов. На рисунке — один из таких рибозимов, обладающих рибонуклеазной активностью.
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Идея того, что жизнь могла возникнуть на основе самореплицирующихся молекул РНК, уже не нова. В самом деле, РНК совмещает в себе как функцию хранения наследственной информации, так и способность к биохимическому катализу. Сейчас гипотеза РНК-мира из чисто умозрительной теории превратилась в теоретическую модель, имеющую хорошую доказательную и экспериментальную базу. Безусловно, эта теория вызывает много вопросов, но, тем не менее, она по полному праву может быть названа одной из наиболее обоснованных гипотез возникновения жизни на Земле.
Конкурс «био/мол/текст»-2013
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2013 в номинации «Лучший обзор».
Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
Противоречия гипотезы мира РНК
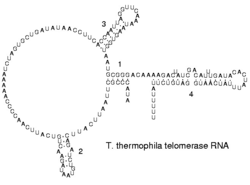
Идея мира РНК была высказана в 1968 году Карлом Вёзе [1], а окончательно сформулирована в 1986 году нобелевским лауреатом Уолтером Гильбертом. То, что РНК способна как хранить наследственную информацию, так и выполнять работу (например, при биосинтезе белка), было известно и ранее. Но окончательно гипотеза мира РНК смогла сформироваться лишь после открытия в 1981 году рибосомальной РНК из ресничного простейшего Tetrahymena, которая способна к автосплайсингу. Осуществляется это следующим образом: к интронной последовательности РНК прикрепляется нуклеотид G, далее цепь разрезается в месте присоединения нуклеотида. После этого происходит окончательное вырезание интрона и сшивание экзонов. Более того, эта интронная последовательность обладает рибонуклеазной активностью, т.е. она способна связываться с субстратной РНК и специфично разрезать её. Такие свойства рибонуклеиновому интрону придаёт его способность к образованию сложных трёхмерных структур.
Однако платой за высокую лабильность РНК служит её склонность к быстрой деградации. Здесь мы и сталкиваемся с первой трудностью концепции РНК-мира. Как молекула может служить надёжным хранилищем генетической информации, если время её жизни мало?
У млекопитающих время жизни мРНК в клетках составляет от нескольких минут до нескольких часов, максимум дней. У бактерий и вовсе, мРНК «живёт» от нескольких секунд до часа с небольшим. Согласитесь, недолго для надёжного хранилища информации! Тем более, в пребиотических условиях, агрессивная среда которых мало способствовала стабильности молекул.
Это противоречие способны разрешить некоторые предположения. Считается, что первые РНК могли размножаться в микрополостях во льду. В подтверждение этому, по данным ряда экспериментов, максимальная рибозимная активность РНК наблюдается при температуре около −8 °С. Возможно, это связано с тем, что при подобных температурах увеличивается концентрация РНК и понижается активность воды. Однако вероятная сложность здесь заключается в том, что РНК при низких температурах обретают повышенную склонность к образованию водородных связей между комплементарным нуклеотидами, что ведёт к образованию межмолекулярных комплексов и снижению каталитической активности [2].
Следующей большой трудностью является склонность РНК к гидролизу при pH>6. Фосфодиэфирные связи между нуклеотидами наиболее стабильны при рН, лежащих в пределах 4–5.
Также двоякую роль играют и ионы Mg 2+ : с одной стороны, они стабилизируют вторичную и третичную структуры РНК (что критично для способности к катализу), с другой же, их высокая концентрация способствует деградации молекул. Выше упоминалось, что молекулы РНК наиболее стабильны в кислой среде. В этих условиях цитозин и аденозин протонируются, тем самым обретая дополнительный положительный заряд, что снижает потребность в катионах. К примеру, при рН=4 некоторые рибозимы сохраняют свою активность даже в отсутствие ионов [2].
РНК является весьма сложной молекулой, и вероятность её внезапного возникновения из отдельных атомов или фрагментов крайне низка. Действительно, сложно себе представить, как могли соединиться вместе азотистое основание, рибоза и фосфат, образовав нуклеотид. Однако Санчез, Оргел, Паунер и Сазердэнд показали возможность синтеза пиримидинов из молекул, вероятно, имевшихся в пребиотических условиях Земли [3].
Также важно понять, каким образом осуществлялась полимеризация первых нуклеотидов в полимерные цепочки. Относительна недавно была обнаружена важная роль различных минералов и ионов металлов в катализе при образовании биополимеров [4]. К примеру, монтмориллонит катализирует полимеризацию нуклеотидов, 5′-фосфат которых ранее был активирован имидазолом. Более того, монтмориллонит способен образовывать везикулы из простых жирных кислот [4]. Таким образом, этот минерал, с одной стороны, способствует полимеризации нуклеотидов, а с другой — образованию мембранных структур.
Гипотетически, существует множество вариантов соединения рибонуклеотидов друг с другом через различные атомы рибозы. Однако в живых организмах нуклеотиды соединены друг с другом через 3′,5′-фосфодиэфирную связь (за некоторыми исключения: например, кэп в мРНК эукариот присоединяется через 5′,5′-связь). Недавние исследования Шостака показали, что рибозимы, имеющие в своём составе нуклеотиды, соединённые как через 3′,5′-связь, так и через 2’,5′-связь, частично сохраняли каталитические свойства [5]. Вероятно, в первых рибонуклеиновых полимерах могли реализовываться различные варианты фосфодиэфирной связи, однако эволюцией была отобрана именно 3′,5′-связь.
Зачастую каталитической активностью обладают лишь длинные цепочки РНК. Это один из основных объектов критики теории РНК-мира, ибо случайное возникновение длинных последовательностей, способных выполнять биохимическую работу, весьма маловероятно. Одна из лучших рибозимных репликаз, созданных на сегодня, способна реплицировать до 95 нуклеотидов [6], однако сама она при этом имеет длину в 190 нуклеотидов (см. врезку). Длина этой последовательности слишком велика для спонтанного возникновения в пребиотических условиях. Исследования in vitro показывают, что для выделения молекул, способных к катализу, требуется около 10 13 —10 14 молекул РНК [2] — довольно много для того, чтобы столь длинный рибозим мог появиться в готовом виде. Однако открытие коротких рибозимов ставит под сомнение идею того, что для появления РНК-катлизаторов требуются астрономические количества молекул. В самом деле, получены полирибонуклеотиды c активными дуплексами, способными к самовырезанию, имеющие длину лишь 7 остатков [2]. Более того, были получены данные, что даже рибозим, урезанный всего лишь до пяти нуклеотидов, сохранял свои ферментативные способности [2]. Но каталитическая активность у минирибозимов значительно ниже, чем у их более длинных «собратьев». Из этого следует, что короткие рибозимы могли быть эволюционными предшественниками длинных. Со временем они приобрели бóльшую длину, которая способствовала обретению более правильной структуры и, как следствие, улучшению каталитических свойств.
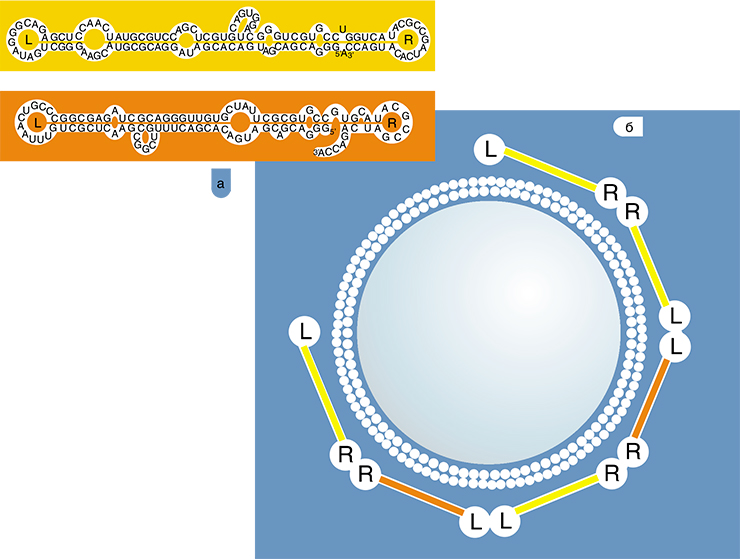
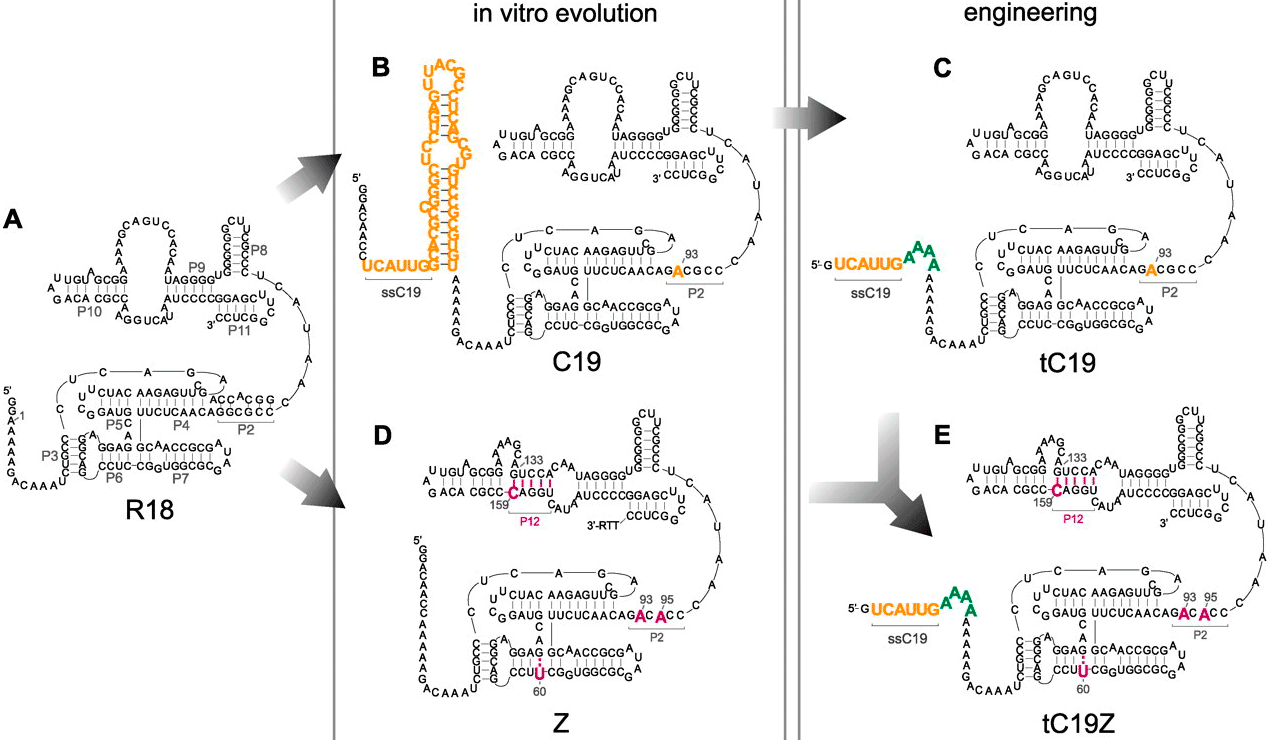
Рибозимные репликазы
Для того, чтобы в мире РНК полирибонуклеотиды могли размножаться, должны были существовать рибозимные аналоги белковых полимераз. В современных живых организмах рибозимы с таким видом активности не обнаружены, однако подобные молекулы были созданы искусственно. Молекулярные биологи из Великобритании обратили внимание на ранее известный рибозим R18, обладающий полимеразной активностью [6]. Он и стал объектом эксперимента: путём искусственной эволюции и разумного планирования из исходного рибозима были получены четыре новые молекулы с улучшенными каталитическими свойствами [7]. Дело в том, что исходный рибозим R18 (обозначен на картинке буквой А) был способен реплицировать лишь фрагменты РНК длиной до 20 нуклеотидов. Также им могла быть реплицирована далеко не каждая последовательность РНК, а лишь узкий круг определённых матриц [7]. Учёные пошли двумя путями:
В результате, полезные свойства рибозимов tC19 и Z удалось объединить в одном, названном tC19Z. Данный рибозим способен копировать как довольно широкий круг матриц, так и достаточно длинные последовательности [7].
Интроны, способные вырезаться самостоятельно, были обнаружены в тирозиновой тРНК таких сложных организмов, как человек и цветковое двудольное растение Arabidopsis thaliana. Эти 12-ти и 20-ти нуклеотидные участки в клетке вырезаются путём сплайсинга с участием белков, однако этот интрон показал способность вырезать самого себя и без участия ферментов.
РНК-переключатели
Ограниченная каталитическая способность рибозимов часто становится ещё одним хлипким краеугольным камнем теории мира РНК. Критики теории считают, что тот минимум химических реакций, который необходим для осуществления метаболизма в мире РНК, не может быть обеспечен одними лишь рибозимами. Подавляющее большинство РНК-катализаторов катализируют лишь разрыв и создание фософодиэфирных связей между нуклеотидами. Кажется, что молекулы РНК со своими четырьмя весьма схожими мономерами безнадёжно проигрывают в химическом разнообразии белкам, которые имеют в своём составе 20 аминокислот, весьма различных по свойствам. Однако не стоит забывать, что многие белковые ферменты для выполнения активной работы должны присоединить лиганды — кофакторы, — без которых ферментативная активность попросту исчезает.
И здесь стоит вспомнить об РНК-перключателях или рибопереключателях (англ. riboswitches). Что же это такое? Как известно, информация об аминокислотной последовательности белка передаётся в рибосому через мРНК. Матричная РНК транскрибируется с ДНК посредством фермента ДНК-полимераза II. В данном случае, помимо самого гена, транскрибируется участок впереди него, на котором и расположен рибоперключатель [8]. РНК-переключатель представляет собой участок мРНК, способный связывать молекулу строго определённого вещества. После связывания переключатель меняет свою пространственную конфигурацию, что делает невозможной дальнейшую транскрипцию [8].
Важно понимать принцип работы РНК-переключателей, поэтому скажем пару слов об их устройстве. Состоит он из двух частей: из аптамера и «экспрессионной платформы». Аптамер, по сути, является рецептором, который с очень высокой селективностью связывается с определённой молекулой. Эффекторной молекулой для аптамера является молекула, производимая белком, ген которого и регулируется переключателем. «Экспрессионная платформа» и есть сам РНК-переключатель, который после связывания рецептора с лигандом меняют конфигурацию и препятствует дальнейшей транскрипции.
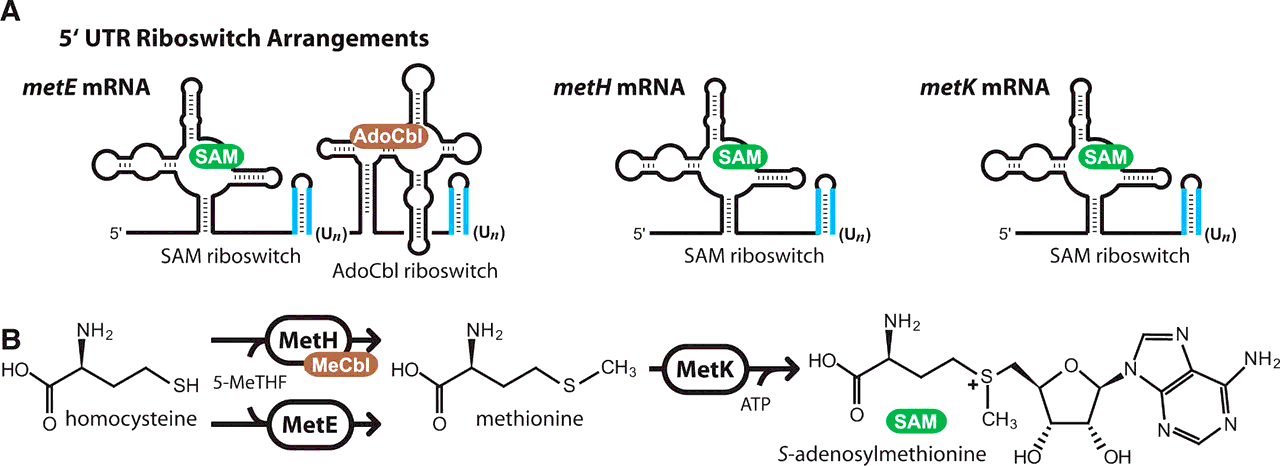
Однако существуют и РНК-переключатели, действующие по более сложному механизму. Например, рибопереключатель, контролирующий транскрипцию гена metE бактерии Bacillus clausii, является двойным, т.е. имеет два рецепторных участка, связывающих две разных молекулы [9]. Разберём данный механизм подробнее.
Ген metE кодирует фермент, превращающий гомоцистеин в аминокислоту метионин. Затем метионин используется (уже другим ферментом) для синтеза S-аденозилметионина (или проще — SAM). Помимо гена metE, существует и другой ген — metН. Белок гена metН катализирует ту же реакцию, но с большей эффективностью, чем metE. Однако metН для своей работы требует кофермент — метилкобаламин (или MeCbl), синтезируемый из аденозилкобаламина (или AdoCbl). Так вот, транскрипт metE имеет РНК-переключатель, который содержит два связывающих участка: один для SAM, другой — для AdoCbl. Данный переключатель способен действовать как логический элемент NOR (и/или) [9]. То есть, для выключения metE достаточно связывания с рецепторами рибопереключателя либо одной из эффекторных молекул, либо сразу обеих. Сам механизм прерывания трансляции основан на образовании шпильки путём удаления шести нуклеотидов из рибопереключателя (рис. 1А). Логику действий такого элемента NOR можно описать так: «Я подавляю транскрипцию, если в среде присутствует либо вещество А, либо вещество В, либо оба вещества сразу». Остаётся только удивляться, сколь красивы и элегантны решения Природы!
Рисунок 1. Работа рибопереключателей. А — Рибопереключатели на транскриптах генов metE, metH и metK. Голубым обозначены шпилечные структуры, образуемые в результате вырезания шести или более уридиновых нуклеотидов. Видно, что у metE имеется два акцепторных и два шпилечных участка. В — Путь биосинтеза S-аденозилметионина. На первом этапе гомоцистеин преобразуется в амикислоту метионин. Это превращение может быть катализировано одним из двух ферментов: metE или metH. metH проводит эту реакцию с большей эффективностью, однако требует для своей работы дополнительного вещества (кофактора). На втором этапе фермент metK превращает метионин в S-аденозилметионин.
Между тем, РНК-переключатели способны связывать значительное число белковых кофакторов, таких как флавинмононуклеотид, тиаминпирофосфат, тетрагидрофолат, S-аденозилметионин, аденозилкобаламин [8]. Изначально считалось, что РНК-переключатели способны лишь подавлять экспрессию генов [8], но позже были получены данные, свидетельствующие о том, что некоторые переключатели, напротив, ее усиливают. Сами по себе РНК-переключатели представляют весьма интересное явление, так как они демонстрируют возможность регуляции работы генов без прямого участия белков — иными словами, демонстрирует самодостаточность и универсальность РНК. Судя по всему, РНК-переключатели являются очень древним механизмом: так, они обнаружены во всех доменах живой природы: у бактерий, архей и эукариот [8]. Похоже, что, по меньшей мере, некоторые из современных кофакторов белков были прямиком заимствованы из мира РНК. Можно нарисовать примерно такую картину: рибозимы изначально использовали многие из современных кофаторов для своих целей, однако с появлением более эффективных белковых ферментов эти кофакторы были заимствованы последними.
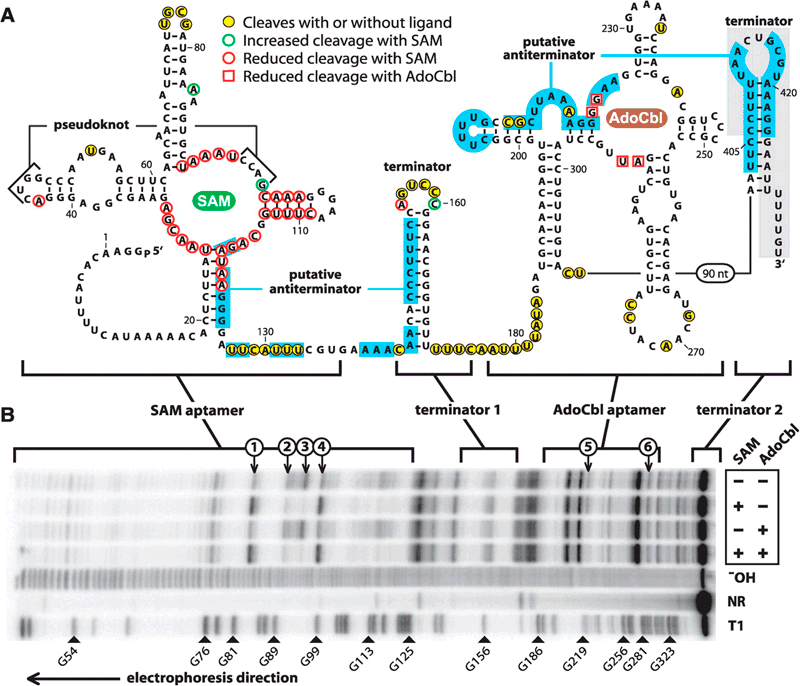
Рисунок 2. Вторичная структура РНК-переключателя гена metE. Выделены акцепторы — сайты связывания с молекулами SAM и AdoCbl, а также шпилечные терминирующие структуры.
Геномные тэги и тРНК
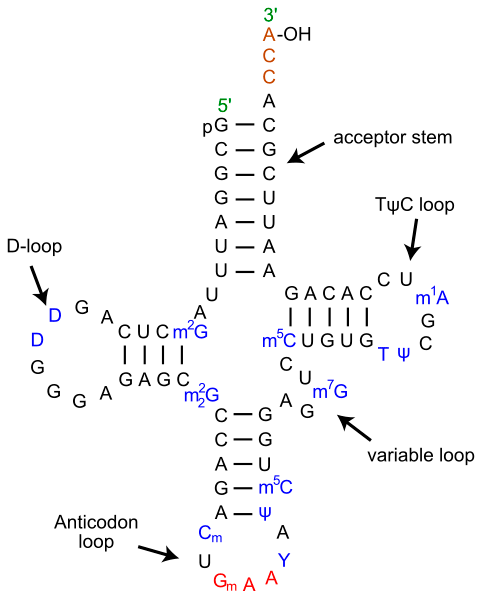
Рисунок 3. Вторичная структура тРНК. На рисунке отчётливо видна характерная для тРНК вторичная структура в виде «клеверного листа». В верхней половине молекулы на 3′-конце расположена CCA-область и акцепторная петля, связывающая аминокислоту. В нижней части молекулы находится антикодоновая петля, ответственная за комплементарное связывание с кодоном мРНК. Согласно гипотезе геномного тэга, верхняя и нижняя половины тРНК эволюционировали по отдельности, причём верхняя половина древнее нижней.
Всем хорошо известна важная роль тРНК в биосинтезе белка. Однако у тРНК и подобных ей молекул есть другая, менее известная, но не менее важная функция: в различных репликативных процессах они исполняют роль праймеров и шаблонов. Это могут быть процессы репликации одноцепочечной вирусной РНК, репликация митохондриальной ДНК у грибов, репликации теломер [10].
Обратимся к вирусной РНК. 3′-конец многих бактериальных вирусов и вирусов растений структурно очень похож на «верхнюю половину» современной тРНК (та часть молекулы, которая связывается с аминокислотой; рис. 3). Подобные участки, расположенные на 3′-концах, названы «геномными тэгами» [10]. Тэг играет роль шаблона при инициации репликации вирусной РНК. Более того, эти участки бывают настолько похожи на «настоящие» тРНК [10], что могут быть аминоацилированы (т.е. к ним может быть присоединена аминокислота) при помощи фермента аминоацил-тРНК-синтетазы.
Также репликация многих РНК у ретровирусов начинается с того, что к сайту связывания праймера на вирусной РНК присоединяется тРНК хозяйского организма [9]. Тем самым видно, что тРНК современных организмов способны также служить и праймерами. Затем, используя тРНК как праймер, обратная транскриптаза копирует вирусный РНК-геном в ДНК.
Возможно ли, что тРНК сегодняшних организмов произошли от древних геномных тэгов? Алан Вейнер и Нэнси Мэйцелс [10] отвечают на этот вопрос утвердительно. Согласно их теории, верхняя и нижняя половинки тРНК эволюционировали по-отдельности, причём верхняя часть тРНК появилась раньше нижней и является потомком геномных тэгов [10].
Происхождение рибосом
При построении гипотезы мира РНК много внимания уделяется и происхождению рибосом, потому что их образование фактически можно приравнять к переходу от РНК-катализа к белковому процессу. Как известно, рибосома состоит из двух субъединиц: малой и большой. Ключевую роль в синтезе белковой цепи играет большая субъединица рибосомы, в то время как маленькая считывает мРНК. Модель происхождения одной из молекул большой субъединицы была предложена канадскими биохимиками Константином Боковым и Сергеем Штейнбергом [11].
Они сосредоточили внимание на 23s-рРНК (состоящей из шести доменов, I–VI), так как именно в этой молекуле находится функциональный центр, ответственный за реакцию транспептидации (присоединение новой аминокислоты к растущей полипептидной цепи). Данная молекула содержит около трёх тысяч нуклеотидов и способна образовывать сложные трёхмерные структуры. Важную роль в поддержании трёхмерной структуры молекулы играют так называемые А-минорные связи [11]. Они представляют собой связи между «стопками» нуклеотидов (как правило, аденозинов [11]) с участками, образующими двойные спирали. Связи формируются между спиралями и стопками, расположенными в разных областях молекулы.
23s-рРНК слишком сложна, чтобы она могла появиться сразу в готовом виде [12]. Соответственно, в молекуле должна присутствовать некая более простая структура, с которой и началась её эволюция. Особое внимание исследователей привлёк домен V [11]. Интересным в нём было то, что он содержит большое количество двойных спиралей при фактически полном отсутствии аденозиновых стопок. Вот что пишут по этому поводу авторы исследования: «Чтобы объяснить аномалию, имеющую место в домене V, мы предположили, что это отражает порядок, в котором различные части присоединялись к 23s-рРНК по мере её эволюции. В А-минорных мотивах конформационная стабильность аденозиновых стопок зависит от присутствия двойных спиралей, в то время как двойные спирали способны сохранять стабильную структуру сами по себе» [11]. Из этого следует, что домен V является наиболее древней частью молекулы: его спиральные участки, что придают стабильность всей молекуле, должны были появиться раньше других частей, содержащих аденозиновые стопки. Более того, именно в пятом домене находится функциональный центр, ответственный за формирование пептидной связи в процессе биосинтеза белка.
Выходит, что пятый домен является и функциональным центром молекулы, и её структурным остовом. Это говорит о том, что эволюция 23s-рРНК началась именно с него. Далее авторы попытались реконструировать эволюцию 23s-рРНК. Для этого они разбили молекулу на 60 относительно небольших участков и попытались «разобрать» её так, чтобы, убирая части поэтапно, не повредить структуру оставшейся молекулы. Опустив детали, укажем, что вывод был именно такой: эволюция этой молекулы началась именно с пептидил-трансферазного центра пятого домена, так как при разборке он оставался последним неповреждённым участком (см. рис. 4). Исследователи считают, что именно эта структура и является древней «проторибосомой». Способна ли эта маленькая часть огромной молекулы выполнять свою работу самостоятельно? Исследования дают положительный ответ. В ходе экспериментов были получены искусственно выведенные рибозимы, способные осуществлять реакцию транспептидации [12].
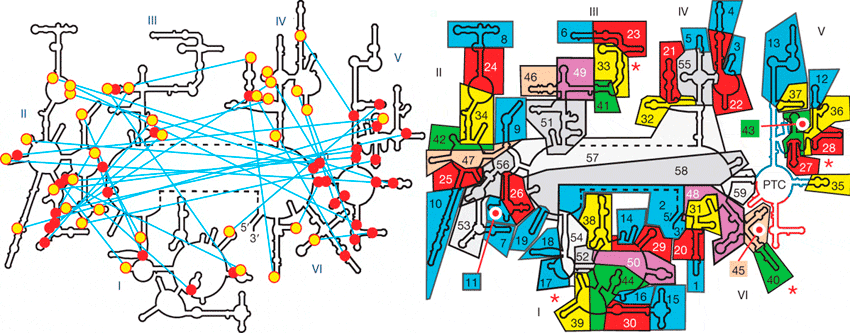
Рисунок 4. Эволюция «проторибосомы». Слева — Вторичная структура 23s-рРНК. Красные кружочки изображают спиральные участки, жёлтые — аденозиновые «стопки». Голубые линии показывают А-минорные связи. Римские цифры обозначают домены молекулы. Отчётливо видно, что наибольшее количество спиральных участков находится в домене V. Справа — Для того чтобы выяснить процесс эволюции 23s-рРНК, авторы разбили молекулу на 60 структурных блоков. Далее они попытались «разобрать» молекулу так, чтобы при последовательном удалении этих блоков молекула продолжала работать [12]. Сначала они отделили 19 блоков, не повредив при этом оставшиеся. После удалось отделить ещё 11 блоков, а затем ещё последовательно 9, 5, 3, 3, 2, 2, 2. Затем ещё три блока оказалось возможным отделить по одному [12].
По всей видимости, именно пятый домен послужил «стартовой точкой» в эволюции 23s-рРНК. Позже к нему начали добавляться различные блоки, улучшающие работы молекулы. Изначально к проторибосоме присоединилось восемь блоков, образовавших «основание», что повлекло за собой увеличение стабильности всей молекулы. Затем добавились следующие 12 блоков, которые образовали структуры, позволяющие соединяться большой и малой субъединицам друг с другом. Последними добавились блоки, образующие т.н. «протуберанцы» — выросты на поверхности большой субъединицы [12]. Функция этих выростов в том, чтобы помочь рибосоме выбрать нужную аминоацил-тРНК, а также «выпустить на волю» ту тРНК, которая уже отдала свою аминокислоту растущей белковой молекуле.
Следы мира РНК
Наследие мира РНК можно обнаружить в любом живом организме. Вспомним рибосомы, которые, по всей видимости, являются реликтами очень давней эпохи, ведь структурно и функционально рибосомы крайне схожи и у человека, и у дождевого червя, и у кишечной палочки. Главный переносчик энергии в клетке — молекула аденозинтрифосфата — представляет собой не что иное, как аденозин с двумя дополнительными фосфатами. Такие важнейшие молекулы, как переносчики электронов ФАД и НАД также являются модифицированными нуклеотидами. Конечно, гипотеза мира РНК ещё не доказана, да и нет гарантий, что когда-нибудь это случится. Но факт того, что важнейшие процессы в клетке протекают при активном участии РНК и рибонуклеотидов, может служить веским доводом в пользу истинности этой теории.
Двуликие геномы! Что такое амбисенсные вирусные РНК?
Двусмысленные вирусные геномы содержат участки как положительной, так и отрицательной «полярности»
здесь и далее рисунки Андрея Занкевича
Автор
Редактор
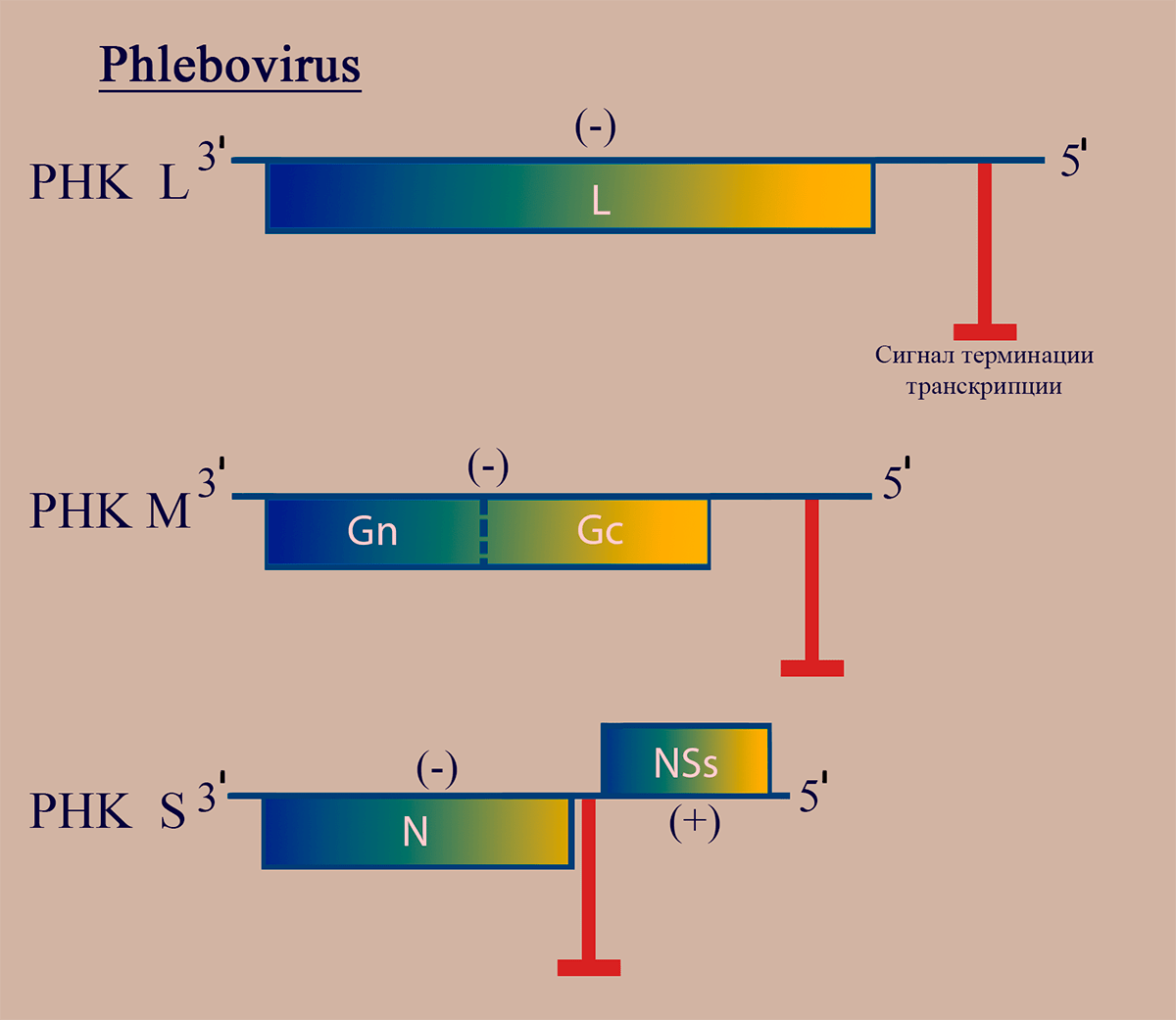
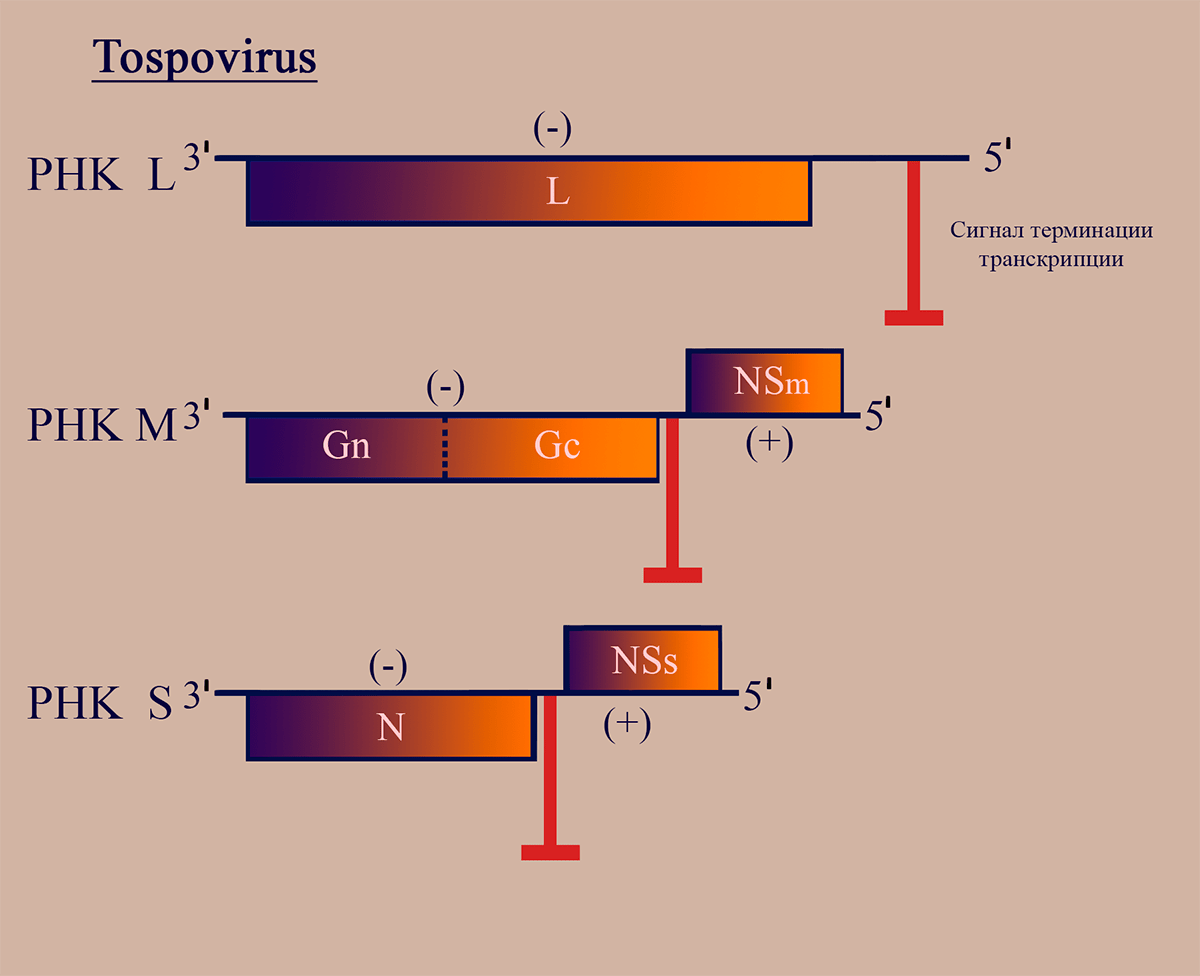
Статья на конкурс «Био/Мол/Текст»: Некоторые РНК-вирусы человека, животных и растений демонстрируют чудеса организации структуры генома, который, хотя и представлен одноцепочечной молекулой РНК, кодирует две трансляционные рамки, направленные в разные стороны. Что это за вирусы, и как им это удаётся? Давайте попробуем разобраться.
Конкурс «Био/Мол/Текст»-2020/2021
Эта работа опубликована в номинации «Вирусы и микроорганизмы» конкурса «Био/Мол/Текст»-2020/2021.
Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.
Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Напомним, что РНК (рибонуклеиновая кислота) — это такая молекула, представляющая собой одну цепочку нуклеотидов. В составе каждого нуклеотида присутствует остаток моносахарида рибозы. На сегодняшний день известно множество разных типов РНК, которые выполняют совершенно разные функции: от кодирования клеточных белков (мРНК) до противовирусной защиты (некоторые микроРНК) [1–5]. РНК, входящие в состав многих вирусов, могут иметь ряд оригинальных функций, таких как регуляция времени экспрессии различных вирусных генов путем изменения пространственной организации цепи РНК или привлечение клеточных белковых комплексов.
Биологи привыкли думать об РНК главным образом как о «молекуле-посреднике» между ДНК и белком. Именно молекулы матричной РНК (мРНК) распознаются рибосомами — молекулярными машинками, расшифровывающими последовательность РНК в процессе синтеза белка. мРНК имеют в своем составе кодирующие последовательности и, как правило, некодирующие области на 5′- и 3′-концах. Для мРНК эукариот характерно наличие особой кэп-структуры (которая узнается рибосомой) на 5′-конце и полиаденозиновой последовательности на 3′-конце («ключик» для выхода из ядра, вдобавок повышающий стабильность такой мРНК). мРНК называют РНК положительной полярности, или (+)РНК, то есть РНК, с которой не нужно проводить никаких дополнительных операций — у нее есть всё, что нужно для «посадки» рибосомы и последующей трансляции! У некоторых вирусов встречаются молекулы РНК отрицательной полярности, или (–)РНК, несущие комплементарные кодирующим последовательностям участки. В таком случае для образования вирусной мРНК необходима эта самая (–)РНК, а также вирусный фермент, осуществляющий матричный синтез комплементарной РНК-цепи.
Но бывает ли такое, что в пределах одной молекулы РНК одна ее часть, кодирующая некоторый белковый продукт, имеет положительную полярность, в то время как другая часть цепи представлена участком отрицательной полярности, кодирующим другой белок? Могла ли такая молекула возникнуть в процессе эволюции живых форм?
Ответ — да! И для того, чтобы разобраться, как функционируют такие молекулы, нам предстоит погрузиться в таинственный мир вирусов.
Давным-давно, в далекой-далекой галактике.
Сегодня очень популярна гипотеза «РНК-мира» [6], указывающая на РНК как на главного кандидата в прародители жизни на нашей планете. Поскольку РНК может как кодировать информацию, так и проявлять иногда каталитическую (рибозимную) активность (то есть специфически ускорять протекание определенных химических реакций), молекулы РНК, включающие обе эти функции, вполне могли бы являться первыми объектами живой природы, так как при наличии субстрата они способны реплицировать сами себя.
Как известно, все формы жизни обладают определенной наследственностью, которая определяет степень генетической идентичности живых объектов. В качестве молекул, ответственных за поддержание такой наследственной идентичности, выступают нуклеиновые кислоты (ДНК и РНК). Клеточные формы жизни для хранения и передачи информации используют только один тип нуклеиновых кислот — дезоксирибонуклеиновую кислоту (ДНК), в то время как вирусы в качестве основной молекулы наследственности могут использовать либо ДНК, либо РНК.
В случае ДНК-содержащих вирусов реализуется, как правило, Центральная догма молекулярной биологии в классическом виде: попав в клетку, ДНК удваивается в процессе репликации вирусного генома, на матрице ДНК в ходе транскрипции синтезируются мРНК, которые затем прочитываются рибосомой, синтезирующей по ним вирусные белки, то есть осуществляется трансляция. Далее вирусные белки ассоциируются с ДНК-геномом вируса в вирусную частицу (вирион), которая способна заражать новые клетки.
Очевидно, что РНК-содержащие вирусы используют иные стратегии размножения и, следовательно, реализации своего генома. Непривычные для большинства биологов молекулярные механизмы, которые используются такими вирусами, вероятно, унаследованы от далеких предков из того самого РНК-мира.
Размножение РНК-вирусов подразумевает использование разных типов РНК:
Немного истории
Первым найденным РНК-вирусом стал бактериофаг f2, инфицирующий бактерию кишечную палочку (Escherichia coli) [7]. Выделенная геномная РНК фага f2 имела свойства мРНК, то есть она распознавалась рибосомой и могла транслироваться. На родственном РНК-бактериофаге Qβ была изучена РНК-зависимая РНК-полимераза (RdRp), которая, как оказалось, может синтезировать цепь РНК на матрице другой цепи РНК, то есть осуществлять репликацию вирусного РНК-генома! В ходе работы с РНК-бактериофагами f2 и его родственником Qβ были получены общие представления о биологии таких РНК-вирусов [8].
РНК, способную распознаваться рибосомой с осуществлением синтеза белка, назвали «(+)РНК». Эта РНК, попав в клетку-хозяина, может сразу использоваться в качестве мРНК для синтеза вирусных белков. У многих вирусов такая (+)РНК инфекционна сама по себе, т. к. кодирует все нужные для полноценной вирусной инфекции белки, включая RdRp, осуществляющую репликацию генетического материала вируса.
После РНК-бактериофагов были найдены (+)РНК-вирусы животных, такие, как вирус полиомиелита [9], [10], представитель группы пикорнавирусов. Подобные вирусы не содержат репликативных белков в составе вирусной частицы (вириона).
Вирус везикулярного стоматита (VSV), как и вирус полиомиелита, был также одним из первых исследованных РНК-вирусов животных, однако в составе вириона нашли фермент RdRp, синтезирующий комплементарную (антигеномную) цепь РНК [11]. Антигеномная цепь является интермедиатом репликации и не участвует в трансляции. Матрицами для синтеза белка в данном случае выступают более короткие вирусные мРНК (субгеномные РНК), транскрибируемые с геномной цепи. Хотя антигеномная РНК не транслируется, ее последовательность совпадает с последовательностями мРНК, поэтому говорят, что она имеет ту же полярность — положительную. Итак, в рассматриваемом случае антигеномная и субгеномные цепи являются (+)РНК, а геномная РНК играет роль матрицы для синтеза (+)РНК и оттого называется «РНК противоположной полярности», то есть «(–)РНК». У (–)РНК-вирусов как раз такая РНК в качестве геномной упаковывается в вирион вместе с вирусной RdRp, которая ответственна за матричный синтез антигеномной и субгеномных (+)РНК после проникновения в клетку. Cреди (–)РНК вирусов выделяют вирусы с несегментированным геномом (вирион содержит одну молекулу (–)РНК, вместе с RdRp необходимую для инфекции; порядок Mononegavirales) и сегментированным геномом (для инфекции необходимо несколько разных молекул геномной РНК, каждая из которых связана со своей молекулой RdRp; порядок Articulavirales). Хорошо известный вирус гриппа А является представителем второй группы. Каждая (–)РНК (геномный сегмент), упакованная в вирусную частицу, «обёрнута» молекулами белка нуклеокапсида NP, в комплексе с которым образуется РНП (рибонуклеопротеин). Также в этот комплекс входит мультисубъединичная RdRp.
Встречаются вирусы, геном которых представлен двухцепочечной РНК. Как и в случае (–)РНК-вирусов, у дцРНК-вирусов во время репликации в клетке первым делом происходит синтез (+)цепи. Вирусные частицы этой группы также включают в свой состав RdRp.
Наша статья посвящена очень занятной группе вирусов, имеющих «двусмысленный РНК-геном». Сегментированная природа генома роднит их с представителями порядка Articulavirales, однако, в отличие от последних, один или два РНК-сегмента являются «(±)РНК». Такие РНК называют амбисенсными: это значит, что в пределах одной молекулы РНК есть последовательности, по смыслу соответствующие мРНК ((+)участки), а также участки отрицательной полярности ((–)участки), то есть комплементарные мРНК. Согласно таксономии, вирусы с двусмысленным РНК-геномом определяют в семейства Bunyaviridae и Arenaviridae.
Исторически одним из первых выделенных вирусов с двусмысленной РНК был флебовирус — вирус лихорадки долины Рифт (RVFV) [12]. Открытие амбисенсной природы РНК некоторых вирусов [13], [14] пришлось на период, когда были достаточно хорошо исследованы (+)- и (–)РНК-содержащие вирусы, что и позволило предположить возможность «двусмысленной» молекулы РНК в составе таких вирусов.
Вирусы с двусмысленным РНК-геномом из семейства Bunyaviridae
Вирусные частицы (вирионы) Bunyaviridae диаметром от 80 до 130 нанометров могут иметь изменчивую (плеоморфную) форму. Липопротеидная оболочка, образованная фосфолипидной мембраной и вирусными гликопротеинами Gn и Gc, содержит внутри три нуклеокапсида (рибонуклеопротеина, состоящих из молекулы РНК (сегмента), «одетой» в молекулы белка нуклеокапсида N, и ассоциированной с ней одной молекулы репликазы L (RdRp)). Три сегмента РНК-генома, несущих на концах комплементарные участки (благодаря которым РНК «циклизуются» в вирионе), получили названия в соответствии с длинами их нуклеотидной последовательности: L (large,
7000 нуклеотидных остатков), M (medium,
3000 н.о.), S (small,
1000 н.о.) (рис. 1.). В семействе встречаются (–)РНК-вирусы (роды Orthobunyavirus, Hantavirus и Nairovirus), имеющие концептуальную схожесть молекулярной стратегии репликации с таковой, например, вируса гриппа. Однако вирусы семейства Bunyaviridae не имеют матриксного белка — широко распространенного типа полипротеинов, встречающегося у большинства липид-содержащих РНК-вирусов животных и человека.
Рисунок 1. Схематичное изображение структуры вириона флебовирусов
В семействе Bunyaviridae роды Phlebovirus, Tospovirus и Tenuivirus являются вирусами с двусмысленным РНК-геномом и, в отличие от остальных представителей семейства, имеют чуть более длинный S-сегмент генома (РНК S) (±)полярности. Род Tospovirus имеет вдобавок (+)участок на РНК M, который делает и эту РНК амбисенсной.
Флебовирусы
Вирусы рода Phlebovirus выделяют практически по всему миру и относят к нетаксономической группе арбовирусов, распространяющихся в членистоногих переносчиках и в позвоночных, на которых питаются переносчики. Члены этого рода переносятся кровососущими членистоногими. Инфекции не обходят стороной человека: вирусы сицилийской и неаполитанской москитных лихорадок широко распространены по территории Средиземноморья [15]. Среди симптомов таких инфекций — продолжительная сильная лихорадка, тошнота, рвота, диарея и головные боли. Вирус Тосканы, также переносимый москитами, обладает способностью проникать в нервную ткань и, вдобавок к вышеперечисленным симптомам, вызывает асептический менингит и менингоэнцефалит. Флебовирусы, переносимые клещами, например, вирус Бханджа, вирус тяжелой лихорадки с синдромом тромбоцитопении, или вирус Хартленд, вызывают серьезные вспышки инфекций среди людей [16].
Эти вирусы получили свое имя от латинского названия москитов (Phlebotominae), которые являются их основными переносчиками. Вирионы флебовирусов имеют диаметр 100-125 нанометров. Внутри вириона находятся три вирусных рибонуклеопротеина (вРНП), содержащих геномные сегменты, однако для вируса лихорадки долины Рифт (RVFV) было показано [17], что вирионы также могут содержать ещё три дополнительных вРНП, образованных цепочками антигеномных РНК, комплементарных геномным вирусным РНК. Рецептор-распознающий аппарат вирусов представлен гетеродимерами гликопротеинов Gn и Gc, которые организованным способом распределены по мембране вириона.
Структура генома флебовирусов
Геном флебовирусов как и других представителей семейства Bunyaviridae, включает три молекулы РНК: PHК L, РНК M, РНК S, имеющие на 5′- и 3′- концах уникальные для каждого геномного сегмента комплементарные последовательности. РНК L (–)полярности кодирует белок репликазы L. (–)РНК M кодирует предшественник гликопротеинов G1 и G2. (±)РНК S кодирует белок нуклеокапсида N на (–)полярном участке (ближе к 3′) и неструктурный белок NSs на (+)полярном участке (ближе к 5′) (рис. 2).
Рисунок 2. Схема структуры генома флебовирусов. Отмечены участки РНК, обладающие (–)- и (+)полярностью. Пунктирной линией обозначен сайт протеолиза белкового продукта.
NSs выполняет ряд функций, среди которых подавление индукции интерферона, усиление репликации и транскрипции вирусной РНК и определение круга хозяев [18]. NSs через цепочку белковых факторов способен приводить к инактивации противовирусной протеинкиназы R организма-хозяина [19].
При одевании вирусных РНК белок N распознаёт последовательность на ее 5′-конце. В вирионе каждая молекула РНП закольцована за счет комплементарных взаимодействий 5′- и 3′-концевых последовательностей (образование т.н. «ручек сковороды»). Таким образом, сегменты генома организуются в шпилечные структуры с короткими (около 12 пар нуклеотидных остатков) стебельками и большими (весь остальной геном) петлями, которые покрыты белком N.
Главный промотор транскрипции и репликации располагается в области спаренных 5′- и 3′-концевых участков («ручки»). Транскрипция и репликация генома флебовирусов осуществляются репликазой L (RdRp).
Как вирусы «воруют» у клеток кэп для синтеза своих мРНК?
Зрелая мРНК эукариот на 5′-конце имеет т.н. кэп — 7-метилгуанозин-5′-трифосфат, соединенный с соседним нуклеотидом 5′,5′-трифосфатной связью. Такая структура делает 5′-конец устойчивым к многим 5′-экзонуклеазам (ферментам, которые «едят» цепочку нуклеотидов с 5′-конца), но самое важное — она распознается рибосомой и необходима для осуществления трансляции.
Кажется, что синтез белков вирусов эукариот возможен только в том случае, если вирусные мРНК имеют кэп. Разные группы вирусов решают «вопрос кэпа» по-разному: кто-то использует ковалентно-пришитый к 5′-концу белок, имитирующий кэп, кто-то имеет образованные вторичными структурами РНК внутренние сайты посадки рибосом (IRES), кто-то может кодировать свои системы кэпирования или привлекать клеточный аппарат созревания РНК. В случае (±)РНК-вирусов, равно как и для многих (–)РНК-вирусов, имеет место процесс, называемый «стащить кэп» (cap snatching). Рассмотрим этот механизм на примере флебовирусов.
Белок L имеет РНК-полимеразную (т.е. может синтезировать комплементарную РНК-цепь) и эндонуклеазную (т.е. может разрезать цепочку нуклеиновой кислоты в определенных сайтах) активности. Последняя направлена на создание разрыва в 5′-нетранслируемой области (НТО) клеточных мРНК, что ведет к декэпированию этих мРНК. Продукт этого «откусывания», короткая кэпированная РНК, используется в дальнейшем в качестве затравки для транскрипции вирусной РНК в цитоплазме. После осуществления такого разрыва вирусная репликаза вместе с 5′-концевым фрагментом клеточной мРНК запускает транскрипцию на матрице геномной вирусной РНК [18]. Таким образом синтезируются способные взаимодействовать с рибосомами субгеномные вирусные РНК. Подход «стащить кэп» не используется для репликации вирусных РНК, то есть для синтеза геномных и антигеномных РНК.
Механизмы транскрипции и репликации РНК флебовирусов
Транскрипция кодирующей белок N последовательности на РНК S, как и для генов других геномных сегментов, происходит с участием геномной (–)РНК по принципу «стащить кэп», а мРНК, кодирующая белок NSs (закодирован в (+)последовательности РНК S), транскрибируется по этому же принципу, но с антигеномной цепи. То есть (+)участок геномной цепи не способен сразу распознаваться рибосомой — для трансляции этого участка необходимо сначала синтезировать полноразмерную антигеномную РНК, с нее — содержащую клеточный кэп субгеномную РНК, и только на субгеномную РНК «сядет» рибосома.
Остановка транскрипции (–)участка РНК S определяется межгенным сигналом терминации. Похожие сигналы терминации находятся в 5′-концевой области РНК M и РНК L. В результате синтезируются кэпированные, но неполиаденилированные (и, следовательно, не такие стабильные, как клеточные мРНК) субгеномные РНК [18]. Также было показано [17], что в инфицированных клетках наблюдается ранняя экспрессия белка NSs, к тому же при детальном анализе состава вирионов обнаружили, что в вирусную частицу может упаковываться как три геномных цепи, так и еще три антигеномных цепи. Считается, что антигеномная РНК S присутствует в вирионе для осуществления ранней транскрипции мРНК, кодирующей NSs, поскольку этот неструктурный белок способен регулировать клеточные процессы, и чем раньше он начнёт работать в зараженной клетке, тем интенсивнее будет протекать вирусная инфекция.
Когда белка N накапливается некоторое «пороговое» количество, происходит переключение режима работы белка L с транскрипционного на репликационный, в результате чего синтезируются не субгеномные РНК, а антигеномные. Инициация репликации не требует затравок клеточной природы, полимеризация комплементарной цепи начинается с одного рибонуклеотида, который и является затравкой [18]. Репликация прекращается, когда репликаза доходит до конца геномной цепи. Геномные РНК синтезируются по аналогичной схеме с антигеномных цепей. Все вышеописанные процессы протекают в цитоплазме — для эффективных транскрипции, репликации, созревания гликопротеинов и, в конце концов, формирования вирусных частиц необходимо образование «вирусных фабрик», представляющих собой трубчатые структуры, образованные мембранами комплекса Гольджи. Такие «фабрики» позволяют повысить локальную концентрацию компонентов репликации вируса [20].
Жизненный цикл флебовирусов
Жизненный цикл состоит из следующих стадий (рис. 3):
Рисунок 3. Схема, демонстрирующая основные этапы цикла флебовируса
Тосповирусы и тенуивирусы
Тосповирусы имеют сходную с флебовирусами структуру вириона. Они являются патогенами растений, использующими в качестве переносчика и второго хозяина трипсов, отряд мелких насекомых-фитофагов [21] и способными к межклеточному транспорту через плазмодесмы в растениях благодаря наличию транспортного белка NSm. Этот белок не входит в состав вириона и синтезируется в течение короткого периода на ранних стадиях инфекции. Он способен связываться с белком нуклеокапсида N, вирусной РНК и клеточными белками, оказываясь ответственным не только за межклеточный транспорт вРНП, без упаковки в вирион, но и за образование вышеупомянутых «вирусных фабрик» в клетке, что в совокупности сказывается на степени вирулентности тосповирусов [22].
Название рода Tospovirus происходит от сокращения названия вируса пятнистого увядания томатов (tomato spotted wilt virus, ТоSWV), впервые выделенного в 1930 году из зараженных растений томата. Этот вирус имеет очень широкий спектр хозяев и важное хозяйственное значение, борьба с ним ведется, в основном, за счет контроля численности трипсов.
Структура генома тосповирусов и тенуивирусов
Представители родов Тospovirus и Tenuivirus (тенуивирусы близки к тосповирусам, но не имеют липидной оболочки) являются единственными известными РНКвирусами растений с двусмысленным геномом [23]. Геном тосповирусов представлен тремя РНК-сегментами: большим, средним и малым (L, M, S). РНК L кодирует репликазу L. РНК S, подобно таковой у флебовирусов, кодирует белок нуклеокапсида N в (–)области и неструктурный белок NSs в (+)области. Эти области не пересекаются, они разделены межгенным некодирующим участком, содержащим сигналы терминации транскрипции. М-сегмент генома имеет принципиально отличную от РНК М флебовирусов структуру, являясь амбисенсной РНК. РНК М тосповирусов имеет область (–)полярности, в которой находится последовательность, кодирующая мРНК GnGc — предшественника поверхностных гликопротеинов, а также участок (+)полярности в 5′-области, кодирующий белок межклеточного транспорта NSm. Эти последовательности также разделены межгенным участком (рис. 4). Механизмы транскрипции и репликации РНК этих вирусов сходны с таковыми у флебовирусов [18].
Рисунок 4. Схема структуры генома тосповирусов. Отмечены участки РНК, обладающие (–)- и (+)полярностью. Пунктирной линией обозначен сайт протеолиза белкового продукта.
Отдельного внимания заслуживает неструктурный белок, закодированный в S-сегменте генома тосповирусов — NSs. Основной его функцией является супрессия противовирусного сайленсинга РНК, системы малых интерферирующих РНК [5], [24], распознающих вирусные РНК, что приводит к деградации последних [25]. Логично предположить, что синтез такого белка должен происходить как можно раньше, поэтому, возможно, по аналогии с белком NSs флебовирусов, ранняя транскрипция такой последовательности происходит в результате наличия в вирионе, помимо геномной цепи РНК S, еще и соответствующей ей антигеномной.
Вирусы с двусмысленным РНК-геномом из семейства Arenaviridae
Помимо семейства Bunyaviridae, амбисенсные РНК имеют представители семейства Arenaviridae. Аренавирусы являются таксономической группой вирусов позвоночных с сегментированным двусмысленным РНК-геномом. Вирусы, инфицирующие млекопитающих, определены в род Mammarenavirus, а заражающие рептилий — в роды Reptarenavirus и Hartmanivirus [26].
Вирионы аренавирусов, как и рассмотренных выше буньявирусов, плеоморфны, а их диаметр может варьировать от 40 до 200 нанометров в зависимости от вида, однако и частицы одного вида могут заметно различаться по размерам [27]. Границы вириона представлены липопротеидной оболочкой — производной клеточной мембраны, модифицированной равномерно распределёнными гликопротеиновыми комплексами (гетеродимерный гликопротеин GP1/GP2). Гликопротеины синтезируются в виде предшественника, который разрезается примерно пополам клеточной протеиназой на рецептор-распознающую субъединицу GP1 и трансмембранную субъединицу GP2. Последняя ответственна за слияние мембран при проникновении в цитоплазму [28]. В вирионе гликопротеины ассоциированны с лежащими на внутренней стороне мембраны молекулами матриксного белка Z, выстилающего внутреннюю поверхность мембраны, и белка нуклеокапсида N. Белок N способен связываться с РНК, распознавать кэп и ингибировать интерфероновый ответ. Структурный белок Z в клетке выполняет ряд функций (в том числе ингибирование трансляции клеточных мРНК и подавление апоптоза), являясь фактором созревания вирусных частиц (отвечает за инициацию сборки вирионов и за их отпочковывание).
Во время сборки вирусных частиц при формировании внешней оболочки иногда происходит захват субъединиц клеточных рибосом, по всей видимости, не играющих роли в вирусной инфекции (рис. 5).
Рисунок 5. Схематичное изображение структуры вириона аренавирусов
Значительная часть представителей семейства вызывает хронические и, как правило, бессимптомные инфекции у грызунов. При контакте человека с такими вирусами может развиваться острая и тяжелая инфекция, часто — геморрагическая лихорадка (например, в случае инфекции вирусом лихорадки Ласса, LasV). Вирус лимфоцитарного хориоменингита (LCMV), первый выделенный аренавирус, является нейроинвазивным. Попав в организм человека (например, через выделения грызунов), вирионы с током крови преодолевают гематоэнцефалический барьер центральной нервной системы и вызывают воспаления мозговых оболочек [29].
Структура генома аренавирусов
Геном аренавирусов имеет ряд особенностей и представлен двумя сегментами (РНК L
3000 н.о.), циклизованными уже известными нам «ручками сковороды» и закрученными в спиральный рибонуклеопротеиновый комплекс (рис. 6). Обе молекулы РНК — двусмысленные!
Рисунок 6. Схема структуры генома аренавирусов. Отмечены участки РНК, обладающие (–)- и (+)полярностью. Пунктирными линиями обозначены сайты протеолиза белковых продуктов.
РНК L на (–)участке несет последовательность, комплементарную гену репликазы L, и рамку матриксного и регуляторного белка Z на (+)участке в 5′-концевой части геномной РНК.
РНК S кодирует белок нуклеокапсида N в области (–)полярности и содержит рамку считывания GP1GP2 — предшественника поверхностных гликопротеинов GP1/GP2 (также в 5′-концевой части геномного сегмента).
(–)- и (+)участки разделены межгенными сайтами, образующими прочные вторичные структуры шпилечного характера. На 5′-конце геномных и антигеномных цепей присутствует сигнал инициации инкапсидации (то есть «одевания» РНК вирусными белками с образованием вРНП), распознаваемый белком N [18].
Транскрипция и репликация генома аренавирусов
Оба процесса проходят в цитоплазме инфицированной клетки. Транскрипция начинается при участии репликазы L по уже описанному выше для флебовирусов принципу «стащить кэп» (cap snatching). Терминация транскрипции обусловлена наличием соответствующего сигнала в стабильных шпильках межгенного пространства геномной или антигеномной РНК. Вирусные субгеномные РНК не полиаденилируются [18].
Переключение на репликацию связано с наличием белка N: когда его накапливается такое количество, что он начинает покрывать строящиеся цепи РНК, это, вероятно, влияет на конформацию репликазы и приводит к проскоку сигналов терминации транскрипции в виде межгенных шпилек. РНК S при репликации накапливается в больших количествах, так как нужно много копий белка нуклеокапсида, а также гликопротеинов (для экспрессии последних необходим предварительный синтез антигеномной РНК).
Заключение
Принимая во внимание всё вышеизложенное, можно сделать выводы относительно общих особенностей вирусов, содержащих амбисенсную РНК. Геном таких вирусов является сегментированным, и хотя бы один сегмент представлен амбисенсной РНК. Каждый геномный сегмент содержит комплементарные 3′- и 5′-концевые последовательности, образующие «ручки сковороды». В составе этого не очень протяженного дуплекса в геномной РНК присутствует главный промотор транскрипции и репликации, распознаваемый репликазой L. 5′- концевые последовательности геномных и антигеномных молекул РНК связываются белком нуклеокапсида N. Затравкой для синтеза вирусных мРНК, как и в случае типичных вирусов с сегментированным (–)РНК-геномом, является «откушенный» кэпированный фрагмент клеточной мРНК.
Что же касается самих амбисенсных РНК, они содержат последовательности отрицательной полярности в 3′-части и положительной полярности в 5′-части геномной цепи. Терминация транскрипции в таких двусмысленных РНК связана с наличием соответствующих сигналов в межгенном участке. При этом (+)участок амбисенсной РНК не может сразу выступать в качестве мРНК, необходим последовательный синтез антигеномной, а только потом субгеномной РНК положительной полярности. Все эти процессы занимают определенное время, поэтому вопрос «отсрочки» синтеза белков из (+)участка геномной РНК может решаться для вируса путем включения в зрелую вирусную частицу, помимо геномной (±)РНК, ещё и антигеномной (±)РНК.
Такая необычная организация двусмысленных геномных сегментов является интересным способом представления двух кодирующих последовательностей в одном геномном сегменте. На примере вирусов с двусмысленными РНК-геномами заметно, насколько изобретательной может быть эволюция вирусных РНК. Поскольку вирусы с двусмысленными РНК-геномами до сих пор удерживают определенную нишу, можно утверждать, что такой способ кодирования обладает некоторыми преимуществами по сравнению с более привычным для родственных вирусов способом, использующим только (–)РНК-сегменты.
Как возникли амбисенсные РНК и почему поддержались отбором, до сих пор остается одной из загадок современной вирусологии.
И как сказал один известный принц: «Есть многое на свете, друг Горацио, что и не снилось нашим мудрецам!»
Благодарности от автора
Я благодарю доктора биологических наук, профессора кафедры вирусологии биологического факультета МГУ им. М.В. Ломоносова Аграновского Алексея Анатольевича за интересные и содержательные лекции по молекулярным процессам РНК-вирусов и вдохновение на написание данной статьи. Также выражаю благодарность художнику Андрею Занкевичу, чьи наглядные и яркие иллюстрации украшают данную статью.