жировая дистрофия печени диффузная форма
Диффузные изменения печени по типу жирового гепатоза: причины, симптомы, лечение
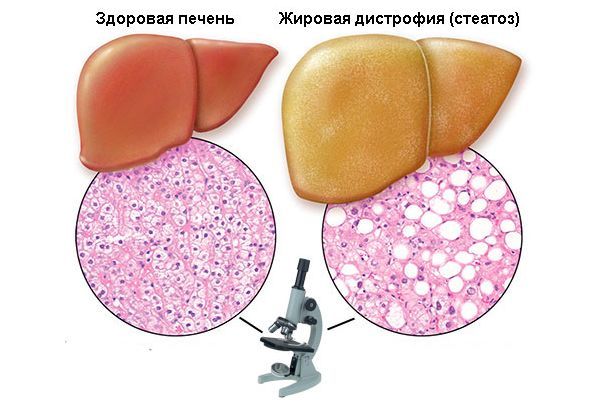
Ткани здоровой печени однородны, по ним проходят кровеносные сосуды и желчные протоки. Диффузные изменения печени по типу жирового гепатоза характеризуются тем, что в клетках печени — гепатоцитах — оседает и накапливается избыток жира. Нормальные клетки органа при этом постепенно погибают. Печень становится неоднородной, причем, чаще всего при диффузной инфильтрации она практически вся подвергается изменениям.
Выделяют три вида диффузной жировой инфильтрации:
Причины заболевания
Спровоцировать диффузные изменения печени по типу гепатоза могут:
К сожалению, диффузный гепатоз печени не всегда удается отличить от хронического воспалительного процесса, тем более, нелегко определить его причину, чтобы назначить правильное лечение. Поэтому, наряду с лабораторными анализами и ультразвуковым исследованием печени, назначают биопсию и компьютерную томографию.
Симптомы и лечение
Диффузный жировой гепатоз печени сопровождается симптомами, которые характерны практически для всех заболеваний этого органа, а именно:
Иногда заболевание протекает без ярко выраженных симптомов, обостряясь при увеличении физических нагрузок, переедании, злоупотреблении алкоголем. Его терапия требует комплексного подхода, так как необходимо добиться устранения причины разрушения клеток печени. Нужно как медикаментозное лечение, так и длительное соблюдение (на протяжении нескольких месяцев) строгой диеты, назначенной врачом. Восстановление клеток печени невозможно, если продолжать употреблять алкогольные напитки, курить, есть жирную пищу.
Для восстановления гепатоцитов применяются гепатопротекторы. Иногда врач, кроме диеты, назначает биологически активные добавки к пище.
В процессе выздоровления и после него необходимо постоянно следить за весом, отказаться от алкоголя и курения, продолжать придерживаться диеты. Важно добиться нормализации работы нервной системы, улучшения иммунитета.
Все это поможет избежать рецидивов заболевания в будущем.
Жировая дистрофия печени
Общие сведения
Печень принимает активное участие в обмене жиров. Жиры, поступающие с пищей расщепляются в кишечнике с помощью ферментов и всасываются в кровеносное русло. Оттуда они попадают в печень, где преобразуются в триглицериды, холестерин, фосфолипиды и другие необходимые для нашего организма вещества. Жировая инфильтрация печени возникает в случае накопления в печени высокого количества триглицеридов. При жировой дистрофии содержание триглицеридов может достигать более 50% ее массы (в норме – не более 5 %). Факторы ведущие к этому состоянию разнообразны: повышенное поступление жирных кислот с пищей, повышенное образование триглицеридов в печени, нарушение транспорта триглицеридов из печени в жировую ткань, где триглицериды в норме запасаются в виде жира. В зависимости от характера отложения жира жировая дистрофия печени разделяется на крупнокапельную и мелкокапельную (размер капелек жира в клетках печени).
Причины заболевания
Симптомы
Пациенты с жировым гепатозом жалоб обычно не предъявляют. Течение болезни стертое, медленно прогрессирующее. Со времени появляются постоянные тупые боли в правом подреберье, могут быть тошнота, рвота, нарушения стула.
Очень редко наблюдается жировая дистрофия печени с выраженной клинической картиной: сильные боли в животе, желтуха, похудание, кожный зуд.
Диагностика
Заподозрить жировую дистрофию врач –терапевт может уже при клиническом осмотре по увеличению печени в размерах при пальпации живота. Увеличение печени подтверждают с помощью УЗИ брюшной полости. В биохимическом анализе крови обнаруживают повышение печеночных ферментов (АсАТ, АлАТ, щелочная фосфатаза). В некоторых случаях для подтверждения диагноза проводят КТ, МРТ, биопсию печени.
Лечение
Тактика лечения зависит от причины, вызвавшей заболевание. Правильное питание, отказ от алкоголя, коррекция метаболических нарушений, как правило, приводят к улучшению состояния. Назначают диету с повышенным содержанием белков, ограничением жиров, особенно животного происхождения. Жировая дистрофия печени, связанная с алкоголизмом при продолжении употребления алкоголя со временем только прогрессирует.
Неалкогольный стеатоз печени, диагностика, лечебные подходы
Рассмотрены факторы риска развития неалкогольной жировой болезни печени, первичная и фторичная формы заболевания, подходы к диагностике стеатоза и фиброза печени, общие принципы лечения пациентов, включая диетотерапию, воздействие на метаболический сндром
Factors of non-alcoholis fatty disease of liver development risk have been analyzed, as well as primary and secondary forms of disease, approaches to diagnostic of steatosis hepatis and fibrosis, general principles of treatment including diet therapy, metabolic syndrome effect, gastroprotectors application.
Неалкогольный стеатоз печени (неалкогольная жировая болезнь печени (НАЖБП), жировая дистрофия печени, жировая печень, жировая инфильтрация) — первичное заболевание печени или синдром, формируемый избыточным накоплением жиров (преимущественно триглицеридов) в печени. Если рассматривать эту нозологию с количественной точки зрения, то «жир» должен составлять не менее 5–10% веса печени, или более 5% гепатоцитов должны содержать липиды (гистологически) [1].
Если не вмешиваться в течение болезни, то в 12–14% НАЖБП трансформируется в стеатогепатит, в 5–10% случаев — в фиброз, в 0–5% фиброз переходит в цирроз печени; в 13% случаев стеатогепатит сразу трансформируется в цирроз печени [2].
Эти данные позволяют понять, почему эта проблема на сегодняшний день вызывает всеобщий интерес, если при этом будут ясны этиология и патогенез, то будет понятно, как наиболее эффективно лечить эту часто встречаемую патологию. Уже сейчас понятно, что у части больных это может оказаться болезнью, а у части — симптомом или синдромом.
Признанными факторами риска развития НАЖБП являются:
Перечисленные факторы риска НАЖБП показывают, что значительная часть их является компонентами метаболического синдрома (МС), который представляет собой комплекс взаимосвязанных факторов (гиперинсулинемия с инсулинорезистентностью — сахарный диабет 2-го типа (СД 2-го типа), висцеральное ожирение, атерогенная дислипидемия, артериальная гипертензия, микроальбуминурия, гиперкоагуляция, гиперурикемия, подагра, НАЖБП). МС составляет основу патогенеза многих сердечно-сосудистых заболеваний и указывает на тесную связь их с НАЖБП. Таким образом, круг заболеваний, который формирует НАЖБП, заметно расширяется и включает не только стеатогепатит, фиброз, цирроз печени, но и артериальную гипертонию, ишемическую болезнь сердца, инфаркт миокарда и сердечную недостаточность. По крайней мере, если прямые связи этих состояний требуют дальнейшего изучения доказательной базы, их взаимное влияние несомненно [6].
Эпидемиологически различают: первичную (метаболическую) и вторичную НАЖБП. К первичной форме относят большинство состояний, развивающихся при различных метаболических расстройствах (они перечислены выше). К вторичной форме НАЖБП относят состояния, которые формируются: алиментарными нарушениями (переедание, голодание, парентеральное питание, трофологическая недостаточность — квашиоркор); лекарственными воздействиями и взаимоотношениями, которые реализуются на уровне печеночного метаболизма; гепатотропными ядами; синдромом избыточного бактериального роста кишечника; заболеваниями тонкой кишки, сопровождаемыми синдромом нарушенного пищеварения; резекцией тонкой кишки, тонкотолстокишечным свищом, функциональной недостаточностью поджелудочной железы; болезнями печени, в т. ч. и генетически детерминированными, острой жировой болезнью беременных и др. [7–9].
Если врач (исследователь) располагает морфологическим материалом (биопсия печени), то морфологически различают три степени стеатоза:
Приведя морфологическую классификацию, мы должны констатировать, что эти данные носят условный характер, так как процесс никогда не носит равномерно-диффузного характера, и в каждый конкретный момент мы рассматриваем ограниченный фрагмент ткани, и уверенности в том, что в другом биоптате мы получим то же самое, нет, и, наконец, 3-я степень жировой инфильтрации печени должна была бы сопровождаться функциональной печеночной недостаточностью (хотя бы по каким-либо компонентам: синтетическая функция, дезинтоксикационная функция, билиарная состоятельность и др.), что практически не свойственно НАЖБП.
В вышеизложенном материале показаны факторы и состояния метаболизма, которые могут участвовать в развитии НАЖБП, а в качестве современной модели патогенеза предложена теория «двух ударов»:
первый — развитие жировой дистрофии;
второй — стеатогепатит.
При ожирении, особенно висцеральном, увеличивается поступление в печень свободных жирных кислот (СЖК), при этом развивается стеатоз печени (первый удар). В условиях инсулинорезистентности увеличивается липолиз в жировой ткани, а избыток СЖК поступает в печень. В итоге количество жирных кислот в гепатоците резко возрастает, формируется жировая дистрофия гепатоцитов. Одновременно или последовательно развивается окислительный стресс — «второй удар» с формированием воспалительной реакции и развитием стеатогепатита. Это связано в значительной степени с тем, что функциональная способность митохондрий истощается, включается микросомальное окисление липидов в системе цитохрома, что приводит к образованию активных форм кислорода и повышению продукции провоспалительных цитокининов с формированием воспаления в печени, гибели гепатоцитов, обусловленной цитотоксическими эффектами TNF-альфа1 — одного из основных индукторов апоптоза [10, 11]. Последующие этапы развития патологии печени и их интенсивность (фиброз, цирроз) зависят от сохраняющихся факторов формирования стеатоза и отсутствия эффективной фармакотерапии.
Диагностика НАЖБП и состояний ее прогрессирования (стеатоз печени, стеатогепатит, фиброз, цирроз)
Жировая дистрофия печени — формально морфологическое понятие, и, казалось бы, диагностика должна была бы сводиться к биопсии печени. Однако такого решения международными гастроэнтерологическими ассоциациями не принято и вопрос обсуждается. Это связано с тем, что жировая дистрофия — понятие динамическое (она может активизироваться или подвергаться обратному развитию, может носить как относительно диффузный, так и очаговый характер). Биоптат всегда представлен ограниченным участком, и трактовка данных всегда достаточно условна. Если признать биопсию как обязательный диагностический критерий, то ее нужно проводить достаточно часто; сама биопсия чревата осложнениями, а метод исследования не должен быть опаснее самой болезни. Отсутствие решения о биопсии не является отрицательным фактором, тем более что на сегодняшний день стеатоз печени это понятие клинико-морфологическое с наличием многих факторов, участвующих в патогенезе.
Из представленных выше данных видно, что диагностика может начаться на разных стадиях болезни: стеатоз → стеатогепатит → фиброз → цирроз, и в диагностический алгоритм должны входить методы, определяющие не только жировую дистрофию, но и стадию ее.
Так, на стадии стеатоза печени основным симптомом является гепатомегалия (обнаруженная случайно или при диспансерном обследовании). Биохимический профиль (аспартатаминотрансфераза (АСТ), аланинаминотрансфераза (АЛТ), щелочная фосфотаза (ЩФ), гаммаглутамилтранспептидаза (ГГТ), холестерин, билирубин) устанавливает при этом наличие или отсутствие стеатогепатита. При повышении уровня трансаминаз необходимо проведение вирусологических исследований (которые либо подтвердят, либо отвергнут вирусные формы гепатита), а также диагностика других форм гепатита: аутоиммунного, билиарного, первичного склерозирующего холангита. Ультрозвуковое исследование не только устанавливает увеличение размеров печени и селезенки, но и признаки портальной гипертензии (по диаметру селезеночной вены и размерам селезенки). Менее употребляемым (а может быть, и известным) является оценка жировой инфильтрации печени, состоящая в измерении «столба затухания», по динамике которого в разные промежутки времени можно судить о степени жировой дистрофии (рис.) (методика УЗИ описана) [12].
Более ранние модели ультразвуковых аппаратов оценивали денситометрические показатели (по динамике которых можно было судить о динамике и степени стеатоза). В настоящее время денситометрические показатели получают с помощью компьютерной томографии печени. Рассматривая патогенез НАЖБП, оценивают общий осмотр, антропометрические показатели (определение массы тела и окружности талии — ОТ). Так как МС занимает значительное место в формировании стеатоза, то в диагностике необходимо оценивать: абдоминальное ожирение — ОТ > 102 см у мужчин, > 88 см у женщин; триглицериды > 150 мг/дл; липопротеины высокой плотности (ЛПВП): 130/85 мм рт. ст; индекс массы тела (ИМТ) > 25 кг/м 2 ; гликемия натощак > 110 мг/дл; гликемия через 2 часа после нагрузки глюкозой 110–126 мг/дл; СД 2-го типа, инсулинорезистентность.
Представленные выше данные рекомендуются ВОЗ и Американской ассоциацией клинических эндокринологов. Важным диагностическим аспектом является также установление фиброза и его степени. Несмотря на то, что фиброз также понятие морфологическое, его определяют по различным расчетным показателям. С нашей точки зрения дискриминантная счетная шкала Bonacini, определяющая индекс фиброза (ИФ), является удобным методом, соответствующим стадиям фиброза. Мы провели сравнительное изучение расчетного показателя ИФ с результатами биопсий. Эти показатели представлены в табл. 1 и 2.
Практическое значение ИФ:
1) ИФ, оцененный по дискриминантной счетной шкале, достоверно коррелируется со стадией фиброза печени по данным пункционной биопсии;
2) изучение ИФ позволяет с высокой степенью вероятности оценить стадию фиброза и использовать его для динамического наблюдения за интенсивностью фиброзообразования у больных с хроническим гепатитом, НАЖБП и другими печеночными диффузными заболеваниями, в том числе и для оценки эффективности проводимой терапии [13].
И наконец, если проводится пункционная биопсия печени, то она назначается, как правило, в случае дифференциальной диагностики опухолевых образований, в т. ч. и очаговой формы стеатоза. При этом в ткани печени этих больных выявляются:
Диагноз НАЖБП (стеатоз печени) формулируется на основании совокупности следующих симптомов и положений:
Диагностика также предполагает исключение основных печеночных нозологических форм:
Таким образом, диагноз формируется с определения гепатомегалии, определения патогенетических факторов, способствующих стеатозу, и исключения других диффузных форм поражения печени.
Лечебные принципы
Так как основным фактором развития неалкогольного стеатоза печени является избыточная масса тела (МТ), то снижение МТ является основополагающим условием лечения больных НАЖБП, что достигается изменением образа жизни, включающем диетические мероприятия и физическую активность, в т. ч. и в случаях, когда необходимость в снижении МТ отсутствует [14]. Диета должна быть гипокалорийной — 25 мг/кг в сутки с ограничением жиров животного происхождения (30–90 г/день) и уменьшением углеводов (особенно быстро усваиваемых) — 150 мг/сутки. Жиры должны быть преимущественно полиненасыщенными, которые содержатся в рыбе, орехах; важно употреблять не менее 15 г клетчатки за счет фруктов и овощей, а также продукты, богатые витамином А.
Помимо диеты необходимо как минимум 30 минут ежедневных аэробных физических нагрузок (плавание, ходьба, гимнастический зал). Физическая активность сама по себе снижает инсулинорезистентность и улучшает качество жизни [15].
Вторым важным компонентом терапии является воздействие на метаболический синдром и инсулинорезистентность в частности. Из препаратов, ориентированных на ее коррекцию, наиболее изучен метформин [16, 17]. При этом показано, что лечение метформином приводит к улучшению лабораторных и морфологических показателей воспалительной активности в печении. При СД 2-го типа используются инсулиновые сенситайзеры, при этом метаанализ не показал преимуществ их влияния на инсулинорезистентность [18].
Третьим компонентом терапии является исключение использования гепатотоксических лекарственных средств и препаратов, вызывающих повреждение печени (основным морфологическим субстратом этого повреждения является стеатоз печени и стеатогепатит). В этом отношении важным является сбор лекарственного анамнеза и отказ от препарата (препаратов), повреждающих печень.
Так как синдром избыточного бактериального роста (СИБР) играет важную роль в формировании стеатоза печени, то его необходимо диагностировать и проводить коррекцию (препараты с антибактериальным действием — желательно не всасывающиеся; пробиотики; регуляторы моторики, печеночные протекторы), причем выбор терапии зависит от исходной патологии, формирующей СИБР.
Не совсем корректно на сегодняшний день решается вопрос об использовании печеночных протекторов. Есть работы, показывающие их малую эффективность, есть работы, которые показывают их высокую эффективность. Создается впечатление, что их использование не учитывает стадию НАЖБП. Если есть признаки стеатогепатита, фиброза, цирроза печени, то их использование представляется обоснованным. Хотелось бы представить аналитические данные, на основании которых и в зависимости от количества факторов, участвующих в патогенезе НАЖБП, можно выбрать гепатопротектор (табл. 3).
Из представленной таблицы видно (введены наиболее употребляемые протекторы, при желании ее можно расширить, введя другие протекторы), что препараты урсодезоксихолевой кислоты (Урсосан) действуют на максимальное количество патогенетических звеньев поражения печени.
Мы хотим представить результаты лечения Урсосаном больных НАЖБП. Изучено 30 больных (у 15 из них в основе лежало ожирение, у 15 — МС; женщин было 20, мужчин — 10; возраст от 30 до 65 лет (средний возраст 45 ± 6,0 лет).
Критериями отбора служили: повышение уровня АСТ — в 2–4 раза; АЛТ — в 2–3 раза; ИМТ > 31,1 кг/м 2 у мужчин и ИМТ > 32,3 кг/м 2 у женщин. Больные получали Урсосан в дозе 13–15 мг/кг веса в сутки; 15 больных в течение 2 месяцев, 15 больных продолжали прием препарата до 6 месяцев. Результаты лечения представлены в табл. 4–6.
Критерием исключения служили: вирусная природа болезни; сопутствующая патология в стадии декомпенсации; прием препаратов, потенциально способных формировать (поддерживать) жировую дистрофию печени.
2-я группа продолжала получать Урсосан в той же дозе 6 месяцев (при нормальных биохимических показателях). При этом стабилизировался аппетит, постепенно (1 кг/месяц) уменьшалась масса тела. По данным УЗИ — структура и размер печени существенно не изменились, продолжалась динамика по «столбу затухания» (табл. 6).
Таким образом, по нашим данным использование печеночных протекторов у больных НАЖБП в стадии стеатогепатита эффективно, что выражается в нормализации биохимических показателей и уменьшении жировой инфильтрации печени (по данным УЗИ — уменьшение «столба затухания» сигнала), что в целом является важным обоснованием их использования.
Литература
О. Н. Минушкин, доктор медицинских наук, профессор
ФГБУ УНМЦ Управления делами Президента РФ, Москва
Жировая дегенерация печени (неалкогольный гепатоз)
Жировой гепатоз — заболевание печени, при котором в печеночной ткани происходит накопление жиров (увеличение количества липидов). Болезнь часто связывают с употреблением алкоголя, но она может быть вызвана и другими причинами.
Что провоцирует жировую дегенерацию печени?
Метаболические факторы, нарушения обмена веществ. Неалкогольный стеатоз часто вызывает высокая инсулинорезистентность, при которой ткани становятся менее чувствительными к инсулину. Из-за этого может увеличиваться количество глюкозы, повышаться уровень инсулина. При высоком уровне инсулина расщепление липидов происходит быстрее, из-за чего в тканях печени начинается накопление триглицеридов. Без лечения возникает дисбаланс в работе печени, гепатоциты начинают погибать, что провоцирует воспаление и формирование фиброзной ткани.
Употребление гепатотоксических веществ. Чаще всего это — лекарственные средства, метаболизирующиеся в печени. Их регулярный прием приводит к повреждению и гибели гепатоцитов, провоцирует накопление жира в печеночных тканях.
Нарушения микрофлоры кишечника. При активном росте числа бактерий в тонком кишечнике патогены могут попадать в воротную вену, провоцировать иммунную реакцию, воспаление, приводящее к формированию фиброзной ткани. По такому же принципу гепатоз могут провоцировать и некоторые другие заболевания органов ЖКТ.
Нерациональное питание. Нарушать работу печени и провоцировать накопление жиров в ее клетках может голодание или, напротив, переедание. Опасным является несбалансированный рацион, в котором преобладает жирная, содержащая быстрые углеводы еда.
Некоторые хронические болезни. Провоцировать гепатоз могут сердечная, дыхательная недостаточность, сахарный диабет, проблемы с ЖКТ, злокачественные новообразования.
Среди возможных причин жирового гепатоза — наследственная предрасположенность, избыточная выработка соматотропина, хроническая или частая интоксикация, хирургические вмешательства, ожирение (особенно опасно ожирение абдоминального типа). Риск появления заболевания и тяжесть его течения увеличиваются с возрастом: люди старше 45 лет подвержены неалкогольному стеатозу в большей степени.
Мы перезвоним в течение 30 секунд
Симптомы
Опасность неалкогольного гепатоза — в бессимптомном течении. Болезнь никак не проявляет себя до тех пор, пока поражение гепатоцитов не станет серьезным. На стадиях, когда процесс обратим, а лечение не требует серьезных усилий, у жировой дегенерации печени нет симптомов, и диагностировать ее можно только при обращении к врачу.
По мере развития гепатоза, появляется симптоматика:
Классификация
Диагностика и лечение
Обращение к врачу рекомендовано при появлении симптомов жирового гепатоза либо при наличии заболеваний, состояний, которые могут его провоцировать (ожирение, повышение уровня инсулина, нарушения обмена веществ и т.п.). Для диагностики используют методы визуального обследования: УЗИ, МРТ. Возможно проведение биопсии.
При диагностике по УЗИ выявляется увеличение печени, повышение ее эхогенности с сохранением однородности тканей. МРТ используют для визуальной диагностики на более поздних стадиях заболевания. Оно позволяет выявить уменьшение или увеличение размеров органа, наличие локальных участков жировой инфильтрации, оценить состояние инфильтрованной жиром ткани.
Жировая дегенерация печени обратима только на начальных стадиях, до начала внутриклеточного или внеклеточного ожирения органа. Для пациентов с риском появления гепатоза, обусловленным возрастом старше 45 лет или состоянием здоровья, рекомендуется регулярное проведение диагностики для оценки состояния печени. При выявлении заболевания план лечения формируют с учетом стадии гепатоза, наличия сопутствующих заболеваний, возраста и состояния здоровья. Без лечения жировая дегенерация печени осложняется воспалением, появлением фиброзной ткани, возможно развитие цирроза, печеночной недостаточности.
Общие принципы лечения:
Цель лечения — остановить воспалительный процесс и некроз клеток, улучшить биохимические показатели крови, нормализовать обмен веществ, стимулировать регенерацию гепатоцитов.
Дополнительно медцентр «Панацея» рекомендует изменить образ жизни: организовать сбалансированное питание, увеличить количество физических нагрузок, исключить употребление жирного, спиртного.
Мы перезвоним в течение 30 секунд
Стеатоз печени
Стеатоз (жировая дистрофия печени, жировая инфильтрация печени) – заболевание, входящее в группу гепатозов – патологий, характеризующихся нарушением обменных процессов в печеночных клетках с последующим развитием дистрофии ткани.
При стеатозе в гепатоцитах происходит накопление жира. Когда его становится очень много, он разрывает клетку и выходит в межклеточное пространство. Впоследствии вокруг жировой капли формируется оболочка, превращая ее в кисту. Первоначально жировых кист в печени очень мало, они единичные. Однако по мере прогрессирования процесса могут страдать целые группы клеток, а потом стеатоз может захватить всю ткань, вызывая диффузное ожирение печени.
Причины и классификация стеатоза
Существуют две основные причины развития стеатоза:
Поэтому в зависимости от причины различают две формы заболевания – первичную и вторичную.
Первичный стеатоз зачастую возникает в результате метаболических нарушений, спровоцированных эндогенными факторами (ожирением, гиперлипидемией, сахарным диабетом). Вторичная форма является ответом на внешнее воздействие, при котором в организме возникают сбои в обменных процессах. Это может происходить из-за бесконтрольного приема лекарственных препаратов, употребления алкоголя, длительного парентерального питания, оперативного вмешательства на органы пищеварительного тракта.
Симптомы
Заболевание обычно протекает медленно. Очень часто симптомы патологического процесса вообще отсутствуют. В таких случаях его выявляют случайно при обследовании совершенно по другому поводу.
Наиболее распространенными клиническими признаками стеатоза являются:
Диагностика
Развитие стеатоза печени заподозрить сложно, поскольку признаки заболевания неспецифичны. Наиболее информативным методом диагностики является биопсия печени. Также иногда назначаются УЗИ, КТ или МРТ.
Кроме того, пациенту рекомендуется сдать кровь на маркеры аутоиммунного повреждения печени, на гормоны щитовидной железы, а также на наличие специфических антител к ряду вирусных инфекций.
Лечение
Лечение стеатоза заключается в устранении причин, вызвавших заболевание, с последующей нормализацией процессов метаболизма. При этом врач в любом случае оценивает алиментарный статус и назначает диету. В основе лечебного питания – ограничение употребления жиров животного происхождения и быстрых углеводов. Параллельно с этим пациентам рекомендуют посильные физические нагрузки, благодаря которым происходит ускорение утилизации жирных кислот.
Медикаментозное лечение часто играет вспомогательную роль. Пациентам назначают:
К таким препаратам относится Фосфоглив*. Он может устранять причины повреждений и способствовать восстановлению клеток печени.
.jpg)
_550.gif)
_550.gif)
.gif)